数字化实验是研究化学变化的重要手段,为验证次氯酸光照分解的产物,某同学采用三种传感器分别测得氯水光照过程中pH、Cl-浓度、 体积分数的变化,实验数据如图所示,下列叙述错误的是
体积分数的变化,实验数据如图所示,下列叙述错误的是
 体积分数的变化,实验数据如图所示,下列叙述错误的是
体积分数的变化,实验数据如图所示,下列叙述错误的是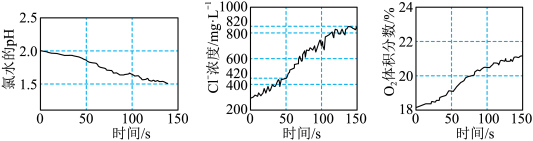
A.从0s到150s,溶液pH降低的原因是 右移 右移 |
B.氯水在光照过程中可能出现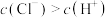 |
C.从50 s到150 s, 的平均生成速率约为 的平均生成速率约为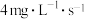 |
D.从0 s到150 s,溶液中 增加到起始浓度的 增加到起始浓度的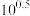 倍 倍 |
2024·黑龙江·模拟预测 查看更多[1]
(已下线)化学(新七省高考卷01)(14+4模式)-2024年高考押题预测卷
更新时间:2024-05-02 10:30:00
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列物质久置于空气中易发生化学变化的有
①氯水、②碳酸钠晶体、③烧碱、④漂白粉、⑤过氧化钠、⑥碳酸氢钠
①氯水、②碳酸钠晶体、③烧碱、④漂白粉、⑤过氧化钠、⑥碳酸氢钠
| A.3种 | B.4种 | C.5种 | D.6种 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列各组中的离子,不能在溶液中大量共存的是
A. 、Na+、 、Na+、 、Cl- 、Cl- | B.Na+、H+、 、Cl- 、Cl- |
C.Na+、K+、OH-、 | D.H+、Na+、Cl-、ClO- |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】反应速率v和反应物浓度的关系是用实验方法测定的。化学反应H2(g)+Cl2(g)=2HCl(g)的反应速率v可表示为v=kcm(H2)cn(Cl2),式中k为反应速率常数,m、n值可由下表中数据确定。
下列说法正确的是( )
| 实验序号 | c(H2)/(mol•L-1) | c(Cl2)/(mol•L-1) | v/(mol•L-1•s-1) |
| ① | 1.0 | 1.0 | 1.0k |
| ② | 2.0 | 1.0 | 2.0k |
| ③ | 2.0 | 4.0 | 4.0k |
| A.在上述反应中,H2、HCl、Cl2的反应速率之比为1:1:2 |
| B.加入催化剂,正反应速率增大,逆反应速率减小 |
C.上述化学反应速率表达式中m=1、n= |
| D.相同条件下,H2的浓度对反应速率的影响小于Cl2的浓度对反应速率的影响 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】HI常用作还原剂,受热发生反应: 。一定温度时,向1L密闭容器中充入
。一定温度时,向1L密闭容器中充入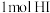 ,体系中
,体系中 与反应时间t的关系如图。下列说法中错误的是
与反应时间t的关系如图。下列说法中错误的是
 。一定温度时,向1L密闭容器中充入
。一定温度时,向1L密闭容器中充入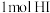 ,体系中
,体系中 与反应时间t的关系如图。下列说法中错误的是
与反应时间t的关系如图。下列说法中错误的是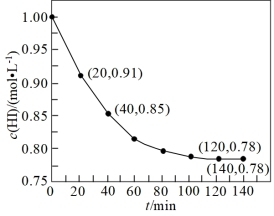
A. 内, 内, |
B.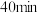 时, 时, |
C. 时,反应达到了平衡状态 时,反应达到了平衡状态 |
D. 时,向该容器中再充入 时,向该容器中再充入 ,化学反应速率不变 ,化学反应速率不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列关于电解质溶液的叙述正确的是
A.常温下电离常数为Ka的酸HA溶液中c(H+)=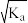 mol·L-1 mol·L-1 |
B.向0.1mol·L-1的氨水中加入少量硫酸铵固体,则溶液中 增大 增大 |
| C.0.2mol·L-1CH3COOH溶液与0.1mol·L-1NaOH溶液等体积混合2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) |
| D.HF比HCN易电离,则NaF溶液的pH比同浓度NaCN溶液的pH大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】酒石酸是葡萄酒中主要的有机酸之一,它的结构式为 (简写为
(简写为 )。已知:25℃时,
)。已知:25℃时, 和
和 的电离平衡常数如下:
的电离平衡常数如下:
下列说法正确的是( )
 (简写为
(简写为 )。已知:25℃时,
)。已知:25℃时, 和
和 的电离平衡常数如下:
的电离平衡常数如下:| 化学式 |  |  |
| 电离平衡常数 |  , , |  , , |
A. 和 和 溶液均呈碱性 溶液均呈碱性 |
B.在 溶液中通入足量 溶液中通入足量 生成的盐是 生成的盐是 |
C.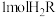 分别与足量的 分别与足量的 、 、 、 、 反应消耗三者的物质的量之比为 反应消耗三者的物质的量之比为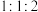 |
D.25℃时,将等物质的量浓度的 和 和 溶液等体积混合,所得溶液中各离子浓度大小顺序为: 溶液等体积混合,所得溶液中各离子浓度大小顺序为: |
您最近一年使用:0次


 能自发进行,则其
能自发进行,则其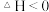
 等物质的量混合的溶液中不存在水解平衡
等物质的量混合的溶液中不存在水解平衡
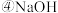 中,
中, 的大小顺序是
的大小顺序是


