铬是一种重要的元素,在合金、电镀、鞣制领域都有重要的应用,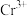 的配位能力很强,可以形成多种配离子。
的配位能力很强,可以形成多种配离子。
(1)基态 原子价层电子的轨道表达式为
原子价层电子的轨道表达式为___________ ,同周期元素的基态原子最外层电子数与 相同的元素有
相同的元素有___________ (写元素符号)。
(2)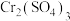 是最重要的铬(Ⅲ)盐之一,阴离子
是最重要的铬(Ⅲ)盐之一,阴离子 的空间构型为
的空间构型为___________ ,基态 原子核外电子中成对电子数和未成对电子数之比为
原子核外电子中成对电子数和未成对电子数之比为___________ 。
(3) 中
中 的数目为
的数目为___________ ,含有的的配体是___________ ,配位数是___________ ,配位原子是___________ 。
(4)比较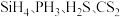 的键角,按由大到小顺序排列:
的键角,按由大到小顺序排列:___________ 。
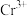 的配位能力很强,可以形成多种配离子。
的配位能力很强,可以形成多种配离子。(1)基态
 原子价层电子的轨道表达式为
原子价层电子的轨道表达式为 相同的元素有
相同的元素有(2)
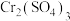 是最重要的铬(Ⅲ)盐之一,阴离子
是最重要的铬(Ⅲ)盐之一,阴离子 的空间构型为
的空间构型为 原子核外电子中成对电子数和未成对电子数之比为
原子核外电子中成对电子数和未成对电子数之比为(3)
 中
中 的数目为
的数目为(4)比较
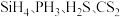 的键角,按由大到小顺序排列:
的键角,按由大到小顺序排列:
更新时间:2024-05-08 14:18:01
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】下表给出了某几种元素原子的原子结构示意图、核外电子排布式、轨道表示式或价电子排布式,分别判断其元素符号、原子序数并指出其在周期表中的位置。
| 元素 | 元素符号 | 原子序数 | 区 | 周期 | 族 | |
| A |  | |||||
| B |  | |||||
| C | 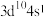 | |||||
| D | 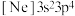 | |||||
| E | 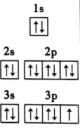 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硅是典型的半导体元素,在电子、材料等领域应用广泛。请回答下列问题:
(1)基态硅(Si)原子的核外电子排布式为_______ 。
(2)碳(C)、硅(Si)、锗(Ge)是同族元素。
①基态C原子的价层电子排布图为_______ ;基态C原子核外电子的空间运动状态有_______ 种。
②基态Si原子的核外电子占据_______ 个能层,_______ 个能级。
③Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______ ,微粒之间存在的相互作用是_______ 。
④Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是_______ 。
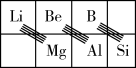
(3)在元素周期表中,某些元素与其右下方的主族元素(如图所示)的一些性质是相似的。如Be与Al的化学性质相似,Be与NaOH溶液反应生成Na2BeO2和H2,请写出Be(OH)2与NaOH溶液反应的离子方程式_______ 。
(1)基态硅(Si)原子的核外电子排布式为
(2)碳(C)、硅(Si)、锗(Ge)是同族元素。
①基态C原子的价层电子排布图为
②基态Si原子的核外电子占据
③Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
④Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是
(3)在元素周期表中,某些元素与其右下方的主族元素(如图所示)的一些性质是相似的。如Be与Al的化学性质相似,Be与NaOH溶液反应生成Na2BeO2和H2,请写出Be(OH)2与NaOH溶液反应的离子方程式

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】随着石油资源的日趋紧张,天然气资源的开发利用受到越来越多的关注。以天然气(主要成分是 )为原料经合成气(主要成分为
)为原料经合成气(主要成分为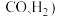 制化学品,是目前天然气转化利用的主要技术路线。而采用渣油、煤、焦炭为原料制合成气,常因含羰基铁
制化学品,是目前天然气转化利用的主要技术路线。而采用渣油、煤、焦炭为原料制合成气,常因含羰基铁 等而导致以合成气为原料合成甲醇和合成氨等生产过程中的催化剂产生中毒。请回答下列问题:
等而导致以合成气为原料合成甲醇和合成氨等生产过程中的催化剂产生中毒。请回答下列问题:
(1) 中铁的化合价为0,写出铁原子的基态电子排布式:
中铁的化合价为0,写出铁原子的基态电子排布式:_______ 。
(2)与 互为等电子体的分子和离子分别为
互为等电子体的分子和离子分别为_____ 和_______ (各举一种即可,填化学式), 分子的电子式为
分子的电子式为_______ , 分子的结构式可表示成
分子的结构式可表示成_______ 。
(3)在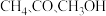 中,碳原子采取
中,碳原子采取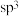 杂化的分子有
杂化的分子有_______ 。
(4) 分子中,
分子中,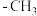 中的碳原子采用杂化
中的碳原子采用杂化_______ 方式,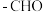 中的碳原子采取杂化方式
中的碳原子采取杂化方式_______ 。
 )为原料经合成气(主要成分为
)为原料经合成气(主要成分为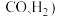 制化学品,是目前天然气转化利用的主要技术路线。而采用渣油、煤、焦炭为原料制合成气,常因含羰基铁
制化学品,是目前天然气转化利用的主要技术路线。而采用渣油、煤、焦炭为原料制合成气,常因含羰基铁 等而导致以合成气为原料合成甲醇和合成氨等生产过程中的催化剂产生中毒。请回答下列问题:
等而导致以合成气为原料合成甲醇和合成氨等生产过程中的催化剂产生中毒。请回答下列问题:(1)
 中铁的化合价为0,写出铁原子的基态电子排布式:
中铁的化合价为0,写出铁原子的基态电子排布式:(2)与
 互为等电子体的分子和离子分别为
互为等电子体的分子和离子分别为 分子的电子式为
分子的电子式为 分子的结构式可表示成
分子的结构式可表示成(3)在
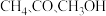 中,碳原子采取
中,碳原子采取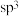 杂化的分子有
杂化的分子有(4)
 分子中,
分子中,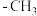 中的碳原子采用杂化
中的碳原子采用杂化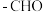 中的碳原子采取杂化方式
中的碳原子采取杂化方式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)N的核外电子排布式为____ ,Cu的外围电子排布式为 _____ ,CO2的其中一种等电子体的化学式或符号是____ ,[Co(NH3)4 Cl2] Cl中,中心原子的配位数是__________ 。
(2)SO3 2-离子中,孤对电子数是____ ,价层电子对数是 ____ ,VSEPR构型是 _____ ,立体构型是_____ ,S采取的杂化方式是_____ 。
(3)乙炔与氢氰酸反应可得丙烯腈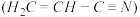 。丙烯腈分子中碳原子轨道杂化类型是
。丙烯腈分子中碳原子轨道杂化类型是______ 、_____ ;分子中处于同一平面上的原子数目最多为_________ 。
(4)丙烯(CH3—CH =CH2)分子中,官能团上的碳原子采取的是____ 杂化方式,分子中有____ 个s-sp3 键,
键,____ 个sp2 -sp3 键和
键和___ 个p-p 键。
键。
(2)SO3 2-离子中,孤对电子数是
(3)乙炔与氢氰酸反应可得丙烯腈
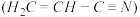 。丙烯腈分子中碳原子轨道杂化类型是
。丙烯腈分子中碳原子轨道杂化类型是(4)丙烯(CH3—CH =CH2)分子中,官能团上的碳原子采取的是
 键,
键, 键和
键和 键。
键。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子为三维完全对称结构,其立体几何构型称为__ ;也可以得到偏钒酸钠(除了水外,无其他产物),其阴离子呈如图所示的无限链状结构,钒原子位于四面体的体心,氧原子位于四面体的顶点,偏钒酸钠的化学式为__ 。


您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】联氨( )又称肼,在航天、能源等领域具有广泛应用。分子模型如图所示,
)又称肼,在航天、能源等领域具有广泛应用。分子模型如图所示, 分子中所有原子均达到稀有气体原子的稳定结构。实验室利用
分子中所有原子均达到稀有气体原子的稳定结构。实验室利用 在一定条件下合成
在一定条件下合成 。
。
②原子总数相同,价电子总数相同的分子具有相似的化学键特征和立体结构。
(1)氮的最高价氧化物对应水化物的酸性比磷酸的酸性___________ 。(填“强”或者“弱”)
(2) 的空间构型为
的空间构型为___________ ,键角___________ 。
(3)写出 的电子式
的电子式___________ 。
(4) 受热分解过程中断裂的化学键属于___________。
受热分解过程中断裂的化学键属于___________。
(5)写出 的电子式
的电子式___________ 。
(6)由 可知
可知 是
是___________ 。
A.酸 B.碱
(7)选择足量的盐酸或NaOH溶液与 充分反应,生成盐的化学式为
充分反应,生成盐的化学式为___________ 。
(8)发射卫星时可用 为燃料,
为燃料, 为助燃剂,这两种物质反应放出大量能量,生成无毒无害的物质。此过程中氧化剂与还原剂的物质的量之比为
为助燃剂,这两种物质反应放出大量能量,生成无毒无害的物质。此过程中氧化剂与还原剂的物质的量之比为___________ 。
(9)在催化剂作用下,肼蒸气受热可分解生成 和一种能使湿润红色石蕊试纸变蓝的气体。写出该反应的化学方程式:
和一种能使湿润红色石蕊试纸变蓝的气体。写出该反应的化学方程式:___________ 。
 )又称肼,在航天、能源等领域具有广泛应用。分子模型如图所示,
)又称肼,在航天、能源等领域具有广泛应用。分子模型如图所示, 分子中所有原子均达到稀有气体原子的稳定结构。实验室利用
分子中所有原子均达到稀有气体原子的稳定结构。实验室利用 在一定条件下合成
在一定条件下合成 。
。
②原子总数相同,价电子总数相同的分子具有相似的化学键特征和立体结构。
(1)氮的最高价氧化物对应水化物的酸性比磷酸的酸性
(2)
 的空间构型为
的空间构型为(3)写出
 的电子式
的电子式(4)
 受热分解过程中断裂的化学键属于___________。
受热分解过程中断裂的化学键属于___________。| A.范德华力 | B.极性共价键 | C.非极性共价键 | D.氢键 |
(5)写出
 的电子式
的电子式(6)由
 可知
可知 是
是A.酸 B.碱
(7)选择足量的盐酸或NaOH溶液与
 充分反应,生成盐的化学式为
充分反应,生成盐的化学式为(8)发射卫星时可用
 为燃料,
为燃料, 为助燃剂,这两种物质反应放出大量能量,生成无毒无害的物质。此过程中氧化剂与还原剂的物质的量之比为
为助燃剂,这两种物质反应放出大量能量,生成无毒无害的物质。此过程中氧化剂与还原剂的物质的量之比为(9)在催化剂作用下,肼蒸气受热可分解生成
 和一种能使湿润红色石蕊试纸变蓝的气体。写出该反应的化学方程式:
和一种能使湿润红色石蕊试纸变蓝的气体。写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】第IIIA族的元素由于最外能层的p能级中有空轨道,故称为缺电子元素。
(1)已知气态氯化铝的化学式为Al2Cl6,写出Al2Cl6的结构式____________________ ;
(2)硼酸的结构式可表示为 ,但硼酸溶于水后,1个硼酸分子与水作用,只能产生1个H+,请写出硼酸溶于水后溶液显酸性的离子方程式:
,但硼酸溶于水后,1个硼酸分子与水作用,只能产生1个H+,请写出硼酸溶于水后溶液显酸性的离子方程式:________________________
(1)已知气态氯化铝的化学式为Al2Cl6,写出Al2Cl6的结构式
(2)硼酸的结构式可表示为
 ,但硼酸溶于水后,1个硼酸分子与水作用,只能产生1个H+,请写出硼酸溶于水后溶液显酸性的离子方程式:
,但硼酸溶于水后,1个硼酸分子与水作用,只能产生1个H+,请写出硼酸溶于水后溶液显酸性的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】卤素互化物、拟卤素与卤素单质的结构,性质相似。常见的卤素互化物有ICl、IBr等,拟卤素有(CN)2、(SCN)2等。
(1)卤族元素位于元素周期表的_______ 。
(2)79Br和81Br这两种核素的中子数之差的绝对值为_______ 。
(3)①Cl2;②ICl;③IBr三种物质熔点由高到低的顺序为_______ 。
(4)①已知CN-与N2结构相似,CN-的电子式为______ 。
②推算HCN分子中σ键与π键数目之比为_______ 。
③关于氨基氰(N≡C-NH2)分子的说法中正确的是_______ 。
A.C原子采用sp3杂化
B.N原子的杂化形式有sp与sp3杂化
C.C≡N键的键长大于C-N键
D.所有原子满足8电子稳定结构
开采的金矿可用氰化法提取,步骤如下:
i.将金矿砂溶于pH为10.5~11的KCN溶液,并鼓入空气,过滤除去矿渣,得含K[Au(CN)2]的滤液;
ii.向滤液中加入足量金属锌,得单质金。Zn+2K[Au(CN)2]=2Au+K2[Zn(CN)4]
(5)K[Au(CN)2]中Au+的配体为______ 。
(6)K2[Zn(CN)4]中Au+的配位数为______ 。
(7)i中反应的离子方程式为:_______ 。
 Au+
Au+ CN-+
CN-+ _______+
_______+ _______=
_______= [Au(CN)2]-+
[Au(CN)2]-+ _______
_______
(8)已知Ka(HCN)=4.0×10-10。i中,pH<10.5会导致相同时间内Au的浸取率下降,原因_______ 。
(1)卤族元素位于元素周期表的
| A.s区 | B.p区 | C.d区 | D.f区 |
(3)①Cl2;②ICl;③IBr三种物质熔点由高到低的顺序为
| A.①>②>③ | B.③>②>① | C.②>①>③ | D.③>①>② |
②推算HCN分子中σ键与π键数目之比为
③关于氨基氰(N≡C-NH2)分子的说法中正确的是
A.C原子采用sp3杂化
B.N原子的杂化形式有sp与sp3杂化
C.C≡N键的键长大于C-N键
D.所有原子满足8电子稳定结构
开采的金矿可用氰化法提取,步骤如下:
i.将金矿砂溶于pH为10.5~11的KCN溶液,并鼓入空气,过滤除去矿渣,得含K[Au(CN)2]的滤液;
ii.向滤液中加入足量金属锌,得单质金。Zn+2K[Au(CN)2]=2Au+K2[Zn(CN)4]
(5)K[Au(CN)2]中Au+的配体为
(6)K2[Zn(CN)4]中Au+的配位数为
(7)i中反应的离子方程式为:
 Au+
Au+ CN-+
CN-+ _______+
_______+ _______=
_______= [Au(CN)2]-+
[Au(CN)2]-+ _______
_______(8)已知Ka(HCN)=4.0×10-10。i中,pH<10.5会导致相同时间内Au的浸取率下降,原因
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】联氨(N2H4)可以用于处理高压锅炉水中的氧,防止锅炉被腐蚀,其中一种可能的反应机理如图所示。回答下列问题:
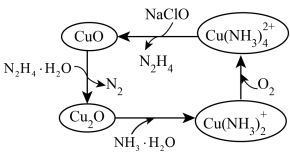
(1)1 mol N2H4·H2O含σ键的数目为______ 。
(2)Cu2O与NH3·H2O反应能形成较稳定的 的原因是
的原因是____ 。
(3)N2H4与O2的相对分子质量相近,但N2H4的熔点(2℃),沸点(114℃)分别远远高于O2的熔点(218℃),沸点(183℃),原因是____ 。
(4)NaClO发生水解可生成HClO,HClO的空间构型是___ ,中心原子的杂化类型是___ 。

(1)1 mol N2H4·H2O含σ键的数目为
(2)Cu2O与NH3·H2O反应能形成较稳定的
 的原因是
的原因是(3)N2H4与O2的相对分子质量相近,但N2H4的熔点(2℃),沸点(114℃)分别远远高于O2的熔点(218℃),沸点(183℃),原因是
(4)NaClO发生水解可生成HClO,HClO的空间构型是
您最近一年使用:0次



