下表为元素周期表的一部分,其中的编号代表对应的元素
(1)g元素位于元素周期表的位置___________ ,基态 的电子排布式为
的电子排布式为___________ ,占据___________ 个原子轨道。
(2)表中属于 区的元素是
区的元素是___________ (填元素名称),其形成的常见阳离子中化学性质较稳定的___________ (填离子符号)。
(3)某种离子化合物由a、d两元素形成,猜测其电子式为___________ 。
(4)与 同周期的所有元素的基态原子中未成对电子数最多的是
同周期的所有元素的基态原子中未成对电子数最多的是___________ (填元素符号),价电子数与族系数不同的过渡元素有___________ 种。
(5) 是第五周期的稀有气体元素,与
是第五周期的稀有气体元素,与 形成的
形成的 室温下易升华。下列对
室温下易升华。下列对 中心原子杂化方式推断合理的是___________(填标号)。
中心原子杂化方式推断合理的是___________(填标号)。
(6)原子中运动的电子有两种相反的自旋状态,若有一种自旋状态用 ,则与之相反的用
,则与之相反的用 ,称为电子的自旋磁量子数,基态
,称为电子的自旋磁量子数,基态 原子核外电子自旋磁量子数的代数和为
原子核外电子自旋磁量子数的代数和为___________ 。

(1)g元素位于元素周期表的位置
 的电子排布式为
的电子排布式为(2)表中属于
 区的元素是
区的元素是(3)某种离子化合物由a、d两元素形成,猜测其电子式为
(4)与
 同周期的所有元素的基态原子中未成对电子数最多的是
同周期的所有元素的基态原子中未成对电子数最多的是(5)
 是第五周期的稀有气体元素,与
是第五周期的稀有气体元素,与 形成的
形成的 室温下易升华。下列对
室温下易升华。下列对 中心原子杂化方式推断合理的是___________(填标号)。
中心原子杂化方式推断合理的是___________(填标号)。A. | B. | C. | D. |
(6)原子中运动的电子有两种相反的自旋状态,若有一种自旋状态用
 ,则与之相反的用
,则与之相反的用 ,称为电子的自旋磁量子数,基态
,称为电子的自旋磁量子数,基态 原子核外电子自旋磁量子数的代数和为
原子核外电子自旋磁量子数的代数和为
更新时间:2024-05-09 14:27:10
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表为周期表的一部分。
请按要求回答下列问题:
(1)①~⑨九种元素中非金属性最强的是______ (填元素符号)。
(2)元素⑧在元素周期表中的位置为______________ ;由①、④、⑥三种元素组成的化合物,其电子式是__________ 。
(3)元素③、⑨的最高价氧化物对应的水化物的酸性较强的是____ (填化学式)。
(4)③、④、⑧三种元素的原子半径由大到小的顺序是____ (填元素符号)。
(5)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式是__________
① | |||||||
② | ③ | ④ | ⑤ | ||||
⑥ | ⑦ | ⑧ | ⑨ | ||||
(1)①~⑨九种元素中非金属性最强的是
(2)元素⑧在元素周期表中的位置为
(3)元素③、⑨的最高价氧化物对应的水化物的酸性较强的是
(4)③、④、⑧三种元素的原子半径由大到小的顺序是
(5)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】短周期元素A、B、D、E、G、J在周期表中的位置如下:
根据上表回答问题:
(1)D在周期表中的位置是_________ 。
(2)A、B、E、G的原子半径由大到小的顺序是_________ (填元素符号)。
(3)B的最高价氧化物的电子式为_________ 。
(4)用电子式表示A与J形成化合物的过程:_________ 。
(5)上述六种元素中的二种元素组成的物质中,含有极性键和非极性键的共价化合物是_________ (写结构式),含有非极性键的离子化合物是_________ (写电子式)。
(6)E与G的最高价氧化物对应水化物发生反应的离子方程式分别为:_________ 。
(7)下图模型表示a、b、c、d四种分子中:
a. b.
b. c.
c.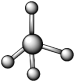 d.
d.
则a是_________ 、b是_________ 、c是_________ 、d是_________ (写分子式)。
| A | |||||||
| B | D | ||||||
| E | G | J | |||||
(1)D在周期表中的位置是
(2)A、B、E、G的原子半径由大到小的顺序是
(3)B的最高价氧化物的电子式为
(4)用电子式表示A与J形成化合物的过程:
(5)上述六种元素中的二种元素组成的物质中,含有极性键和非极性键的共价化合物是
(6)E与G的最高价氧化物对应水化物发生反应的离子方程式分别为:
(7)下图模型表示a、b、c、d四种分子中:
a.
 b.
b. c.
c. d.
d.
则a是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是__________ ,只有负价而无正价的是__________ , 可用于制半导体材料的元素是_______ 。
(2)最高价氧化物的水化物碱性最强的是__________ ,酸性最强的是_____ ,呈两性的是__________ ;
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的__________ ;
(4)在B、C、D、J、 E、F、G、H中,原子半径最大的是__________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | J | F | H | I |
(2)最高价氧化物的水化物碱性最强的是
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的
(4)在B、C、D、J、 E、F、G、H中,原子半径最大的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化钪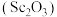 可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。以钛白工业废酸(含
可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。以钛白工业废酸(含 、
、 等离子)为原料制备氧化钪
等离子)为原料制备氧化钪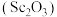 的一种流程如下图。
的一种流程如下图。
(1)基态钪原子的价层电子排布式为___________ 。
(2)“萃取”时,钛白工业废酸中加入 可降低钛的萃取率,可能是生成了难萃取的
可降低钛的萃取率,可能是生成了难萃取的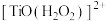 ,其中
,其中 的作用是
的作用是___________ (填标号)。
A.作氧化剂 B.作还原剂 C.提供配体
(3)“洗涤”时,洗涤剂是用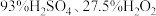 和
和 三种试剂按一定比例混合而成。实验室中混合三种试剂的操作是:将A试剂沿烧杯内壁缓慢注入B试剂中,并用玻璃棒不断搅拌,冷却后再将所得混合液缓慢注入C试剂中,并不断搅拌,则A、C分别对应上述试剂中的
三种试剂按一定比例混合而成。实验室中混合三种试剂的操作是:将A试剂沿烧杯内壁缓慢注入B试剂中,并用玻璃棒不断搅拌,冷却后再将所得混合液缓慢注入C试剂中,并不断搅拌,则A、C分别对应上述试剂中的___________ 、___________ 。
(4)萃取剂萃取 的原理为
的原理为 (
(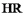 代表萃取剂)。在“反萃取”中,加入
代表萃取剂)。在“反萃取”中,加入 溶液后生成
溶液后生成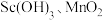 等物质,其中生成含
等物质,其中生成含 化合物的化学方程式为
化合物的化学方程式为___________ 。 时,经“反萃取”后所得滤液的
时,经“反萃取”后所得滤液的 ,则残留的
,则残留的 浓度为
浓度为___________  (已知:
(已知: 时,
时, 。
。
(5)“沉钪”时用到草酸。已知草酸的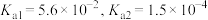 ,则在
,则在 时,
时, 的草酸溶液中
的草酸溶液中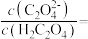
___________ 。
(6)在空气中焙烧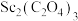 的化学方程式为
的化学方程式为___________ 。
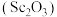 可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。以钛白工业废酸(含
可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。以钛白工业废酸(含 、
、 等离子)为原料制备氧化钪
等离子)为原料制备氧化钪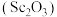 的一种流程如下图。
的一种流程如下图。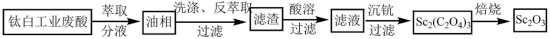
(1)基态钪原子的价层电子排布式为
(2)“萃取”时,钛白工业废酸中加入
 可降低钛的萃取率,可能是生成了难萃取的
可降低钛的萃取率,可能是生成了难萃取的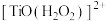 ,其中
,其中 的作用是
的作用是A.作氧化剂 B.作还原剂 C.提供配体
(3)“洗涤”时,洗涤剂是用
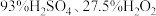 和
和 三种试剂按一定比例混合而成。实验室中混合三种试剂的操作是:将A试剂沿烧杯内壁缓慢注入B试剂中,并用玻璃棒不断搅拌,冷却后再将所得混合液缓慢注入C试剂中,并不断搅拌,则A、C分别对应上述试剂中的
三种试剂按一定比例混合而成。实验室中混合三种试剂的操作是:将A试剂沿烧杯内壁缓慢注入B试剂中,并用玻璃棒不断搅拌,冷却后再将所得混合液缓慢注入C试剂中,并不断搅拌,则A、C分别对应上述试剂中的(4)萃取剂萃取
 的原理为
的原理为 (
(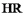 代表萃取剂)。在“反萃取”中,加入
代表萃取剂)。在“反萃取”中,加入 溶液后生成
溶液后生成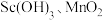 等物质,其中生成含
等物质,其中生成含 化合物的化学方程式为
化合物的化学方程式为 时,经“反萃取”后所得滤液的
时,经“反萃取”后所得滤液的 ,则残留的
,则残留的 浓度为
浓度为 (已知:
(已知: 时,
时, 。
。(5)“沉钪”时用到草酸。已知草酸的
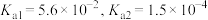 ,则在
,则在 时,
时, 的草酸溶液中
的草酸溶液中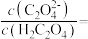
(6)在空气中焙烧
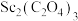 的化学方程式为
的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】元素周期表中第四周期中的某些元素在生产、生活中有着广泛的应用。
(1)基态铬原子的价电子排布式为___________ 。
(2)Cr与K位于同一周期且最外层电子数相同,两种元素原子第一电离能的大小关系为K___________ Cr(填“>”或“<”)。
(3)实验室常用KSCN溶液检验Fe3+的存在,KSCN中非金属元素的电负性由小到大的顺序为___________ (用元素符号表示),SCN−的几何构型为___________ ,中心原子的杂化类型为___________ 。
(4)GaN、GaP、GaAs的熔点如下表,它们的晶体类型与硅类似,都是良好的半导体材料。解释它们熔点变化的原因___________ 。
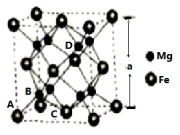
(5)某铁镁合金的晶胞如图所示,镁原子的配位数为___________ ,晶胞有两种基本要素:一种是原子坐标参数,表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0,0,0),B为( ,
, ,
, ),C为(
),C为( ,
, ,0),则D点坐标参数为
,0),则D点坐标参数为___________ ;另外一种是晶胞参数,已知铁镁合金的晶胞参数为a pm,则铁镁之间的最短距离为___________ ,该合金的密度为___________ g·cm-3(只列出计算式即可)。
(1)基态铬原子的价电子排布式为
(2)Cr与K位于同一周期且最外层电子数相同,两种元素原子第一电离能的大小关系为K
(3)实验室常用KSCN溶液检验Fe3+的存在,KSCN中非金属元素的电负性由小到大的顺序为
(4)GaN、GaP、GaAs的熔点如下表,它们的晶体类型与硅类似,都是良好的半导体材料。解释它们熔点变化的原因
| 晶体 | GaN | GaP | GaAs |
| 熔点/℃ | 1700 | 1480 | 1238 |
(5)某铁镁合金的晶胞如图所示,镁原子的配位数为
 ,
, ,
, ),C为(
),C为( ,
, ,0),则D点坐标参数为
,0),则D点坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】运用物质结构与性质的相关知识,回答下列问题:
(1) 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是___________ 。基态 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有___________ 个伸展方向,原子轨道呈___________ 形。
(2) 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为___________ , 价电子轨道表示式为
价电子轨道表示式为___________ 。
(3)GaAs的晶胞结构如图所示。___________ 。
(1)
 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有(2)
 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为 价电子轨道表示式为
价电子轨道表示式为(3)GaAs的晶胞结构如图所示。

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】以Cu2O、ZnO等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:
(1)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是_______ 。
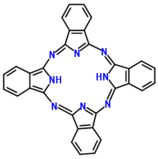
(2)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价值。酞菁分子结构如下图,分子中所有原子共平面,所有N原子的杂化轨道类型相同,均采取_______ 杂化。邻苯二甲酸酐( )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺(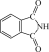 )都是合成酞菁的原料,后者熔点高于前者,主要原因是
)都是合成酞菁的原料,后者熔点高于前者,主要原因是_______ 。
(3)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为_______ 。
(4)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小于Zn-O键,原因是_______ 。
(5)下图为某ZnO晶胞示意图,下图是若干晶胞无隙并置而成的底面O原子排列局部平面图。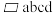 为所取晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母表示出与所取晶胞相邻的两个晶胞的底面
为所取晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母表示出与所取晶胞相邻的两个晶胞的底面_______ 、_______ 。

(1)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是
(2)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价值。酞菁分子结构如下图,分子中所有原子共平面,所有N原子的杂化轨道类型相同,均采取
 )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺( )都是合成酞菁的原料,后者熔点高于前者,主要原因是
)都是合成酞菁的原料,后者熔点高于前者,主要原因是
(3)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为
(4)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小于Zn-O键,原因是
(5)下图为某ZnO晶胞示意图,下图是若干晶胞无隙并置而成的底面O原子排列局部平面图。
 为所取晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母表示出与所取晶胞相邻的两个晶胞的底面
为所取晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母表示出与所取晶胞相邻的两个晶胞的底面
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】卤素单质及其化合物在科研和工农业生产中有着广泛的应用。请回答:
(1) 和
和 中心原子的杂化方式分别为
中心原子的杂化方式分别为________ 和_______ 。第一电离能介于B、N之间的第二周期元素有______ 种。
(2)卤化物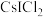 受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为
受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为____ (写化学式)。解释X的熔点比Y高的原因_____ 。
(3)一种铜的溴化物立方晶胞如图所示。

该化合物的化学式为______ ,在晶体中与Cu距离最近且相等的Cu有___ 个,若该晶体密度为
 ,化合物式量为M,则该晶体中Cu原子与Br原子的最小核间距为
,化合物式量为M,则该晶体中Cu原子与Br原子的最小核间距为______ pm(写出表达式,阿伏加德罗常数为 )。
)。
(1)
 和
和 中心原子的杂化方式分别为
中心原子的杂化方式分别为(2)卤化物
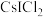 受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为
受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为(3)一种铜的溴化物立方晶胞如图所示。

该化合物的化学式为

 ,化合物式量为M,则该晶体中Cu原子与Br原子的最小核间距为
,化合物式量为M,则该晶体中Cu原子与Br原子的最小核间距为 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铂钴合金是以铂为基含钴二元合金,在高温下,铂与钴可无限互溶,其固溶体为面心立方晶格。铂钴合金磁性极强,磁稳定性较高,耐化学腐蚀性很好,主要用于航天航空仪表、电子钟表、磁控管等。
(1)基态钴原子的价电子排布图为___________ 。
(2)二氯二吡啶合铂是由Pt2+、Cl-和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体 如图
如图 。科学研究表明,顺式分子具有抗癌活性。
。科学研究表明,顺式分子具有抗癌活性。

①吡啶分子是大体积平面配体,结构简式如图所示。吡啶分子中N原子的杂化方式是____ ,分子中的大π键可用符号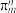 表示,其中m表示参与形成大π键的原子个数,n表示参与形成大π键的电子个数。则吡啶中的大π键应表示为
表示,其中m表示参与形成大π键的原子个数,n表示参与形成大π键的电子个数。则吡啶中的大π键应表示为_____ 。

②二氯二吡啶合铂分子中所含的C、N、Cl三种元素的第一电离能由大到小的顺序是_____ 。
③二氯二吡啶合铂分子中存在的微粒间作用力有_________  填字母
填字母 。
。
 离子键
离子键  配位键
配位键  金属键
金属键  非极性键
非极性键  氢键
氢键  极性键
极性键
④反式二氯二吡啶合铂分子是_________  填“极性分子”或“非极性分子”
填“极性分子”或“非极性分子” 。
。
⑤二氯二吡啶合铂分子是平面结构,Pt2+的配位数是4,但是其轨道杂化方式并不是sp3,简述理由______________ 。
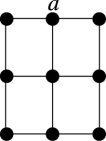
(3)筑波材料科学国家实验室一个科研小组发现了在5K下呈现超导性的晶体CoO2,该晶体具有层状结构 如图所示,小球表示Co原子,大球表示O原子
如图所示,小球表示Co原子,大球表示O原子 。图中用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是
。图中用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是__________  填字母
填字母 。
。

(4)金属铂晶体中,铂原子的配位数为12,其立方晶胞沿x、y或z轴的投影图如图所示。若金属铂的密度为d g∙cm-3,则晶胞参数a=_________ nm(列计算式)。
(1)基态钴原子的价电子排布图为
(2)二氯二吡啶合铂是由Pt2+、Cl-和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体
 如图
如图 。科学研究表明,顺式分子具有抗癌活性。
。科学研究表明,顺式分子具有抗癌活性。
①吡啶分子是大体积平面配体,结构简式如图所示。吡啶分子中N原子的杂化方式是
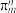 表示,其中m表示参与形成大π键的原子个数,n表示参与形成大π键的电子个数。则吡啶中的大π键应表示为
表示,其中m表示参与形成大π键的原子个数,n表示参与形成大π键的电子个数。则吡啶中的大π键应表示为
②二氯二吡啶合铂分子中所含的C、N、Cl三种元素的第一电离能由大到小的顺序是
③二氯二吡啶合铂分子中存在的微粒间作用力有
 填字母
填字母 。
。 离子键
离子键  配位键
配位键  金属键
金属键  非极性键
非极性键  氢键
氢键  极性键
极性键④反式二氯二吡啶合铂分子是
 填“极性分子”或“非极性分子”
填“极性分子”或“非极性分子” 。
。⑤二氯二吡啶合铂分子是平面结构,Pt2+的配位数是4,但是其轨道杂化方式并不是sp3,简述理由
(3)筑波材料科学国家实验室一个科研小组发现了在5K下呈现超导性的晶体CoO2,该晶体具有层状结构
 如图所示,小球表示Co原子,大球表示O原子
如图所示,小球表示Co原子,大球表示O原子 。图中用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是
。图中用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是 填字母
填字母 。
。
(4)金属铂晶体中,铂原子的配位数为12,其立方晶胞沿x、y或z轴的投影图如图所示。若金属铂的密度为d g∙cm-3,则晶胞参数a=

您最近一年使用:0次



