回答下列问题。
(1)白磷(P4)在氯气中燃烧可生成 PCl3 和 PCl5。
①形成 PCl5时,P 原子的一个 3s 电子激发入 3d 轨道后参与成键,该激发态的价电子排布式为___________ 。
②研究表明,在加压条件下 PCl5 于 148℃液化时能发生与水类似的自偶电离,形成一种能导电的熔体,其电离方程式为___________ ,产生的阳离子的空间结构形状为___________ 。
(2)分子中的大π键可用符号 表示,其中 m 代表参与形成大π键的原子数,n 代表参与形成大键的电子数(如苯分子中的大π键可表示为
表示,其中 m 代表参与形成大π键的原子数,n 代表参与形成大键的电子数(如苯分子中的大π键可表示为 )。一种观点认为,苯酚羟基中的 O 原子是 sp2 杂化则苯酚中的大π键可表示为
)。一种观点认为,苯酚羟基中的 O 原子是 sp2 杂化则苯酚中的大π键可表示为___________ ,一定在同一平面上的原子有___________ 个。乙醇显中性而苯酚显酸性的原因是:___________ 。
(3)硫化锌精矿是冶炼金属锌的主要原料,六方硫化锌(纤锌矿型)的平行六面体晶胞如图 2 所示,晶体中正负离子的配位数之比为___________ 。___________ g•cm-3。
(1)白磷(P4)在氯气中燃烧可生成 PCl3 和 PCl5。
①形成 PCl5时,P 原子的一个 3s 电子激发入 3d 轨道后参与成键,该激发态的价电子排布式为
②研究表明,在加压条件下 PCl5 于 148℃液化时能发生与水类似的自偶电离,形成一种能导电的熔体,其电离方程式为
(2)分子中的大π键可用符号
 表示,其中 m 代表参与形成大π键的原子数,n 代表参与形成大键的电子数(如苯分子中的大π键可表示为
表示,其中 m 代表参与形成大π键的原子数,n 代表参与形成大键的电子数(如苯分子中的大π键可表示为 )。一种观点认为,苯酚羟基中的 O 原子是 sp2 杂化则苯酚中的大π键可表示为
)。一种观点认为,苯酚羟基中的 O 原子是 sp2 杂化则苯酚中的大π键可表示为(3)硫化锌精矿是冶炼金属锌的主要原料,六方硫化锌(纤锌矿型)的平行六面体晶胞如图 2 所示,晶体中正负离子的配位数之比为


更新时间:2024-05-16 16:33:18
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】以CO2为原料催化加氢可以制备CH4、CH3OH、C2H4, 为我国科学家发明的二氧化碳加氢的一种催化剂。回答下列问题:
为我国科学家发明的二氧化碳加氢的一种催化剂。回答下列问题:
(1)基态 原子电子排布式为
原子电子排布式为___________ ,其核外不同能量状态的电子有___________ 种。
(2)CO 中的大
中的大 键可表示为
键可表示为___________ ,同一周期第一电离能大趋势在逐渐增大,但是存在反常,比如 ,请解释原因:
,请解释原因:___________ 。
(3) 催化加氢制备
催化加氢制备 的化学方程式为CO2+3H2=CH3OH+H2O。
的化学方程式为CO2+3H2=CH3OH+H2O。
①等物质的量的CH3OH和CO2分子中 键数目之比为
键数目之比为___________ 。
②沸点:CH3OH___________ (填“>”或“<”)CH4,其原因为___________ 。
(4)四方体 晶胞结构如图所示,原子坐标参数表示晶胞内部各原子的相对位置,
晶胞结构如图所示,原子坐标参数表示晶胞内部各原子的相对位置, 、
、 、
、 原子的坐标参数分别为(0,0,0)、(
原子的坐标参数分别为(0,0,0)、( ,0,
,0, )、(
)、( ,
, ,
, )。
)。___________ ,配位数为___________ 。
②假设ZrO2的密度为 ,摩尔质量为
,摩尔质量为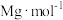 ,
, 表示阿伏加德罗常数的值,则晶胞中Zr和O原子的最短距离为
表示阿伏加德罗常数的值,则晶胞中Zr和O原子的最短距离为___________  (列出算式即可)。
(列出算式即可)。
③将该晶体沿体对角线的方向投影如下图所示,请将O2-涂黑___________ 。
 为我国科学家发明的二氧化碳加氢的一种催化剂。回答下列问题:
为我国科学家发明的二氧化碳加氢的一种催化剂。回答下列问题:(1)基态
 原子电子排布式为
原子电子排布式为(2)CO
 中的大
中的大 键可表示为
键可表示为 ,请解释原因:
,请解释原因:(3)
 催化加氢制备
催化加氢制备 的化学方程式为CO2+3H2=CH3OH+H2O。
的化学方程式为CO2+3H2=CH3OH+H2O。①等物质的量的CH3OH和CO2分子中
 键数目之比为
键数目之比为②沸点:CH3OH
(4)四方体
 晶胞结构如图所示,原子坐标参数表示晶胞内部各原子的相对位置,
晶胞结构如图所示,原子坐标参数表示晶胞内部各原子的相对位置, 、
、 、
、 原子的坐标参数分别为(0,0,0)、(
原子的坐标参数分别为(0,0,0)、( ,0,
,0, )、(
)、( ,
, ,
, )。
)。
②假设ZrO2的密度为
 ,摩尔质量为
,摩尔质量为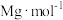 ,
, 表示阿伏加德罗常数的值,则晶胞中Zr和O原子的最短距离为
表示阿伏加德罗常数的值,则晶胞中Zr和O原子的最短距离为 (列出算式即可)。
(列出算式即可)。③将该晶体沿体对角线的方向投影如下图所示,请将O2-涂黑

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】碳和硅均为元素周期表中第Ⅳ A族的元素,其单质和化合物有着重要应用。
(1)石墨烯是只有一个碳原子直径厚度的单层石墨,最早是由科学家用机械剥离的方法从石墨中分离出来,其部分性能优于传统的硅材料,具有广泛的应用前景。
①写出基态碳原子的电子排布式________ 。石墨烯中C的杂化类型为________ 。
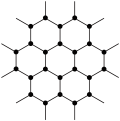
②下图为单层石墨烯的结构示意图。12 g的石墨烯中由C原子连接成的六元环的物质的量约为________ mol。
③石墨烯加氢制得的石墨烷,可用 表示。下列有关叙述正确的是
表示。下列有关叙述正确的是________ 。
a.石墨烷属于烷烃 b.石墨烷难溶于水
c.石墨烷中所有碳原子共平面 d.石墨烷可以发生加成反应
④石墨烯可由加热 晶体脱除
晶体脱除 的方法制得。该过程属于
的方法制得。该过程属于________ 。
a.物理变化 b.分解反应 c.氧化还原反应
(2) 的晶体结构与晶体硅类似。
的晶体结构与晶体硅类似。 的晶体类型为
的晶体类型为________ ,晶体中 原子与
原子与 键的数目之比为
键的数目之比为________ 。
(3) 与
与 空间构型相似,但性质不同:前者不易与水反应,但后者与水剧烈反应,生成两种酸和一种气体,写出该反应的化学方程式:
空间构型相似,但性质不同:前者不易与水反应,但后者与水剧烈反应,生成两种酸和一种气体,写出该反应的化学方程式:__________________________ 。
(1)石墨烯是只有一个碳原子直径厚度的单层石墨,最早是由科学家用机械剥离的方法从石墨中分离出来,其部分性能优于传统的硅材料,具有广泛的应用前景。
①写出基态碳原子的电子排布式
②下图为单层石墨烯的结构示意图。12 g的石墨烯中由C原子连接成的六元环的物质的量约为

③石墨烯加氢制得的石墨烷,可用
 表示。下列有关叙述正确的是
表示。下列有关叙述正确的是a.石墨烷属于烷烃 b.石墨烷难溶于水
c.石墨烷中所有碳原子共平面 d.石墨烷可以发生加成反应
④石墨烯可由加热
 晶体脱除
晶体脱除 的方法制得。该过程属于
的方法制得。该过程属于a.物理变化 b.分解反应 c.氧化还原反应
(2)
 的晶体结构与晶体硅类似。
的晶体结构与晶体硅类似。 的晶体类型为
的晶体类型为 原子与
原子与 键的数目之比为
键的数目之比为(3)
 与
与 空间构型相似,但性质不同:前者不易与水反应,但后者与水剧烈反应,生成两种酸和一种气体,写出该反应的化学方程式:
空间构型相似,但性质不同:前者不易与水反应,但后者与水剧烈反应,生成两种酸和一种气体,写出该反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】元素周期表中的六种元素A、B、C、D、E、F,原子序数依次增大。
(1)写出E的基态原子的电子排布式:______ 。
(2)A、B形成的AB-常作为配位化合物中的配体。在AB-中,元素A的原子采取sp杂化,则A与B形成的化学键中含有的σ键与π的数目之比为______ 。
(3)D与E形成的化合物晶体的晶胞如图所示。在该晶胞中,E离子的数目为______ ;该化合物的化学式为______ 。

(4)在D的氢化物(H2D)中,D原子轨道的杂化类型是______ 。
(5)C的氢化物(H2C)在乙醇中的溶解度大于H2D,其原因是_____ 。
(6)D与C可形成的DC 的空间结构为
的空间结构为______ (用文字描述)。
(7)E、F均能与AB-形成配离子,已知E2+与AB-形成配离子时,配位数为4;F+与AB-形成配离子时,配位数为2。工业上常用F+与AB-形成的配离子与单质E反应,生成E2+与AB-形成的配离子和F单质来提取F,写出上述反应的离子方程式:______ 。
| A的基态原子价层电子排布为nsnnpn; |
| B的基态原子2p能级有3个单电子; |
| C的原子最外层电子数是其内层的3倍; |
| D的基态原子3p轨道上有4个电子; |
| E2+的d轨道中有10个电子; |
| F单质在金属活动性顺序中排在最末位。 |
(2)A、B形成的AB-常作为配位化合物中的配体。在AB-中,元素A的原子采取sp杂化,则A与B形成的化学键中含有的σ键与π的数目之比为
(3)D与E形成的化合物晶体的晶胞如图所示。在该晶胞中,E离子的数目为

(4)在D的氢化物(H2D)中,D原子轨道的杂化类型是
(5)C的氢化物(H2C)在乙醇中的溶解度大于H2D,其原因是
(6)D与C可形成的DC
 的空间结构为
的空间结构为(7)E、F均能与AB-形成配离子,已知E2+与AB-形成配离子时,配位数为4;F+与AB-形成配离子时,配位数为2。工业上常用F+与AB-形成的配离子与单质E反应,生成E2+与AB-形成的配离子和F单质来提取F,写出上述反应的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】硼(B)是一种重要的元素,硼及其化合物在工农业生产、材料、医疗领域都有广泛的用途。回答下列问题:
(1)区分晶体硼和无定形硼最可靠的科学方法为对固体进行_______ ,晶体硼的单质的基本结构单元为正二十面体,能自发呈现多面体外形,这种性质称为晶体的_______ 。
(2)①氨硼烷(NH3BH3)是一种新型储氢材料,其分子中存在配位键,则氨硼烷分子结构式为:_______ (标出配位键)。
②硼氢化钠(NaBH4)是一种重要的储氢载体,其阴离子空间构型是_______ (填名称)。
(3)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构如下图所示。

上图中,B原子填充在N原子的四面体空隙,且占据此类空隙的比例为_______ ,如果该晶胞边长为apm,c原子的坐标参数为(0,0,0),e为( ,
, ,0),f为(
,0),f为( ,0,
,0, ),则d原子的坐标参数为
),则d原子的坐标参数为_______ ,该晶体的密度为 _______ g•cm-3.(设阿伏加德罗常数的值为NA,1pm = 10-10cm)。
(1)区分晶体硼和无定形硼最可靠的科学方法为对固体进行
(2)①氨硼烷(NH3BH3)是一种新型储氢材料,其分子中存在配位键,则氨硼烷分子结构式为:
②硼氢化钠(NaBH4)是一种重要的储氢载体,其阴离子空间构型是
(3)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构如下图所示。

上图中,B原子填充在N原子的四面体空隙,且占据此类空隙的比例为
 ,
, ,0),f为(
,0),f为( ,0,
,0, ),则d原子的坐标参数为
),则d原子的坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】常见的太阳能电池有单晶硅太阳能电池、多晶硅太阳能电池、GaAs太阳能电池及铜铟镓硒薄膜太阳能电池等。
(1)Cu+在基态时的价电子排布式为__________________ 。
(2)砷、硒是第四周期的相邻元素,已知砷的第一电离能大于硒。请从原子结构的角度加以解释___________________________ 。
(3)GaAs熔点1238℃,难溶于溶剂。其晶体类型为_____________ 。
(4)AsF3的空间构型是:______________ 。
(5)硼酸(H3BO3)本身不能电离出H+,在水中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。
①[B(OH)4]-中B原子的杂化类型为________ 。
②[B(OH)4]-的结构式为____________________ 。
(6)金刚石的晶胞如图,若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅:若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。

①金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是_______________________ (用化学式表示)。
②立方氮化硼(BN)晶体的结构与金刚石相似,硬度与金刚石相当,立方氮化硼的密度是ρ g·㎝-3,,则晶胞边长为___________ 。(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
(1)Cu+在基态时的价电子排布式为
(2)砷、硒是第四周期的相邻元素,已知砷的第一电离能大于硒。请从原子结构的角度加以解释
(3)GaAs熔点1238℃,难溶于溶剂。其晶体类型为
(4)AsF3的空间构型是:
(5)硼酸(H3BO3)本身不能电离出H+,在水中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。
①[B(OH)4]-中B原子的杂化类型为
②[B(OH)4]-的结构式为
(6)金刚石的晶胞如图,若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅:若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。

①金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是
②立方氮化硼(BN)晶体的结构与金刚石相似,硬度与金刚石相当,立方氮化硼的密度是ρ g·㎝-3,,则晶胞边长为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】第四周期中某些元素的相关化合物在化工、医药、材料等领域有着广泛应用。
(1)现代化学中,常利用_________ 上的特征谱线来鉴定元素。Ga的外围电子排布式为:_____________________ ,基态Ga原子核外有______ 种运动状态不同的电子。
(2)锗、砷、硒、溴的第一电离能由大到小的顺序为____________ (用元素符号表示);其中锗的化合物四氯化锗可用作光导纤维掺杂剂,其熔点为-49.5℃,沸点为83.1℃,则其晶体类型为_________ ,中心原子的杂化类型为________ ;砷酸的酸性弱于硒酸,从分子结构的角度解释原因_______________________ 。
(3)铁能形成[Fe(Bipy)2C12]ClO4等多种配合物(Bipy结构如下图A)。

①该配合物中中心原子的化合价为________ ;与中心原子形成配位键的原子是________ 。
②与ClO4-互为等电子体的一种非极性分子是_______ (举1例)。
③1 mol Bipy中所含σ键______ mol。
(4)钛(Ti)被誉为“21世纪金属”,Ti晶体的堆积方式是六方最密堆积如图B所示,晶胞可用图C表示。设金属Ti的原子半径为a cm,空间利用率为__________ 。设晶胞中A点原子的坐标为(1,0,0),C点原子的坐标为(0,1,0),D点原子的坐标为(0,0,1),则B点原子的坐标为________________ 。
(1)现代化学中,常利用
(2)锗、砷、硒、溴的第一电离能由大到小的顺序为
(3)铁能形成[Fe(Bipy)2C12]ClO4等多种配合物(Bipy结构如下图A)。

①该配合物中中心原子的化合价为
②与ClO4-互为等电子体的一种非极性分子是
③1 mol Bipy中所含σ键
(4)钛(Ti)被誉为“21世纪金属”,Ti晶体的堆积方式是六方最密堆积如图B所示,晶胞可用图C表示。设金属Ti的原子半径为a cm,空间利用率为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】氮化镓(GaN)具有优异的光电性能。一种利用炼锌矿渣[主要含铁酸镓 、铁酸锌
、铁酸锌 、
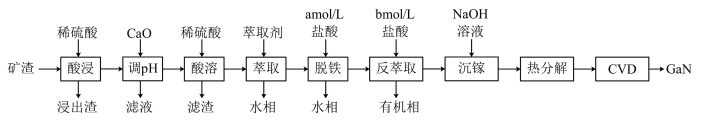
、 ]制备GaN的工艺流程如下:
]制备GaN的工艺流程如下:
已知:
①Ga与Al同主族,化学性质相似。
②常温下,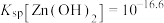 ,
,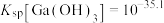 ,
, 。
。
③ 、
、 在该工艺条件下的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系见下表。
在该工艺条件下的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系见下表。
回答下列问题:
(1)“酸浸”时能提高反应速率的措施有___________ (答1条即可),“酸浸”时 发生反应的离子方程式为
发生反应的离子方程式为___________ 。“酸溶”所得滤渣的主要成分是(填化学式)。
(2)“酸浸”所得浸出液中 、
、 浓度分别为
浓度分别为 、
、 。常温下,为尽可能多地提取
。常温下,为尽可能多地提取 并确保不混入
并确保不混入 ,用CaO“调pH”时须不能大于
,用CaO“调pH”时须不能大于___________ (假设调pH时溶液体积不变)。
(3)“脱铁”和“反萃取”时,所用盐酸的浓度a=___________ ,b=___________ (选填上表中盐酸的浓度)。
(4)“沉镓”时,若加入NaOH的量过多,会导致 的沉淀率降低,原因是
的沉淀率降低,原因是___________ (用离子方程式表示)。
(5)利用CVD(化学气相沉积)技术,将热分解得到的 与
与 在高温下反应可制得GaN,同时生成另一种产物,该反应化学方程式为
在高温下反应可制得GaN,同时生成另一种产物,该反应化学方程式为___________ 。
(6)①GaN的熔点为1700℃, 的熔点为77.9℃,推测它们的晶体类型依次为
的熔点为77.9℃,推测它们的晶体类型依次为___________ 、___________ 。
②基态Ga原子的价层电子排布图为___________ 。
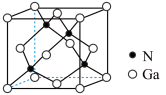
GaN晶体的一种立方晶胞如图所示。该晶胞边长为anm,GaN的式量为Mr,则该晶体密度为___________ g/cm3(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 、铁酸锌
、铁酸锌 、
、 ]制备GaN的工艺流程如下:
]制备GaN的工艺流程如下:
已知:
①Ga与Al同主族,化学性质相似。
②常温下,
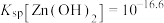 ,
,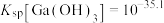 ,
, 。
。③
 、
、 在该工艺条件下的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系见下表。
在该工艺条件下的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系见下表。| 盐酸浓度/mol/L | 反萃取率/% | |
 |  | |
| 2 | 86.9 | 9.4 |
| 4 | 69.1 | 52.1 |
| 6 | 17.5 | 71.3 |
(1)“酸浸”时能提高反应速率的措施有
 发生反应的离子方程式为
发生反应的离子方程式为(2)“酸浸”所得浸出液中
 、
、 浓度分别为
浓度分别为 、
、 。常温下,为尽可能多地提取
。常温下,为尽可能多地提取 并确保不混入
并确保不混入 ,用CaO“调pH”时须不能大于
,用CaO“调pH”时须不能大于(3)“脱铁”和“反萃取”时,所用盐酸的浓度a=
(4)“沉镓”时,若加入NaOH的量过多,会导致
 的沉淀率降低,原因是
的沉淀率降低,原因是(5)利用CVD(化学气相沉积)技术,将热分解得到的
 与
与 在高温下反应可制得GaN,同时生成另一种产物,该反应化学方程式为
在高温下反应可制得GaN,同时生成另一种产物,该反应化学方程式为(6)①GaN的熔点为1700℃,
 的熔点为77.9℃,推测它们的晶体类型依次为
的熔点为77.9℃,推测它们的晶体类型依次为②基态Ga原子的价层电子排布图为

GaN晶体的一种立方晶胞如图所示。该晶胞边长为anm,GaN的式量为Mr,则该晶体密度为
 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】氧族元素是元素周期表中第VIA族元素,包含氧(O)、硫(S)、硒(Se)、碲(Te)、钋(Po)五种元素,它们及其化合物在生产、生活中有着广泛的应用。请回答下列问题:
(1)基态 原子的核外电子排布式为
原子的核外电子排布式为____ 。
(2)H2O、H2S、H2Se、H2Te的沸点由高到低的顺序为____ ,原因是____ 。
(3)SO 与SO
与SO 相比,键角较小的是
相比,键角较小的是___ (填离子符号),原因是____ 。
(4)依布硒是一种有机硒化物,具有良好的抗炎活性,其结构简式为 。依布硒分子中
。依布硒分子中 、C原子的杂化类型分别为
、C原子的杂化类型分别为____ 、____ 。
(5)国家速滑馆又称为“冰丝带”,所用的碲化镉(CdTe)“发电玻璃”被誉为“挂在墙上的油田”。碲化镉立方晶胞结构如图。

①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。已知晶胞中A、B原子的分数坐标分别为A(0,0,0)、B( ,
, ,
, ),则C点原子的分数坐标为
),则C点原子的分数坐标为____ 。
②碲化镉晶体的密度为ρg•cm-3,设NA为阿伏加德罗常数的值,则其晶胞边长为a=____ 。
(1)基态
 原子的核外电子排布式为
原子的核外电子排布式为(2)H2O、H2S、H2Se、H2Te的沸点由高到低的顺序为
(3)SO
 与SO
与SO 相比,键角较小的是
相比,键角较小的是(4)依布硒是一种有机硒化物,具有良好的抗炎活性,其结构简式为
 。依布硒分子中
。依布硒分子中 、C原子的杂化类型分别为
、C原子的杂化类型分别为(5)国家速滑馆又称为“冰丝带”,所用的碲化镉(CdTe)“发电玻璃”被誉为“挂在墙上的油田”。碲化镉立方晶胞结构如图。

①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。已知晶胞中A、B原子的分数坐标分别为A(0,0,0)、B(
 ,
, ,
, ),则C点原子的分数坐标为
),则C点原子的分数坐标为②碲化镉晶体的密度为ρg•cm-3,设NA为阿伏加德罗常数的值,则其晶胞边长为a=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】西北工业大学曾华强课题组借用足球烯核心,成功实现了高效且选择性可精准定制的离子跨膜运输,如图所示。

已知:图甲中的有机物为“冠醚”,命名规则是“环上原子个数-冠醚-氧原子个数”。
请回答下列问题:
(1)基态Cs原子的价层电子的轨道表示式为___________ 。基态K原子的核外电子云有___________ 个伸展方向。
(2)运输Cs+的冠醚名称是___________ 。冠醚分子中氧原子的杂化类型是___________ ,冠醚与碱金属离子之间存在微弱的配位键,配位原子是___________ (填元素符号)。
(3)几种冠醚与识别的碱金属离子的有关数据如下表所示:
18-冠醚-6不能识别和运输Na+和Cs+的原因是___________ 。
(4)碱金属氯化物中NaCl 、KCl、RbCl、 CsCl熔点由高到低顺序为___________ ,理由是___________ 。
(5) 具有反萤石结构,晶胞如图所示。已知晶胞参数为0.4665nm,阿伏加德罗常数的值为
具有反萤石结构,晶胞如图所示。已知晶胞参数为0.4665nm,阿伏加德罗常数的值为 ,则
,则 的密度为
的密度为___________  (列出计算式)。若该立方晶胞中原子A的坐标参数为(0,1,0),则原子B的坐标参数为
(列出计算式)。若该立方晶胞中原子A的坐标参数为(0,1,0),则原子B的坐标参数为___________ 。


已知:图甲中的有机物为“冠醚”,命名规则是“环上原子个数-冠醚-氧原子个数”。
请回答下列问题:
(1)基态Cs原子的价层电子的轨道表示式为
(2)运输Cs+的冠醚名称是
(3)几种冠醚与识别的碱金属离子的有关数据如下表所示:
| 冠醚 | 冠醚空腔直径/pm | 适合的粒子直径/pm |
| 12-冠醚- 4 | 120~ 150 | Li+ (152) |
| 15 -冠醚- 5 | 170~ 220 | Na+ (204) |
| 18 -冠醚- 6 | 260~ 320 | K+ (276) |
| —— | 340~ 430 | Rb+ (304) |
| Cs+ (334) |
(4)碱金属氯化物中NaCl 、KCl、RbCl、 CsCl熔点由高到低顺序为
(5)
 具有反萤石结构,晶胞如图所示。已知晶胞参数为0.4665nm,阿伏加德罗常数的值为
具有反萤石结构,晶胞如图所示。已知晶胞参数为0.4665nm,阿伏加德罗常数的值为 ,则
,则 的密度为
的密度为 (列出计算式)。若该立方晶胞中原子A的坐标参数为(0,1,0),则原子B的坐标参数为
(列出计算式)。若该立方晶胞中原子A的坐标参数为(0,1,0),则原子B的坐标参数为
您最近一年使用:0次



