设 为阿伏加德罗常数的值。钛镍记忆合金用于制造神舟十四号飞船的天线。钛酸亚铁高温(FeTiO3)通过以下反应转化为Ti,用于冶炼钛:
为阿伏加德罗常数的值。钛镍记忆合金用于制造神舟十四号飞船的天线。钛酸亚铁高温(FeTiO3)通过以下反应转化为Ti,用于冶炼钛: 。下列说法错误的是
。下列说法错误的是
 为阿伏加德罗常数的值。钛镍记忆合金用于制造神舟十四号飞船的天线。钛酸亚铁高温(FeTiO3)通过以下反应转化为Ti,用于冶炼钛:
为阿伏加德罗常数的值。钛镍记忆合金用于制造神舟十四号飞船的天线。钛酸亚铁高温(FeTiO3)通过以下反应转化为Ti,用于冶炼钛: 。下列说法错误的是
。下列说法错误的是A.每生成1mol 转移电子数为7 转移电子数为7 | B.1mol基态Ti原子中未成对电子数为2 |
C.1mol 中含5 中含5 配位键 配位键 | D.2L1mol/L的 溶液中,阳离子数目大于2 溶液中,阳离子数目大于2 |
更新时间:2024-05-24 22:07:18
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】研究性学习小组进行了一系列化学实验后,发现高锰酸钾分解后的含锰元素的化合物都能和浓盐酸反应制得氯气,且锰化合物的还原产物也是MnCl2,他们将6.32gKMnO4粉末加热一段时间,也不知道高锰酸钾是否完全分解,收集到0.112L气体后便停止加热了,冷却后放入足量的浓盐酸再加热,又收集到气体体积是(上述气体体积都折合成标准状况)
| A.0.448L | B.2.016L | C.2.240L | D.无法确定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A.在过氧化钠与水的反应中,每生成0.1mol氧气,转移的电子数目为0.4NA |
| B.氢氧燃料电池正极消耗22.4L气体时,电路中通过的电子数目为4NA |
| C.在30g二氧化硅晶体中含有的共价键数目为2NA |
| D.将常温下含NA个NO2、N2O4分子的混合气体冷却至标准状况,其体积约为22.4L(已知2NO2⇌N2O4) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】设NA表示阿伏加 德罗常数的值,下列说法中正确的是( )
①过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA
②5NH4NO3 2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75NA
③2L0.5mol/L亚硫酸溶液中含有的H+为2NA
④3mol单质铁完全转化为Fe3O4,失去8NA个电子
⑤密闭容器中2molNO与1molO2充分反应后,产物的分子数为2NA
⑥将100mL0.1mol/L的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA
①过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA
②5NH4NO3
 2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75NA③2L0.5mol/L亚硫酸溶液中含有的H+为2NA
④3mol单质铁完全转化为Fe3O4,失去8NA个电子
⑤密闭容器中2molNO与1molO2充分反应后,产物的分子数为2NA
⑥将100mL0.1mol/L的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA
| A.①③⑤ | B.④⑤⑥ | C.①②④ | D.①⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】阿伏加德罗常数的值为NA.下列说法不正确的是
| A.标准状况下,将22.4LCl2通入水中,溶液中Cl-、ClO-之和数目为2 NA |
| B.1molO2在反应中作氧化剂时,所得电子数可能为2NA |
| C.常温常压下,3.2g O2与O3的混合物中含有氧原子个数为0.2 NA |
| D.同温同压下,20mL二氧化碳气体和60mL氧气所含原子个数比为1:2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】若用NA表示阿伏加德罗常数的值,下列叙述错误的是
| A.在1 L0.10 mol/L碳酸钠溶液中阴离子总数大于0.1NA |
| B.锌与某浓度的浓硫酸反应,生成SO2和H2的混合气体22.4 L(标准状况),锌失去电子数目为2NA |
| C.0.1 mol Cl2和足量的铁粉反应,转移的电子数目为0.2NA |
| D.1 mol D2O质子数目为12NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】室温下,通过下列实验探究Na2C2O4溶液的性质。下列说法不正确的是
已知:25℃时Ka1(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5。
已知:25℃时Ka1(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5。
| 实验 | 实验操作和现象 |
| 1 | 用pH计测得0.0100mol·L-1Na2C2O4溶液pH为8.60 |
| 2 | 向0.0100mol·L-1Na2C2O4溶液中滴加稀盐酸至溶液pH=7 |
| 3 | 向0.0100mol·L-1Na2C2O4溶液中滴加等浓度、等体积稀盐酸 |
| 4 | 向0.0100mol·L-1Na2C2O4溶液中加入足量稀硫酸酸化后,再滴加KMnO4溶液,溶液紫红色褪去 |
A.实验1溶液中存在:c(OH-)=c(H+)+2c(H2C2O4)+c(HC2O ) ) |
B.实验2溶液中存在:c(Na+)=c((HC2O )+2c(C2O )+2c(C2O ) ) |
C.实验3溶液中存在:c(HC2O )>c(C2O )>c(C2O )>c(H2C2O4) )>c(H2C2O4) |
D.实验4中滴加KMnO4溶液所发生的离子方程式为:5H2C2O4+2MnO +6H+=10CO2↑+2Mn2++8H2O +6H+=10CO2↑+2Mn2++8H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,向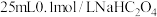 溶液中加入
溶液中加入 固体或通入
固体或通入 气体,已知:
气体,已知: 的电离平衡常数
的电离平衡常数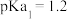 ,
, 。下列有关叙述正确的是
。下列有关叙述正确的是
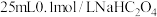 溶液中加入
溶液中加入 固体或通入
固体或通入 气体,已知:
气体,已知: 的电离平衡常数
的电离平衡常数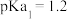 ,
, 。下列有关叙述正确的是
。下列有关叙述正确的是A. 溶液中存在: 溶液中存在: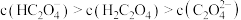 |
B.加入 固体或通入 固体或通入 气体的过程中,水的电离程度均减小 气体的过程中,水的电离程度均减小 |
C.加入 固体至 固体至 ,此时 ,此时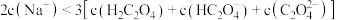 |
D.当 时,溶液中离子浓度满足: 时,溶液中离子浓度满足: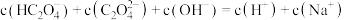 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列说法不正确的是
| A.0.1mol•L-1CH3COOH溶液加水稀释,CH3COO-数目增多,c(OH-)增大 |
B.室温下,NaHSO3溶液的pH<7,说明 的电离程度大于其水解程度 的电离程度大于其水解程度 |
| C.酸碱质子理论认为,凡能给出质子(H+)的物质都是酸,凡能接受质子的物质都是碱。由该理论可知:NaHCO3、H2O、Al(OH)3均可称为酸碱两性物质 |
| D.25℃时0.1mol•L-1的H2S水溶液中,加入一定量的NaOH溶液,当溶液中存在:c(Na+)=c(S2-)+c(HS-)+c(H2S)时,溶液的主要溶质为Na2S |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某物质 A 的实验式为CoCl3·4NH3, 1molA 中加入足量的 AgNO3溶液中能生成1mol白色沉淀,以强碱处理并没有NH3放出,则关于此化合物的说法中不正确的是
| A.Co3+与NH3、Cl-形成配位键 | B.配合物配位数为6 |
| C.该配合物可能是平面正方形结构 | D.此配合物可写成[Co (NH3) 4Cl2]Cl |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】1825年偶然地发现了组成为KCl•PtCl2•C2H4•H2O的黄色晶体,其中含乙烯,配位化学确立后,证明其中存在组成为[PtCl3(C2H4)]-的配合物,铂的配合物顺式二氯二氨合铂[常称“顺铂”;化学式为[Pt(NH3)2Cl2]具有抗癌活性。下列说法正确的是
| A.C2H4为极性分子 |
| B.H2O的VSEPR模型为V形 |
| C.Pt(NH3)2Cl2分子结构是以Pt为中心的四面体形 |
| D.NH3分子中的H-N-H键的键角小于顺铂中的H-N-H键 |
您最近一年使用:0次

 2HNO3+4N2↑+9H2O反应中,生成28gN2,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28gN2,转移的电子数目为3.75NA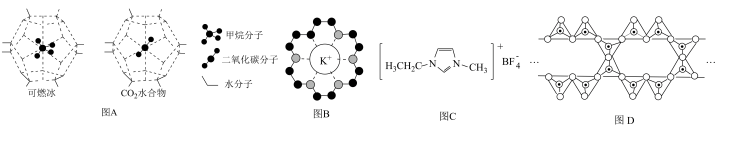
 结合,体现了超分子“分子识别”的特征
结合,体现了超分子“分子识别”的特征 摩尔质量更大,故具有更高的熔、沸点
摩尔质量更大,故具有更高的熔、沸点 表示硅氧四面体,则该硅酸盐阴离子的通式为
表示硅氧四面体,则该硅酸盐阴离子的通式为


