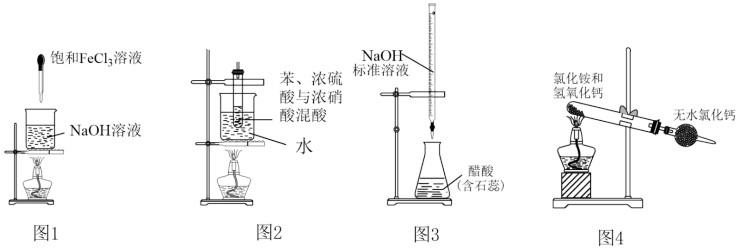
下列各组实验所得结论或推论正确的是
选项 | 实验操作及现象 | 结论或推论 |
A | 向0.1mol·L⁻¹NaHA溶液中滴加酚酞溶液,溶液变为浅红色 | Kw<Ka1·Ka2(Ka1和Ka2为H₂A的电离平衡常数) |
B | 取少量蔗糖水解液,加入新制的氢氧化铜悬浊液,加热至沸腾,未见砖红色沉淀产生 | 蔗糖在酸性条件下不能水解 |
C | 相同条件下,分别取等体积的SO₂和CO₂的饱和水溶液于试管中,测pH,前者小 | 酸性:H₂SO₃>H₂CO₃ |
D | 把苯和液溴的混合液中加入铁粉中,将产生的气体通入CCl₄,再通入AgNO₃溶液,产生淡黄色沉淀 | 苯与溴发生了取代反应生成了HBr |
| A.A | B.B | C.C | D.D |
更新时间:2024-05-22 15:22:02
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】一定条件下,CH3COONa溶液存在水解平衡:CH3COO-+H2O CH3COOH+OH-,下列说法正确的是
CH3COOH+OH-,下列说法正确的是
 CH3COOH+OH-,下列说法正确的是
CH3COOH+OH-,下列说法正确的是| A.加入少量固体FeCl3,c(CH3COO-)增大 |
| B.加入少量NaOH固体,c(CH3COO-)增大 |
| C.稀释溶液,溶液的pH增大 |
| D.加入适量醋酸得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,向10 0.1
0.1 的
的 溶液中逐滴滴入0.1
溶液中逐滴滴入0.1 的
的 溶液,所得溶液电导率及
溶液,所得溶液电导率及 变化如图所示,已知
变化如图所示,已知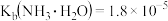 。下列分析错误的是
。下列分析错误的是

 0.1
0.1 的
的 溶液中逐滴滴入0.1
溶液中逐滴滴入0.1 的
的 溶液,所得溶液电导率及
溶液,所得溶液电导率及 变化如图所示,已知
变化如图所示,已知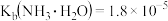 。下列分析错误的是
。下列分析错误的是
A.曲线Ⅰ表示溶液的 变化情况 变化情况 |
B. 为弱酸,其电离常数 为弱酸,其电离常数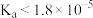 |
C.开始阶段溶液电导率增大是因为生成了强电解质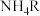 |
| D.溶液中水的电离程度变化趋势与曲线Ⅱ相似 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】在实验室中,下列除杂的方法中正确的是( )
| A.溴苯中混有溴,加入KI溶液,振荡,用汽油萃取出溴苯 |
| B.乙烷中混有乙烯,通入H2在一定条件下反应,使乙烯转化为乙烷 |
| C.硝基苯中混有浓硫酸和浓硝酸,将其倒入NaOH溶液中,静置、分液 |
| D.乙烯中混有CO2和SO2,将其通入酸性KMnO4溶液中洗气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在各类化学实验中常常用到导管,如实验室制备硝基苯,装置如图。下列关于长导管的用途的叙述中错误的是
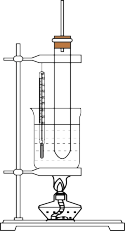

| A.实验室制备硝基苯,长导管的主要作用是:冷凝和回流 |
| B.加热密闭装置,防止容器内压力过高,可用导管进行导气减压 |
| C.长导管冷凝时,冷却剂是空气 |
| D.长导管可以代替玻璃棒进行使用 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验的操作、现象、解释或结论都正确的是
| 操作 | 现象 | 解释或结论 | |
| A | 甲苯与高锰酸钾溶液混合振荡 | 水层紫红色褪去 | 苯环对甲基有活化作用 |
| B | FeCl3、KI混合溶液中滴加KSCN溶液 | 溶液呈红色 | FeCl3不与KI反应 |
| C | 向氯化铜溶液中逐滴加入氨水 | 产生沉淀继而溶解 | 氢氧化铜有两性 |
| D | 向20%蔗糖溶液中加入少量稀硫酸,加热;再加入银氨溶液并水浴加热 | 未出现银镜 | 蔗糖未水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】根据实验操作和现象所得出的结论正确的是 ( )
| 选项 | 实验操作和现象 | 结论 |
| A | 向NaI溶液中滴入少量新制氯水和苯,振荡、静置,溶液上层呈紫色 | I-还原性强于Cl- |
| B | 向某溶液中滴加H2O2溶液后再加入KSCN,溶液呈红色 | 溶液中一定含有Fe2+ |
| C | 测定等浓度的Na2CO3和Na2SO3溶液的pH,Na2CO3的pH大于Na2SO3溶液 | S的非金属性比C强 |
| D | 向蔗糖溶液中加入少量稀硫酸并加热,冷却,加入新制Cu(OH)2悬浊液,加热,未出现红色沉淀 | 蔗糖未水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次


 溶液和
溶液和 溶液的
溶液的 溶液中滴入少量酸性
溶液中滴入少量酸性 溶液,观察
溶液,观察 有还原性
有还原性 溶液和
溶液和 溶液的
溶液的 的酸性弱于
的酸性弱于

 溶液中加1mL
溶液中加1mL 溶液,产生白色沉淀;再加入1mL
溶液,产生白色沉淀;再加入1mL 溶液,产生红褐色沉淀。
溶液,产生红褐色沉淀。 沉淀转化为
沉淀转化为 沉淀
沉淀