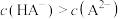食醋是厨房常用的调味品,25℃时, 的
的 ,醋酸溶液加水稀释后,下列说法正确的是
,醋酸溶液加水稀释后,下列说法正确的是
 的
的 ,醋酸溶液加水稀释后,下列说法正确的是
,醋酸溶液加水稀释后,下列说法正确的是A. 数目增多 数目增多 |
B. 增大 增大 |
C. 的电离程度减小 的电离程度减小 |
D. 减小 减小 |
更新时间:2024-05-23 19:55:07
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】在0.1 mol•L﹣1 CH3COOH溶液中存在如下电离平衡:CH3COOH⇌CH3COO﹣+H+,下列叙述正确的是
| A.加入水时,平衡向逆反应方向移动 |
| B.加入少量NaOH固体,平衡向正反应方向移动 |
| C.加入少量0.1 mol•L﹣1 HCl溶液,平衡向逆反应方向移动,溶液中c(H+)减小 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列事实与水解平衡有关的是
A.向10mL氨水中加入蒸馏水, 的数目增多 的数目增多 |
| B.随着温度的升高,水的离子积增大 |
C.加CuO除去 溶液中的 溶液中的 杂质 杂质 |
D. 溶液遇到闪锌矿(ZnS),会慢慢转化为铜蓝(CuS) 溶液遇到闪锌矿(ZnS),会慢慢转化为铜蓝(CuS) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】等浓度的下列稀溶液:①乙酸 Ka:1.76×10—5、②HClO Ka:2.95×10—8、③碳酸 Ka1:4.30×10—7、④乙醇,它们的pH由小到大排列正确的是( )
| A.④②③① | B.③①②④ | C.①②③④ | D.①③②④ |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】常温下,次氯酸电离平衡体系中各成分的组成分数 [
[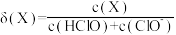 ,X为
,X为 或
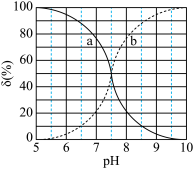
或 ]与pH的关系如图所示。下列有关说法正确的是
]与pH的关系如图所示。下列有关说法正确的是
 [
[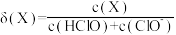 ,X为
,X为 或
或 ]与pH的关系如图所示。下列有关说法正确的是
]与pH的关系如图所示。下列有关说法正确的是
A.次氯酸的电离方程式为 |
B.曲线b表示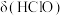 的变化 的变化 |
C.次氯酸电离常数 约为 约为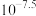 |
D.向次氯酸溶液中加 溶液, 溶液, 将增大 将增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列有关比较中,大小顺序排列正确的是
| A.原子半径: N>O>F>Ne |
| B.热稳定性: PH3>H2S> HBr>NH3 |
| C.物质的熔点:石英>氯化钠晶体>碘单质 |
D.结合H+的能力: CO >CH3COO->OH- >CH3COO->OH- |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】已知:常温下,一元弱碱BOH的电离平衡常数Kb=1.0×10−9。在100mL0.1 mol∙L−1BOH溶液中加入等体积的水稀释,下列叙述正确的是
| A.稀释前,溶液的pH≈9 |
B.稀释后,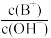 变大 变大 |
| C.稀释后BOH的电离度增大,溶液的pH也增大 |
| D.稀释前后溶液中均存在c(BOH)>c(B+)>c(OH-) |
您最近一年使用:0次

 CH3COO- + H+,下列叙述不正确的是
CH3COO- + H+,下列叙述不正确的是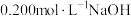 溶液滴定
溶液滴定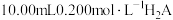 溶液,加入NaOH溶液的体积、
溶液,加入NaOH溶液的体积、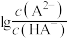 与pH的变化关系如图所示。下列说法正确的是
与pH的变化关系如图所示。下列说法正确的是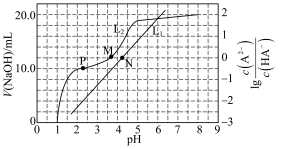
 表示加入NaOH溶液的体积与pH的变化关系
表示加入NaOH溶液的体积与pH的变化关系 的第二步电离常数
的第二步电离常数 的数量级为
的数量级为