在0.1 mol•L﹣1 CH3COOH溶液中存在如下电离平衡:CH3COOH⇌CH3COO﹣+H+,下列叙述正确的是
| A.加入水时,平衡向逆反应方向移动 |
| B.加入少量NaOH固体,平衡向正反应方向移动 |
| C.加入少量0.1 mol•L﹣1 HCl溶液,平衡向逆反应方向移动,溶液中c(H+)减小 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
更新时间:2016-09-02 20:40:36
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】常温下,加水稀释冰醋酸,再此过程中始终增大的是
| A.溶液的导电能力 | B.醋酸的电离度 |
C.溶液的 值 值 | D.醋酸的电离平衡常数 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】在一定条件下,HA溶液存在电离平衡:HA H++A--Q。下列说法正确的是
H++A--Q。下列说法正确的是
 H++A--Q。下列说法正确的是
H++A--Q。下列说法正确的是| A.稀释溶液,HA电离平衡常数增大 | B.升高温度,HA电离程度增大 |
| C.加入NaA固体,平衡朝正反应方向移动 | D.加入NaOH固体,溶液pH减小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】已知 的醋酸溶液中存在电离平衡:
的醋酸溶液中存在电离平衡: ,要使溶液中pH增大且平衡向正反应方向移动,可以采取的措施是
,要使溶液中pH增大且平衡向正反应方向移动,可以采取的措施是
 的醋酸溶液中存在电离平衡:
的醋酸溶液中存在电离平衡: ,要使溶液中pH增大且平衡向正反应方向移动,可以采取的措施是
,要使溶液中pH增大且平衡向正反应方向移动,可以采取的措施是| A.加少量烧碱固体 | B.升高温度 |
| C.加少量冰醋酸 | D.加少量 固体 固体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】相同温度下,关于盐酸和醋酸两种溶液的比较,下列说法不正确的是
A.pH相等的两溶液中:c(CH3COOˉ)=c(Clˉ) |
| B.相同物质的量浓度的两溶液导电能力相同 |
| C.氢离子浓度、体积均相同的两溶液,加适量的CH3COONa晶体,两溶液的氢离子浓度都减小 |
| D.pH=3的两溶液分别加水稀释10倍后,醋酸溶液的pH比盐酸小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列叙述正确的是
| A.稀醋酸中加入少量浓醋酸能增大醋酸的电离程度 |
B.若NH4Cl溶液与 NH4HSO4溶液的 相等,则 相等,则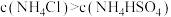 |
C.向盐酸中加入氨水至中性,溶液中 |
| D.AgCl固体在100mL 0.01mol/L NaCl溶液中的 Ksp比在100mL 0.01moL BaCl2中的Ksp大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】能够使CH3COONa溶液pH增大且水解程度减小的条件是
| A.加水 | B.升温 | C.加压 | D.加CH3COONa固体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】一定温度下,在0.1mol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH CH3COO-+H+,对于该平衡,下列叙述正确的是( )
CH3COO-+H+,对于该平衡,下列叙述正确的是( )
 CH3COO-+H+,对于该平衡,下列叙述正确的是( )
CH3COO-+H+,对于该平衡,下列叙述正确的是( )| A.加入少量NaOH固体,平衡向正方向移动,电离平衡常数增大 |
| B.滴加少量0.1mol/LHCl溶液,平衡逆方向移动,溶液中c(H+)增大 |
| C.加水,电离平衡右移,电离程度增大,所有离子浓度增大 |
| D.加入少量NaCl溶液,平衡不移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】室温下,对于10mL  的氨水,下列叙述正确的是
的氨水,下列叙述正确的是
 的氨水,下列叙述正确的是
的氨水,下列叙述正确的是| A.欲使该溶液的pH和电离程度都增大,可通入少量氨气 |
B.加入10mL  的 的 溶液,混合液显中性 溶液,混合液显中性 |
C.加水稀释后,溶液中 不变 不变 |
| D.加水稀释后,溶液中所有离子的浓度均减小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】向纯水中加入硫酸氢钠溶液,则水的电离子平衡是( )
| A.向正反应方向移动 | B.向逆反应方向移动 |
| C.不移动 | D.无法确定 |
您最近一年使用:0次

 H++OH-
H++OH-