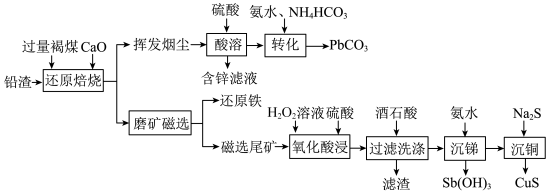
铅渣由多种氧化物及它们相互结合而形成的化合物、固溶体、共晶混合物所组成。对铅渣进行综合利用,回收其中的有价金属(Cu、Fe、Pb、Zn、Sb)的部分工艺流程如下:________________ 。
(2)挥发烟尘中的主要氧化物为PbO—ZnO2。
①区分挥发烟尘中的氧化物是晶体还是非晶体的最可靠的科学方法为__________ (填选项)。
A.核磁共振氢谱 B.X射线衍射 C.质谱法
②“转化”过程中,发生反应的化学方程式为________________ 。
(3)“氧化酸浸”过程中,若将物质的量为3mol的Cu—Sb合金(其中Cu与Sb物质的量之比为1∶2)氧化,至少需要H2O2的物质的量为________ mol。
(4)“过滤洗涤”过程中,加入酒石酸(表示为C4H6O6)发生如下配位反应:
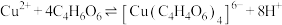 、
、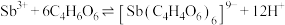
①上述两个配合物中,提供空轨道的元素为____________ (填元素符号)。
②滤渣的主要成分是_____________________ 。
③“过滤洗涤”时,用酒石酸稀溶液洗涤滤渣而不用水。用酒石酸稀溶液洗涤可减少金属离子的损失,原因为______________________ 。
(2)挥发烟尘中的主要氧化物为PbO—ZnO2。
①区分挥发烟尘中的氧化物是晶体还是非晶体的最可靠的科学方法为
A.核磁共振氢谱 B.X射线衍射 C.质谱法
②“转化”过程中,发生反应的化学方程式为
(3)“氧化酸浸”过程中,若将物质的量为3mol的Cu—Sb合金(其中Cu与Sb物质的量之比为1∶2)氧化,至少需要H2O2的物质的量为
(4)“过滤洗涤”过程中,加入酒石酸(表示为C4H6O6)发生如下配位反应:
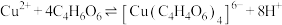 、
、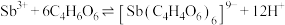
①上述两个配合物中,提供空轨道的元素为
②滤渣的主要成分是
③“过滤洗涤”时,用酒石酸稀溶液洗涤滤渣而不用水。用酒石酸稀溶液洗涤可减少金属离子的损失,原因为
更新时间:2024-05-25 23:39:25
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】[化学——选修3:物质结构与性质]周期表前三周期元素A、B、C、D,原子序数依次增大,A的基态原子的L层电子是K层电子的两倍;B的价电子层中的未成对电子有3个;C与B同族;D的最高价含氧酸为酸性最强的无机含氧酸。请回答下列问题:
(1)C的基态原子的电子排布式为_______ ;D的最高价含氧酸酸性比其低两价的含氧酸酸性强的原因是_____ 。
(2)杂化轨道分为等性和不等性杂化,不等性杂化时在杂化轨道中有不参加成键的孤电子对的存在。A、B、C都能与D形成中心原子杂化方式为______ 的两元共价化合物。其中,属于不等性杂化的是_____ (写化学式)。以上不等性杂化的化合物价层电子对立体构型为___ ,分子立体构型为____ 。
(3)以上不等性杂化化合物成键轨道的夹角_____ (填“大于”、“等于”或“小于”)等性杂化的化合物成键轨道间的夹角。由于C核外比 B多一层电子,C还可以和D形成另一种两元共价化合物。此时C的杂化轨道中没有孤对电子,比起之前C和D的化合物,它的杂化轨道多了一条。其杂化方式为______ 。
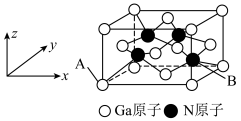
(4)A和B能形成多种结构的晶体。其中一种类似金刚石的结构,硬度比金刚石还大,是一种新型的超硬材料。其结构如下图所示(图1为晶体结构,图2为切片层状结构),其化学式为____ 。实验测得此晶体结构属于六方晶系,晶胞结构见图3。已知图示原子都包含在晶胞内,晶胞参数a="0.64" nm,c="0.24" nm。其晶体密度为____ (已知:a=0.64nm,c=0.24 nm, 结果精确到小数点后第2位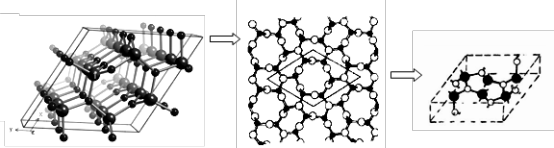
图1 A和B形成的一种晶体结构图 图2 切片层状结构 图3 晶胞结构
(图2和图3中:○为N原子、●为C原子)
(1)C的基态原子的电子排布式为
(2)杂化轨道分为等性和不等性杂化,不等性杂化时在杂化轨道中有不参加成键的孤电子对的存在。A、B、C都能与D形成中心原子杂化方式为
(3)以上不等性杂化化合物成键轨道的夹角
(4)A和B能形成多种结构的晶体。其中一种类似金刚石的结构,硬度比金刚石还大,是一种新型的超硬材料。其结构如下图所示(图1为晶体结构,图2为切片层状结构),其化学式为

图1 A和B形成的一种晶体结构图 图2 切片层状结构 图3 晶胞结构
(图2和图3中:○为N原子、●为C原子)
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】我国科学家选取了33个土壤样本,分别测定大量元素(N、Ca、K、Fe、P)、微量元素(Mn、Zn、Cu、Co、Sn)和重金属(Pb、Cr、Ag、Cd、Hg)的含量,研究表明:15种矿物元素中,5种元素(P、Cu、Zn、Co、Pb)的含量与地理位置有关。回答下列问题:
(1)基态锰原子的价层电子排布式为___________ 。
(2)基态钙原子的核外电子云轮廓图呈球形的能级上填充___________ 个电子,基态钾原子的核外电子云有___________ 个伸展方向。
(3)NH3与H2O可与Zn2+形成配合物[Zn(NH3)3(H2O)]2+。与Zn2+形成配位键的原子是___________ (填元素符号);写出一种与NH3互为等电子体的阳离子:___________ (填化学式)。
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤,在ZnCO3中,阴离子空间构型为___________ 。
(5)已知KH2PO4是次磷酸的正盐, H3PO2的结构式为___________ ,其中P采取___________ 杂化方式。
(6)某磷青铜晶胞结构如下图所示:

①其中原子坐标参数A为(0,0,0);B为(0, ,
, )。则P原子的坐标参数为
)。则P原子的坐标参数为___________ 。
②该晶体中距离Cu原子最近的Sn原子有___________ 个。
③若晶体密度为ag•cm3,最近的Cu原子核间距为___________ pm(用含NA和a的代数式表示)。
(1)基态锰原子的价层电子排布式为
(2)基态钙原子的核外电子云轮廓图呈球形的能级上填充
(3)NH3与H2O可与Zn2+形成配合物[Zn(NH3)3(H2O)]2+。与Zn2+形成配位键的原子是
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤,在ZnCO3中,阴离子空间构型为
(5)已知KH2PO4是次磷酸的正盐, H3PO2的结构式为
(6)某磷青铜晶胞结构如下图所示:

①其中原子坐标参数A为(0,0,0);B为(0,
 ,
, )。则P原子的坐标参数为
)。则P原子的坐标参数为②该晶体中距离Cu原子最近的Sn原子有
③若晶体密度为ag•cm3,最近的Cu原子核间距为
您最近一年使用:0次
【推荐3】铁系元素(铁、钴、镍)构成了丰富的物质世界,其形成的物质在生产生活中用途广泛。回答下列问题:
(1)基态 的单电子数目为
的单电子数目为___________ 。
(2) 中含有的
中含有的 键数目为
键数目为__________ , 分子与
分子与 形成配合物后
形成配合物后 键角
键角___________ (填“变大”“变小”或“不变”)。
(3) 中配体
中配体 的空间结构为
的空间结构为___________ ,N、O原子的第二电离能与第一电离能差值相比更大的是___________ (填元素符号)。
(4)一种铁基超导材料晶胞结构如图a所示,铁原子沿z轴方向的投影如图b所示。该材料的化学式为___________ ,已知体心与顶点的 原子有着相同的化学环境,晶胞中
原子有着相同的化学环境,晶胞中 原子1分数坐标为(0,0,0.628),则
原子1分数坐标为(0,0,0.628),则 原子2的分数坐标为
原子2的分数坐标为___________ ,体心 原子与
原子与 原子1之间的距离为
原子1之间的距离为___________  。
。

(1)基态
 的单电子数目为
的单电子数目为(2)
 中含有的
中含有的 键数目为
键数目为 分子与
分子与 形成配合物后
形成配合物后 键角
键角(3)
 中配体
中配体 的空间结构为
的空间结构为(4)一种铁基超导材料晶胞结构如图a所示,铁原子沿z轴方向的投影如图b所示。该材料的化学式为
 原子有着相同的化学环境,晶胞中
原子有着相同的化学环境,晶胞中 原子1分数坐标为(0,0,0.628),则
原子1分数坐标为(0,0,0.628),则 原子2的分数坐标为
原子2的分数坐标为 原子与
原子与 原子1之间的距离为
原子1之间的距离为 。
。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】冰晶石(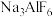 )是工业上电冶铝的助熔剂,可通过反应:
)是工业上电冶铝的助熔剂,可通过反应: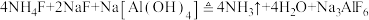 获得。请回答下列问题:
获得。请回答下列问题:
(1)该反应所涉及的物质中, 和
和 均为分子晶体,其中
均为分子晶体,其中 的空间构型为
的空间构型为______ 。由于二者分子间能形成氢键,所以氨气极易溶于水,氨水中最主要的氢键形式为N—H…O,除此以外还存在______ 种不同的氢键。
(2)NaF晶体中阴阳离子半径:
______ (填“>”或“<”) 。NaF的晶体结构与NaCl相同,但NaF的熔点为995℃,NaCl的熔点为801℃,试解释其原因:
。NaF的晶体结构与NaCl相同,但NaF的熔点为995℃,NaCl的熔点为801℃,试解释其原因:______ 。
(3)工业上制备活泼金属大多采用熔融盐酸盐制备,但电解纯净 无法获得金属Al,其原因是
无法获得金属Al,其原因是______ 。熔融态氯化铝可挥发出二聚分子 ,其结构为
,其结构为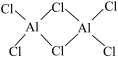 ,
,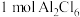 分子中含有配位键的数目为
分子中含有配位键的数目为______ (设 为阿伏加德罗常数的值),
为阿伏加德罗常数的值), 形成
形成 后,键角:Cl—Al—Cl
后,键角:Cl—Al—Cl______ (填“变大”“变小”或“不变”)。
(4)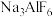 的晶胞结构如图所示:
的晶胞结构如图所示: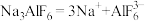 。
。
①晶胞中黑球代表的离子是______ (填“ ”或“
”或“ ”)。
”)。
②下列微粒的VSEPR模型与 相同的是
相同的是______ (填字母)。
A. B.
B. C.
C. D.
D.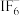
③设阿伏加德罗常数的值为 ,冰晶石的密度为
,冰晶石的密度为______  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
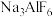 )是工业上电冶铝的助熔剂,可通过反应:
)是工业上电冶铝的助熔剂,可通过反应: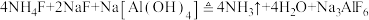 获得。请回答下列问题:
获得。请回答下列问题:(1)该反应所涉及的物质中,
 和
和 均为分子晶体,其中
均为分子晶体,其中 的空间构型为
的空间构型为(2)NaF晶体中阴阳离子半径:

 。NaF的晶体结构与NaCl相同,但NaF的熔点为995℃,NaCl的熔点为801℃,试解释其原因:
。NaF的晶体结构与NaCl相同,但NaF的熔点为995℃,NaCl的熔点为801℃,试解释其原因:(3)工业上制备活泼金属大多采用熔融盐酸盐制备,但电解纯净
 无法获得金属Al,其原因是
无法获得金属Al,其原因是 ,其结构为
,其结构为 ,
,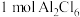 分子中含有配位键的数目为
分子中含有配位键的数目为 为阿伏加德罗常数的值),
为阿伏加德罗常数的值), 形成
形成 后,键角:Cl—Al—Cl
后,键角:Cl—Al—Cl(4)
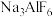 的晶胞结构如图所示:
的晶胞结构如图所示:
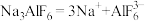 。
。①晶胞中黑球代表的离子是
 ”或“
”或“ ”)。
”)。②下列微粒的VSEPR模型与
 相同的是
相同的是A.
 B.
B. C.
C. D.
D.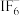
③设阿伏加德罗常数的值为
 ,冰晶石的密度为
,冰晶石的密度为 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)某同学根据上述信息,推断A基态原子的核外电子排布图为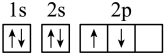 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了________ 。
(2)B元素的电负性_______ (填“大于”、“小于”或“等于”) C元素的电负性。B元素的第一电离能_______ ( 填“大于”、“小于”或“等于”) C元素的第一电离能。
(3)化合物AC和B的单质熔沸点较高的是_______ (填化学式),原因是___________________ 。
(4)E原子中电子占据的最高能层符号是______ ,该能层具有的原子轨道数为______ 。
(5)题中F元素位于元素周期表中的位置为______ ,位于_______ 区(填s、p、d、f或ds)。
(6)B、C的简单氢化物分子结合质子能力较强的是 (写化学式)___________ ,用一个离子方程式加以证明:_____________________ 。
| A元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
| B元素原子的核外p电子数比s电子数少1 |
| C元素基态原子p轨道有两个未成对电子 |
| D原子的第一至第四电离能分别是:I1=738kJ·mol-1;I2=1451kJ·mol-1;I3=7733kJ·mol-1;I4=10540kJ·mol-1 |
| E原子核外所有p轨道全满或半满 |
| F在周期表的第6纵列 |
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(2)B元素的电负性
(3)化合物AC和B的单质熔沸点较高的是
(4)E原子中电子占据的最高能层符号是
(5)题中F元素位于元素周期表中的位置为
(6)B、C的简单氢化物分子结合质子能力较强的是 (写化学式)
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】氮元素是重要的非金属元素,可形成多种铵盐、氮化物、叠氮化物及配合物等。
(1)基态氮原子价电子的轨道表示式(价电子排布图)为___________ ;第二周期元素原子中第一电离能大于氮原子的有___________ 种, 中阴离子的空间构型为
中阴离子的空间构型为___________ 。
(2)C、N、O、S四种元素中,电负性最大的是___________ 。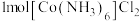 中含有σ键的数目为
中含有σ键的数目为___________ ;已知 比
比 的沸点低得多,试解释原因
的沸点低得多,试解释原因___________ 。
(3)含有多个配位原子的配体与同一中心离子(或原子)通过整合配位成环而形成的配合物为螯合物。一种 配合物的结构如图所示,1mol该螯合物中通过螯合作用形成的配位键有
配合物的结构如图所示,1mol该螯合物中通过螯合作用形成的配位键有___________ mol。 作简单立方堆积,两个立方体共用的面中心存在一个
作简单立方堆积,两个立方体共用的面中心存在一个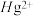 ,
, 位于立方体的体心,相邻的
位于立方体的体心,相邻的 的距离均为apm,阿伏加德罗常数的值为
的距离均为apm,阿伏加德罗常数的值为 ,该物质的化学式为
,该物质的化学式为___________ ,该晶体的密度为___________  。
。 可以与
可以与 、
、 等形成配合物。与
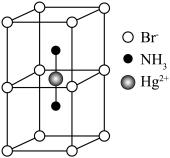
等形成配合物。与 互为等电子体且为非极性分子的化学式为
互为等电子体且为非极性分子的化学式为___________ 。在一定条件下铁形成的晶体的基本结构单元如图1和图2所示,则图1和图2的结构中铁原子的配位数之比为___________ ,两种晶体中空间利用率较高的是___________ 。(填“图1”或“图2”)
(1)基态氮原子价电子的轨道表示式(价电子排布图)为
 中阴离子的空间构型为
中阴离子的空间构型为(2)C、N、O、S四种元素中,电负性最大的是
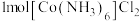 中含有σ键的数目为
中含有σ键的数目为 比
比 的沸点低得多,试解释原因
的沸点低得多,试解释原因(3)含有多个配位原子的配体与同一中心离子(或原子)通过整合配位成环而形成的配合物为螯合物。一种
 配合物的结构如图所示,1mol该螯合物中通过螯合作用形成的配位键有
配合物的结构如图所示,1mol该螯合物中通过螯合作用形成的配位键有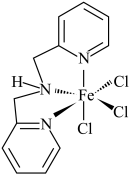
 作简单立方堆积,两个立方体共用的面中心存在一个
作简单立方堆积,两个立方体共用的面中心存在一个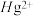 ,
, 位于立方体的体心,相邻的
位于立方体的体心,相邻的 的距离均为apm,阿伏加德罗常数的值为
的距离均为apm,阿伏加德罗常数的值为 ,该物质的化学式为
,该物质的化学式为 。
。
 可以与
可以与 、
、 等形成配合物。与
等形成配合物。与 互为等电子体且为非极性分子的化学式为
互为等电子体且为非极性分子的化学式为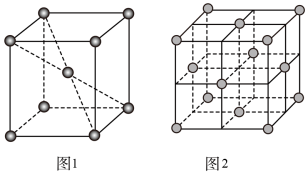
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】超纯 是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯
是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯 方面取得了显著成果,工业上以粗镓为原料,制备超纯
方面取得了显著成果,工业上以粗镓为原料,制备超纯 的工艺流程如下:
的工艺流程如下: 的化学性质和
的化学性质和 相似,
相似, 的熔点为
的熔点为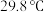 ;
;
② (乙醚)和
(乙醚)和 (三正辛胺)在上述流程中可作为配体;
(三正辛胺)在上述流程中可作为配体;
③相关物质的沸点:
回答下列问题:
(1)晶体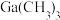 的晶体类型是
的晶体类型是_______ ;
(2)“电解精炼”装置如图所示,电解池温度控制在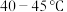 的原因是
的原因是_______ ,阴极的电极反应式为_______ ;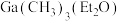 ”工序中的产物还包括
”工序中的产物还包括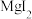 和
和 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_______ ;
(4)“残渣”经纯水处理,能产生可燃性气体,该气体主要成分是_______ ;
(5)下列说法错误的是_______;
(6)直接分解 不能制备超纯
不能制备超纯 ,而本流程采用“配体交换”工艺制备超纯
,而本流程采用“配体交换”工艺制备超纯 的理由是
的理由是_______ ;
(7)比较分子中的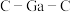 键角大小:
键角大小:
_______  (填“>”“<”或“=”),其原因是
(填“>”“<”或“=”),其原因是_______ 。
 是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯
是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯 方面取得了显著成果,工业上以粗镓为原料,制备超纯
方面取得了显著成果,工业上以粗镓为原料,制备超纯 的工艺流程如下:
的工艺流程如下: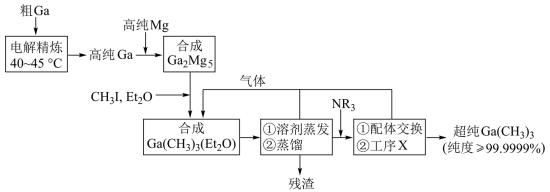
 的化学性质和
的化学性质和 相似,
相似, 的熔点为
的熔点为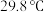 ;
;②
 (乙醚)和
(乙醚)和 (三正辛胺)在上述流程中可作为配体;
(三正辛胺)在上述流程中可作为配体;③相关物质的沸点:
| 物质 | 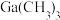 |  | 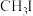 | 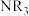 |
沸点/ | 55.7 | 34.6 | 42.4 | 365.8 |
(1)晶体
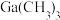 的晶体类型是
的晶体类型是(2)“电解精炼”装置如图所示,电解池温度控制在
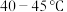 的原因是
的原因是
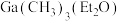 ”工序中的产物还包括
”工序中的产物还包括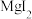 和
和 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(4)“残渣”经纯水处理,能产生可燃性气体,该气体主要成分是
(5)下列说法错误的是_______;
A.流程中 得到了循环利用 得到了循环利用 |
B.流程中,“合成 ”至“工序X”需在无水无氧的条件下进行 ”至“工序X”需在无水无氧的条件下进行 |
C.“工序X”的作用是解配 ,并蒸出 ,并蒸出 |
D.用核磁共振氢谱不能区分 和 和 |
 不能制备超纯
不能制备超纯 ,而本流程采用“配体交换”工艺制备超纯
,而本流程采用“配体交换”工艺制备超纯 的理由是
的理由是(7)比较分子中的
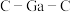 键角大小:
键角大小:
 (填“>”“<”或“=”),其原因是
(填“>”“<”或“=”),其原因是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】按照要求回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过_____ 方法区分晶体、准晶体和非晶体。
(2) 单质为体心立方晶体,其晶胞参数
单质为体心立方晶体,其晶胞参数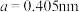 ,晶胞中铁原子的配位数为
,晶胞中铁原子的配位数为______ ,铁原子半径为______ ,列式表示铁晶胞的空间利用率____ 。(不必计算出结果)
(3)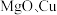 和干冰的晶胞示意图如图:
和干冰的晶胞示意图如图:________ 。
②在 晶体中,与
晶体中,与 相邻且最近的
相邻且最近的 个数为
个数为_______ ; 配位数为
配位数为_______ 。
③每个 晶胞中平均有
晶胞中平均有_____ 个 原子。
原子。
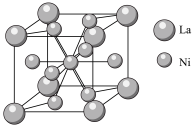
④金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如图所示,若阿伏加德罗常数为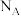 晶胞边长为
晶胞边长为 ,晶胞的密度为
,晶胞的密度为______ 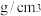 。
。 晶胞中,
晶胞中, 原子半径为
原子半径为 原子半径为
原子半径为 ,阿伏加德罗常数用
,阿伏加德罗常数用 表示,
表示, 的密度可表示为
的密度可表示为____  。
。
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)
 单质为体心立方晶体,其晶胞参数
单质为体心立方晶体,其晶胞参数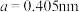 ,晶胞中铁原子的配位数为
,晶胞中铁原子的配位数为(3)
 和干冰的晶胞示意图如图:
和干冰的晶胞示意图如图: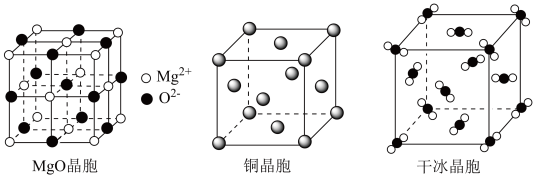
②在
 晶体中,与
晶体中,与 相邻且最近的
相邻且最近的 个数为
个数为 配位数为
配位数为③每个
 晶胞中平均有
晶胞中平均有 原子。
原子。④金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如图所示,若阿伏加德罗常数为
 晶胞边长为
晶胞边长为 ,晶胞的密度为
,晶胞的密度为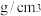 。
。
 晶胞中,
晶胞中, 原子半径为
原子半径为 原子半径为
原子半径为 ,阿伏加德罗常数用
,阿伏加德罗常数用 表示,
表示, 的密度可表示为
的密度可表示为 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】Ni、Co均是重要的战略性金属。从处理后的矿石硝酸浸取液(含Ni2+、Co2+、Al3+、Mg2+)中,利用氨浸工艺可提取Ni、Co,并获得高附加值化工产品。工艺流程如下:

已知:氨性溶液由NH3·H2O、(NH4)2SO3和(NH4)2CO3配制。常温下,Ni2+、Co2+、Co3+与NH3形成可溶于水的配离子:lgKb(NH3·H2O)=-4.7;Co (OH)2易被空气氧化为Co (OH)3;部分氢氧化物的Ksp如下表。
回答下列问题:
(1)活性MgO可与水反应,化学方程式为___________ 。
(2)常温下,pH=9.9的氨性溶液中,c(NH3·H2O)___________ c(NH ) (填“>”“<”或“=”)。
) (填“>”“<”或“=”)。
(3) (NH4)2CO3会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射图谱中,出现了NH4Al(OH)2CO3的明锐衍射峰。
①NH4Al(OH)2CO3属于___________ (填“晶体”或“非晶体”)。
②(NH4)2CO3提高了Ni、Co的浸取速率,其原因是___________ 。
(4)①“析晶”过程中通入的酸性气体A为___________ 。
②由CoCl2可制备AlxCoOy晶体,其立方晶胞如图。Al与O最小间距大于Co与O最小间距,x、y为整数,则Co在晶胞中的位置为___________ ;晶体中一个Al周围与其最近的O的个数为___________ 。

(5)①“结晶纯化”过程中,没有引入新物质。晶体A含6个结晶水,则所得HNO3溶液中n(HNO3)与n(H2O)的比值,理论上最高为___________ 。
②“热解”对于从矿石提取Ni、Co工艺的意义,在于可重复利用HNO3和___________ (填化学式)。

已知:氨性溶液由NH3·H2O、(NH4)2SO3和(NH4)2CO3配制。常温下,Ni2+、Co2+、Co3+与NH3形成可溶于水的配离子:lgKb(NH3·H2O)=-4.7;Co (OH)2易被空气氧化为Co (OH)3;部分氢氧化物的Ksp如下表。
| 氢氧化物 | Co (OH)2 | Co (OH)3 | Ni(OH)2 | Al(OH)3 | Mg(OH)2 |
| Ksp | 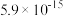 |  |  | 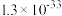 | 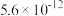 |
(1)活性MgO可与水反应,化学方程式为
(2)常温下,pH=9.9的氨性溶液中,c(NH3·H2O)
 ) (填“>”“<”或“=”)。
) (填“>”“<”或“=”)。(3) (NH4)2CO3会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射图谱中,出现了NH4Al(OH)2CO3的明锐衍射峰。
①NH4Al(OH)2CO3属于
②(NH4)2CO3提高了Ni、Co的浸取速率,其原因是
(4)①“析晶”过程中通入的酸性气体A为
②由CoCl2可制备AlxCoOy晶体,其立方晶胞如图。Al与O最小间距大于Co与O最小间距,x、y为整数,则Co在晶胞中的位置为

(5)①“结晶纯化”过程中,没有引入新物质。晶体A含6个结晶水,则所得HNO3溶液中n(HNO3)与n(H2O)的比值,理论上最高为
②“热解”对于从矿石提取Ni、Co工艺的意义,在于可重复利用HNO3和
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】某兴趣小组用硼镁矿(主要成分为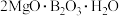 ,含
,含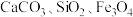 等杂质)联产
等杂质)联产 和
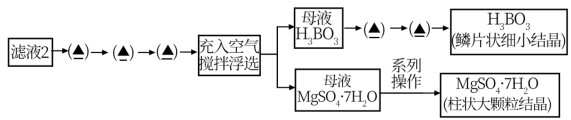
和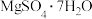 ,流程如下:
,流程如下:
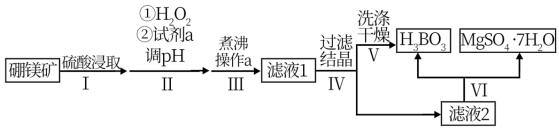
已知: 是一种极弱的酸,可溶于水、乙醇;
是一种极弱的酸,可溶于水、乙醇;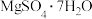 易溶于水,微溶于乙醇;相关物质的溶解度随温度变化如图。
易溶于水,微溶于乙醇;相关物质的溶解度随温度变化如图。

请回答:
(1)步骤I,为加快浸取速率,除适当提高硫酸浓度,还可采取的措施有___________ (任写一种)。
(2)步骤II, 加过量的原因除尽可能将
加过量的原因除尽可能将 氧化完全,还可能是
氧化完全,还可能是___________ 。
(3)下列说法正确的是___________ 。
A.步骤II,试剂a可选择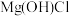
B.步骤III,煮沸的主要目的是除去没反应完的 及其中溶解的
及其中溶解的
C.步骤III,操作a宜采用热过滤
D.步骤IV,用玻璃棒摩擦器壁,促进晶体析出
E.步骤V,晶体置于烘箱中高温烘干
(4)步骤VI,采用浮选工艺有效分离颗粒大小不同的 晶体和
晶体和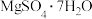 晶体,从下列选项中选出合理的操作:
晶体,从下列选项中选出合理的操作:___________ 。
a.减压蒸发溶剂;
b.加压蒸发溶剂;
c.用布氏漏斗抽滤;
d.用普通漏斗过滤;
e.蒸发至溶液出现晶膜,停止加热;
f.蒸发至溶液中出现大量晶体,停止加热;
g.冷水洗涤;
h.乙醇洗涤;
i.冷却至室温。
(5) 纯度的测定:准确称取制得的晶体试样mg溶于水中,加入足量甘露醇,摇匀后配制成100mL溶液,取25.00mL于锥形瓶中,用酚酞试液作指示剂,用cmol/LNaOH标准液滴定至终点,消耗NaoH溶液VmL。
纯度的测定:准确称取制得的晶体试样mg溶于水中,加入足量甘露醇,摇匀后配制成100mL溶液,取25.00mL于锥形瓶中,用酚酞试液作指示剂,用cmol/LNaOH标准液滴定至终点,消耗NaoH溶液VmL。
已知:i. 与NaOH溶液发生的反应为:
与NaOH溶液发生的反应为: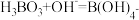
ii. 与甘露醇等多羟基化合物形成稳定的络合物,增大其电离度。
与甘露醇等多羟基化合物形成稳定的络合物,增大其电离度。
2 +
+

 +H++3H2O
+H++3H2O
① 不能直接用NaOH溶液滴定的原因是
不能直接用NaOH溶液滴定的原因是___________ 。
② 的纯度为
的纯度为___________ (用含字母的式子表示)。
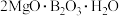 ,含
,含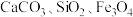 等杂质)联产
等杂质)联产 和
和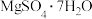 ,流程如下:
,流程如下:
已知:
 是一种极弱的酸,可溶于水、乙醇;
是一种极弱的酸,可溶于水、乙醇;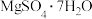 易溶于水,微溶于乙醇;相关物质的溶解度随温度变化如图。
易溶于水,微溶于乙醇;相关物质的溶解度随温度变化如图。
请回答:
(1)步骤I,为加快浸取速率,除适当提高硫酸浓度,还可采取的措施有
(2)步骤II,
 加过量的原因除尽可能将
加过量的原因除尽可能将 氧化完全,还可能是
氧化完全,还可能是(3)下列说法正确的是
A.步骤II,试剂a可选择
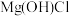
B.步骤III,煮沸的主要目的是除去没反应完的
 及其中溶解的
及其中溶解的
C.步骤III,操作a宜采用热过滤
D.步骤IV,用玻璃棒摩擦器壁,促进晶体析出
E.步骤V,晶体置于烘箱中高温烘干
(4)步骤VI,采用浮选工艺有效分离颗粒大小不同的
 晶体和
晶体和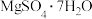 晶体,从下列选项中选出合理的操作:
晶体,从下列选项中选出合理的操作:
a.减压蒸发溶剂;
b.加压蒸发溶剂;
c.用布氏漏斗抽滤;
d.用普通漏斗过滤;
e.蒸发至溶液出现晶膜,停止加热;
f.蒸发至溶液中出现大量晶体,停止加热;
g.冷水洗涤;
h.乙醇洗涤;
i.冷却至室温。
(5)
 纯度的测定:准确称取制得的晶体试样mg溶于水中,加入足量甘露醇,摇匀后配制成100mL溶液,取25.00mL于锥形瓶中,用酚酞试液作指示剂,用cmol/LNaOH标准液滴定至终点,消耗NaoH溶液VmL。
纯度的测定:准确称取制得的晶体试样mg溶于水中,加入足量甘露醇,摇匀后配制成100mL溶液,取25.00mL于锥形瓶中,用酚酞试液作指示剂,用cmol/LNaOH标准液滴定至终点,消耗NaoH溶液VmL。已知:i.
 与NaOH溶液发生的反应为:
与NaOH溶液发生的反应为: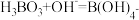
ii.
 与甘露醇等多羟基化合物形成稳定的络合物,增大其电离度。
与甘露醇等多羟基化合物形成稳定的络合物,增大其电离度。2
 +
+

 +H++3H2O
+H++3H2O①
 不能直接用NaOH溶液滴定的原因是
不能直接用NaOH溶液滴定的原因是②
 的纯度为
的纯度为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】某化工厂从废钼(Mo)催化剂(主要成分为MoS2、CoO、Fe2O3、Al2O3)中回收钴、铁、钼等,工艺流程如图:

已知:①“焙烧”过程中MoS2,转化为Na2MoO4,Fe2O3转化为NaFeO2(易水解)。CoO转化为Co3O4;②常温下,Ksp[Fe(OH)3]=8.0×10-38,lg2=0.3。
回答下列问题:
(1)“焙烧”过程中产生的气体I的主要成分为______ 。
(2)“焙烧”'过程中MoS2,转化为Na2MoO4,该反应中氧化剂和还原剂的物质的量之比为______ 。
(3)“焙烧”过程中Al2O3和Na2CO3反应的化学方程式为______ 。
(4)“熔砂”加水溶解时,加热的作用一方面是让可溶物充分溶解,另一方面是______ 。
(5)“滤渣I”中的Co3O4和H2O2、稀H2SO4反应的化学方程式为______ 。
(6)“滤渣Ⅱ”的成分为______ (写化学式)。
(7)常温下,“溶液”中加入NaHCO3溶液调节溶液的pH,当Fe3+恰好完全沉淀时,溶液的pH为______ [已知:c(Fe3+)≤1×10-5mol•L-1时,可以认为Fe3+已完全沉淀]
(8)写出生成CoCO3沉淀的离子方程式______ 。

已知:①“焙烧”过程中MoS2,转化为Na2MoO4,Fe2O3转化为NaFeO2(易水解)。CoO转化为Co3O4;②常温下,Ksp[Fe(OH)3]=8.0×10-38,lg2=0.3。
回答下列问题:
(1)“焙烧”过程中产生的气体I的主要成分为
(2)“焙烧”'过程中MoS2,转化为Na2MoO4,该反应中氧化剂和还原剂的物质的量之比为
(3)“焙烧”过程中Al2O3和Na2CO3反应的化学方程式为
(4)“熔砂”加水溶解时,加热的作用一方面是让可溶物充分溶解,另一方面是
(5)“滤渣I”中的Co3O4和H2O2、稀H2SO4反应的化学方程式为
(6)“滤渣Ⅱ”的成分为
(7)常温下,“溶液”中加入NaHCO3溶液调节溶液的pH,当Fe3+恰好完全沉淀时,溶液的pH为
(8)写出生成CoCO3沉淀的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】一种从废电池正极材料(含铝箔、 、
、 及少量不溶于酸碱的导电剂)中回收各种金属的工艺流程如下:
及少量不溶于酸碱的导电剂)中回收各种金属的工艺流程如下:
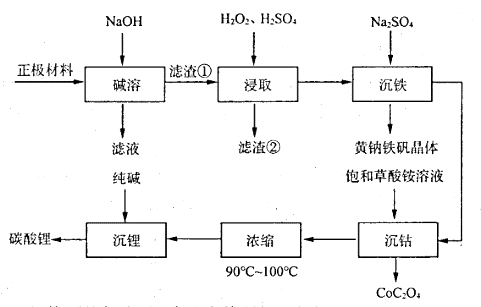
已知:①黄钠铁矾晶体颗粒粗大,沉淀速度快,易于过滤。
②钴酸锂难溶于水,碳酸锂的溶解度随温度升高而降低。
③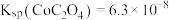 ,
,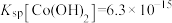 。
。
回答下列问题:
(1)为了提高“碱溶”效率,可以采取的措施是_______ (写出一条即可)。
(2)“浸取”时有无色气体产生,发生反应的离子方程式为_______ 。
(3)“沉钴”时采用饱和草酸铵溶液将钴元素转化为 ,与草酸钠溶液相比效果更好,原因是
,与草酸钠溶液相比效果更好,原因是_______ 。
(4)“沉锂”后得到碳酸锂固体的实验操作为_______ 。
(5)“沉铁”时所得黄钠铁矾的化学式可表示为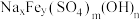 。采用滴定法测定黄钠铁矾样品的组成,实验步骤如下:
。采用滴定法测定黄钠铁矾样品的组成,实验步骤如下:
Ⅰ.称取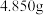 样品,加盐酸完全溶解后,配成
样品,加盐酸完全溶解后,配成 溶液。
溶液。
Ⅱ.量取 溶液,加入足量的KI,用
溶液,加入足量的KI,用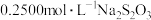 溶液进行滴定至终点
溶液进行滴定至终点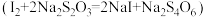 ,消耗
,消耗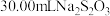 溶液。
溶液。
Ⅲ.另取 溶液,加入足量
溶液,加入足量 溶液,充分反应后过滤、洗涤、干燥,得到沉淀
溶液,充分反应后过滤、洗涤、干燥,得到沉淀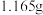 。
。
用 溶液进行滴定时,使用的指示剂为
溶液进行滴定时,使用的指示剂为_______ ;黄钠铁矾的化学式为_______ 。
 、
、 及少量不溶于酸碱的导电剂)中回收各种金属的工艺流程如下:
及少量不溶于酸碱的导电剂)中回收各种金属的工艺流程如下:
已知:①黄钠铁矾晶体颗粒粗大,沉淀速度快,易于过滤。
②钴酸锂难溶于水,碳酸锂的溶解度随温度升高而降低。
③
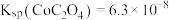 ,
,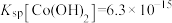 。
。回答下列问题:
(1)为了提高“碱溶”效率,可以采取的措施是
(2)“浸取”时有无色气体产生,发生反应的离子方程式为
(3)“沉钴”时采用饱和草酸铵溶液将钴元素转化为
 ,与草酸钠溶液相比效果更好,原因是
,与草酸钠溶液相比效果更好,原因是(4)“沉锂”后得到碳酸锂固体的实验操作为
(5)“沉铁”时所得黄钠铁矾的化学式可表示为
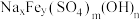 。采用滴定法测定黄钠铁矾样品的组成,实验步骤如下:
。采用滴定法测定黄钠铁矾样品的组成,实验步骤如下:Ⅰ.称取
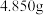 样品,加盐酸完全溶解后,配成
样品,加盐酸完全溶解后,配成 溶液。
溶液。Ⅱ.量取
 溶液,加入足量的KI,用
溶液,加入足量的KI,用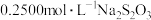 溶液进行滴定至终点
溶液进行滴定至终点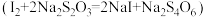 ,消耗
,消耗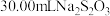 溶液。
溶液。Ⅲ.另取
 溶液,加入足量
溶液,加入足量 溶液,充分反应后过滤、洗涤、干燥,得到沉淀
溶液,充分反应后过滤、洗涤、干燥,得到沉淀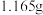 。
。用
 溶液进行滴定时,使用的指示剂为
溶液进行滴定时,使用的指示剂为
您最近一年使用:0次



