为减小CO2对环境的影响,在限制其排放量的同时,应加强对CO2创新利用研究。
(1)如将CO2与H2以1:3的体积比混合。
①适当条件下合成某烃和水,该烃是____(填序号)。
②适当条件下合成燃料甲醇和水。在体积为2L的密闭容器中,充入2 mol CO2和6 mol H2,
一定条件下发生反应:CO2(g) + 3H2(g) = CH3OH(g) + H2O(g) △H=-49.0 kJ/mol
测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
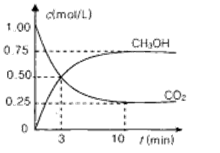
的转化率=;能使平衡体系中n(CH3OH)增大的措施有。
(2)如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4。
已知:①CH4(g)+2O2(g)=CO2(g)+2H2O( l ) △H=-890.3kJ/mol
②2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ/mol
则CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式是。
(3)最近科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇。甲醇可制作燃料电池。写出以氢氧化钾为电解质的甲醇燃料电池负极反应式。当电子转移的物质的量为________时,参加反应的氧气的体积是6.72L(标准状况下)。
(4)某同学用沉淀法测定含有较高浓度CO2的空气中CO2的含量,经查得一些物质在20℃的数据如下表。
吸收CO2最合适的试剂是____(填“Ca(OH)2”或“Ba(OH)2”)溶液。
(1)如将CO2与H2以1:3的体积比混合。
①适当条件下合成某烃和水,该烃是____(填序号)。
| A.烷烃 | B.烯烃 | C.炔烃 | D.苯的同系物 |
②适当条件下合成燃料甲醇和水。在体积为2L的密闭容器中,充入2 mol CO2和6 mol H2,
一定条件下发生反应:CO2(g) + 3H2(g) = CH3OH(g) + H2O(g) △H=-49.0 kJ/mol
测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。

的转化率=;能使平衡体系中n(CH3OH)增大的措施有。
(2)如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4。
已知:①CH4(g)+2O2(g)=CO2(g)+2H2O( l ) △H=-890.3kJ/mol
②2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ/mol
则CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式是。
(3)最近科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇。甲醇可制作燃料电池。写出以氢氧化钾为电解质的甲醇燃料电池负极反应式。当电子转移的物质的量为________时,参加反应的氧气的体积是6.72L(标准状况下)。
(4)某同学用沉淀法测定含有较高浓度CO2的空气中CO2的含量,经查得一些物质在20℃的数据如下表。
| 溶解度(s)/g | 溶度积(Ksp) | ||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 |
吸收CO2最合适的试剂是____(填“Ca(OH)2”或“Ba(OH)2”)溶液。
更新时间:2016-12-08 23:09:58
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】电冶金
利用电解熔融盐或氧化物的方法来冶炼活泼金属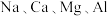 等.
等.
利用电解熔融盐或氧化物的方法来冶炼活泼金属
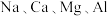 等.
等.| 总反应化学方程式 | 阳极、阴极反应式 | |
| 冶炼钠 | 阳极: 阴极: | |
| 冶炼镁 | 阳极: 阴极: | |
| 冶炼铝 | 阳极: 阴极: |
您最近一年使用:0次
【推荐2】(1)下列有关电化学的图示中,完全正确的是_____________
A.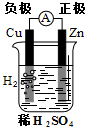 Cu-Zn原电池 B.
Cu-Zn原电池 B.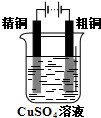 粗铜精炼
粗铜精炼
C.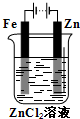 铁片镀锌 D.
铁片镀锌 D.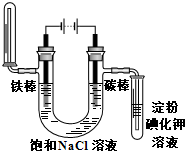 验证气体产物
验证气体产物
(2)碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中可与碘化物作用生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如图所示。
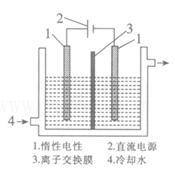
请回答下列问题:
a.碘是_________ (填颜色)固体物质,实验室常用_______ 方法来分离提纯含有少量泥沙杂质的固体碘。
b.电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:3I2+6KOH==5KI+KIO3+3H2O,将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。
电解时,阳极上发生反应的电极反应式为________ ,每生成1mol KIO3,电路中通过的电子的物质的量为________ 。
c.电解过程中,为确定电解是否完成,需检验电解液中是否有I-。请设计一个检验电解液中是否有I-的简单实验方案,并按要求填写下表。
可供选择的试剂:淀粉溶液、淀粉-KI试纸、过氧化氢溶液、稀硫酸(用其中的一种或多种均可。)
d.电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:
阳极电解液→①蒸发浓缩→②→③过滤→④洗涤→⑤→碘酸钾晶体
步骤②的操作名称是______________ ,步骤⑤的操作名称是________ 。步骤④洗涤晶体的目的是_________________ 。
A.
 Cu-Zn原电池 B.
Cu-Zn原电池 B. 粗铜精炼
粗铜精炼C.
 铁片镀锌 D.
铁片镀锌 D. 验证气体产物
验证气体产物(2)碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中可与碘化物作用生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如图所示。

请回答下列问题:
a.碘是
b.电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:3I2+6KOH==5KI+KIO3+3H2O,将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。
电解时,阳极上发生反应的电极反应式为
c.电解过程中,为确定电解是否完成,需检验电解液中是否有I-。请设计一个检验电解液中是否有I-的简单实验方案,并按要求填写下表。
可供选择的试剂:淀粉溶液、淀粉-KI试纸、过氧化氢溶液、稀硫酸(用其中的一种或多种均可。)
| 实验方法 | 实验现象及结论 |
d.电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:
阳极电解液→①蒸发浓缩→②→③过滤→④洗涤→⑤→碘酸钾晶体
步骤②的操作名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y 都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:
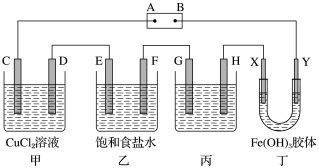
(1)电源A 极的名称是________ 。
(2)甲装置中电解反应的总化学方程式是__________________ 。
(3)如果收集乙装置中产生的气体,两种气体的体积比是________ 。
(4)欲用丙装置精炼铜,G应该是____ (填“纯铜”或“粗铜”),电解液的成分是______ 。
(5)已知氢氧化铁胶体中含有带正电荷的红褐色的粒子,那么装置丁中的现象是________________ 。
(6)在实验室电解500 mL 0.03 mol/L的NaCl溶液,通电一段时间后溶液中c(OH-)为1×10-2 mol/L(设电解时溶液的体积变化忽略不计),阴极产生___ mL(标况)气体,溶液中NaCl的浓度为_______ mol/L。

(1)电源A 极的名称是
(2)甲装置中电解反应的总化学方程式是
(3)如果收集乙装置中产生的气体,两种气体的体积比是
(4)欲用丙装置精炼铜,G应该是
(5)已知氢氧化铁胶体中含有带正电荷的红褐色的粒子,那么装置丁中的现象是
(6)在实验室电解500 mL 0.03 mol/L的NaCl溶液,通电一段时间后溶液中c(OH-)为1×10-2 mol/L(设电解时溶液的体积变化忽略不计),阴极产生
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求回答下列问题
(1)已知下列热化学方程式:
①2H2(g)+O2(g)= 2H2O(l) △H = -571.6kJ·mol-1
②C(s)+ O2(g)= CO2(g) △H = -393.5kJ·mol-1
③C(s)+ H2O(g) = CO(g)+ H2(g) △H = +131.5kJ·mol-1
上述反应中属于放热反应的是____ (填序号,下同),属于吸热反应的是____ 。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ∆H=-1275.6kJ·mol-1
②H2O(l)=H2O(g) ∆H=+44.0 kJ·mol-1
写出表示甲醇燃烧热的热化学方程式_______ 。
(3)依据事实,写出下列反应的热化学方程式。
①1molN2(g)适量O2(g)反应生成NO(g),需吸收68 kJ的热量,该反应的热化学方程式为_______ 。
②在25℃、101kpa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为______ 。
(1)已知下列热化学方程式:
①2H2(g)+O2(g)= 2H2O(l) △H = -571.6kJ·mol-1
②C(s)+ O2(g)= CO2(g) △H = -393.5kJ·mol-1
③C(s)+ H2O(g) = CO(g)+ H2(g) △H = +131.5kJ·mol-1
上述反应中属于放热反应的是
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ∆H=-1275.6kJ·mol-1
②H2O(l)=H2O(g) ∆H=+44.0 kJ·mol-1
写出表示甲醇燃烧热的热化学方程式
(3)依据事实,写出下列反应的热化学方程式。
①1molN2(g)适量O2(g)反应生成NO(g),需吸收68 kJ的热量,该反应的热化学方程式为
②在25℃、101kpa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】依据事实,写出下列反应的热化学方程式。
(1)在101 kPa时,H2在1.00 mol O2中完全燃烧生成2.00 mol液态H2O,放出571.6 kJ的热量,表示H2燃烧热的热化学方程式为___________________ 。
(2)卫星发射时可用肼(N2H4)为燃料,3.2 g N2H4(气态)在O2(气态)中燃烧,生成N2(气态)和H2O(气态),放出53.4 kJ的热量___________________ 。
(3)已知CO(g)和CH3OH(l)的燃烧热ΔH分别为-283.0kJ·mol-1和-726.5kJ·mol-1。写出CH3OH(l)不完全燃烧生成CO和液态水的热化学方程式___________________ 。
(4)已知稀溶液中,1mol H2SO4与NaOH溶液恰好完全反应时,放出114.6kJ的热量,表示其中和热的热化学方程式___________________ 。
(5)已知:C(s)+O2(g)=CO2(g) ΔH=-437.3 kJ·mol-1
H2(g)+ O2(g)=H2O(g) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(g) ΔH=-285.8 kJ·mol-1
CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
则碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式是___________________ 。
(6)NaBH4(s)与H2O(l)反应生成NaBO2(s)和H2(g)。在25 ℃、101 kPa下,已知每消耗3.8 g NaBH4(s)放热21.6 kJ,该反应的热化学方程式是___________________ 。
(1)在101 kPa时,H2在1.00 mol O2中完全燃烧生成2.00 mol液态H2O,放出571.6 kJ的热量,表示H2燃烧热的热化学方程式为
(2)卫星发射时可用肼(N2H4)为燃料,3.2 g N2H4(气态)在O2(气态)中燃烧,生成N2(气态)和H2O(气态),放出53.4 kJ的热量
(3)已知CO(g)和CH3OH(l)的燃烧热ΔH分别为-283.0kJ·mol-1和-726.5kJ·mol-1。写出CH3OH(l)不完全燃烧生成CO和液态水的热化学方程式
(4)已知稀溶液中,1mol H2SO4与NaOH溶液恰好完全反应时,放出114.6kJ的热量,表示其中和热的热化学方程式
(5)已知:C(s)+O2(g)=CO2(g) ΔH=-437.3 kJ·mol-1
H2(g)+
 O2(g)=H2O(g) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(g) ΔH=-285.8 kJ·mol-1CO(g)+
 O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1则碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式是
(6)NaBH4(s)与H2O(l)反应生成NaBO2(s)和H2(g)。在25 ℃、101 kPa下,已知每消耗3.8 g NaBH4(s)放热21.6 kJ,该反应的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.现有下列物质①熔化的NaCl②盐酸③氯气④冰醋酸⑤铜⑥酒精⑦硫酸氢钠⑧液氨⑨SO2⑩Al2O3,请按要求回答下列问题。
(1)属于强电解质的是_______ (填序号)
(2)在上述状态下能导电的是_______ (填序号)
(3)属于非电解质,但溶于水后的水溶液能导电的是_______ (填序号)
II.工业合成氨N2(g)+3H2(g) 2NH3(g) ∆H=-92.2kJ∙mol-1,一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示:
2NH3(g) ∆H=-92.2kJ∙mol-1,一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示:
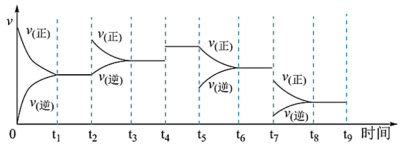
(4)其中 t4时刻所对应的实验条件改变是_____ ,t5时刻所对应的实验条件改变是_____ ,平衡常数最大的时间段是_____ 。
(5)为了提高平衡混合物中氨的含量,根据化学平衡移动原理,仅从理论上分析合成氨适宜的条件是_______(填字母)。
(6)实际生产中一般采用的反应条件为400~500℃,原因是_______ 。
(1)属于强电解质的是
(2)在上述状态下能导电的是
(3)属于非电解质,但溶于水后的水溶液能导电的是
II.工业合成氨N2(g)+3H2(g)
 2NH3(g) ∆H=-92.2kJ∙mol-1,一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示:
2NH3(g) ∆H=-92.2kJ∙mol-1,一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示:
(4)其中 t4时刻所对应的实验条件改变是
(5)为了提高平衡混合物中氨的含量,根据化学平衡移动原理,仅从理论上分析合成氨适宜的条件是_______(填字母)。
| A.高温低压 | B.低温高压 | C.高温高压 | D.低温低压 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同但形状不同的MnO2分别加入盛有15 mL 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
(1)该反应是___________ 反应(填放热或吸热)。
(2)实验结果表明,粉末状催化剂的催化效果比较好,原因是___________ 。
Ⅱ.某可逆反应在体积为2 L的密闭容器中进行,0~3分钟各物质的物质的量的变化情况如图所示(A、B、C均为气体)
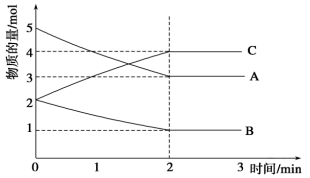
(3)该反应的化学方程式为___________ 。
(4)反应开始至2分钟末,用C的浓度变化表示的反应速率为___________ 。
(5)能说明该反应已达到平衡状态的是___________ (填字母符号)。
A.v(A)=2v(B) B.容器内压强保持不变
C.2v(A)逆=v(B)正 D.容器内混合气体的密度保持不变
(6)在密闭容器里,通入a mol A(g)、b mol B(g)、c mol C(g),发生上述反应,当改变下列条件时,反应速率会增大的是___________ (填字母符号)。
A.升高温度 B.加入催化剂 C.增大容器体积 D.通入不参加反应的其他气体,增大压强
| MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5 min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30 min |
(1)该反应是
(2)实验结果表明,粉末状催化剂的催化效果比较好,原因是
Ⅱ.某可逆反应在体积为2 L的密闭容器中进行,0~3分钟各物质的物质的量的变化情况如图所示(A、B、C均为气体)

(3)该反应的化学方程式为
(4)反应开始至2分钟末,用C的浓度变化表示的反应速率为
(5)能说明该反应已达到平衡状态的是
A.v(A)=2v(B) B.容器内压强保持不变
C.2v(A)逆=v(B)正 D.容器内混合气体的密度保持不变
(6)在密闭容器里,通入a mol A(g)、b mol B(g)、c mol C(g),发生上述反应,当改变下列条件时,反应速率会增大的是
A.升高温度 B.加入催化剂 C.增大容器体积 D.通入不参加反应的其他气体,增大压强
您最近一年使用:0次
【推荐3】反应 可用于汽车尾气净化。在恒温恒容密闭容器中加入一定量反应物,获得如下数据:
可用于汽车尾气净化。在恒温恒容密闭容器中加入一定量反应物,获得如下数据:
(1)
___________ ,
___________ 。
(2)CO的平衡转化率为___________ 。
(3)该温度下该反应的K的数值为___________ 。
(4)该温度下,按未知浓度配比进行反应,某时刻测得如下数据:
此时反应向___________ 方向(填“正反应”或者“逆反应”)进行,结合计算说明理由:___________ 。
 可用于汽车尾气净化。在恒温恒容密闭容器中加入一定量反应物,获得如下数据:
可用于汽车尾气净化。在恒温恒容密闭容器中加入一定量反应物,获得如下数据: |  |  |  | |
起始时各物质的物质的量浓度/( ) ) | 0.4 | 0.4 | 0 | 0 |
平衡时各物质的物质的量浓度/( ) ) | 0.2 | x | y | z |


(2)CO的平衡转化率为
(3)该温度下该反应的K的数值为
(4)该温度下,按未知浓度配比进行反应,某时刻测得如下数据:
 |  | 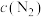 |  | |
某时刻各物质的物质的量浓度/( ) ) | 0.5 | 0.5 | 0.1 | 0.5 |
您最近一年使用:0次

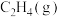 与适量
与适量 反应,生成
反应,生成 和
和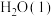 ,放出1411kJ的热量
,放出1411kJ的热量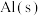 与适量
与适量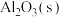 ,放出834.9kJ的热量
,放出834.9kJ的热量

