I.现有下列物质①熔化的NaCl②盐酸③氯气④冰醋酸⑤铜⑥酒精⑦硫酸氢钠⑧液氨⑨SO2⑩Al2O3,请按要求回答下列问题。
(1)属于强电解质的是_______ (填序号)
(2)在上述状态下能导电的是_______ (填序号)
(3)属于非电解质,但溶于水后的水溶液能导电的是_______ (填序号)
II.工业合成氨N2(g)+3H2(g) 2NH3(g) ∆H=-92.2kJ∙mol-1,一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示:
2NH3(g) ∆H=-92.2kJ∙mol-1,一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示:
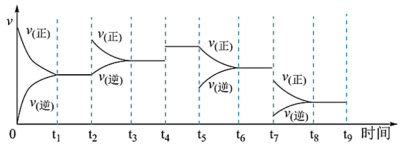
(4)其中 t4时刻所对应的实验条件改变是_____ ,t5时刻所对应的实验条件改变是_____ ,平衡常数最大的时间段是_____ 。
(5)为了提高平衡混合物中氨的含量,根据化学平衡移动原理,仅从理论上分析合成氨适宜的条件是_______(填字母)。
(6)实际生产中一般采用的反应条件为400~500℃,原因是_______ 。
(1)属于强电解质的是
(2)在上述状态下能导电的是
(3)属于非电解质,但溶于水后的水溶液能导电的是
II.工业合成氨N2(g)+3H2(g)
 2NH3(g) ∆H=-92.2kJ∙mol-1,一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示:
2NH3(g) ∆H=-92.2kJ∙mol-1,一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如图所示:
(4)其中 t4时刻所对应的实验条件改变是
(5)为了提高平衡混合物中氨的含量,根据化学平衡移动原理,仅从理论上分析合成氨适宜的条件是_______(填字母)。
| A.高温低压 | B.低温高压 | C.高温高压 | D.低温低压 |
更新时间:2022-10-12 17:34:51
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有以下物质:①NaHSO4晶体,②液态O2 ,③冰醋酸(固态醋酸), ④汞,⑤BaSO4固体,⑥Fe(OH)3 胶体,⑦酒精(C2H5OH) ,⑧熔化KNO3,⑨盐酸,⑩金属钠,请回答下列问题(用序号):
(1)以上物质中能导电的是__________
(2)以上物质属于电解质的是_____________
(3)以上物质中属于非电解质的是_______
(4)请写出①在熔融状态下的电离方程式________________
(5)a. 写出制备⑥的实验操作为_________ ;
b. 制备⑥的离子方程式为____________________ ,
c. 在制得的⑥中逐滴加入稀硫酸的实验现象为_____________________________ 。
(6)写出⑩在加热条件下与氧气反应的化学方程式________________________ 。若将2.3克钠放入97.7克水中,生成的溶液中溶质的质量分数_________ (填“大于”、“小于” 或“等于”)2.3%。
(7)标准状况下,CO与CO2相对于②的密度为1,则混合气体中CO与CO2的比例为_________ 。
(1)以上物质中能导电的是
(2)以上物质属于电解质的是
(3)以上物质中属于非电解质的是
(4)请写出①在熔融状态下的电离方程式
(5)a. 写出制备⑥的实验操作为
b. 制备⑥的离子方程式为
c. 在制得的⑥中逐滴加入稀硫酸的实验现象为
(6)写出⑩在加热条件下与氧气反应的化学方程式
(7)标准状况下,CO与CO2相对于②的密度为1,则混合气体中CO与CO2的比例为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有下列物质:① 碳棒 ② 盐酸 ③ H2SO4 ④氨水 ⑤ 熔融KOH ⑥ NH3 ⑦ CCl4 ⑧ CO2 ⑨冰醋酸 ⑩ NaHSO4固体
(1)上述物质中,可导电的是:_______________________ ;
(2)上述物质中,属于非电解质的是:_________________ ;
(3)上述物质中,属于电解质但不导电的是:_________________ ;
(4)上述物质中,属于弱电解质的是:__________________ ;
(5)写出 ⑨、⑩ 两种物质在水溶液中的电离方程式:
⑨:________________________________________________ ;
⑩:________________________________________________ 。
(1)上述物质中,可导电的是:
(2)上述物质中,属于非电解质的是:
(3)上述物质中,属于电解质但不导电的是:
(4)上述物质中,属于弱电解质的是:
(5)写出 ⑨、⑩ 两种物质在水溶液中的电离方程式:
⑨:
⑩:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下列物质中:A.KI(s) B.C2H5OH(l) C.Cl2(g) D.CH3COOH(l)E.BaSO4(s) F.NaHSO4(aq) G.石墨(s) H.蔗糖(s) I.NaOH(l) J.硫酸 K.盐酸
(1)属于非电解质的是____________ (填序号,下同),属于强电解质的是____________ ,属于弱电解质的是____________ 。
(2)能直接导电的是________________ ,电解质中能溶于水,且水溶液能导电是________________ 。
(1)属于非电解质的是
(2)能直接导电的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)有以下六种物质:①乙醇;②0.1mol/LNa2CO3溶液;③NaOH固体;④液态氯化氢;⑤纯CH3COOH;⑥石墨。上述状态下的物质中,能导电的有___________ (填序号,下同),属于电解质的有___________ 。
(2)磁性氧化铁的化学式___________ ,Fe2O3的俗称___________
(3)MgCl2的电子式是___________ HClO的结构式是___________ CO2 的空间构型是___________
(1)有以下六种物质:①乙醇;②0.1mol/LNa2CO3溶液;③NaOH固体;④液态氯化氢;⑤纯CH3COOH;⑥石墨。上述状态下的物质中,能导电的有
(2)磁性氧化铁的化学式
(3)MgCl2的电子式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)以下物质:①NaCl晶体 ②液态SO3 ③液态的醋酸 ④铝 ⑤BaSO4固体 ⑥稀盐酸 ⑦酒精(C2H5OH) ⑧熔融KNO3
其中属于电解质的是______ (填编号,下同),属于非电解质的是______ ,能导电的是_______ 。
(2)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中Fe2+发生________ 反应,说明亚硝酸钠具有______ 性;误食亚硝酸钠中毒,可服维生素C缓解,说明维生素C具有______ 性。
其中属于电解质的是
(2)人体血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能。亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+转化为Fe3+,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中Fe2+发生
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】尿素[CO(NH2)2]是首个由无机物人工合成的有机物。
(1)工业上用CO2和NH3在一定条件下合成,其反应方程式__________ 。
(2)在一个2L的密闭容器内,当起始投入量氨碳比 ,CO2的转化率随时间的变化关系如下图所示。
,CO2的转化率随时间的变化关系如下图所示。
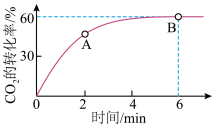
① A点的逆反应速率v逆(CO2)__________________ B点的正反应速率为v正(CO2)(填“大于”、“小于”或“等于”)
②假设氨的起始投入量为8mol,求从开始到达到平衡状态这段时间内v(NH3)=_________________ 。
③NH3的平衡转化率为____________________ 。
④单纯从制备的成本角度考虑,我们希望氨碳比 尽可能
尽可能__________ (“大”、“小”)因为_________ 。
(1)工业上用CO2和NH3在一定条件下合成,其反应方程式
(2)在一个2L的密闭容器内,当起始投入量氨碳比
 ,CO2的转化率随时间的变化关系如下图所示。
,CO2的转化率随时间的变化关系如下图所示。
① A点的逆反应速率v逆(CO2)
②假设氨的起始投入量为8mol,求从开始到达到平衡状态这段时间内v(NH3)=
③NH3的平衡转化率为
④单纯从制备的成本角度考虑,我们希望氨碳比
 尽可能
尽可能
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在400℃,1.01×105Pa时,将一定量的SO2和14molO2压入一个装有催化剂的VL密闭反应器中,发生2SO2+O2 2SO3的反应,并且在10min后达到平衡时,测得容器内有2molSO2和12molO2。
2SO3的反应,并且在10min后达到平衡时,测得容器内有2molSO2和12molO2。
(1)SO2的起始浓度为____ ,SO3(气)的平衡浓度为_____ ;
(2)平衡时SO3(气)占总体积的百分数为___ ,此时体系压强为反应起始时体系压强的____ 倍;
(3)10min时达到平衡后,压缩反应器体积为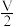 ,一段时间后,达到新的平衡,此时SO3(气)的浓度
,一段时间后,达到新的平衡,此时SO3(气)的浓度_ (大于、小于、等于)10min时SO3(气)浓度的2倍。
(4)10min时达到平衡后,保持容器体积不变,向容器中再充入1molSO2,O2的转化率___ (增大、减小、不变)
 2SO3的反应,并且在10min后达到平衡时,测得容器内有2molSO2和12molO2。
2SO3的反应,并且在10min后达到平衡时,测得容器内有2molSO2和12molO2。(1)SO2的起始浓度为
(2)平衡时SO3(气)占总体积的百分数为
(3)10min时达到平衡后,压缩反应器体积为
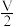 ,一段时间后,达到新的平衡,此时SO3(气)的浓度
,一段时间后,达到新的平衡,此时SO3(气)的浓度(4)10min时达到平衡后,保持容器体积不变,向容器中再充入1molSO2,O2的转化率
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在水溶液中橙色的Cr2O72-与黄色的CrO42-有下列平衡关系:Cr2O72-+H2O 2CrO42-+2H+把重铬酸钾K2Cr2O7溶于水配成的稀溶液是橙色的.
2CrO42-+2H+把重铬酸钾K2Cr2O7溶于水配成的稀溶液是橙色的.
(1)向上述溶液中加入NaOH溶液,溶液呈______ 色
(2)向已加入NaOH溶液的(1)溶液中再加入过量稀硫酸,则溶液呈______ 色
(3)向原溶液中逐渐加入足量硝酸钡溶液 已知BaCrO4为黄色沉淀
已知BaCrO4为黄色沉淀 ,则平衡
,则平衡 ______  填“向左移动”或“向右移动”
填“向左移动”或“向右移动” ,溶液颜色将
,溶液颜色将 ______ .
 2CrO42-+2H+把重铬酸钾K2Cr2O7溶于水配成的稀溶液是橙色的.
2CrO42-+2H+把重铬酸钾K2Cr2O7溶于水配成的稀溶液是橙色的.(1)向上述溶液中加入NaOH溶液,溶液呈

(2)向已加入NaOH溶液的(1)溶液中再加入过量稀硫酸,则溶液呈

(3)向原溶液中逐渐加入足量硝酸钡溶液
 已知BaCrO4为黄色沉淀
已知BaCrO4为黄色沉淀 ,则平衡
,则平衡  填“向左移动”或“向右移动”
填“向左移动”或“向右移动” ,溶液颜色将
,溶液颜色将
您最近一年使用:0次
【推荐1】除电解法,工业炼镁还可采用硅热法(Pidgeon法)。即以煅白(CaO·MgO)为原料与硅铁(含硅75%的硅铁合金)混合置于密闭还原炉,1200℃下发生反应:2(CaO·MgO)(s) + Si(s)  Ca2SiO4 (l) + 2Mg(g)
Ca2SiO4 (l) + 2Mg(g)
(1)已知还原性:Mg > Si,上述反应仍能发生的原因是______________________________________ 。
(2)由图,推测上述反应正向为______ (填“吸热”或“放热”) 反应;平衡后若其他条件不变,将还原炉体积缩小一半,则达到新平衡时Mg(g)的浓度将______ (填“升高” 、“降低”或“不变”)。

(3)如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,下列说法正确的是_____ (填序号)。
a. 反应物不再转化为生成物 b. 炉内Ca2SiO4与CaO·MgO的质量比保持不变
c. 平衡常数到达最大值 d. 单位时间内,n(CaO·MgO)消耗 : n(Ca2SiO4)生成 = 2 : 1
(4)若还原炉容积为400m3,原料中煅白质量为9.6 t,5小时后,测得煅白的转化率为50%,计算这段时间内Mg的生成速率___________ 。
 Ca2SiO4 (l) + 2Mg(g)
Ca2SiO4 (l) + 2Mg(g) (1)已知还原性:Mg > Si,上述反应仍能发生的原因是
(2)由图,推测上述反应正向为

(3)如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,下列说法正确的是
a. 反应物不再转化为生成物 b. 炉内Ca2SiO4与CaO·MgO的质量比保持不变
c. 平衡常数到达最大值 d. 单位时间内,n(CaO·MgO)消耗 : n(Ca2SiO4)生成 = 2 : 1
(4)若还原炉容积为400m3,原料中煅白质量为9.6 t,5小时后,测得煅白的转化率为50%,计算这段时间内Mg的生成速率
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图表示298K时,N2、H2与NH3的平均能量与合成氨反应的活化能的曲线图,据图回答下列问题:

(1)若反应中生成2mol氨,则反应____ (填“吸热”或“放热”)____ kJ。
(2)图中曲线____ (填“a”或“b”)表示加入铁触媒的能量变化曲线,铁触媒能加快反应速率的原理是_____ 。
(3)合成氨反应中平衡混合物中氨的体积分数与压强、温度的关系如图所示。若曲线a对应的温度为500℃,则曲线b对应的温度可能是_____ (填字母)。


(1)若反应中生成2mol氨,则反应
(2)图中曲线
(3)合成氨反应中平衡混合物中氨的体积分数与压强、温度的关系如图所示。若曲线a对应的温度为500℃,则曲线b对应的温度可能是

| A.600℃ | B.550℃ | C.500℃ | D.450℃ |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】甲醇是一种重要的化工原料,具有开发和应用的广阔前景。工业上使用水煤气(CO与H2的混合气体)转化成甲醇,反应为CO(g)+2H2(g)⇌CH3OH(g) △H。在体积可变的密闭容器中投入0.5molCO和0.75molH2,不同条件下发生上述反应。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图所示。
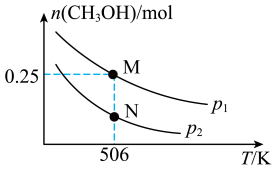
(1)根据图象判断△H_______ 0(填“<”或“>”);M点H2的转化率为_______ 。
(2)M点对应的平衡混合气体的体积为1L,则506K时该反应平衡常数K=_______ 。
(3)下列叙述能说明上述反应达到化学平衡状态的_______ (填字母序号)。
a.v(H2)=2v(CH3OH)
b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变
(4)平衡后再加入0.5molCO和0.75molH2后重新到达平衡,则CO的转化率_______ (填“增大”、“不变”或“减小”)。

(1)根据图象判断△H
(2)M点对应的平衡混合气体的体积为1L,则506K时该反应平衡常数K=
(3)下列叙述能说明上述反应达到化学平衡状态的
a.v(H2)=2v(CH3OH)
b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变
(4)平衡后再加入0.5molCO和0.75molH2后重新到达平衡,则CO的转化率
您最近一年使用:0次



