将某黄铜矿(主要成分为CuFeS2)和O2在一定温度范围内发生反应,反应所得固体混合物X中含有CuSO4、FeSO4、Fe2(SO4)3及少量SiO2等,除杂后可制得纯净的胆矾晶体(CuSO4·5H2O)。
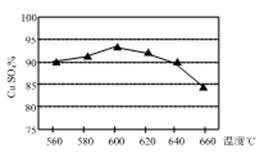
(1)实验测得温度对反应所得固体混合物中水溶性铜(CuSO4)的含量的影响如图所示。生产过程中应将温度控制在_____ 左右,温度升高至一定程度后,水溶性铜含量下降的可能原因是_____ 。
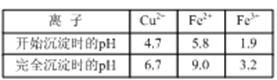
(2)下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。实验中可选用的试剂和用品:稀硫酸、3 % H2O2溶液、CuO、玻璃棒、精密pH试纸。
①实验时需用约3 %的H2O2溶液100 mL,现用市售30%(密度近似为1g•cm-3)的H2O2来配制,其具体配制方法是_____ 。
②补充完整由反应所得固体混合物X制得纯净胆矾晶体的实验步骤:
第一步:将混合物加入过量稀硫酸,搅拌、充分反应,过滤。
第二步:_____ 。
第三步:_____ ,过滤。
第四步:_____ 、冷却结晶。
第五步:过滤、洗涤,低温干燥。
(3)在酸性、有氧条件下,一种叫Thibacillus ferroxidans的细菌能将黄铜矿转化成硫酸盐,该过程反应的离子方程式为_________ 。
(1)实验测得温度对反应所得固体混合物中水溶性铜(CuSO4)的含量的影响如图所示。生产过程中应将温度控制在

(2)下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。实验中可选用的试剂和用品:稀硫酸、3 % H2O2溶液、CuO、玻璃棒、精密pH试纸。

①实验时需用约3 %的H2O2溶液100 mL,现用市售30%(密度近似为1g•cm-3)的H2O2来配制,其具体配制方法是
②补充完整由反应所得固体混合物X制得纯净胆矾晶体的实验步骤:
第一步:将混合物加入过量稀硫酸,搅拌、充分反应,过滤。
第二步:
第三步:
第四步:
第五步:过滤、洗涤,低温干燥。
(3)在酸性、有氧条件下,一种叫Thibacillus ferroxidans的细菌能将黄铜矿转化成硫酸盐,该过程反应的离子方程式为
更新时间:2019-01-30 18:14:09
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】某研究小组同学在实验室用卤块制备少量Mg(ClO3)2·6H2O,其流程如图所示:
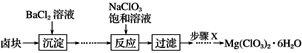
已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
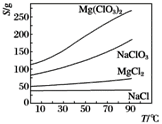
②四种化合物的溶解度(S)随温度(T)的变化曲线如图所示。
③形成氢氧化物沉淀时,不同离子对应溶液的pH如下:Fe2+开始沉淀的pH为5.8,完全沉淀的pH为8.8;Fe3+开始沉淀的pH为1.1,完全沉淀的pH为3.2;Mg2+开始沉淀的pH为8.2,完全沉淀的pH为11。
④可选用的试剂:H2O2、稀硫酸、KMnO4溶液、MgCl2溶液、MgO。
(1)步骤X包含的操作为___________ 、 ___________ 、____________ 、过滤洗涤并干燥。
(2)加入BaCl2溶液沉淀后需经过两步实验步骤才进行下步反应,请写出这两步实验步骤:
①________________________________________________________________________ ;
②_______________________________________________________________________ ;
(3)加入NaClO3饱和溶液发生反应的化学方程式为_______________________________ 。
(4)将Mg(ClO3)2加入到含有KSCN的FeSO4溶液中立即出现红色,写出相关反应的离子方程式______________ 。

已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
②四种化合物的溶解度(S)随温度(T)的变化曲线如图所示。

③形成氢氧化物沉淀时,不同离子对应溶液的pH如下:Fe2+开始沉淀的pH为5.8,完全沉淀的pH为8.8;Fe3+开始沉淀的pH为1.1,完全沉淀的pH为3.2;Mg2+开始沉淀的pH为8.2,完全沉淀的pH为11。
④可选用的试剂:H2O2、稀硫酸、KMnO4溶液、MgCl2溶液、MgO。
(1)步骤X包含的操作为
(2)加入BaCl2溶液沉淀后需经过两步实验步骤才进行下步反应,请写出这两步实验步骤:
①
②
(3)加入NaClO3饱和溶液发生反应的化学方程式为
(4)将Mg(ClO3)2加入到含有KSCN的FeSO4溶液中立即出现红色,写出相关反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】湿式吸收一电解再生法,是采用氧化一电解的双反应器对含硫化氢的废气进行脱硫制氢。实验表明,双反应器法可以在较宽的范围内实现对硫化氢的有效吸收,并可同时制取氢气和硫磺,该法基本流程见图l,其中氧化吸收器中为FeCl3溶液,电解反应器可实现FeCl3溶液的恢复及H2的制备。
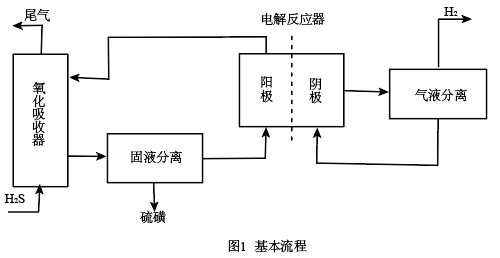
(1)氧化反应器中发生的主要反应的离子有程式为________
(2)电解反应器中,阳极反应式是________
(3)某研究小组在实验室中模拟上述过程,研究FeCl3溶液吸收H2S气体的效率,实验时要先向FeCl3溶液中通入N2,其目的是________ 。对影响吸收效率的因素提出如下假设,请你完成假设二和假设三:
假设一:H2S气体的通入速率;
假设二:______________ ;
假设三:______________ 。
请你设计实验就假设一进行验证,将实验步骤及结论补充完整(注:可用pH计测量溶液中的H+浓度)
(4)将FeCl3溶液吸收H2S气体后的溶液过滤后,取少量向其中加入BaCl2溶液,发现有白色沉淀生成(注:BaS溶于盐酸)。则白色沉淀可能是_______ 你的判断理由是_______

(1)氧化反应器中发生的主要反应的离子有程式为
(2)电解反应器中,阳极反应式是
(3)某研究小组在实验室中模拟上述过程,研究FeCl3溶液吸收H2S气体的效率,实验时要先向FeCl3溶液中通入N2,其目的是
假设一:H2S气体的通入速率;
假设二:
假设三:
请你设计实验就假设一进行验证,将实验步骤及结论补充完整(注:可用pH计测量溶液中的H+浓度)
| 实验步骤及结论 别取等体积、等浓度的FeCl3溶液于不同的试管中; ② ③ ④ ⑤结论: |
(4)将FeCl3溶液吸收H2S气体后的溶液过滤后,取少量向其中加入BaCl2溶液,发现有白色沉淀生成(注:BaS溶于盐酸)。则白色沉淀可能是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】氮化硅可用作高温陶瓷复合材料,在航空航天、汽车发动机、军事工业等领域有着广泛的应用。由石英砂合成氮化硅粉末的路线如图所示。

其中—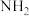 中各元素的化合价与
中各元素的化合价与 相同。请回答下列问题:
相同。请回答下列问题:
(1)石英砂不能与碱性物质共同存放,以NaOH为例,用化学方程式解释其原因:___________ 。
(2)图示①~④的变化中,属于氧化还原反应的是___________ 。
(3)反应①的化学方程式为___________ 。
(4) 在潮湿的空气中剧烈水解,产生白雾,在军事工业中用于制造烟雾剂。
在潮湿的空气中剧烈水解,产生白雾,在军事工业中用于制造烟雾剂。 和水反应的化学方程式为
和水反应的化学方程式为___________ 。
(5)在反应⑤中,3 mol 在高温下加热可得1mol氮化硅粉末和8molA气体,则氮化硅的化学式为
在高温下加热可得1mol氮化硅粉末和8molA气体,则氮化硅的化学式为___________ 。

其中—
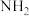 中各元素的化合价与
中各元素的化合价与 相同。请回答下列问题:
相同。请回答下列问题:(1)石英砂不能与碱性物质共同存放,以NaOH为例,用化学方程式解释其原因:
(2)图示①~④的变化中,属于氧化还原反应的是
(3)反应①的化学方程式为
(4)
 在潮湿的空气中剧烈水解,产生白雾,在军事工业中用于制造烟雾剂。
在潮湿的空气中剧烈水解,产生白雾,在军事工业中用于制造烟雾剂。 和水反应的化学方程式为
和水反应的化学方程式为(5)在反应⑤中,3 mol
 在高温下加热可得1mol氮化硅粉末和8molA气体,则氮化硅的化学式为
在高温下加热可得1mol氮化硅粉末和8molA气体,则氮化硅的化学式为
您最近一年使用:0次
【推荐1】利用某含铁矿渣(Fe2O3约40%、Al2O3约10%、MgO约5%、SiO2约45%)制备草酸合铁(III)酸钾晶体{化学式为K3[Fe(C2O4)3·3H2O]}的流程如下:
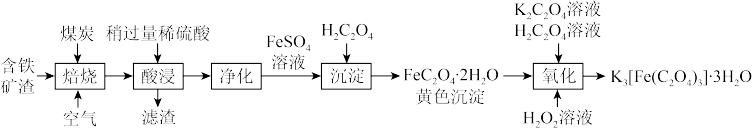
已知:草酸合铁(Ⅲ)酸钾晶体易溶于水且溶解度随温度升高明显增大,难溶于乙醇,对光敏感,光照下即发生分解;草酸钾微溶于乙醇。
回答下列问题:
(1)“焙烧”的目的是_______ ;滤渣的主要成分为_______ (写化学式)。
(2)“净化”时,滴加氨水除去Al3+,若常温时, Ksp[Al(OH)3]=1.0 ×10-32,理论上使Al3+恰好沉淀完全[即溶液中c(A13+ )=1×10-5 mol· L-1]时,溶液的pH为_______ 。
(3)“氧化”这一步 ,是依次加入一定量的饱和K2C2O4溶液、H2C2O4溶液、3%H2O2溶液,不断搅拌溶液并维持在40℃左右。充分反应后,沉淀溶解,溶液的pH保持在4~5,此时溶液呈翠绿色,趁热将溶液过滤到烧杯中,_______ (补充必要的步骤) ,得草酸合铁( III )酸钾晶体。
(4)写出“氧化”时反应的离子方程式:_______ ;“氧化”时,加入H2O2溶液的量过多,会使产品纯度下降的原因是_______ 。
(5)草酸合铁(Ⅲ )酸钾晶体光照下立即发生分解生成两种草酸盐 、CO2等,写出该反应的化学方程式:_______ 。

已知:草酸合铁(Ⅲ)酸钾晶体易溶于水且溶解度随温度升高明显增大,难溶于乙醇,对光敏感,光照下即发生分解;草酸钾微溶于乙醇。
回答下列问题:
(1)“焙烧”的目的是
(2)“净化”时,滴加氨水除去Al3+,若常温时, Ksp[Al(OH)3]=1.0 ×10-32,理论上使Al3+恰好沉淀完全[即溶液中c(A13+ )=1×10-5 mol· L-1]时,溶液的pH为
(3)“氧化”这一步 ,是依次加入一定量的饱和K2C2O4溶液、H2C2O4溶液、3%H2O2溶液,不断搅拌溶液并维持在40℃左右。充分反应后,沉淀溶解,溶液的pH保持在4~5,此时溶液呈翠绿色,趁热将溶液过滤到烧杯中,
(4)写出“氧化”时反应的离子方程式:
(5)草酸合铁(Ⅲ )酸钾晶体光照下立即发生分解生成两种草酸盐 、CO2等,写出该反应的化学方程式:
您最近一年使用:0次
【推荐2】钒铬还原渣是钠化提钒过程的固体废弃物,主要成分为VO2•xH2O、Cr(OH)3及少量SiO2。用钒铬还原渣获得Na2Cr2O7•2H2O和V2O5•xH2O的工艺流程如图:

已知:①“酸浸”初始温度为70℃,VO2•xH2O转化为VO2+;
②Ksp[Cr(OH)3]=1×10-30。
回答下列问题:
(1)“滤渣”的主要成分是____ ,提高“酸浸”时的浸出率,可采用的措施有____ (答出1条即可).
(2)“氧化”时生成 ,发生反应的离方程式为
,发生反应的离方程式为____ 。
(3)“含Cr3+净化液”中c(Cr3+)=0.001 mol•L-1,则“水解沉钒”调pH最大值不超过____ 。
(4)“一系列操作”包括蒸发浓缩、____ 、干燥。
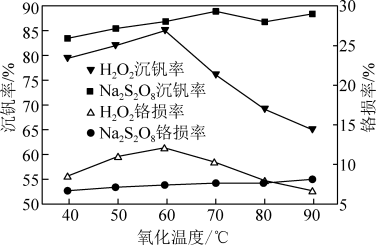
(5)查阅资料发现“氧化”时用Na2S2O8代替H2O2更好,温度对沉钒、铬损的影响如图所示,用Na2S2O8进行“氧化”时,应选择的适宜温度为____ ,选用Na2S2O8的原因是____ 。

已知:①“酸浸”初始温度为70℃,VO2•xH2O转化为VO2+;
②Ksp[Cr(OH)3]=1×10-30。
回答下列问题:
(1)“滤渣”的主要成分是
(2)“氧化”时生成
 ,发生反应的离方程式为
,发生反应的离方程式为(3)“含Cr3+净化液”中c(Cr3+)=0.001 mol•L-1,则“水解沉钒”调pH最大值不超过
(4)“一系列操作”包括蒸发浓缩、
(5)查阅资料发现“氧化”时用Na2S2O8代替H2O2更好,温度对沉钒、铬损的影响如图所示,用Na2S2O8进行“氧化”时,应选择的适宜温度为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】高铁酸钾(K2FeO4)是一种高效且多功能的新型绿色净水剂,一种以Mn、Fe及MnO2制备高铁酸钾和重要的催化剂MnO2的流程如下图所示:
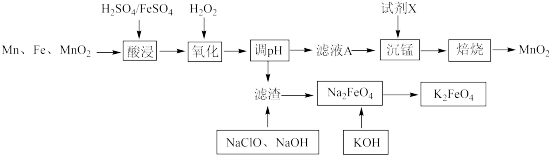
已知:部分金属离子在溶液中沉淀的pH见下表。

回答下列问题:
(1)酸浸的目的是在酸性条件下 将
将 还原成稳定的
还原成稳定的 ,写出该反应的离子方程式:
,写出该反应的离子方程式:_______ 。
(2)调节pH的范围是_______ ,由滤渣生成 的离子方程式为
的离子方程式为_______ 。
(3)已知试剂X为 ,分析当温度超过60℃时,锰沉淀率随温度升高下降的原因是
,分析当温度超过60℃时,锰沉淀率随温度升高下降的原因是_______ ,若用 替代试剂X,沉锰得到的固体混合物中可能会混有
替代试剂X,沉锰得到的固体混合物中可能会混有_______ 杂质。
(4)某温度下,若要从 含
含 的循环母液中沉淀
的循环母液中沉淀 (浓度降至
(浓度降至 ),理论上需加入
),理论上需加入 固体的物质的量不少于
固体的物质的量不少于_______ mol。(已知该温度下 的
的 ,不考虑水解和溶液体积变化)
,不考虑水解和溶液体积变化)
(5)在水处理中, 中的铁元素转化为
中的铁元素转化为 胶体,使水中悬浮颗粒聚沉。胶体区别于其他分散系的本质特征是
胶体,使水中悬浮颗粒聚沉。胶体区别于其他分散系的本质特征是_______ 。

已知:部分金属离子在溶液中沉淀的pH见下表。
| 金属离子 |  |  |  |
| 开始沉淀的pH | 1.9 | 7.0 | 8.1 |
| 完全沉淀的pH | 3.2 | 9.0 | 10.1 |

回答下列问题:
(1)酸浸的目的是在酸性条件下
 将
将 还原成稳定的
还原成稳定的 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(2)调节pH的范围是
 的离子方程式为
的离子方程式为(3)已知试剂X为
 ,分析当温度超过60℃时,锰沉淀率随温度升高下降的原因是
,分析当温度超过60℃时,锰沉淀率随温度升高下降的原因是 替代试剂X,沉锰得到的固体混合物中可能会混有
替代试剂X,沉锰得到的固体混合物中可能会混有(4)某温度下,若要从
 含
含 的循环母液中沉淀
的循环母液中沉淀 (浓度降至
(浓度降至 ),理论上需加入
),理论上需加入 固体的物质的量不少于
固体的物质的量不少于 的
的 ,不考虑水解和溶液体积变化)
,不考虑水解和溶液体积变化)(5)在水处理中,
 中的铁元素转化为
中的铁元素转化为 胶体,使水中悬浮颗粒聚沉。胶体区别于其他分散系的本质特征是
胶体,使水中悬浮颗粒聚沉。胶体区别于其他分散系的本质特征是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】海洋资源的利用具有广阔前景.
(1)如图是从海水中提取镁的简单流程.

工业上常用于沉淀Mg2+的试剂A是______ (填物质名称),Mg(OH)2转化为MgCl2的离子方程式是______ .
(2)海带灰中富含以I﹣形式存在的碘元素。实验室提取I2的途径如下所示:
干海带 海带灰
海带灰 滤液
滤液
 I2
I2
①灼烧海带至灰烬时所用的主要仪器名称是______ .
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式______ .
③反应结束后,加入CCl4作萃取剂,采用萃取﹣分液的方法从碘水中提取碘,主要操作步骤如图:
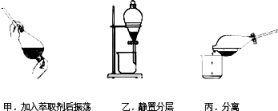
甲、乙、丙3步实验操作中,不正确的是______ (填“甲”、“乙”或“丙”).
(1)如图是从海水中提取镁的简单流程.

工业上常用于沉淀Mg2+的试剂A是
(2)海带灰中富含以I﹣形式存在的碘元素。实验室提取I2的途径如下所示:
干海带
 海带灰
海带灰 滤液
滤液
 I2
I2①灼烧海带至灰烬时所用的主要仪器名称是
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
③反应结束后,加入CCl4作萃取剂,采用萃取﹣分液的方法从碘水中提取碘,主要操作步骤如图:

甲、乙、丙3步实验操作中,不正确的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】某研究性学习小组为了测定某品牌铝合金(主要成分为Al2O3、MgO、CuO、SiO2)中铝的含量,现设计了如下实验:
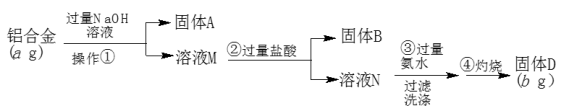
请回答下列问题:
(1)固体A的成分是_______ (填写化学式);操作①的名称是_______ 。
(2)步骤③中生成沉淀的离子方程式为_______ 。
(3)固体B的主要成分为_______ (填写化学式)。
(4)该样品中铝的质量分数是_______ 。(用含a、b代数式表示)

请回答下列问题:
(1)固体A的成分是
(2)步骤③中生成沉淀的离子方程式为
(3)固体B的主要成分为
(4)该样品中铝的质量分数是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
I.(1)取一定量氯化亚铁固体,配制成0.1 mol/L 的溶液。检验溶液是否被氧化的方法:_______ 。
II.工业上用赤铁矿(含Fe2O3、FeO,也含有Al2O3、MnO2、CuO等)制备绿矾FeSO4·7H2O的流程如下:
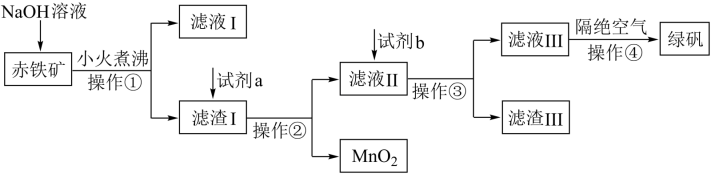
(2)氢氧化钠溶液加入赤铁矿中发生反应的离子方程式为_______ 。
(3)向滤渣I中加入过量的试剂a为_______ ,试剂b要加入过量,试剂b为_______ 。
(4)操作④隔绝空气的目的是_______ 。
Ⅲ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(5)干法制备高铁酸钠的主要反应为:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,该反应中Na2O2是_______ (填氧化剂、还原剂),与CO2反应的化学反应方程式_______ 。
(6)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O。
、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:_______ 。
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为_______ mol。
I.(1)取一定量氯化亚铁固体,配制成0.1 mol/L 的溶液。检验溶液是否被氧化的方法:
II.工业上用赤铁矿(含Fe2O3、FeO,也含有Al2O3、MnO2、CuO等)制备绿矾FeSO4·7H2O的流程如下:

(2)氢氧化钠溶液加入赤铁矿中发生反应的离子方程式为
(3)向滤渣I中加入过量的试剂a为
(4)操作④隔绝空气的目的是
Ⅲ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(5)干法制备高铁酸钠的主要反应为:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,该反应中Na2O2是
(6)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。
、Cl-、H2O。①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为
您最近一年使用:0次



