三颈瓶在化学实验中的应用非常广泛,下面是三颈瓶在部分无机实验或有机实验中的一些应用。
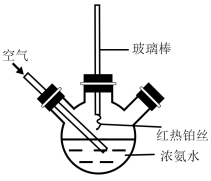
(1)在如图所示装置中,进行氨的催化氧化实验:向三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶子并接近液面。反应过程中可观察到瓶中有红棕色气体产生,铂丝始终保持红热。实验过程中NH3∙H2O的电离程度____ (填“变大”、“变小”或“不变”)
Ⅱ.实验室用下图所示装置制备氨基甲酸铵(NH2COONH4),其反应化学方程式:2NH3(g)+CO2(g) NH2COONH4(s)该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵。
NH2COONH4(s)该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵。
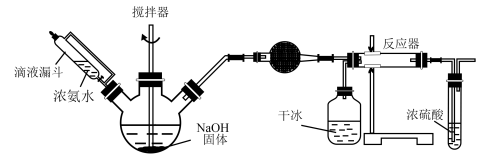
(2)写出加入药品之前实验操作的要点_______ ;反应中若有水存在则生成碳酸氢铵的化学方程式是________________________ 。
(3)干燥管中盛放的药品是______ 。简述左侧三颈瓶装置制取氨气的原理________ 。
(4)对比碳酸盐和酸的反应制取CO2,该实验利用干冰升华产生气体CO2的有优点有_____ .
(5)有同学认为该实验装置存在安全问题,请问可能面临的安全问题是________ 。
(6)氨基甲酸氨可用作肥料,其肥效比尿素[CO(NH2)2]_______ (填“高”或“低”),在潮湿的空气中释放出氨而变成碳酸氢铵。取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7830g,用足量石灰水充分处理后,使样品中碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000g,则样品中氨基甲酸铵的物质的量分数是_____________ 。
(1)在如图所示装置中,进行氨的催化氧化实验:向三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶子并接近液面。反应过程中可观察到瓶中有红棕色气体产生,铂丝始终保持红热。实验过程中NH3∙H2O的电离程度

Ⅱ.实验室用下图所示装置制备氨基甲酸铵(NH2COONH4),其反应化学方程式:2NH3(g)+CO2(g)
 NH2COONH4(s)该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵。
NH2COONH4(s)该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵。
(2)写出加入药品之前实验操作的要点
(3)干燥管中盛放的药品是
(4)对比碳酸盐和酸的反应制取CO2,该实验利用干冰升华产生气体CO2的有优点有
(5)有同学认为该实验装置存在安全问题,请问可能面临的安全问题是
(6)氨基甲酸氨可用作肥料,其肥效比尿素[CO(NH2)2]
更新时间:2016-12-09 07:57:35
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】Ⅰ.某化合物M(仅含三种短周期元素)是一种储氢材料。为探究M的组成和性质,设计并完成如下实验:
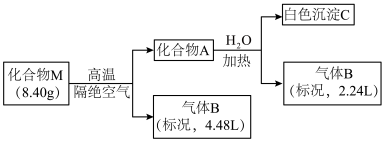
已知:化合物A仅含两种元素;气体B能使湿润的红色石蕊试纸变蓝。
请回答:(1)化合物M的组成元素是______________ (用元素符号表示)。
(2)化合物A与水反应的化学方程式是______________________ 。
(3)镁带在足量气体B中燃烧可生成化合物M和一种单质气体,该反应的化学方程式是______ 。
II.无机盐X仅由三种短周期元素组成,其相对分子质量为238,原子个数比为1︰1︰4。将23.8gX与水共热,生成一种有特殊臭味的气体单质A和某强酸的酸式盐溶液B,B的焰色反应呈黄色,在溶液B中加入足量的BaCl2溶液,产生46.6g白色沉淀。请推测并回答:
(4)单质A有很强的氧化性,可用于净化空气,饮用水消毒等。A中组成元素的简单离子结构示意图为___________________________ 。
(5)X的化学式_____________ 。
(6)实验室可通过低温电解B溶液制备X。该电解反应的化学方程式___________________ 。
(7)X氧化能力强,对环境友好,可用于脱硝、脱硫。在碱性条件下,X氧化NO的离子方程式_____________________ 。
(8)X溶液与铜反应时先慢后快。某同学认为除反应放热这一因素外,还有一种可能是反应生成的Cu2+对后续反应起催化作用,为此他设计了如下实验方案:取少量铜粉置于试管中,先加入少量CuSO4溶液,再加入X溶液,振荡,观察现象。若加入硫酸铜溶液的反应快,说明Cu2+起了催化作用,反之Cu2+不起作用。写出X与铜反应的化学方程式________ ,判断该同学设计的验证方法合理性并说明理由_________ 。

已知:化合物A仅含两种元素;气体B能使湿润的红色石蕊试纸变蓝。
请回答:(1)化合物M的组成元素是
(2)化合物A与水反应的化学方程式是
(3)镁带在足量气体B中燃烧可生成化合物M和一种单质气体,该反应的化学方程式是
II.无机盐X仅由三种短周期元素组成,其相对分子质量为238,原子个数比为1︰1︰4。将23.8gX与水共热,生成一种有特殊臭味的气体单质A和某强酸的酸式盐溶液B,B的焰色反应呈黄色,在溶液B中加入足量的BaCl2溶液,产生46.6g白色沉淀。请推测并回答:
(4)单质A有很强的氧化性,可用于净化空气,饮用水消毒等。A中组成元素的简单离子结构示意图为
(5)X的化学式
(6)实验室可通过低温电解B溶液制备X。该电解反应的化学方程式
(7)X氧化能力强,对环境友好,可用于脱硝、脱硫。在碱性条件下,X氧化NO的离子方程式
(8)X溶液与铜反应时先慢后快。某同学认为除反应放热这一因素外,还有一种可能是反应生成的Cu2+对后续反应起催化作用,为此他设计了如下实验方案:取少量铜粉置于试管中,先加入少量CuSO4溶液,再加入X溶液,振荡,观察现象。若加入硫酸铜溶液的反应快,说明Cu2+起了催化作用,反之Cu2+不起作用。写出X与铜反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】氨是重要的化工原料,回答下列问题:
I.氨气的制备

(1)制取并收集一瓶干燥氨气,上述装置的连接顺序为A→_____→_____→C→____,____ ,制气时的化学方程式为___________ ,收集时气体从___________ 口进入
II.氨气的性质
(2)装置如图所示,打开止水夹,用热毛巾将烧瓶捂热,水上喷形成红色喷泉,说明氨气___________ 。

III.氨气的用途
利用下图装置由氨制硝酸,实验时戊中溶液呈淡黄色时关闭分液漏斗活塞。

(3)Na2O2的作用___________ ,证明有硝酸生成的实验是___________ ,发生反应的离子方程式___________ 。
(4)实验中的氮氧化物(NOx)尾气折算成标准状况下的体积为aL,完全吸收时,烧杯中c(NaOH)至少是___________ mol/L(忽略溶液体积变化)。
I.氨气的制备

(1)制取并收集一瓶干燥氨气,上述装置的连接顺序为A→_____→_____→C→____,
II.氨气的性质
(2)装置如图所示,打开止水夹,用热毛巾将烧瓶捂热,水上喷形成红色喷泉,说明氨气

III.氨气的用途
利用下图装置由氨制硝酸,实验时戊中溶液呈淡黄色时关闭分液漏斗活塞。

(3)Na2O2的作用
(4)实验中的氮氧化物(NOx)尾气折算成标准状况下的体积为aL,完全吸收时,烧杯中c(NaOH)至少是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】侯德榜为我国化工事业的发展做出了卓越贡献,是我国近代化学工业的奠基人之一,他结合中国国情对氨碱法进行改进,确定了新的工艺流程——侯氏制碱法:将氨碱法和合成氨法两种工艺联合起来,方法流程如图所示。
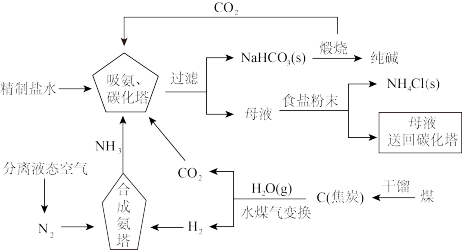
回答下列问题:
(1)向精制盐水中通入 、
、 的顺序及理由为
的顺序及理由为___________ (提示:从两种气体的溶解度进行分析)。
(2)写出 煅烧时发生反应的化学方程式:
煅烧时发生反应的化学方程式:___________ 。
(3)该流程中循环利用的物质为___________ 。
(4)侯氏制碱法除了制取得到纯碱,还生成了一种副产品___________ (填名称),可以用来___________ 。
(5)所得纯碱中可能含有少量 杂质,可以通过如下方法测定纯碱中碳酸钠的质量分数:
杂质,可以通过如下方法测定纯碱中碳酸钠的质量分数:
ⅰ.称取ag样品,溶于水中;
ⅱ.加入足量氯化钙溶液;
ⅲ.过滤、洗涤、干燥、称量,所得沉淀质量为bg。
①证明所加氯化钙溶液已经足量的方法是___________ 。
②该样品中碳酸钠的质量分数为___________ %(用含a、b的代数式表示)。

回答下列问题:
(1)向精制盐水中通入
 、
、 的顺序及理由为
的顺序及理由为(2)写出
 煅烧时发生反应的化学方程式:
煅烧时发生反应的化学方程式:(3)该流程中循环利用的物质为
(4)侯氏制碱法除了制取得到纯碱,还生成了一种副产品
(5)所得纯碱中可能含有少量
 杂质,可以通过如下方法测定纯碱中碳酸钠的质量分数:
杂质,可以通过如下方法测定纯碱中碳酸钠的质量分数:ⅰ.称取ag样品,溶于水中;
ⅱ.加入足量氯化钙溶液;
ⅲ.过滤、洗涤、干燥、称量,所得沉淀质量为bg。
①证明所加氯化钙溶液已经足量的方法是
②该样品中碳酸钠的质量分数为
您最近一年使用:0次
【推荐1】Ⅰ.某课外活动小组欲利用CuO与NH3的反应研究NH3的性质与分子组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:
(1)仪器a的名称为____ ;仪器b中的试剂不能为下列中的_____ (填字母)

(2)装置B的作用是______
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管收集到无色无味的气体,写出装置C中发生反应的化学方程式_____
(4)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢的原子个数比为_____ (用含m、n字母的代数式表示)
Ⅱ.铁是生产生活中常用金属
(1)写出铁与水蒸气的反应方程式_____ 。
(2)氯化亚铁溶液在空气中易被氧化,检验溶液是否变质所加试剂为___ (写化学式),向氯化亚铁溶液中加入烧碱溶液,现象为___
(1)仪器a的名称为
| A.氧化钙 | B.碱石灰 | C.石灰石 | D.氢氧化钠 |

(2)装置B的作用是
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管收集到无色无味的气体,写出装置C中发生反应的化学方程式
(4)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢的原子个数比为
Ⅱ.铁是生产生活中常用金属
(1)写出铁与水蒸气的反应方程式
(2)氯化亚铁溶液在空气中易被氧化,检验溶液是否变质所加试剂为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】选择性催化还原是在有催化剂的条件下将NOx转变为N2和H2O,这是目前国外硝酸厂进行尾气治理普遍采用的一种方法.某小组同学拟验证NO.被氨气还原并测算其转化率.
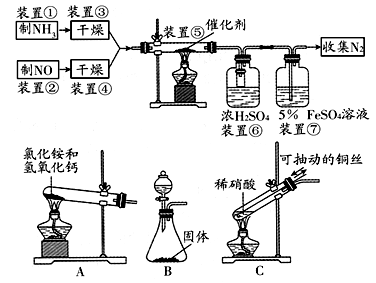
请回答下列问题:
(1)若制取氨气用A装置,则发生反应的化学方程式为_____________________ ;若用B装置制取氨气,则分液漏斗和锥形瓶中盛放的药品分别是___________ ;
(2)用C装置制取NO时,用可抽动的铜丝,其优点是__________________________ ;其反应的离子方程式为____________________________________________ ;
(3)装置⑦的作用可能是________________________________________ ;
(4)装置⑤中的化学方程式是_____________________________ ,若进入装置⑤的NO共2688 mL(标况下),氨气过量,最后收集到标况下2016 mL N2 ,则NO的转化率为___________ .

请回答下列问题:
(1)若制取氨气用A装置,则发生反应的化学方程式为
(2)用C装置制取NO时,用可抽动的铜丝,其优点是
(3)装置⑦的作用可能是
(4)装置⑤中的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】硫氰化钾 是一种用途广泛的化工原料,常用于染料、药物的生产。实验小组设计如图所示的实验装置模拟工业制备
是一种用途广泛的化工原料,常用于染料、药物的生产。实验小组设计如图所示的实验装置模拟工业制备 并进行相关探究实验。
并进行相关探究实验。

已知:① 是一种不溶于水且密度大于水的非极性试剂;
是一种不溶于水且密度大于水的非极性试剂;
② 。
。
请回答下列问题:
(1) 的电子式为
的电子式为___________ 。
(2)装置A用于实验室制备氨气,该反应的化学方程式为___________ 。
(3)装置B中,三口烧瓶内盛有 、水和固体催化剂,通入氨气的导管需要插入
、水和固体催化剂,通入氨气的导管需要插入 液体中,其目的是
液体中,其目的是___________ 。
(4)待三口烧瓶内液体不再分层时,熄灭装置A处的酒精灯,关闭 ,移开水浴。将装置B继续加热至
,移开水浴。将装置B继续加热至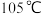 ,待
,待 完全分解后,打开
完全分解后,打开 ,缓缓滴入适量
,缓缓滴入适量 溶液,充分反应后制得
溶液,充分反应后制得 溶液。装置C中仪器a的名称为
溶液。装置C中仪器a的名称为___________ ,装置C处的烧杯中产生淡黄色浑浊的原因是___________ (用离子方程式表示)。
(5)过滤装置C中吸收尾气后的悬浊液,得到滤液x。现取少量滤液x进行如图所示的探究实验。
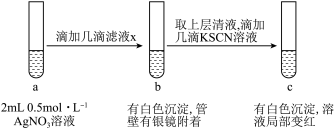
已知: 。
。
①试管b中产生银镜的原因是___________ (用离子方程式表示)。
②观察到试管c中出现上述实验现象后,用力振荡试管c,又观察到红色褪去且白色沉淀增多,结合平衡移动的知识解释其原因___________ 。
 是一种用途广泛的化工原料,常用于染料、药物的生产。实验小组设计如图所示的实验装置模拟工业制备
是一种用途广泛的化工原料,常用于染料、药物的生产。实验小组设计如图所示的实验装置模拟工业制备 并进行相关探究实验。
并进行相关探究实验。
已知:①
 是一种不溶于水且密度大于水的非极性试剂;
是一种不溶于水且密度大于水的非极性试剂;②
 。
。请回答下列问题:
(1)
 的电子式为
的电子式为(2)装置A用于实验室制备氨气,该反应的化学方程式为
(3)装置B中,三口烧瓶内盛有
 、水和固体催化剂,通入氨气的导管需要插入
、水和固体催化剂,通入氨气的导管需要插入 液体中,其目的是
液体中,其目的是(4)待三口烧瓶内液体不再分层时,熄灭装置A处的酒精灯,关闭
 ,移开水浴。将装置B继续加热至
,移开水浴。将装置B继续加热至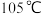 ,待
,待 完全分解后,打开
完全分解后,打开 ,缓缓滴入适量
,缓缓滴入适量 溶液,充分反应后制得
溶液,充分反应后制得 溶液。装置C中仪器a的名称为
溶液。装置C中仪器a的名称为(5)过滤装置C中吸收尾气后的悬浊液,得到滤液x。现取少量滤液x进行如图所示的探究实验。

已知:
 。
。①试管b中产生银镜的原因是
②观察到试管c中出现上述实验现象后,用力振荡试管c,又观察到红色褪去且白色沉淀增多,结合平衡移动的知识解释其原因
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】回收利用含硫烟气有利于节约资源、保护环境。
I.含H2S的烟气回收
(1)将一部分含H2S的烟气在空气中燃烧,将燃烧所得产物与剩余烟气混合,冷却后可回收得到硫磺(S8)。该工艺中涉及反应如下:
反应1: ;
;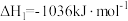
反应2: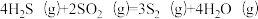 ;
;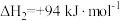
反应3: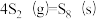 ;
;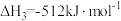
①反应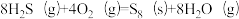 的△H=
的△H=_______ kJ∙mol-1。
②相同条件下需控制反应1与反应2中的烟气体积比为1:2的原因是_______ 。
Ⅱ.含SO2的烟气回收
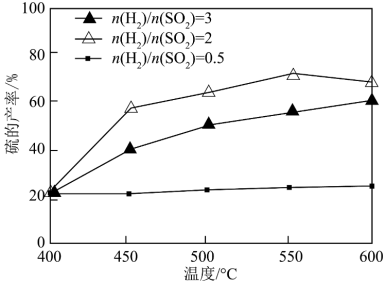
(2)以FeS2/Al2O3为催化剂,用H2还原SO2制S。
其他条件一定,改变起始时H2与SO2的比例,反应相同时间,测得S的产率随温度的变化关系如图所示。500℃,n(H2)/n(SO2)=3时硫的产率比n(H2)/n(SO2)=2时小的原因可能是_______ 。
(3)以V2O5/炭基材料为催化剂,SO2在炭表面被氧气催化氧化为SO3,SO3再转化为硫酸盐等。
①V2O5/炭基材料脱硫涉及反应: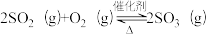 ,下列关于该反应的说法正确的是
,下列关于该反应的说法正确的是_______ (填字母序号)。
a.通入过量空气,可提高SO2的平衡转化率
b.当n(SO2):n(SO3)=l:1时,可判断反应达到平衡
c.使SO3液化从平衡体系中分离,能加快正反应速率,增大SO2转化率
②450℃、在V2O5催化下,SO2和O2的反应过程是按照如下两步完成的:
反应I:_______(快反应)
反应Ⅱ: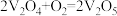 (慢反应)
(慢反应)
请补充上述反应的化学方程式_______ ,决定总反应速率快慢的是反应_______ (填“I”或“Ⅱ”)。
Ⅲ.工业上可采取多种方法减少SO2的排放,回答下列方法中的问题。
(4)方法1(双碱法):用NaOH溶液吸收SO2,并用CaO使NaOH再生NaOH溶液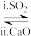 Na2SO3溶液
Na2SO3溶液
①写出过程i的离子方程式:_______ 。
②CaO在水中存在如下转化: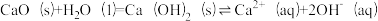
从平衡移动的角度,简述过程i中NaOH再生的原理:_______ 。
方法2:用氨水除去SO2
③已知25℃,NH3·H2O的 ,H2SO3的
,H2SO3的 ,
, 。若氨水的浓度为2.0mol∙L-1,溶液中的c(OH-)=
。若氨水的浓度为2.0mol∙L-1,溶液中的c(OH-)=_______ mol∙L-1。将SO2通入该氨水中,当c(OH-)降至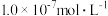 时,溶液中的
时,溶液中的
_______ 。
I.含H2S的烟气回收
(1)将一部分含H2S的烟气在空气中燃烧,将燃烧所得产物与剩余烟气混合,冷却后可回收得到硫磺(S8)。该工艺中涉及反应如下:
反应1:
 ;
;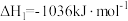
反应2:
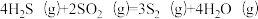 ;
;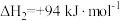
反应3:
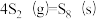 ;
;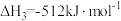
①反应
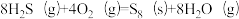 的△H=
的△H=②相同条件下需控制反应1与反应2中的烟气体积比为1:2的原因是
Ⅱ.含SO2的烟气回收
(2)以FeS2/Al2O3为催化剂,用H2还原SO2制S。
其他条件一定,改变起始时H2与SO2的比例,反应相同时间,测得S的产率随温度的变化关系如图所示。500℃,n(H2)/n(SO2)=3时硫的产率比n(H2)/n(SO2)=2时小的原因可能是

(3)以V2O5/炭基材料为催化剂,SO2在炭表面被氧气催化氧化为SO3,SO3再转化为硫酸盐等。
①V2O5/炭基材料脱硫涉及反应:
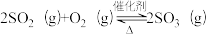 ,下列关于该反应的说法正确的是
,下列关于该反应的说法正确的是a.通入过量空气,可提高SO2的平衡转化率
b.当n(SO2):n(SO3)=l:1时,可判断反应达到平衡
c.使SO3液化从平衡体系中分离,能加快正反应速率,增大SO2转化率
②450℃、在V2O5催化下,SO2和O2的反应过程是按照如下两步完成的:
反应I:_______(快反应)
反应Ⅱ:
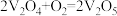 (慢反应)
(慢反应)请补充上述反应的化学方程式
Ⅲ.工业上可采取多种方法减少SO2的排放,回答下列方法中的问题。
(4)方法1(双碱法):用NaOH溶液吸收SO2,并用CaO使NaOH再生NaOH溶液
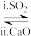 Na2SO3溶液
Na2SO3溶液①写出过程i的离子方程式:
②CaO在水中存在如下转化:
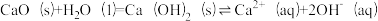
从平衡移动的角度,简述过程i中NaOH再生的原理:
方法2:用氨水除去SO2
③已知25℃,NH3·H2O的
 ,H2SO3的
,H2SO3的 ,
, 。若氨水的浓度为2.0mol∙L-1,溶液中的c(OH-)=
。若氨水的浓度为2.0mol∙L-1,溶液中的c(OH-)=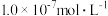 时,溶液中的
时,溶液中的
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】近年来,为应对温室气体排放问题和日益增长的能源需求问题,CO2综合利用技术作为潜在的解决方案受到了研究者的广泛关注。请按照要求回答问题
(1)CO常用于工业冶炼金属,下图是在不同温度下CO还原四种金属氧化物达平衡后气体中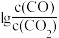 与温度(t)的关系曲线图。下列说法正确的是
与温度(t)的关系曲线图。下列说法正确的是________ 。(填序号)
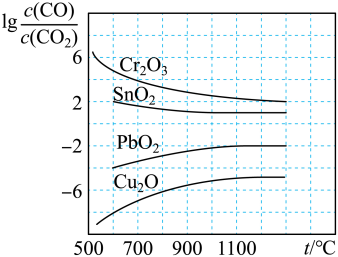
A 工业上可以通过增高反应装置来延长矿石和CO接触的时间,减少尾气中CO的含量
B CO不适宜用于工业冶炼金属铬(Cr)
C 工业冶炼金属铜(Cu)时较低的温度有利于提高CO的利用率
D CO还原PbO2的反应△H>0
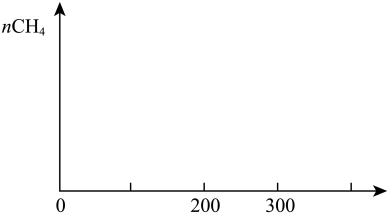
(2)一定条件下Pd-Mg/SiO2催化剂可使CO2 “甲烷化”变废为宝 ,最佳催化温度是200℃~300℃左右,超过300℃催化剂会完全失活、反应停止。向密闭容器通入v(CO2):v(H2)=1:4的反应气体,常温进料开始加热,画出生成甲烷的量随温度的变化曲线
,最佳催化温度是200℃~300℃左右,超过300℃催化剂会完全失活、反应停止。向密闭容器通入v(CO2):v(H2)=1:4的反应气体,常温进料开始加热,画出生成甲烷的量随温度的变化曲线_________ 。
(3)在载人航天器中应用电化学原理,以Pt为阳极,Pb(CO2的载体)为阴极KHCO3溶液为电解质溶液,还原消除航天器内CO2同时产生O2和新的能源CO,则阴极的电极反应式为___________ ;室温下H2CO3电离常数约为K1=4×10-7,K2=5×10-11,则0.025 mol·L-1的H2CO3溶液的pH约等于__________ (不考虑第二步电离和H2O的电离)
(1)CO常用于工业冶炼金属,下图是在不同温度下CO还原四种金属氧化物达平衡后气体中
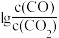 与温度(t)的关系曲线图。下列说法正确的是
与温度(t)的关系曲线图。下列说法正确的是
A 工业上可以通过增高反应装置来延长矿石和CO接触的时间,减少尾气中CO的含量
B CO不适宜用于工业冶炼金属铬(Cr)
C 工业冶炼金属铜(Cu)时较低的温度有利于提高CO的利用率
D CO还原PbO2的反应△H>0
(2)一定条件下Pd-Mg/SiO2催化剂可使CO2 “甲烷化”变废为宝
 ,最佳催化温度是200℃~300℃左右,超过300℃催化剂会完全失活、反应停止。向密闭容器通入v(CO2):v(H2)=1:4的反应气体,常温进料开始加热,画出生成甲烷的量随温度的变化曲线
,最佳催化温度是200℃~300℃左右,超过300℃催化剂会完全失活、反应停止。向密闭容器通入v(CO2):v(H2)=1:4的反应气体,常温进料开始加热,画出生成甲烷的量随温度的变化曲线
(3)在载人航天器中应用电化学原理,以Pt为阳极,Pb(CO2的载体)为阴极KHCO3溶液为电解质溶液,还原消除航天器内CO2同时产生O2和新的能源CO,则阴极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】氧族元素及其化合物在生产、生活中发挥着重要的作用。回答下列问题:
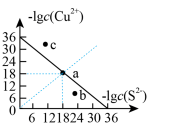
(1)工业上常用硫化物(FeS等)作沉淀剂除去废水中的Cu2+等重金属离子。已知常温下 饱和溶液中,
饱和溶液中,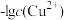 和
和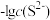 关系如图所示,
关系如图所示,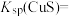
___________ ;图中a、b、c三点对应的溶液中,一定存在 沉淀的是
沉淀的是___________ (填序号)。
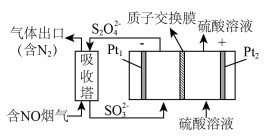
(2)工业上常用连二亚硫酸钠 消除烟气中的
消除烟气中的 ,通过电解可使
,通过电解可使 再生,装置如图所示。吸收塔内发生的离子反应方程式为
再生,装置如图所示。吸收塔内发生的离子反应方程式为___________ 。吸收塔内每吸收 的
的 ,理论上
,理论上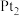 电极上会放出
电极上会放出___________  气体(气体体积均为标准状况)。
气体(气体体积均为标准状况)。
(3)硒是人体必需的微量元素。工业上将含硒工业废料处理得到亚硒酸( )和硒酸(
)和硒酸(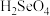 ),进而制备单质硒。亚硒酸(
),进而制备单质硒。亚硒酸( )在溶液中存在多种微粒形态,25℃时各微粒的分布系数
)在溶液中存在多种微粒形态,25℃时各微粒的分布系数 与溶液pH的关系如图所示。(分布系数即组分的平衡浓度占总浓度的分数)
与溶液pH的关系如图所示。(分布系数即组分的平衡浓度占总浓度的分数)
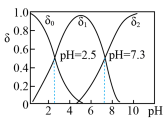
①将 滴入
滴入 溶液中,当pH达到2.0时,发生反应的离子方程式是
溶液中,当pH达到2.0时,发生反应的离子方程式是___________ 。
②25℃时,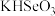 溶液的pH<7,通过计算和必要的文字加以解释:
溶液的pH<7,通过计算和必要的文字加以解释:___________ 。
③已知硒酸的电离方程式为: ,
, 。25℃时,下列关于
。25℃时,下列关于
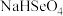 溶液的说法错误的是
溶液的说法错误的是___________ 。
A.
B.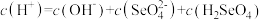
C.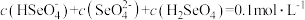
D.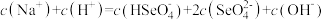
(1)工业上常用硫化物(FeS等)作沉淀剂除去废水中的Cu2+等重金属离子。已知常温下
 饱和溶液中,
饱和溶液中,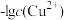 和
和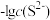 关系如图所示,
关系如图所示,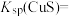
 沉淀的是
沉淀的是
(2)工业上常用连二亚硫酸钠
 消除烟气中的
消除烟气中的 ,通过电解可使
,通过电解可使 再生,装置如图所示。吸收塔内发生的离子反应方程式为
再生,装置如图所示。吸收塔内发生的离子反应方程式为 的
的 ,理论上
,理论上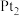 电极上会放出
电极上会放出 气体(气体体积均为标准状况)。
气体(气体体积均为标准状况)。
(3)硒是人体必需的微量元素。工业上将含硒工业废料处理得到亚硒酸(
 )和硒酸(
)和硒酸(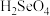 ),进而制备单质硒。亚硒酸(
),进而制备单质硒。亚硒酸( )在溶液中存在多种微粒形态,25℃时各微粒的分布系数
)在溶液中存在多种微粒形态,25℃时各微粒的分布系数 与溶液pH的关系如图所示。(分布系数即组分的平衡浓度占总浓度的分数)
与溶液pH的关系如图所示。(分布系数即组分的平衡浓度占总浓度的分数)
①将
 滴入
滴入 溶液中,当pH达到2.0时,发生反应的离子方程式是
溶液中,当pH达到2.0时,发生反应的离子方程式是②25℃时,
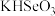 溶液的pH<7,通过计算和必要的文字加以解释:
溶液的pH<7,通过计算和必要的文字加以解释:③已知硒酸的电离方程式为:
 ,
, 。25℃时,下列关于
。25℃时,下列关于
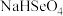 溶液的说法错误的是
溶液的说法错误的是A.

B.
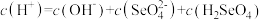
C.
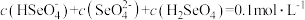
D.
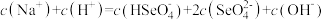
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】CS(NH2)2 (硫脲)是一种白色晶体,139C时 溶解度为9.2g·(100gH2O)-1,可用于制造药物、染料等。由H2NCN(氰氨)与Na2S溶液等作原料,在约50°C、pH 10~11时制取,实验装置(夹持及加热装置已略)如下:
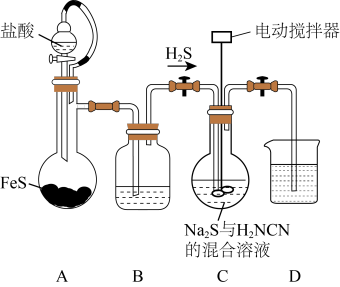
(1)装置B、D中盛放的试剂分别是__________ 、 _________ 。
(2)装置C合适的加热方式是___________ 。
(3)烧瓶中Na2S与等物质的量的H2NCN反应的化学方程式为_________________________________ ;以合适的流速通入H2S的目的是_________________________ 。
(4)实验过程中需分次加入H2NCN并继续通入H2S,经多次重复直至液体中出现絮状物。设计后续操作以从装置C的反应液中分离得到硫脲晶体的实验方案:______________________ [实验中必须使用的试剂:NaOH溶液]。

(1)装置B、D中盛放的试剂分别是
(2)装置C合适的加热方式是
(3)烧瓶中Na2S与等物质的量的H2NCN反应的化学方程式为
(4)实验过程中需分次加入H2NCN并继续通入H2S,经多次重复直至液体中出现絮状物。设计后续操作以从装置C的反应液中分离得到硫脲晶体的实验方案:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】实验室制硝基苯的主要步骤如下:
① 在250mL的圆底烧瓶中放入17.7 mL苯,配上一个双孔橡皮塞,一个孔插入一支100℃温度计,其水银球要进入液面下,另一个孔插入长颈漏斗,仪器装置如图所示。

②通过长颈漏斗上口将已配制好的混酸分多次加入烧瓶中。每加一次,必须振荡烧瓶,当反应物温度不再上升而趋下降时,才可继续加混酸。反应温度应保持在40—50℃,若超过50℃,可用冷水浴冷却烧瓶,加料完毕后,把烧瓶放在水浴上加热,约10分钟内把水浴加热到55-60℃,并保持30分钟,间歇地振荡烧瓶。
③冷却后将反应物倒入分液漏斗,静置分层,分出酸液和粗硝基苯,由于工业浓H2SO4中含有少量汞盐等杂质有催化作用,使反应产物中含有苦味酸(2,4,6-三硝基苯酚)和2,4-二硝基苯酚使粗硝基苯呈浅黄色,此外还含有间二硝基苯。已知:苦味酸与2,4-二硝基苯酚均有酸性,能与碱反应;间二硝基苯性质与硝基苯类似。请回答下列问题
(1)步骤①中长颈漏斗的作用
a_______________________ ,b _______________ 。
(2)步骤 ②中,每加入一次混酸,必须振荡烧瓶的目的_____________________ 。
(3)步骤②中,需严格控制温度的原因___________________________________ 。
(4)步骤③中,静置分层后,粗硝基苯在分液漏斗_____ 层。
(5)要将粗硝基苯中混有少量酸液、苦味酸、2,4一二硝基苯酚以及二硝基苯,除去得到纯净的硝基苯必须进行的五步操作名称为a__________ 、 b _____________ 、c _________ 、 d _____________ 、e_________ 。
① 在250mL的圆底烧瓶中放入17.7 mL苯,配上一个双孔橡皮塞,一个孔插入一支100℃温度计,其水银球要进入液面下,另一个孔插入长颈漏斗,仪器装置如图所示。

②通过长颈漏斗上口将已配制好的混酸分多次加入烧瓶中。每加一次,必须振荡烧瓶,当反应物温度不再上升而趋下降时,才可继续加混酸。反应温度应保持在40—50℃,若超过50℃,可用冷水浴冷却烧瓶,加料完毕后,把烧瓶放在水浴上加热,约10分钟内把水浴加热到55-60℃,并保持30分钟,间歇地振荡烧瓶。
③冷却后将反应物倒入分液漏斗,静置分层,分出酸液和粗硝基苯,由于工业浓H2SO4中含有少量汞盐等杂质有催化作用,使反应产物中含有苦味酸(2,4,6-三硝基苯酚)和2,4-二硝基苯酚使粗硝基苯呈浅黄色,此外还含有间二硝基苯。已知:苦味酸与2,4-二硝基苯酚均有酸性,能与碱反应;间二硝基苯性质与硝基苯类似。请回答下列问题
(1)步骤①中长颈漏斗的作用
a
(2)步骤 ②中,每加入一次混酸,必须振荡烧瓶的目的
(3)步骤②中,需严格控制温度的原因
(4)步骤③中,静置分层后,粗硝基苯在分液漏斗
(5)要将粗硝基苯中混有少量酸液、苦味酸、2,4一二硝基苯酚以及二硝基苯,除去得到纯净的硝基苯必须进行的五步操作名称为a
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】工业中测定铁矿石中铁的含量,目前以氯化亚锡—三氯化钛还原三价铁,再用重铬酸钾滴定法为主。
已知:
回答下列问题:
(1)由 配制氯化亚锡(SnCl2)溶液时,需加入
配制氯化亚锡(SnCl2)溶液时,需加入_____ 。
(2)在1000℃下,利用氢气还原四氯化钛(TiCl4)制备三氯化钛(TiCl3)的装置如图所示。
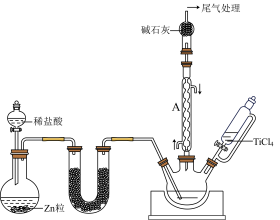
①U形管中可填充的药品为_____ (填字母)。
a.浓硫酸 b.碱石灰 c.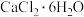 d.五氧化二磷
d.五氧化二磷
仪器A的名称是_____ ,利用本实验中制备氢气的装置,还可以制备硫化氢、氨气、二氧化碳、二氧化硫气体中的_____ 种气体(填字母)。
A.1 B.2 C.3 D.4
②三颈瓶应选用石英材质,不能用普通玻璃材质的原因为_____ 。
③安装好实验装置进行实验,实验步骤如下:检查装置的气密性后,加入药品;打开分液漏斗的活塞,_____ (按正确的顺序填入下列步骤的字母)。
a.打开恒压滴液漏斗,加入TiCl4,加热至1000℃,反应一段时间
b.收集气体,检验纯度
c.关闭分液漏斗的活塞
d.停止加热,冷却
(3)铁矿石铁含量的测定,步骤如下:
Ⅰ、取0.4000g铁矿石样品,加入5mL盐酸,趁热滴加氯化亚锡至溶液变为浅黄色。
Ⅱ、向上述溶液中滴加4滴Na2WO4溶液,然后滴加TiCl3溶液充分还原 ,当
,当 还原完全时,
还原完全时, 过量与
过量与 生成蓝色
生成蓝色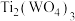 ,再滴加稀K2Cr2O7溶液至蓝色消失,除去过量的
,再滴加稀K2Cr2O7溶液至蓝色消失,除去过量的 。
。
Ⅲ、向溶液中加入适量浓硫酸、浓磷酸和硫酸锰溶液(硫酸锰溶液的作用是消除 的影响),加入指示剂二苯胺磺酸铵,用
的影响),加入指示剂二苯胺磺酸铵,用 K2Cr2O7标准溶液滴定至终点,消耗标准溶液10mL(已知:
K2Cr2O7标准溶液滴定至终点,消耗标准溶液10mL(已知: 被还原为
被还原为 )。
)。
①计算样品中铁元素的质量分数为_____ %。
②下列操作将导致样品中含铁量的测定值偏高的是_____ (填字母)。
a.步骤Ⅰ中样品溶解不充分
b.步骤Ⅱ中未加入稀K2Cr2O7溶液
c.步骤Ⅲ中未加入MnSO4溶液
d.步骤Ⅲ中读数时,滴定前平视,滴定后俯视
已知:
| 颜色 | 熔点/℃ | 沸点/℃ | 化学性质 | |
| TiCl3 | 紫色 | 440 | 660 | 遇水强烈水解,强还原性 |
| TiCl4 | 无色 | -25 | 136 | 遇水强烈水解 |
| SnCl2 | 白色 | 37.7 | 623 | 易水解,强还原性 |
(1)由
 配制氯化亚锡(SnCl2)溶液时,需加入
配制氯化亚锡(SnCl2)溶液时,需加入(2)在1000℃下,利用氢气还原四氯化钛(TiCl4)制备三氯化钛(TiCl3)的装置如图所示。

①U形管中可填充的药品为
a.浓硫酸 b.碱石灰 c.
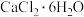 d.五氧化二磷
d.五氧化二磷仪器A的名称是
A.1 B.2 C.3 D.4
②三颈瓶应选用石英材质,不能用普通玻璃材质的原因为
③安装好实验装置进行实验,实验步骤如下:检查装置的气密性后,加入药品;打开分液漏斗的活塞,
a.打开恒压滴液漏斗,加入TiCl4,加热至1000℃,反应一段时间
b.收集气体,检验纯度
c.关闭分液漏斗的活塞
d.停止加热,冷却
(3)铁矿石铁含量的测定,步骤如下:
Ⅰ、取0.4000g铁矿石样品,加入5mL盐酸,趁热滴加氯化亚锡至溶液变为浅黄色。
Ⅱ、向上述溶液中滴加4滴Na2WO4溶液,然后滴加TiCl3溶液充分还原
 ,当
,当 还原完全时,
还原完全时, 过量与
过量与 生成蓝色
生成蓝色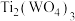 ,再滴加稀K2Cr2O7溶液至蓝色消失,除去过量的
,再滴加稀K2Cr2O7溶液至蓝色消失,除去过量的 。
。Ⅲ、向溶液中加入适量浓硫酸、浓磷酸和硫酸锰溶液(硫酸锰溶液的作用是消除
 的影响),加入指示剂二苯胺磺酸铵,用
的影响),加入指示剂二苯胺磺酸铵,用 K2Cr2O7标准溶液滴定至终点,消耗标准溶液10mL(已知:
K2Cr2O7标准溶液滴定至终点,消耗标准溶液10mL(已知: 被还原为
被还原为 )。
)。①计算样品中铁元素的质量分数为
②下列操作将导致样品中含铁量的测定值偏高的是
a.步骤Ⅰ中样品溶解不充分
b.步骤Ⅱ中未加入稀K2Cr2O7溶液
c.步骤Ⅲ中未加入MnSO4溶液
d.步骤Ⅲ中读数时,滴定前平视,滴定后俯视
您最近一年使用:0次



