水是地球表面上普遍存在的化合物,我们可以用我们学习的物质结构与性质的有关知识去认识它。
(1)水的组成元素为氢和氧。氧的基态原子的价电子排布图为______________ ,氧的第一电离能在同周期元素中由大到小排第______ 位。
(2)根据杂化轨道理论,水分子中的氧原子采取的杂化形式是_______ ;根据价层电子对互斥理论,水分子的VSEPR模型名称为______________ ;根据等电子体原理,写出水合氢离子的一个等电子体(写结构式)_____________ 。
(3)水分子可以形成许多水合物。
①水分子可以作配体和铜离子形成水合铜离子[Cu(H2O)4]2+,1mol水合铜离子中含有σ键数目为_________ 。
②图是水合盐酸晶体H5O2+·Cl-中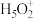 离子的结构。
离子的结构。
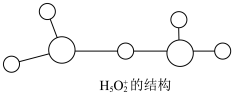
在该离子中,存在的作用力有______________ 。
a.配位键
b.极性键
c.非极性键
d.离子键
e.金属键
f.氢键
g.范德华力
h.π键
i.σ键
(4)韩国首尔大学科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成了“暖冰”。请从结构上解释生成暖冰的原因_________________________________ 。
(5)最新研究发现,水能凝结成13种类型的结晶体,除普通冰以外其余各自的冰都有自己奇特的性质:有在-30℃才凝固的超低温冰,它的坚硬程度可和钢相媲美,能抵挡炮弹轰击;有在180℃高温下依然不变的热冰;还有的冰密度比水大,号称重冰。图为冰的一种骨架形式,依此为单位向空间延伸。
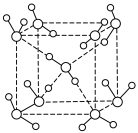
①该冰中的每个水分子有_________ 个氢键;
②冰融化后,在液态水中,水分子之间仍保留有大量氢键将水分子联系在一起,分子间除了无规则的分布及冰结构碎片以外,一般认为还会有大量呈动态平衡的、不完整的多面体的连接方式。下图的五角十二面体是冰熔化形成的理想多面体结构。假设图中的冰熔化后的液态水全部形成下图的五角十二面体,且该多面体之间无氢键,则该冰熔化过程中氢键被破坏的百分比为________ 。
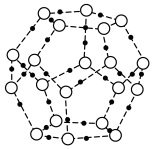
③如果不考虑晶体和键的类型,哪一物质的空间连接方式与这种冰连接类似?____________ ;
④已知O-H…O距离为295pm,列式计算此种冰晶体的密度_______________ g/cm3(已知2952=8.70×104,2953=2.57×107, =1.41,
=1.41, =1.73)。
=1.73)。
(1)水的组成元素为氢和氧。氧的基态原子的价电子排布图为
(2)根据杂化轨道理论,水分子中的氧原子采取的杂化形式是
(3)水分子可以形成许多水合物。
①水分子可以作配体和铜离子形成水合铜离子[Cu(H2O)4]2+,1mol水合铜离子中含有σ键数目为
②图是水合盐酸晶体H5O2+·Cl-中
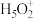 离子的结构。
离子的结构。
在该离子中,存在的作用力有
a.配位键
b.极性键
c.非极性键
d.离子键
e.金属键
f.氢键
g.范德华力
h.π键
i.σ键
(4)韩国首尔大学科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成了“暖冰”。请从结构上解释生成暖冰的原因
(5)最新研究发现,水能凝结成13种类型的结晶体,除普通冰以外其余各自的冰都有自己奇特的性质:有在-30℃才凝固的超低温冰,它的坚硬程度可和钢相媲美,能抵挡炮弹轰击;有在180℃高温下依然不变的热冰;还有的冰密度比水大,号称重冰。图为冰的一种骨架形式,依此为单位向空间延伸。

①该冰中的每个水分子有
②冰融化后,在液态水中,水分子之间仍保留有大量氢键将水分子联系在一起,分子间除了无规则的分布及冰结构碎片以外,一般认为还会有大量呈动态平衡的、不完整的多面体的连接方式。下图的五角十二面体是冰熔化形成的理想多面体结构。假设图中的冰熔化后的液态水全部形成下图的五角十二面体,且该多面体之间无氢键,则该冰熔化过程中氢键被破坏的百分比为

③如果不考虑晶体和键的类型,哪一物质的空间连接方式与这种冰连接类似?
④已知O-H…O距离为295pm,列式计算此种冰晶体的密度
 =1.41,
=1.41, =1.73)。
=1.73)。
更新时间:2016-12-09 08:00:53
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】硅铁合金广泛应用于冶金工业,可用于铸铁时的脱氧剂、添加剂等,回答下列问题:
(1)基态Fe原子价层电子的电子排布图为________ ,基态Si原子电子占据最高能级的电子云轮廓图为________ 形。
(2)绿帘石的组成为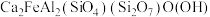 ,将其改写成氧化物的形式为
,将其改写成氧化物的形式为_____________ .
(3) 分子的中心原子的价层电子对数为
分子的中心原子的价层电子对数为________ ,分子的立体构型为________ ;四卤化硅的熔、沸点如下,分析其变化规律及原因________________________________ 。
(4) 可与乙二胺(
可与乙二胺( ,简写为en)发生如下反应:
,简写为en)发生如下反应:
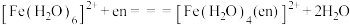 。
。 的中心离子的配位数为
的中心离子的配位数为________ ;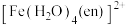 中的配位原子为
中的配位原子为________ 。
(5)在硅酸盐中, 四面体(图a)通过共用顶角氧离子可形成多种结构形式。图b为一种多硅酸根,其中Si原子的杂化形式为
四面体(图a)通过共用顶角氧离子可形成多种结构形式。图b为一种多硅酸根,其中Si原子的杂化形式为________ ,化学式为________________ 。
(1)基态Fe原子价层电子的电子排布图为
(2)绿帘石的组成为
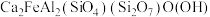 ,将其改写成氧化物的形式为
,将其改写成氧化物的形式为(3)
 分子的中心原子的价层电子对数为
分子的中心原子的价层电子对数为 |  |  |  | |
| 熔点/K | 182.8 | 202.7 | 278.5 | 393.6 |
| 沸点/K | 177.4 | 330.1 | 408 | 460.6 |
(4)
 可与乙二胺(
可与乙二胺( ,简写为en)发生如下反应:
,简写为en)发生如下反应:
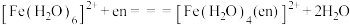 。
。 的中心离子的配位数为
的中心离子的配位数为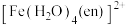 中的配位原子为
中的配位原子为(5)在硅酸盐中,
 四面体(图a)通过共用顶角氧离子可形成多种结构形式。图b为一种多硅酸根,其中Si原子的杂化形式为
四面体(图a)通过共用顶角氧离子可形成多种结构形式。图b为一种多硅酸根,其中Si原子的杂化形式为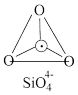  O· Si O· Si 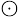  |  |
| 图a | 图b |
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】亚铁氰化钾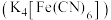 又称黄血盐,用于检验
又称黄血盐,用于检验 ,也用作实验的防结剂。回答问题:
,也用作实验的防结剂。回答问题:
(1)N的基态原子的轨道表示式(电子排布图)为______ 。
(2)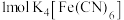 中含
中含 键的数目为
键的数目为______  ,C、N、K的第一电离能由大到小的排序为
,C、N、K的第一电离能由大到小的排序为______ 。
(3)实验室常用 检验
检验 ,生成难溶盐
,生成难溶盐 ,则反应的离子方程式为
,则反应的离子方程式为______ 。
(4)黄血盐可与高锰酸钾溶液反应: (未配平)。若有
(未配平)。若有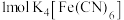 被氧化,则消耗高锰酸钾的物质的量为
被氧化,则消耗高锰酸钾的物质的量为______ , 的电子式为
的电子式为______ 。
(5)含氧有机物中,氧原子的成键方式不同会导致有机物性质不同。解释 的沸点高于
的沸点高于 的原因为
的原因为______ 。
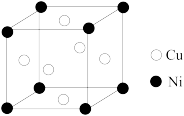
(6)某镍白铜合金的立方晶胞结构如图所示。则晶胞中铜和镍原子个数比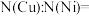
______ 。
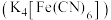 又称黄血盐,用于检验
又称黄血盐,用于检验 ,也用作实验的防结剂。回答问题:
,也用作实验的防结剂。回答问题:(1)N的基态原子的轨道表示式(电子排布图)为
(2)
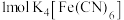 中含
中含 键的数目为
键的数目为 ,C、N、K的第一电离能由大到小的排序为
,C、N、K的第一电离能由大到小的排序为(3)实验室常用
 检验
检验 ,生成难溶盐
,生成难溶盐 ,则反应的离子方程式为
,则反应的离子方程式为(4)黄血盐可与高锰酸钾溶液反应:
 (未配平)。若有
(未配平)。若有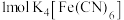 被氧化,则消耗高锰酸钾的物质的量为
被氧化,则消耗高锰酸钾的物质的量为 的电子式为
的电子式为(5)含氧有机物中,氧原子的成键方式不同会导致有机物性质不同。解释
 的沸点高于
的沸点高于 的原因为
的原因为(6)某镍白铜合金的立方晶胞结构如图所示。则晶胞中铜和镍原子个数比
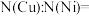

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
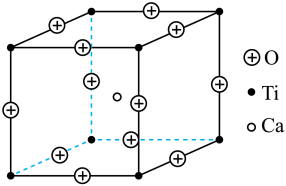
【推荐3】在高温超导领域中,有一种化合物叫钙钛矿,其晶胞如图所示。回答下列问题:
(1)基态 原子的价层电子轨道表示式为
原子的价层电子轨道表示式为___________ 。
(2)基态 原子中,两种自旋状态的电子数之比为
原子中,两种自旋状态的电子数之比为___________ 。
(3)硬度:
___________ (填“>”、“<”或“=”) ,理由为
,理由为___________ 。
(4)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,
表示, 即称为电子的自旋磁量子数。对于基态氧原子,其价电子自旋磁量子数的代数和为
即称为电子的自旋磁量子数。对于基态氧原子,其价电子自旋磁量子数的代数和为___________ 。
(5)钙钛矿晶体的化学式为 :
:
① 的晶体内存在
的晶体内存在___________ (填标号)。
A.金属键 B.氢键 C.离子键
②每个钛离子周围与它最近且等距离的氧离子共有___________ 个。

(1)基态
 原子的价层电子轨道表示式为
原子的价层电子轨道表示式为(2)基态
 原子中,两种自旋状态的电子数之比为
原子中,两种自旋状态的电子数之比为(3)硬度:

 ,理由为
,理由为(4)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示,
表示, 即称为电子的自旋磁量子数。对于基态氧原子,其价电子自旋磁量子数的代数和为
即称为电子的自旋磁量子数。对于基态氧原子,其价电子自旋磁量子数的代数和为(5)钙钛矿晶体的化学式为
 :
:①
 的晶体内存在
的晶体内存在A.金属键 B.氢键 C.离子键
②每个钛离子周围与它最近且等距离的氧离子共有
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Cu的基态原子价电子排布式为_____________ ,
②Ni的基态原子共___________ 有种不同能级的电子。
(2)制备CrO2Cl2的反应为K2Cr2O7+3CCl4=2KCl+2CrO2Cl2+3COCl2↑
①上述化学方程式中非金属元素电负性由大到小的顺序是,______ (用元素符号表示)。
②COCl2分子中各原子均满足8电子稳定结构,COCl2分子中σ键和π键的个数比为______ ;中心原子的杂化方式为______ 。
③NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的离子半径分别为6.910-2nm和7.810-2nm,则熔点NiO____ FeO (填“>”、“<”或“=”),原因是_______ 。
(3)Ni和La的合金是目前使用广泛的储氢材料。该合金的晶胞结构如下图所示:

①该晶体的化学式为__________ 。
②已知该晶体的摩尔质量为Mg /mol,密度为dg/cm3,设NA为阿伏伽德罗常数的值。则该晶胞的体积是__________ cm3 (用M、d、NA的代数式表示)。
③该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子比较稳定。已知:标准状况下氢气的密度为ρg/cm3,储氢能力=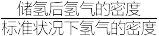 ,若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为
,若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为__________ (用M、d、ρ的代数式表示) 。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Cu的基态原子价电子排布式为
②Ni的基态原子共
(2)制备CrO2Cl2的反应为K2Cr2O7+3CCl4=2KCl+2CrO2Cl2+3COCl2↑
①上述化学方程式中非金属元素电负性由大到小的顺序是,
②COCl2分子中各原子均满足8电子稳定结构,COCl2分子中σ键和π键的个数比为
③NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的离子半径分别为6.910-2nm和7.810-2nm,则熔点NiO
(3)Ni和La的合金是目前使用广泛的储氢材料。该合金的晶胞结构如下图所示:

①该晶体的化学式为
②已知该晶体的摩尔质量为Mg /mol,密度为dg/cm3,设NA为阿伏伽德罗常数的值。则该晶胞的体积是
③该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子比较稳定。已知:标准状况下氢气的密度为ρg/cm3,储氢能力=
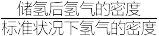 ,若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为
,若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】回答下列问题:
(1)SiC晶体结构同金刚石相似,SiC晶体熔点_______ (填“高于”或“低于”)金刚石熔点,SiC晶体中最小环上有_______ 个C原子。
(2)PCl3分子的空间构型为_______ ,其中心原子的杂化方式为_______ 。
(3)用一种试剂鉴别苯酚溶液、乙醛溶液、己烷、己烯四种无色液体,该试剂为_______ (填名称)。
(4)短周期元素X、Y、Z原子序数依次增大。X是周期表中原子半径最小的元素。Y原子核外电子有六种不同的运动状态。Z基态原子核外L层有2个未成对的电子,则由X、Y、Z能组成的化合物可能为_______。
(5) 的结构如图:
的结构如图: 中S—O—O
中S—O—O_______ (填“是”或“不是”)在一条直线上。
② 中的O—O比H2O2中的更
中的O—O比H2O2中的更_______ (填“难”或“易”)断裂。
(1)SiC晶体结构同金刚石相似,SiC晶体熔点
(2)PCl3分子的空间构型为
(3)用一种试剂鉴别苯酚溶液、乙醛溶液、己烷、己烯四种无色液体,该试剂为
(4)短周期元素X、Y、Z原子序数依次增大。X是周期表中原子半径最小的元素。Y原子核外电子有六种不同的运动状态。Z基态原子核外L层有2个未成对的电子,则由X、Y、Z能组成的化合物可能为_______。
| A.X2YZ | B.X2YZ4 | C.X2Y2Z4 | D.XYZ3 |
 的结构如图:
的结构如图:
 中S—O—O
中S—O—O②
 中的O—O比H2O2中的更
中的O—O比H2O2中的更
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】化合物G是某化工生产中的重要中间体,其合成路线如下:
(注Me: Et:
Et: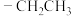 )
)
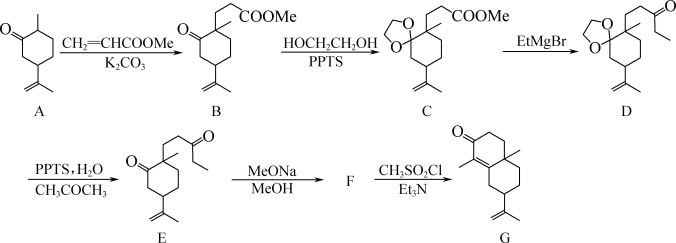
(1)A→B的反应类型为_______ 。
(2)1mol有机物B中所含π键的数目为_______ mol。
(3)E→F的反应类型为加成反应,则F的结构简式为_______ 。
(4)E的一种同分异构体同时满足下列条件,写出一种该同分异构体的结构简式:_______ 。
①能与 溶液发生显色反应;②有四种不同化学环境的氢原子。
溶液发生显色反应;②有四种不同化学环境的氢原子。
(5)已知: ,写出以
,写出以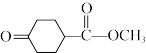 、
、 和
和 为原料制备
为原料制备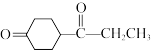 的合成路线流程图
的合成路线流程图_______ (无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
(注Me:
 Et:
Et: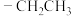 )
)
(1)A→B的反应类型为
(2)1mol有机物B中所含π键的数目为
(3)E→F的反应类型为加成反应,则F的结构简式为
(4)E的一种同分异构体同时满足下列条件,写出一种该同分异构体的结构简式:
①能与
 溶液发生显色反应;②有四种不同化学环境的氢原子。
溶液发生显色反应;②有四种不同化学环境的氢原子。(5)已知:
 ,写出以
,写出以 、
、 和
和 为原料制备
为原料制备 的合成路线流程图
的合成路线流程图
您最近一年使用:0次
【推荐1】(CN)2、(OCN)2等被称为拟卤素,(CN)2在一定条件下氢化可以得到乙二胺(H2NCH2CH2NH2)。回答下列问题:
(1)Fe4[Fe(CN)6]3是较早发现的CN-配合物,其中铁元素呈现两种不同的价态。写出外界离子基态核外电子排布式:________________ 。
(2)与OCN-互为等电子体的分子为________ (填分子式)。
(3)1 mol(CN)2中含有π键的数目为________ 。
(4)乙二胺中C原子的轨道杂化方式为________ 。
(5)乙二胺易溶于水,除因为是极性分子外,还可能的原因为________ 。
(6)含CN-的配合物常用于冶炼黄金。金的晶胞结构如下图所示,晶体中每个Au原子周围紧邻且等距的Au原子有________ 个。
(1)Fe4[Fe(CN)6]3是较早发现的CN-配合物,其中铁元素呈现两种不同的价态。写出外界离子基态核外电子排布式:
(2)与OCN-互为等电子体的分子为
(3)1 mol(CN)2中含有π键的数目为
(4)乙二胺中C原子的轨道杂化方式为
(5)乙二胺易溶于水,除因为是极性分子外,还可能的原因为
(6)含CN-的配合物常用于冶炼黄金。金的晶胞结构如下图所示,晶体中每个Au原子周围紧邻且等距的Au原子有

您最近一年使用:0次
【推荐2】 年春晚中舞蹈诗剧
年春晚中舞蹈诗剧 只此青绿
只此青绿 生动还原了北宋名画,
生动还原了北宋名画, 千里江山图
千里江山图 之所以色彩艳丽,璀璨夺目,与所使用矿物颜料有关。回答下列问题:
之所以色彩艳丽,璀璨夺目,与所使用矿物颜料有关。回答下列问题:
(1)石青,又名蓝矿石,化学式为Cu3(CO3)2(OH)2,基态 核外电子的运动状态有
核外电子的运动状态有 ___________ 种, 的空间构型为
的空间构型为 ___________ ,请写出 的一种等电子体
的一种等电子体___________ 。
(2)亚铁氰化钾,化学式为 ,呈黄色结晶性粉末。
,呈黄色结晶性粉末。 的电子式为
的电子式为___________  中C原子的杂化方式
中C原子的杂化方式 ___________ ,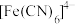 中
中 键和
键和 键的数目之比为
键的数目之比为 ___________ 。
(3)无水CrCl3和氨分子作用能形成某种有色配合物,该配合物的组成相当于CrCl3·6NH3。已知:若加入AgNO3溶液,能从该配合物的水溶液中将所有的氯沉淀为AgCl;若加入NaOH溶液并加热,无刺激性气体产生。请从配合物的形式推算出它的内界和外界,写出该配合物的化学式___________ 。
 年春晚中舞蹈诗剧
年春晚中舞蹈诗剧 只此青绿
只此青绿 生动还原了北宋名画,
生动还原了北宋名画, 千里江山图
千里江山图 之所以色彩艳丽,璀璨夺目,与所使用矿物颜料有关。回答下列问题:
之所以色彩艳丽,璀璨夺目,与所使用矿物颜料有关。回答下列问题:(1)石青,又名蓝矿石,化学式为Cu3(CO3)2(OH)2,基态
 核外电子的运动状态有
核外电子的运动状态有  的空间构型为
的空间构型为  的一种等电子体
的一种等电子体(2)亚铁氰化钾,化学式为
 ,呈黄色结晶性粉末。
,呈黄色结晶性粉末。 的电子式为
的电子式为 中C原子的杂化方式
中C原子的杂化方式 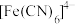 中
中 键和
键和 键的数目之比为
键的数目之比为 (3)无水CrCl3和氨分子作用能形成某种有色配合物,该配合物的组成相当于CrCl3·6NH3。已知:若加入AgNO3溶液,能从该配合物的水溶液中将所有的氯沉淀为AgCl;若加入NaOH溶液并加热,无刺激性气体产生。请从配合物的形式推算出它的内界和外界,写出该配合物的化学式
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】Ⅰ.硫是一种重要的非金属元素,广泛存在于自然界,回答下列问题:
(1)基态硫原子的价层电子排布图是___________ ,最高能级电子所在的原子轨道为___________ 形。
(2)①硫单质的一种结构为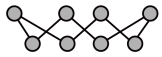 ,S原子杂化方式为
,S原子杂化方式为___________ ; 分子的空间构型是
分子的空间构型是___________ 。
② 、
、 、
、 键角由大到小的顺序是
键角由大到小的顺序是___________ 。
③比较沸点高低: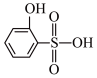
___________ (填“>”或“<”)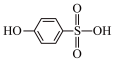 。
。
(3)Fe位于周期表的___________ 区,基态Fe原子的核外电子有___________ 种空间运动状态,Fe与CO形成的化合物Fe(CO)5常温下呈液态,熔点为﹣20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于___________ (填晶体类型)。
(4)ZnS晶胞如图所示:
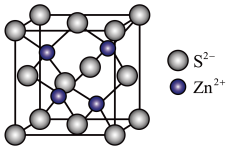
①由图可知,每个 周围与它最接近且距离相等的
周围与它最接近且距离相等的 有
有___________ 个。
②已知该晶胞密度为 ,阿伏加德罗常数为NA,则晶胞边长为
,阿伏加德罗常数为NA,则晶胞边长为___________ pm。
(学法题)根据所学知识分析归纳,计算晶体密度的关键是___________
(5)早在西汉时期的《淮南万毕术》中记载“曾青得铁则化为铜”,这是有关“湿法炼铜”最早文献记录。若向盛有硫酸铜的试管里加入氨水,首先生成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液。
①写出蓝色沉淀溶解的离子方程式___________ ;
②若向该深蓝色透明溶液中加入溶剂___________ ,将有深蓝色晶体析出,写出该晶体的化学式___________ 。
(1)基态硫原子的价层电子排布图是
(2)①硫单质的一种结构为
 ,S原子杂化方式为
,S原子杂化方式为 分子的空间构型是
分子的空间构型是②
 、
、 、
、 键角由大到小的顺序是
键角由大到小的顺序是③比较沸点高低:

 。
。(3)Fe位于周期表的
(4)ZnS晶胞如图所示:

①由图可知,每个
 周围与它最接近且距离相等的
周围与它最接近且距离相等的 有
有②已知该晶胞密度为
 ,阿伏加德罗常数为NA,则晶胞边长为
,阿伏加德罗常数为NA,则晶胞边长为(学法题)根据所学知识分析归纳,计算晶体密度的关键是
(5)早在西汉时期的《淮南万毕术》中记载“曾青得铁则化为铜”,这是有关“湿法炼铜”最早文献记录。若向盛有硫酸铜的试管里加入氨水,首先生成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液。
①写出蓝色沉淀溶解的离子方程式
②若向该深蓝色透明溶液中加入溶剂
您最近一年使用:0次
【推荐1】 (丙烯)是重要基本有机原料。
(丙烯)是重要基本有机原料。 (丙烷)催化脱氢制
(丙烷)催化脱氢制 过程如下:
过程如下:
Ⅰ.主反应: ;
;
Ⅱ.副反应: 。
。
回答下列问题:
(1)已知断裂 下列化学键所需能量如下表:
下列化学键所需能量如下表:
上述主反应的
___________  。
。
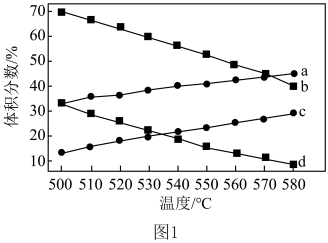
(2)一定条件下, 催化脱氢制
催化脱氢制 发生上述Ⅰ、Ⅱ反应,
发生上述Ⅰ、Ⅱ反应, 和
和 的平衡体积分数与温度、压强的关系如图1所示(图中压强分别为
的平衡体积分数与温度、压强的关系如图1所示(图中压强分别为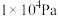 和
和 )。
)。 时,图中表示
时,图中表示 和
和 积分数变化的曲线分别为
积分数变化的曲线分别为___________ 、___________ 。
②提高 催化脱氢制
催化脱氢制 的反应平衡转化率的方法是
的反应平衡转化率的方法是___________ (任写一种)。
(3)在压力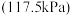 恒定,以
恒定,以 作为稀释气,不同水烃比
作为稀释气,不同水烃比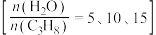 时,
时, 催化脱氢制备
催化脱氢制备 反应(上述反应Ⅰ、Ⅱ)平衡转化率随温度的变化曲线如图2所示。
反应(上述反应Ⅰ、Ⅱ)平衡转化率随温度的变化曲线如图2所示。 平衡转化率相同时,水烃比越高,对应的反应温度越
平衡转化率相同时,水烃比越高,对应的反应温度越___________ (填“高”或“低”)。
②相同温度下,水烃比远大于15:1时,丙烷的消耗速率明显下降,可能的原因是:
ⅰ.丙烷的浓度过低;
ⅱ.___________ 。
③M点对应条件下,若 的选择性为
的选择性为 ,则反应Ⅰ的分压平衡常数
,则反应Ⅰ的分压平衡常数 为
为___________ kPa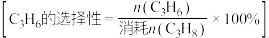 。
。
(4)利用 的弱氧化性,科研人员开发了
的弱氧化性,科研人员开发了 氧化脱氢制
氧化脱氢制 的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图3所示。
的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图3所示。___________ 。
②该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是___________ 。
(5)研究表明, 氧化脱氢制
氧化脱氢制 的催化剂中含有多种元素,如Cr、Zr、Mg、Fe、Ni等。由Mg、Fe、Ni组成的
的催化剂中含有多种元素,如Cr、Zr、Mg、Fe、Ni等。由Mg、Fe、Ni组成的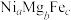 的立方晶胞结构如图4所示。已知晶胞的边长为
的立方晶胞结构如图4所示。已知晶胞的边长为 ,设
,设 为阿伏加德罗常数的值。该晶体密度是
为阿伏加德罗常数的值。该晶体密度是___________  (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
 (丙烯)是重要基本有机原料。
(丙烯)是重要基本有机原料。 (丙烷)催化脱氢制
(丙烷)催化脱氢制 过程如下:
过程如下:Ⅰ.主反应:
 ;
;Ⅱ.副反应:
 。
。回答下列问题:
(1)已知断裂
 下列化学键所需能量如下表:
下列化学键所需能量如下表:| 化学键 |  |  |  |
能量 | 436.0 | 413.4 | 344.7 |

 。
。(2)一定条件下,
 催化脱氢制
催化脱氢制 发生上述Ⅰ、Ⅱ反应,
发生上述Ⅰ、Ⅱ反应, 和
和 的平衡体积分数与温度、压强的关系如图1所示(图中压强分别为
的平衡体积分数与温度、压强的关系如图1所示(图中压强分别为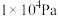 和
和 )。
)。
 时,图中表示
时,图中表示 和
和 积分数变化的曲线分别为
积分数变化的曲线分别为②提高
 催化脱氢制
催化脱氢制 的反应平衡转化率的方法是
的反应平衡转化率的方法是(3)在压力
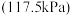 恒定,以
恒定,以 作为稀释气,不同水烃比
作为稀释气,不同水烃比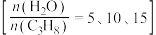 时,
时, 催化脱氢制备
催化脱氢制备 反应(上述反应Ⅰ、Ⅱ)平衡转化率随温度的变化曲线如图2所示。
反应(上述反应Ⅰ、Ⅱ)平衡转化率随温度的变化曲线如图2所示。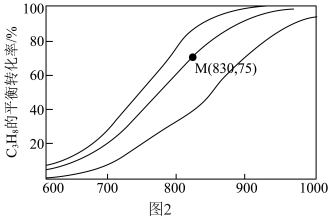
 平衡转化率相同时,水烃比越高,对应的反应温度越
平衡转化率相同时,水烃比越高,对应的反应温度越②相同温度下,水烃比远大于15:1时,丙烷的消耗速率明显下降,可能的原因是:
ⅰ.丙烷的浓度过低;
ⅱ.
③M点对应条件下,若
 的选择性为
的选择性为 ,则反应Ⅰ的分压平衡常数
,则反应Ⅰ的分压平衡常数 为
为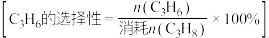 。
。(4)利用
 的弱氧化性,科研人员开发了
的弱氧化性,科研人员开发了 氧化脱氢制
氧化脱氢制 的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图3所示。
的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图3所示。
②该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是
(5)研究表明,
 氧化脱氢制
氧化脱氢制 的催化剂中含有多种元素,如Cr、Zr、Mg、Fe、Ni等。由Mg、Fe、Ni组成的
的催化剂中含有多种元素,如Cr、Zr、Mg、Fe、Ni等。由Mg、Fe、Ni组成的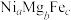 的立方晶胞结构如图4所示。已知晶胞的边长为
的立方晶胞结构如图4所示。已知晶胞的边长为 ,设
,设 为阿伏加德罗常数的值。该晶体密度是
为阿伏加德罗常数的值。该晶体密度是 (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】有色金属资源是全球各国工业发展的重要保证。铁、钴、镍、锰等有色金属及其化合物在机械制造磁性材料、新型电池和高效催化剂等许多领域都有着广泛的应用。请回答下列问题:
(1)Mn(BH4)2是一种储氢材料,Mn2+基态核外电子排布式为_______ ,Mn(BH4)2中B原子的杂化类型为_______ 。推测环硼氮六烷[(HNBH)3]在热水、CH3OH中的溶解性:_______ (填“难”或“易”)溶于热水、CH3OH。
(2)研究发现,在CO2低压合成甲醇反应(CO2+3H2⇌CH3OH+H2O)中,钴氧化物负载的纳米粒子催化剂具有高活性,显示出良好的应用前景。
①第二周期主族元素中,第一电离能比氧大的是_______ (填元素符号)。
②生成物H2O与CH3OH中,沸点较高的是_______ ,原因是_______ 。
③用KCN处理含Co2+的盐溶液,有红色的Co(CN)2析出,将它溶于过量的KCN溶液后,可生成紫色的[Co(CN)6]4-。[Co(CN)6]4-具有强还原性,在加热时能与水反应生成淡黄色的[Co(CN)6]3-,写出该反应的离子方程式:_______ 。[Co(CN)6]3-中所含σ键与π键数目之比为_______ 。
(3)YxNiyBzCw在临界温度15.6K时可实现超导,其晶胞结构如图1所示,则其化学式为_______ 。
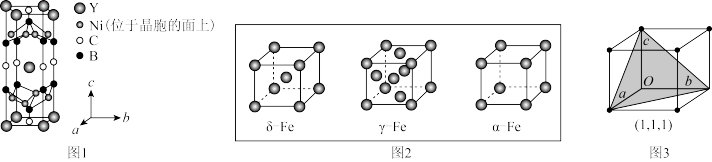
(4)①铁有δ、γ、α三种同素异形体(如图2),若Fe原子半径为rpm,NA表示阿伏加德罗常数的值,则γ-Fe单质的密度为_______ (列出计算式即可)g•cm-3
②在立方晶胞中与晶胞体对角线垂直的面在晶体学中称为(1,1,1)晶面,如图3,则α-Fe晶胞体中(1,1,1)晶面共有_______ 个
(1)Mn(BH4)2是一种储氢材料,Mn2+基态核外电子排布式为
(2)研究发现,在CO2低压合成甲醇反应(CO2+3H2⇌CH3OH+H2O)中,钴氧化物负载的纳米粒子催化剂具有高活性,显示出良好的应用前景。
①第二周期主族元素中,第一电离能比氧大的是
②生成物H2O与CH3OH中,沸点较高的是
③用KCN处理含Co2+的盐溶液,有红色的Co(CN)2析出,将它溶于过量的KCN溶液后,可生成紫色的[Co(CN)6]4-。[Co(CN)6]4-具有强还原性,在加热时能与水反应生成淡黄色的[Co(CN)6]3-,写出该反应的离子方程式:
(3)YxNiyBzCw在临界温度15.6K时可实现超导,其晶胞结构如图1所示,则其化学式为

(4)①铁有δ、γ、α三种同素异形体(如图2),若Fe原子半径为rpm,NA表示阿伏加德罗常数的值,则γ-Fe单质的密度为
②在立方晶胞中与晶胞体对角线垂直的面在晶体学中称为(1,1,1)晶面,如图3,则α-Fe晶胞体中(1,1,1)晶面共有
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】黄铁矿(主要成分为FeS2)是工业制硫酸的主要原料。回答下列问题
(1)基态铁原子的价电子排布图_____________ 。
(2) 制硫酸的过程中会产生SO3, SO3的空间构型是_____ 。
(3) 配合物[Fe(H2N-CH2-CH2-NH2)3]SO4的名称是硫酸三乙二胺合铁(II)。 其中的乙二胺 (H2N-CH2-CH2-NH2)是配体。
① [Fe(H2N-CH2-CH2-NH2)3]SO4的晶体类型属于______ ,其 中 C、N、O的电负性由大到小的顺序为______
③乙二胺分于中氮原子的杂化轨道类型是______ 。乙二胺和偏二甲肼(CH3)2NNH2互为同分异构体。乙二胺的沸点117.2℃,偏二甲肼的沸点63℃。两者沸点不同的主要原因是_________________ 。
(4)铁和铜的电离能数据如下表:
第一电离能与第二电离能之间的差值铜比铁大得多的原因是______ 。

(5)铁原子有两种堆积方式,相应地形成两种晶胞(如图甲、乙所示),其中晶胞乙的堆积方式是______ , 晶胞甲中原子的空间利用率为______ (用含 的代数式表示)。
的代数式表示)。
(1)基态铁原子的价电子排布图
(2) 制硫酸的过程中会产生SO3, SO3的空间构型是
(3) 配合物[Fe(H2N-CH2-CH2-NH2)3]SO4的名称是硫酸三乙二胺合铁(II)。 其中的乙二胺 (H2N-CH2-CH2-NH2)是配体。
① [Fe(H2N-CH2-CH2-NH2)3]SO4的晶体类型属于
③乙二胺分于中氮原子的杂化轨道类型是
(4)铁和铜的电离能数据如下表:
铁 | 铜 | |
第一电能能(kJ/mol) | 759 | 746 |
第二电离能(kJ/mol) | 1561 | 1958 |
第一电离能与第二电离能之间的差值铜比铁大得多的原因是

(5)铁原子有两种堆积方式,相应地形成两种晶胞(如图甲、乙所示),其中晶胞乙的堆积方式是
 的代数式表示)。
的代数式表示)。
您最近一年使用:0次



