用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
(1)该反应的离子方程式___________________________ 。(已知H2C2O4是二元弱酸)
(2)该实验探究的是_____________ 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是_________________ <_____________ (填实验序号)。
(3)若实验①在2min末收集了2.24mL CO2(标准状况下),则在2min末, c( )=
)=__________ mol/L(假设混合液体积为50mL)
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定_____________ 来比较化学反应速率。(一条即可)
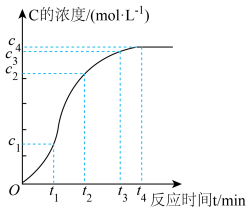
(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:

①__________________________ ;②__________________________ 。
| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.1mol·L-1 H2C2O4溶液 | 30mL 0.01mol·L-1 KMnO4溶液 |
| ② | 20mL 0.2mol·L-1 H2C2O4溶液 | 30mL 0.01mol·L-1 KMnO4溶液 |
(1)该反应的离子方程式
(2)该实验探究的是
(3)若实验①在2min末收集了2.24mL CO2(标准状况下),则在2min末, c(
 )=
)=(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定
(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:

①
更新时间:2016-12-09 09:03:06
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】“花卉保鲜剂”是一种可以延长花期的试剂。如表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)下列“花卉保鲜剂”的成分中,属于非电解质的是______ ,可做杀菌剂的是____
A. 高锰酸钾 B. 硫酸钾 C. 蔗糖 D. 硝酸银 E. 水
(2) 配制1L上述“鲜花保鲜剂”需要高锰酸钾______ mol。
(3)在溶液配制过程中,下列操作会使配制结果无影响的是______ 。
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚配制完一定物质的量浓度的氯化钠溶液未洗涤
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为______ mol/L。
(5)如果用高铁酸钾(K2FeO4)代替高锰酸钾效果会更好,湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O.碱性条件下,氧化剂与还原剂的物质的量的比为3:2发生反应,写出并配平湿法制备高铁酸钾的离子反应方程式___________________________________________________________
| 成分 | 质量(g) | 摩尔质量(g⋅mol−1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 0.87 | 174 |
| 阿司匹林 | 0.17 | 180 |
| 高锰酸钾 | 0.316 | 158 |
| 硝酸银 | 0.0075 | 170 |
(1)下列“花卉保鲜剂”的成分中,属于非电解质的是
A. 高锰酸钾 B. 硫酸钾 C. 蔗糖 D. 硝酸银 E. 水
(2) 配制1L上述“鲜花保鲜剂”需要高锰酸钾
(3)在溶液配制过程中,下列操作会使配制结果无影响的是
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚配制完一定物质的量浓度的氯化钠溶液未洗涤
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为
(5)如果用高铁酸钾(K2FeO4)代替高锰酸钾效果会更好,湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O.碱性条件下,氧化剂与还原剂的物质的量的比为3:2发生反应,写出并配平湿法制备高铁酸钾的离子反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】溴主要以 形式存在于海水中,海水呈弱碱性。工业上制备的Br2的操作步骤为:
形式存在于海水中,海水呈弱碱性。工业上制备的Br2的操作步骤为:
①一定条件下,将Cl2通入浓缩的海水中,生成Br2
②利用热空气将Br2吹出,并用末 溶液吸收吹出的Br2,生成
溶液吸收吹出的Br2,生成 、
、 等
等
③用硫酸酸化步骤②得到的混合物,最终较纯的Br2
(1)Br2可用热空气吹出,其原因是___________ 。
(2)写出步骤③所发生的化学反应方程式___________ 。
(3)步骤②的产品有时运输到目的地后再酸化,主要是因为___________ 。
(4)为了除去工业Br2中微量的Cl2,可向工业Br2中___________ 。
a.通入HBr b.加入 溶液 c.加入
溶液 c.加入 溶液 d.加入
溶液 d.加入 溶液
溶液
 形式存在于海水中,海水呈弱碱性。工业上制备的Br2的操作步骤为:
形式存在于海水中,海水呈弱碱性。工业上制备的Br2的操作步骤为:①一定条件下,将Cl2通入浓缩的海水中,生成Br2
②利用热空气将Br2吹出,并用末
 溶液吸收吹出的Br2,生成
溶液吸收吹出的Br2,生成 、
、 等
等③用硫酸酸化步骤②得到的混合物,最终较纯的Br2
(1)Br2可用热空气吹出,其原因是
(2)写出步骤③所发生的化学反应方程式
(3)步骤②的产品有时运输到目的地后再酸化,主要是因为
(4)为了除去工业Br2中微量的Cl2,可向工业Br2中
a.通入HBr b.加入
 溶液 c.加入
溶液 c.加入 溶液 d.加入
溶液 d.加入 溶液
溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列十种物质:①Cl2 ②铝 ③醋酸(CH3COOH) ④CO2 ⑤H2SO4 ⑥熔融Ba(OH)2 ⑦氨水 ⑧稀硝酸 ⑨Al2(SO4)3固体 ⑩NaHSO4
(1)按物质的分类方法填写表格的空白处:
属于非电解质的是__________ ;属于弱电解质的是________ ;属于强电解质的是__________ ;能导电的是____________ 。
(2)写出③溶于水时的电离方程式________________________________________ 。
(3)实验室常用高锰酸钾固体与浓盐酸在常温下反应来快速制备少量①。反应方程式为: KMnO4 + HCl(浓) —— KCl + MnCl2 + Cl2↑ + H2O(未配平)
配平上述反应并用双线桥法标出反应中电子转移的方向和数目:____________________
KMnO4 + HCl(浓) —— KCl + MnCl2 + Cl2↑ + H2O
(1)按物质的分类方法填写表格的空白处:
属于非电解质的是
(2)写出③溶于水时的电离方程式
(3)实验室常用高锰酸钾固体与浓盐酸在常温下反应来快速制备少量①。反应方程式为: KMnO4 + HCl(浓) —— KCl + MnCl2 + Cl2↑ + H2O(未配平)
配平上述反应并用双线桥法标出反应中电子转移的方向和数目:
KMnO4 + HCl(浓) —— KCl + MnCl2 + Cl2↑ + H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】白醋是烹调中的酸味辅料,能改善调节人体的新陈代谢,其主要成分为CH3COOH,为一元弱酸,回答下列问题:
(1)25℃时,pH=5的醋酸溶液中,由水电离出的c(H+)=_______ mol·L-1
(2)已知CH3COOH的Ka=1.74×10-5,NH3·H2O的Kb=1.74×10-5,则CH3COONH4的浓溶液呈_______ (填“酸性”或“中性”或“碱性”);将CH3COONH4加入到Mg(OH)2悬浊液中,发现沉淀溶解,试解释原因:_______ (用文字和方程式说明)。
(3)用如图所示装置测定Zn和4.0mol·L-1、2.0mol·L-1醋酸的反应速率:

①仪器a的名称为_______ 。
②Zn和醋酸溶液反应的离子方程式为_______ 。
③检查装置气密性的操作方法是_______ 。
④设计实验方案:在不同浓度醋酸溶液下,测定_______ (要求所测得的数据能直观体现反应速率大小)。
(1)25℃时,pH=5的醋酸溶液中,由水电离出的c(H+)=
(2)已知CH3COOH的Ka=1.74×10-5,NH3·H2O的Kb=1.74×10-5,则CH3COONH4的浓溶液呈
(3)用如图所示装置测定Zn和4.0mol·L-1、2.0mol·L-1醋酸的反应速率:

①仪器a的名称为
②Zn和醋酸溶液反应的离子方程式为
③检查装置气密性的操作方法是
④设计实验方案:在不同浓度醋酸溶液下,测定
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL某浓度的稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值,体积已换算成标准状态):
(1)2~3min段的反应速率比1~2min段的反应速率__________ (填“块”或“慢”),原因是______ ;
(2)求2~3min段以HCl的浓度变化来表示的平均反应速率(设溶液体积不变)____________ ;
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,可以在盐酸中分别加入等体积的下列溶液,你认为可行的是(填编号)____________ 。
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
| 时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 0 | 50 | 120 | 232 | 290 | 310 |
(1)2~3min段的反应速率比1~2min段的反应速率
(2)求2~3min段以HCl的浓度变化来表示的平均反应速率(设溶液体积不变)
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,可以在盐酸中分别加入等体积的下列溶液,你认为可行的是(填编号)
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】探究一定条件下反应物浓度对硫代硫酸钠(Na2S2O3)与硫酸反应速率的影响。
【查阅资料】
a.Na2S2O3易溶于水,能与硫酸发生反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O
b.浊度计用于测量浑浊度的变化。产生的沉淀越多,浑浊度(单位为NTU)值越大。
【实验过程】


用如图所示装置进行如表所示的 5 个实验,分别测量混合后溶液达到相同浑浊度的过程中, 浑浊度随时间的变化。实验①~⑤所得数据如图曲线①~⑤所示:
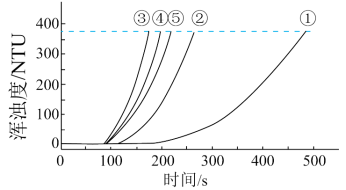
实验数据:
【分析与解释】
(1)实验序号①中,溶液混合后Na2S2O3溶液的初始浓度______ mol/L。
(2)实验③中,x =______ 。
(3)实验①、②、③的目的是______ 。
(4)通过比较①、②、③与③、④、⑤两组实验,可推断:反应物浓度的改变对Na2S2O3与硫酸反应的化学反应速率的影响,Na2S2O3溶液浓度的改变影响更大。该推断的证据是______ 。
【查阅资料】
a.Na2S2O3易溶于水,能与硫酸发生反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O
b.浊度计用于测量浑浊度的变化。产生的沉淀越多,浑浊度(单位为NTU)值越大。
【实验过程】


用如图所示装置进行如表所示的 5 个实验,分别测量混合后溶液达到相同浑浊度的过程中, 浑浊度随时间的变化。实验①~⑤所得数据如图曲线①~⑤所示:

实验数据:
| 实验编号 | Na2S2O3溶液 | H2SO4溶液 | 蒸馏水 | ||
| c / (mol·L-1) | V / mL | c / (mol·L-1) | V / mL | V / mL | |
| ① | 0.1 | 1.5 | 0.1 | 3.5 | 10 |
| ② | 0.1 | 2.5 | 0.1 | 3.5 | 9 |
| ③ | 0.1 | 3.5 | 0.1 | 3.5 | x |
| ④ | 0.1 | 3.5 | 0.1 | 2.5 | 9 |
| ⑤ | 0.1 | 3.5 | 0.1 | 1.5 | 10 |
【分析与解释】
(1)实验序号①中,溶液混合后Na2S2O3溶液的初始浓度
(2)实验③中,x =
(3)实验①、②、③的目的是
(4)通过比较①、②、③与③、④、⑤两组实验,可推断:反应物浓度的改变对Na2S2O3与硫酸反应的化学反应速率的影响,Na2S2O3溶液浓度的改变影响更大。该推断的证据是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】草酸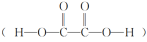 在工业上可作漂白剂、鞣革剂,也是实验室常用试剂。室温下利用H2C2O4溶液和酸性KMnO4溶液的反应探究外界条件对反应速率的影响,设计方案如下:
在工业上可作漂白剂、鞣革剂,也是实验室常用试剂。室温下利用H2C2O4溶液和酸性KMnO4溶液的反应探究外界条件对反应速率的影响,设计方案如下:
(1)上述反应的离子方程式为__ 。
(2)分析数据可得到的结论是__ 。
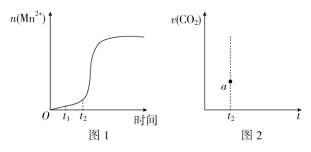
(3)该实验中若n(Mn2+)随时间变化趋势如图1所示,请于图2中画出t2后生成CO2的速率图象(从a点开始作图)___ ,并说明理由:__ 。
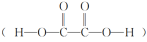 在工业上可作漂白剂、鞣革剂,也是实验室常用试剂。室温下利用H2C2O4溶液和酸性KMnO4溶液的反应探究外界条件对反应速率的影响,设计方案如下:
在工业上可作漂白剂、鞣革剂,也是实验室常用试剂。室温下利用H2C2O4溶液和酸性KMnO4溶液的反应探究外界条件对反应速率的影响,设计方案如下:| 实验编号 | 所加试剂及用量/mL | 溶液颜色褪至无色所需时间/min | |||
| 0.6mol/L H2C2O4溶液 | H2O | 0.01mol/L KMnO4溶液 | 3moL/L稀H2SO4 | ||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 2.0 | 3.0 | 3.0 | 2.0 | 5.2 |
| 3 | 1.0 | 4.0 | 3.0 | 2.0 | 6.4 |
(1)上述反应的离子方程式为
(2)分析数据可得到的结论是
(3)该实验中若n(Mn2+)随时间变化趋势如图1所示,请于图2中画出t2后生成CO2的速率图象(从a点开始作图)

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】清洁能源的综合利用可有效降低碳排放,是实现“碳中和、碳达峰"的重要途径。H2和CO2合成乙醇反应为:2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g)。将等物质的量的CO2和H2充入一刚性容器中,测得平衡时乙醇的体积分数随温度和压强的关系如图甲。
C2H5OH(g)+3H2O(g)。将等物质的量的CO2和H2充入一刚性容器中,测得平衡时乙醇的体积分数随温度和压强的关系如图甲。
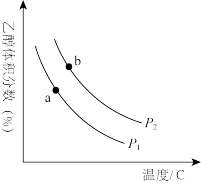
图甲
已知Arrhenius经验公式为Rlnk=- +C(Ea为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的储化效能,进行了实验探究,依据实验数获得图乙曲线。
+C(Ea为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的储化效能,进行了实验探究,依据实验数获得图乙曲线。
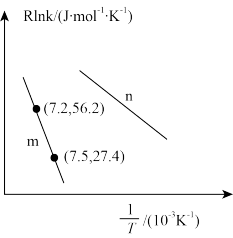
图乙
从图中信息获知催化效能较高的催化剂是____ (“m”或“n”),判断理由是____ 。
 C2H5OH(g)+3H2O(g)。将等物质的量的CO2和H2充入一刚性容器中,测得平衡时乙醇的体积分数随温度和压强的关系如图甲。
C2H5OH(g)+3H2O(g)。将等物质的量的CO2和H2充入一刚性容器中,测得平衡时乙醇的体积分数随温度和压强的关系如图甲。
图甲
已知Arrhenius经验公式为Rlnk=-
 +C(Ea为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的储化效能,进行了实验探究,依据实验数获得图乙曲线。
+C(Ea为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的储化效能,进行了实验探究,依据实验数获得图乙曲线。
图乙
从图中信息获知催化效能较高的催化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】I.完成下列问题
(1)对于Fe+2HCl=FeCl2+H2↑,改变下列条件对生成氢气的速率有何影响?(填“增大”“减小”或“不变”)
①增大铁的质量:___________ ;
②增加盐酸体积:___________ ;
③把铁片改成铁粉:___________ ;
④滴入几滴CuSO4溶液:___________ ;
⑤加入NaCl固体:___________ ;
⑥加入一定体积的Na2SO4溶液:___________ 。
(2)一定温度下,反应N2(g)+O2(g) 2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。
2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。
⑦缩小体积使压强增大:___________ ;
⑧恒容充入N2:___________ ;
⑨恒容充入He:___________ ;
⑩恒压充入He:___________ 。
II.某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下方案。
(3)已知反应后H2C2O4转化为CO2逸出,KMnO4溶液转化为MnSO4,每消耗1molH2C2O4转移___________ mol电子。为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为n(H2C2O4)∶n(KMnO4)≥___________ 。
(1)对于Fe+2HCl=FeCl2+H2↑,改变下列条件对生成氢气的速率有何影响?(填“增大”“减小”或“不变”)
①增大铁的质量:
②增加盐酸体积:
③把铁片改成铁粉:
④滴入几滴CuSO4溶液:
⑤加入NaCl固体:
⑥加入一定体积的Na2SO4溶液:
(2)一定温度下,反应N2(g)+O2(g)
 2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。
2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响(填“增大”“减小”或“不变”)。⑦缩小体积使压强增大:
⑧恒容充入N2:
⑨恒容充入He:
⑩恒压充入He:
II.某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下方案。
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | ||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某温度时,在2L密闭容器中,X、Y、Z 三种物质的物质的量随时间变化的曲线如图所示。由图中数据分析
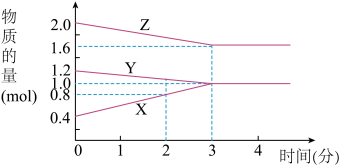
(1)该反应的化学方程式为________ 。
(2)反应开始至2min末,X的反应速率为_________ 。
(3)该反应____________ 。(填序号)
①是可逆反应
②不是可逆反应

(1)该反应的化学方程式为
(2)反应开始至2min末,X的反应速率为
(3)该反应
①是可逆反应
②不是可逆反应
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】一定温度下10L密闭容器中发生某可逆反应,其平衡常数表达为:K= 。
。
根据题意完成下列填空:
(1)写出该反应的化学方程式___ ;若温度升高,K增大,该反应是___ 反应(填“吸热”或“放热”)。
(2)能判断该反应一定达到平衡状态的是___ (选填编号)。
a.v正(H2O)=v逆(H2) b.容器中气体的相对分子质量不随时间改变
c.消耗nmol H2同时消耗nmolCO d.容器中物质的总物质的量不随时间改变
(3)该反应的v正 随时间变化的关系如图。t2时改变了某种条件,改变的条件可能是___ 、___ 。(填写2项)

(4)实验测得t2时刻容器内有1molH2O,5min后H2O的物质的量是0.8mol,这5min内H2O的平均反应速率为___ 。
 。
。根据题意完成下列填空:
(1)写出该反应的化学方程式
(2)能判断该反应一定达到平衡状态的是
a.v正(H2O)=v逆(H2) b.容器中气体的相对分子质量不随时间改变
c.消耗nmol H2同时消耗nmolCO d.容器中物质的总物质的量不随时间改变
(3)该反应的v正 随时间变化的关系如图。t2时改变了某种条件,改变的条件可能是

(4)实验测得t2时刻容器内有1molH2O,5min后H2O的物质的量是0.8mol,这5min内H2O的平均反应速率为
您最近一年使用:0次

 C+D的反应速率,他们将A、B在一定条件下反应并测定反应中生成物C的浓度随反应时间的变化情况,绘制出如图所示的曲线。据此,请完成以下问题:
C+D的反应速率,他们将A、B在一定条件下反应并测定反应中生成物C的浓度随反应时间的变化情况,绘制出如图所示的曲线。据此,请完成以下问题: