碳和碳的化合物在生产、生活中有重要作用,甲醇水蒸气重整制氢系统可能发生下列三个反应:
①CH3OH(g) CO(g)+2H2(g) △H1=+90.8kJ/mol
CO(g)+2H2(g) △H1=+90.8kJ/mol
②CH3OH(g)+H2O(g) CO2(g)+3H2(g) △H2=+49kJ/mol
CO2(g)+3H2(g) △H2=+49kJ/mol
③CO(g)+H2O(g) CO2(g)+H2(g) △H3
CO2(g)+H2(g) △H3
回答下列问题:
(1)△H3=__________ ;
(2)根据化学原理分析升高温度对反应②的影响__________ ;
(3)甲醇使用不当会造成其对水质的污染,用电化学可消除这种污染,其原理是电解CoSO4、稀硫酸和CH3OH混合溶液,将Co2+氧化成Co3+,Co3+再将CH3OH氧化成CO2。
①电解时,阳极的电极反应式为__________ ;
②Co3+氧化CH3OH的离子方程式为__________ 。
(4)控制反应条件,反应①中的产物也可以用来合成甲醇和二甲醚,其中合成二甲醚的化学方程式为3H2(g)+3CO(g)═CH3OCH3(g)+CO2(g),在相同条件下合成二甲醚和合成甲醇的原料平衡转化率随氢碳比[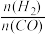 ]的变化如图所示:
]的变化如图所示:
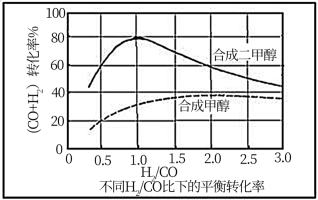
合成二甲醚的最佳氢碳比为__________ ,对于气相反应,用某组分(B)的平衡分压(PB)代替物质的量浓度(cB)也可以表示平衡常数(记作KP),水煤气合成二甲醚的反应的平衡常数表达式为KP=__________ 。
(5)在标态(反应物和产物都处于100kPa)和T(K)条件下由稳定单质生成1mol化合物的焓变称为该物质在T(K)时的标准焓,用符号△Hθ表示。已知石墨和一氧化碳的燃烧热△H分别为-393.5kJ•mol-1和—283.0 kJ •mol-1,则CO2(g)、CO(g)的△Hθ分别为__________ 、__________ 。
①CH3OH(g)
 CO(g)+2H2(g) △H1=+90.8kJ/mol
CO(g)+2H2(g) △H1=+90.8kJ/mol②CH3OH(g)+H2O(g)
 CO2(g)+3H2(g) △H2=+49kJ/mol
CO2(g)+3H2(g) △H2=+49kJ/mol③CO(g)+H2O(g)
 CO2(g)+H2(g) △H3
CO2(g)+H2(g) △H3回答下列问题:
(1)△H3=
(2)根据化学原理分析升高温度对反应②的影响
(3)甲醇使用不当会造成其对水质的污染,用电化学可消除这种污染,其原理是电解CoSO4、稀硫酸和CH3OH混合溶液,将Co2+氧化成Co3+,Co3+再将CH3OH氧化成CO2。
①电解时,阳极的电极反应式为
②Co3+氧化CH3OH的离子方程式为
(4)控制反应条件,反应①中的产物也可以用来合成甲醇和二甲醚,其中合成二甲醚的化学方程式为3H2(g)+3CO(g)═CH3OCH3(g)+CO2(g),在相同条件下合成二甲醚和合成甲醇的原料平衡转化率随氢碳比[
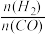 ]的变化如图所示:
]的变化如图所示:
合成二甲醚的最佳氢碳比为
(5)在标态(反应物和产物都处于100kPa)和T(K)条件下由稳定单质生成1mol化合物的焓变称为该物质在T(K)时的标准焓,用符号△Hθ表示。已知石墨和一氧化碳的燃烧热△H分别为-393.5kJ•mol-1和—283.0 kJ •mol-1,则CO2(g)、CO(g)的△Hθ分别为
更新时间:2016-12-09 11:12:07
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ: CO(g) + 2H2(g) CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应Ⅱ: CO2(g) + 3H2(g) CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
①下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
由表中数据判断ΔH1____ 0 (填“>”、“=”或“<”)。
② 某温度下,将2mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为___________ ,此时的温度为_______ (从上表中选择)。
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(l) ΔH1=-1451.6kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2 =-566.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:_________________________________________
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置:

①该电池的能量转化形式为___________________________ 。
②工作一段时间后,测得溶液的pH减小。请写出该电池的负极的电极反应式。_____________________________
③用该电池电解(惰性电极)500mL某CuSO4溶液,电解一段时间后,为使电解质溶液恢复到原状态,需要向溶液中加入9.8g Cu(OH)2固体。则原CuSO4溶液的物质的量浓度为___________ mol/L(假设电解前后溶液体积不变)。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ: CO(g) + 2H2(g)
 CH3OH(g) ΔH1
CH3OH(g) ΔH1反应Ⅱ: CO2(g) + 3H2(g)
 CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2①下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
② 某温度下,将2mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(l) ΔH1=-1451.6kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2 =-566.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置:

①该电池的能量转化形式为
②工作一段时间后,测得溶液的pH减小。请写出该电池的负极的电极反应式。
③用该电池电解(惰性电极)500mL某CuSO4溶液,电解一段时间后,为使电解质溶液恢复到原状态,需要向溶液中加入9.8g Cu(OH)2固体。则原CuSO4溶液的物质的量浓度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】采用 为硝化剂是一种新型的绿色硝化技术,F Daniels等曾利用测压法在刚性反应器中研究了25℃时
为硝化剂是一种新型的绿色硝化技术,F Daniels等曾利用测压法在刚性反应器中研究了25℃时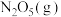 分解反应:
分解反应:

其中 二聚为
二聚为 的反应可以迅速达到平衡,体系的总压强
的反应可以迅速达到平衡,体系的总压强 随时间
随时间 的变化如下表所示(
的变化如下表所示( 时,
时,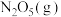 完全分解):
完全分解):
(1)已知: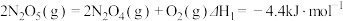
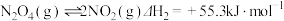
则反应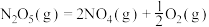 的
的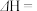
________  。
。
(2)若提高反应温度至35℃,则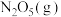 完全分解后体系压强
完全分解后体系压强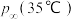
_________ 63.1 (填“大于”“等于”或“小于”),原因是
(填“大于”“等于”或“小于”),原因是_______________ 。
(3)25℃时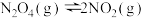 反应的平衡常数
反应的平衡常数
_________  (
( 为以分压表示的平衡常数,计算结果保留1位小数)。下图中可以示意平衡常数
为以分压表示的平衡常数,计算结果保留1位小数)。下图中可以示意平衡常数 随温度T变化趋势的是
随温度T变化趋势的是_________ 。
A. B.
B. C.
C. D.
D.
(4)邻二甲苯经硝化得到两种一硝化产物:3-硝基邻二甲苯(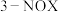 )和4-硝基邻二甲苯(
)和4-硝基邻二甲苯(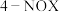 )。某研究小组研究了采用
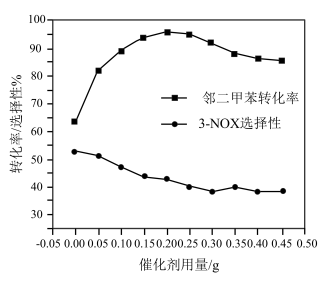
)。某研究小组研究了采用 为硝化剂时催化剂用量对该反应的影响。将一定量的催化剂和邻二甲苯置于反应瓶中,控制温度反应一定时间。测得邻二甲苯的转化率和
为硝化剂时催化剂用量对该反应的影响。将一定量的催化剂和邻二甲苯置于反应瓶中,控制温度反应一定时间。测得邻二甲苯的转化率和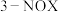 的选择性如图所示:
的选择性如图所示:
①描述并解释 随着催化剂用量的增加,邻二甲苯转化率的变化趋势:________________ 。
②在图中画出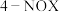 的选择性随催化剂用量变化的曲线
的选择性随催化剂用量变化的曲线________________ 。
 为硝化剂是一种新型的绿色硝化技术,F Daniels等曾利用测压法在刚性反应器中研究了25℃时
为硝化剂是一种新型的绿色硝化技术,F Daniels等曾利用测压法在刚性反应器中研究了25℃时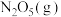 分解反应:
分解反应:
其中
 二聚为
二聚为 的反应可以迅速达到平衡,体系的总压强
的反应可以迅速达到平衡,体系的总压强 随时间
随时间 的变化如下表所示(
的变化如下表所示( 时,
时,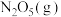 完全分解):
完全分解): | 0 | 40 | 80 | 160 | 260 | 1300 | 1700 |  |
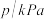 | 35.8 | 40.3 | 42.5 | 45.9 | 49.2 | 61.2 | 62.3 | 63.1 |
(1)已知:
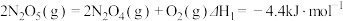
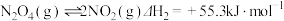
则反应
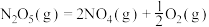 的
的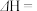
 。
。(2)若提高反应温度至35℃,则
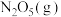 完全分解后体系压强
完全分解后体系压强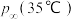
 (填“大于”“等于”或“小于”),原因是
(填“大于”“等于”或“小于”),原因是(3)25℃时
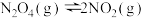 反应的平衡常数
反应的平衡常数
 (
( 为以分压表示的平衡常数,计算结果保留1位小数)。下图中可以示意平衡常数
为以分压表示的平衡常数,计算结果保留1位小数)。下图中可以示意平衡常数 随温度T变化趋势的是
随温度T变化趋势的是A.
 B.
B. C.
C. D.
D.
(4)邻二甲苯经硝化得到两种一硝化产物:3-硝基邻二甲苯(
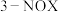 )和4-硝基邻二甲苯(
)和4-硝基邻二甲苯(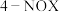 )。某研究小组研究了采用
)。某研究小组研究了采用 为硝化剂时催化剂用量对该反应的影响。将一定量的催化剂和邻二甲苯置于反应瓶中,控制温度反应一定时间。测得邻二甲苯的转化率和
为硝化剂时催化剂用量对该反应的影响。将一定量的催化剂和邻二甲苯置于反应瓶中,控制温度反应一定时间。测得邻二甲苯的转化率和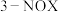 的选择性如图所示:
的选择性如图所示:①
②在图中画出
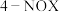 的选择性随催化剂用量变化的曲线
的选择性随催化剂用量变化的曲线
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】“绿水青山就是金山银山”,因此研究 、
、 等大气污染物的妥善处理具有重要意义。
等大气污染物的妥善处理具有重要意义。
(1) 的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的
的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的 。已知吸收过程中相关反应的热化学方程式如下:
。已知吸收过程中相关反应的热化学方程式如下:
①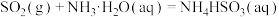
 ;
;
②
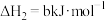 ;
;
③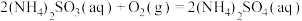
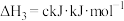 。
。
则反应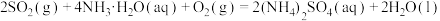 的
的
_____ 
(2)燃煤发电厂常利用反应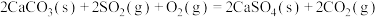
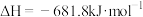 对煤进行脱硫处理来减少
对煤进行脱硫处理来减少 的排放。对于该反应,在
的排放。对于该反应,在 时,借助传感器测得反应在不同时间点上各物质的浓度如下:
时,借助传感器测得反应在不同时间点上各物质的浓度如下:
① 内,平均反应速率
内,平均反应速率
________  ;当升高温度,该反应的平衡常数K
;当升高温度,该反应的平衡常数K________  填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。
② 后,只改变某一条件,反应重新达到平衡。根据上表中的数据判断,改变的条件可能是
后,只改变某一条件,反应重新达到平衡。根据上表中的数据判断,改变的条件可能是________  填字母
填字母 。
。
A.加入一定量的粉状碳酸钙
B.通入一定量的
C.适当缩小容器的体积
D.加入合适的催化剂
(3) 的排放主要来自于汽车尾气,有人利用反应
的排放主要来自于汽车尾气,有人利用反应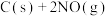

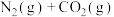
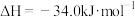 ,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压,测得NO的转化率随温度的变化如图所示:
,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压,测得NO的转化率随温度的变化如图所示:
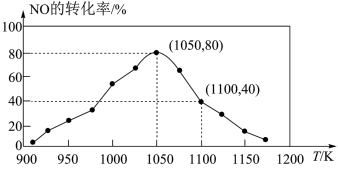
由图可知,1050K前反应中NO的转化率随温度升高而增大,其原因为________ ;在1100K时, 的体积分数为
的体积分数为________ 。
(4)用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数 记作
记作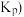 。在1050K、
。在1050K、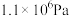 时,该反应的化学平衡常数
时,该反应的化学平衡常数
________  已知:气体分压
已知:气体分压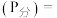 气体总压
气体总压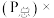 体积分数
体积分数 。
。
(5)为避免汽车尾气中的有害气体对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和NO发生反应

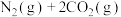
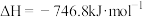 ,生成无毒的
,生成无毒的 和
和 。实验测得,
。实验测得,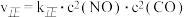 ,
,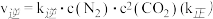 、
、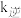 为速率常数,只与温度有关
为速率常数,只与温度有关 。
。
①达到平衡后,仅升高温度,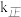 增大的倍数
增大的倍数________  填“
填“ ”“
”“ ”或“
”或“ ”
” 增大的倍数。
增大的倍数。
②若在1L的密闭容器中充入1molCO和1molNO,在一定温度下达到平衡时,CO的转化率为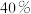 ,则
,则
__________ 。
 、
、 等大气污染物的妥善处理具有重要意义。
等大气污染物的妥善处理具有重要意义。(1)
 的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的
的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的 。已知吸收过程中相关反应的热化学方程式如下:
。已知吸收过程中相关反应的热化学方程式如下:①
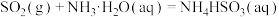
 ;
;②

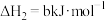 ;
;③
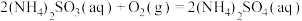
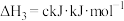 。
。则反应
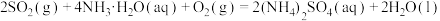 的
的

(2)燃煤发电厂常利用反应
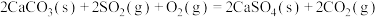
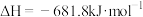 对煤进行脱硫处理来减少
对煤进行脱硫处理来减少 的排放。对于该反应,在
的排放。对于该反应,在 时,借助传感器测得反应在不同时间点上各物质的浓度如下:
时,借助传感器测得反应在不同时间点上各物质的浓度如下:| 0 | 10 | 20 | 30 | 40 | 50 | |
| O2 | 1.00 | 0.79 | 0.60 | 0.60 | 0.64 | 0.64 |
| CO2 | 0 | 0.42 | 0.80 | 0.80 | 0.88 | 0.88 |
①
 内,平均反应速率
内,平均反应速率
 ;当升高温度,该反应的平衡常数K
;当升高温度,该反应的平衡常数K 填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。②
 后,只改变某一条件,反应重新达到平衡。根据上表中的数据判断,改变的条件可能是
后,只改变某一条件,反应重新达到平衡。根据上表中的数据判断,改变的条件可能是 填字母
填字母 。
。A.加入一定量的粉状碳酸钙
B.通入一定量的

C.适当缩小容器的体积
D.加入合适的催化剂
(3)
 的排放主要来自于汽车尾气,有人利用反应
的排放主要来自于汽车尾气,有人利用反应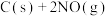

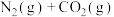
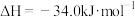 ,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压,测得NO的转化率随温度的变化如图所示:
,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压,测得NO的转化率随温度的变化如图所示:
由图可知,1050K前反应中NO的转化率随温度升高而增大,其原因为
 的体积分数为
的体积分数为(4)用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数
 记作
记作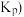 。在1050K、
。在1050K、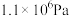 时,该反应的化学平衡常数
时,该反应的化学平衡常数
 已知:气体分压
已知:气体分压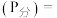 气体总压
气体总压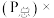 体积分数
体积分数 。
。(5)为避免汽车尾气中的有害气体对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和NO发生反应


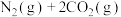
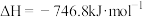 ,生成无毒的
,生成无毒的 和
和 。实验测得,
。实验测得,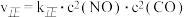 ,
,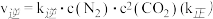 、
、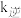 为速率常数,只与温度有关
为速率常数,只与温度有关 。
。①达到平衡后,仅升高温度,
 增大的倍数
增大的倍数 填“
填“ ”“
”“ ”或“
”或“ ”
” 增大的倍数。
增大的倍数。②若在1L的密闭容器中充入1molCO和1molNO,在一定温度下达到平衡时,CO的转化率为
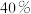 ,则
,则
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】“一碳化学”是指以研究分子中只含一个碳原子的化合物[如甲烷(CH4)、合成气(CO和H2)、CO2、CH3OH等]为原料来合成一系列化工原料和燃料的化学。
(1)已知0.5mol碳单质和0.5mol水蒸气在t℃,pkPa时,完全反应生成一氧化碳和氢气(合成气),吸收了akJ热量。该反应的热化学方程式是:___ 。
(2)也可以利用CO2与CH4生产合成气(CO、H2):
已知:①CH4(g)+2O2(g) CO2(g)+2H2O(g)ΔH1
CO2(g)+2H2O(g)ΔH1
②CO(g)+H2O(g) CO2(g)+H2(g)ΔH2
CO2(g)+H2(g)ΔH2
③2CO(g)+O2(g) 2CO2(g)ΔH3
2CO2(g)ΔH3
则反应CO2(g)+CH4(g) 2CO(g)+2H2(g)ΔH=
2CO(g)+2H2(g)ΔH=____ (用含ΔH1、ΔH2、ΔH3的式子表示)。反应①的平衡常数表达式K=___ 。
(3)CO2经催化加氢可合成乙烯:2CO2(g)+6H2(g) C2H4(g)+4H2O(g),该反应是综合利用CO2的热点研究领域。0.1MPa时,按n(CO2):n(H2)=l:3投料,测得不同温度下平衡时体系中各物质浓度的关系如图。
C2H4(g)+4H2O(g),该反应是综合利用CO2的热点研究领域。0.1MPa时,按n(CO2):n(H2)=l:3投料,测得不同温度下平衡时体系中各物质浓度的关系如图。

该反应是一个___ (填“放热”或“吸热”)反应,曲线___ 代表H2O。其它条件不变,T1℃、0.2MPa下反应达平衡时c(H2)___ M点(填“>”“=”或“<”)。
(1)已知0.5mol碳单质和0.5mol水蒸气在t℃,pkPa时,完全反应生成一氧化碳和氢气(合成气),吸收了akJ热量。该反应的热化学方程式是:
(2)也可以利用CO2与CH4生产合成气(CO、H2):
已知:①CH4(g)+2O2(g)
 CO2(g)+2H2O(g)ΔH1
CO2(g)+2H2O(g)ΔH1②CO(g)+H2O(g)
 CO2(g)+H2(g)ΔH2
CO2(g)+H2(g)ΔH2③2CO(g)+O2(g)
 2CO2(g)ΔH3
2CO2(g)ΔH3则反应CO2(g)+CH4(g)
 2CO(g)+2H2(g)ΔH=
2CO(g)+2H2(g)ΔH=(3)CO2经催化加氢可合成乙烯:2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g),该反应是综合利用CO2的热点研究领域。0.1MPa时,按n(CO2):n(H2)=l:3投料,测得不同温度下平衡时体系中各物质浓度的关系如图。
C2H4(g)+4H2O(g),该反应是综合利用CO2的热点研究领域。0.1MPa时,按n(CO2):n(H2)=l:3投料,测得不同温度下平衡时体系中各物质浓度的关系如图。
该反应是一个
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】在密闭容器中进行反应①Fe(s)+CO2(g)  FeO(s)+CO(g) ΔH1=akJ·mol-
FeO(s)+CO(g) ΔH1=akJ·mol-
反应②2CO(g)+O2(g) 2CO2(g) △H2=b kJ·mol-
2CO2(g) △H2=b kJ·mol-
反应③2Fe(s)+O2(g) 2FeO(s) △H3
2FeO(s) △H3
(1) △H3=___________ (用含a、b的代数式表示)。
(2)反应①的化学平衡常数表达式K=____________ ,已知500℃时反应①的平衡常数K=1,在此温度下2 L密闭容器中进行反应①,Fe和CO2的起始量均为2.0 mol,达到平衡时CO2的转化率为______________ ,CO的平衡浓度为________________ 。
(3)将上述平衡体系升温至700℃,再次达到平衡时体系中CO的浓度是CO2浓度的两倍,则a___________ 0(填“>”、“<”或“=”)。为了加快化学反应速率且使体系中CO的物质的量增加,其他条件不变时,可以采取的措施有__________ (填序号)。
A.缩小反应器体积 B.再通入CO2 c.升高温度 D.使用合适的催化剂
 FeO(s)+CO(g) ΔH1=akJ·mol-
FeO(s)+CO(g) ΔH1=akJ·mol-反应②2CO(g)+O2(g)
 2CO2(g) △H2=b kJ·mol-
2CO2(g) △H2=b kJ·mol-反应③2Fe(s)+O2(g)
 2FeO(s) △H3
2FeO(s) △H3(1) △H3=
(2)反应①的化学平衡常数表达式K=
(3)将上述平衡体系升温至700℃,再次达到平衡时体系中CO的浓度是CO2浓度的两倍,则a
A.缩小反应器体积 B.再通入CO2 c.升高温度 D.使用合适的催化剂
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】“绿水青山就是金山银山”,因此研究NOx、SO2等大气污染物的妥善处理具有重要意义。
(1)SO2的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的SO2。
已知吸收过程中相关反应的热化学方程式如下:
①SO2(g)+NH3·H2O(aq)=NH4HSO3(aq)ΔH1=a kJ·mol-1;
②NH3·H2O(aq)+NH4HSO3(aq)=(NH4)2SO3(aq)+H2O(l)ΔH2=b kJ·mol-1;
③2(NH4)2SO3(aq)+O2(g) = 2(NH4)2SO4(aq)ΔH3=c kJ·kJ·mol-1。
则反应2SO2(g)+4NH3·H2O(aq)+O2(g)=2(NH4)2SO4(aq)+2H2O(l)的ΔH=_______ kJ·mol-1
(2)燃煤发电厂常利用反应:2CaCO3(s)+2SO2(g)+O2(g) = 2CaSO4(s)+2CO2(g)ΔH=-681.8 kJ·mol-1对煤进行脱硫处理来减少SO2的排放。对于该反应,在T℃时,借助传感器测得反应在不同时间点上各物质的浓度如表:
①当升高温度,该反应的平衡常数K_______ (填“增大”“减小”或“不变”)。
②30min后,只改变某一条件,反应重新达到平衡。根据上表中的数据判断,改变的条件可能是_______ (填字母)。
A.加入一定量的粉状碳酸钙 B.通入一定量的O2
C.适当缩小容器的体积 D.加入合适的催化剂
(3)NOx的排放主要来自于汽车尾气,有人利用反应C(s)+2NO(g)⇌N2(g)+CO2(g)ΔH=-34.0 kJ·mol-1,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压,测得NO的转化率随温度的变化如图所示:
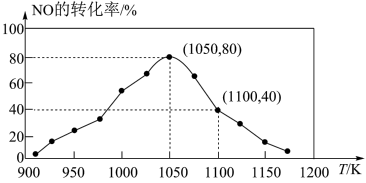
由图可知,1050K前反应中NO的转化率随温度升高而增大,其原因为_______ ;在1100K时,CO2的体积分数为_______ 。
(4)用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106Pa时,该反应的化学平衡常数Kp=_______ [已知:气体分压(P分)=气体总压(P总)×体积分数]。
(5)工业上常用高浓度的 K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如图:

①在阳极区发生的反应包括_______ 和H++HCO =CO2↑+H2O
=CO2↑+H2O
②简述CO 在阴极区再生的原理:
在阴极区再生的原理:_______ 。
(1)SO2的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的SO2。
已知吸收过程中相关反应的热化学方程式如下:
①SO2(g)+NH3·H2O(aq)=NH4HSO3(aq)ΔH1=a kJ·mol-1;
②NH3·H2O(aq)+NH4HSO3(aq)=(NH4)2SO3(aq)+H2O(l)ΔH2=b kJ·mol-1;
③2(NH4)2SO3(aq)+O2(g) = 2(NH4)2SO4(aq)ΔH3=c kJ·kJ·mol-1。
则反应2SO2(g)+4NH3·H2O(aq)+O2(g)=2(NH4)2SO4(aq)+2H2O(l)的ΔH=
(2)燃煤发电厂常利用反应:2CaCO3(s)+2SO2(g)+O2(g) = 2CaSO4(s)+2CO2(g)ΔH=-681.8 kJ·mol-1对煤进行脱硫处理来减少SO2的排放。对于该反应,在T℃时,借助传感器测得反应在不同时间点上各物质的浓度如表:
| 0 | 10 | 20 | 30 | 40 | 50 | |
| O2 | 1.00 | 0.79 | 0.60 | 0.60 | 0.64 | 0.64 |
| CO2 | 0 | 0.42 | 0.80 | 0.80 | 0.88 | 0.88 |
①当升高温度,该反应的平衡常数K
②30min后,只改变某一条件,反应重新达到平衡。根据上表中的数据判断,改变的条件可能是
A.加入一定量的粉状碳酸钙 B.通入一定量的O2
C.适当缩小容器的体积 D.加入合适的催化剂
(3)NOx的排放主要来自于汽车尾气,有人利用反应C(s)+2NO(g)⇌N2(g)+CO2(g)ΔH=-34.0 kJ·mol-1,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压,测得NO的转化率随温度的变化如图所示:

由图可知,1050K前反应中NO的转化率随温度升高而增大,其原因为
(4)用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106Pa时,该反应的化学平衡常数Kp=
(5)工业上常用高浓度的 K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如图:

①在阳极区发生的反应包括
 =CO2↑+H2O
=CO2↑+H2O②简述CO
 在阴极区再生的原理:
在阴极区再生的原理:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】焦炭与CO、H2均是重要的能源,也是重要的化工原料。
(1)已知C、H2、CO的燃烧热(△H)分别为-393.5 kJ·mol-1、-285.8kJ·mol-1、-283 kJ·mol-1,又知水的气化热为+44 kJ/mol。
①焦炭与水蒸气反应生成CO、H2的热化学方程式为___________________ 。
②若将足量焦炭与2mol水蒸气充分反应,当吸收能量为191.7 kJ时,则此时H2O(g)的转化率为_________________ 。
(2)将焦炭与水蒸气置于容积为2L的密闭容器中发生反应:C(s)+H2O(g) CO(g)+H2(g),其中H2O、CO的物质的量随时间的变化曲线如图所示。
CO(g)+H2(g),其中H2O、CO的物质的量随时间的变化曲线如图所示。

①第一个平衡时段的平衡常数是______________ ,若反应进行到2 min时,改变了温度,使曲线发生如图所示的变化,则温度变化为___________ (填“升温”或“降温”)。
②反应至5 min时,若也只改变了某一个条件,使曲线发生如图所示的变化,该条件可能是下述中的____ 。
a.增加了C
b.增加了水蒸气
c.降低了温度
d.增加了压强
(3)假设(2)中反应在第2min时,将容器容积压缩至1 L,请在上图中绘制出能反映H2O、CO物质的量变化趋势的图象。______
(4)若以CO、O2、K2CO3等构成的熔融盐电池为动力,电解400 mL饱和食盐水,则负极上的电极反应式为______________________ ,当有5·6g燃料被消耗时,电解池中溶液的pH=__________ (忽略溶液的体积变化,不考虑能量的其它损耗)。
(1)已知C、H2、CO的燃烧热(△H)分别为-393.5 kJ·mol-1、-285.8kJ·mol-1、-283 kJ·mol-1,又知水的气化热为+44 kJ/mol。
①焦炭与水蒸气反应生成CO、H2的热化学方程式为
②若将足量焦炭与2mol水蒸气充分反应,当吸收能量为191.7 kJ时,则此时H2O(g)的转化率为
(2)将焦炭与水蒸气置于容积为2L的密闭容器中发生反应:C(s)+H2O(g)
 CO(g)+H2(g),其中H2O、CO的物质的量随时间的变化曲线如图所示。
CO(g)+H2(g),其中H2O、CO的物质的量随时间的变化曲线如图所示。
①第一个平衡时段的平衡常数是
②反应至5 min时,若也只改变了某一个条件,使曲线发生如图所示的变化,该条件可能是下述中的
a.增加了C
b.增加了水蒸气
c.降低了温度
d.增加了压强
(3)假设(2)中反应在第2min时,将容器容积压缩至1 L,请在上图中绘制出能反映H2O、CO物质的量变化趋势的图象。
(4)若以CO、O2、K2CO3等构成的熔融盐电池为动力,电解400 mL饱和食盐水,则负极上的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】硫化氢的转化是资源利用和环境保护的重要研究课题。由硫化氢获得硫单质有多种方法。
(1)用FeCl3溶液吸收H2S,得到单质硫;过滤后,再以石墨为电极,在一定条件下电解滤液实现FeCl3溶液的再生。FeCl3与H2S 反应的离子方程式为_____ 。
电解池中H+在阴极放电产生H2,阳极的电极反应为_____ 。
综合分析该工艺的两个反应,可知两个显著优点:①H2S的原子利用率100%;②_____ 。

(2)将 H2S 和空气的混合气体通入 FeCl3、FeCl2、CuCl2的混合溶液中反应回收硫单质,其物质转化如题图1 所示。反应中当有 1molH2S 转化为硫单质时,保持溶液中 Fe3+的物质的量不变,需要消耗 O2的物质的量为_____ 。
(3)工业上常采用图 2 电解装置电解 K4[Fe(CN)6]和KHCO3混合溶液,电解一段时间后,通入H2S加以处理。利用生成的铁的化合物K3[Fe(CN)6]将气态废弃物中的H2S转化为可利用的硫单质,自身转化为K4[Fe(CN)6]。
①电解时,阳极的电极反应式为_____ 。
②当有16 g S析出时,阴极产生的气体在标准状况下的体积为_____ 。
③通入H2S时发生如下反应,补全离子方程式:________________________________________ 。

(1)用FeCl3溶液吸收H2S,得到单质硫;过滤后,再以石墨为电极,在一定条件下电解滤液实现FeCl3溶液的再生。FeCl3与H2S 反应的离子方程式为
电解池中H+在阴极放电产生H2,阳极的电极反应为
综合分析该工艺的两个反应,可知两个显著优点:①H2S的原子利用率100%;②

(2)将 H2S 和空气的混合气体通入 FeCl3、FeCl2、CuCl2的混合溶液中反应回收硫单质,其物质转化如题图1 所示。反应中当有 1molH2S 转化为硫单质时,保持溶液中 Fe3+的物质的量不变,需要消耗 O2的物质的量为
(3)工业上常采用图 2 电解装置电解 K4[Fe(CN)6]和KHCO3混合溶液,电解一段时间后,通入H2S加以处理。利用生成的铁的化合物K3[Fe(CN)6]将气态废弃物中的H2S转化为可利用的硫单质,自身转化为K4[Fe(CN)6]。
①电解时,阳极的电极反应式为
②当有16 g S析出时,阴极产生的气体在标准状况下的体积为
③通入H2S时发生如下反应,补全离子方程式:

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】高氯酸铜易溶于水,在130 ℃时会发生分解反应,是一种燃烧催化剂。HClO4是易挥发的发烟液体,温度高于130 ℃易爆炸。以食盐等为原料制备高氯酸铜晶体[Cu(ClO4)2·6H2O]的一种工艺流程如图:

(1)发生“电解I”时,所用的交换膜是_______ (填“阴”或“阳”)离子交换膜。
(2)已知上述工艺流程中“歧化反应”的氧化产物和还原产物物质的量之比为1︰5,写出该反应的离子方程式:_______ 。
(3)操作a的名称是_______ ,该流程中可循环利用的物质是_______ (填化学式)。
(4)向Cu2(OH)2CO3沉淀中滴加稍过量的HClO4小心搅拌,适度加热后得到蓝色Cu(ClO4)2溶液,同时会产生大量的白雾。加热时温度不能过高的原因是_______ 。
(5)某温度下,高氯酸铜按A、B两种方式同时分解,分解过程中铜的化合价不发生改变。A方式为Cu(ClO4)2 CuCl2+4O2↑,若4 mol高氯酸铜在该温度下按A、B各占50%的方式完全分解,且A、B两种方式转移的电子数之比为8︰7,则B方式为
CuCl2+4O2↑,若4 mol高氯酸铜在该温度下按A、B各占50%的方式完全分解,且A、B两种方式转移的电子数之比为8︰7,则B方式为_______ (用化学方程式表示)。

(1)发生“电解I”时,所用的交换膜是
(2)已知上述工艺流程中“歧化反应”的氧化产物和还原产物物质的量之比为1︰5,写出该反应的离子方程式:
(3)操作a的名称是
(4)向Cu2(OH)2CO3沉淀中滴加稍过量的HClO4小心搅拌,适度加热后得到蓝色Cu(ClO4)2溶液,同时会产生大量的白雾。加热时温度不能过高的原因是
(5)某温度下,高氯酸铜按A、B两种方式同时分解,分解过程中铜的化合价不发生改变。A方式为Cu(ClO4)2
 CuCl2+4O2↑,若4 mol高氯酸铜在该温度下按A、B各占50%的方式完全分解,且A、B两种方式转移的电子数之比为8︰7,则B方式为
CuCl2+4O2↑,若4 mol高氯酸铜在该温度下按A、B各占50%的方式完全分解,且A、B两种方式转移的电子数之比为8︰7,则B方式为
您最近一年使用:0次



