下图中P为一可自由滑动的活塞,K为容器A和B之间的旋塞。将K关闭,在A中充有1molX和1molY,B中充有3molX和3molY。起始时,V(A)=V(B)=1L,在相同的温度和有催化剂存在的条件下,两容器中各自发生反应:
X(g)+Y(g)⇌2Z(g)+W(g);△H<0。
当达到平衡时,V (A)=1.25L。问:
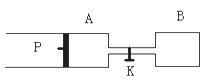
(1)A中Y的转化率为__________ ,A、B中Y的转化率的关系是α(A)___ α(B)(填“<”、“>”或“=”)。
(2)如果将B端改装成与A端一致(如下图),将K关闭,达到平衡后,B的体积为______ L,B中X的体积分数为___________________ 。此时,如果将K打开,A中活塞_________ (填“移动”或“不移动”)。
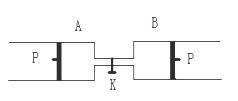
X(g)+Y(g)⇌2Z(g)+W(g);△H<0。
当达到平衡时,V (A)=1.25L。问:

(1)A中Y的转化率为
(2)如果将B端改装成与A端一致(如下图),将K关闭,达到平衡后,B的体积为

9-10高三·四川南充·阶段练习 查看更多[2]
更新时间:2010-12-13 14:03:06
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】已知A(g) +B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
回答下列问题:
(1)该反应的平衡常数表达式K=_____________ ,△H_____ 0(填“<” “>”或 “=”);
(2)830℃时,向体积为10L的密闭容器中充入0.2mol的A和0.2mol的B,如反应初始到10s内A的平均反应速率v(A)=0.001 mol·L-1·s-1,则10s时c(D)=_____ 。此时,该反应是否处于平衡状态:___ (填“是”或“否”)。达到平衡时A的转化率为__________ ,如果这时向该密闭容器中充入1mol氦气,A的转化率__________ (填“变大”、“变小”或“不变”)。
(3)可用于判断该反应达到平衡状态的依据为________ (填选项符号):
a、压强不随时间改变 b、气体的密度不再发生改变
c、c(D)不随时间改变 d、单位时间内生成A和C的物质的量相等
(4)1000℃时反应C(g)+D(g) A(g) +B(g)的平衡常数的值为
A(g) +B(g)的平衡常数的值为___________ 。
 C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:| 温度/0C | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.1 | 1.0 | 0.5 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K=
(2)830℃时,向体积为10L的密闭容器中充入0.2mol的A和0.2mol的B,如反应初始到10s内A的平均反应速率v(A)=0.001 mol·L-1·s-1,则10s时c(D)=
(3)可用于判断该反应达到平衡状态的依据为
a、压强不随时间改变 b、气体的密度不再发生改变
c、c(D)不随时间改变 d、单位时间内生成A和C的物质的量相等
(4)1000℃时反应C(g)+D(g)
 A(g) +B(g)的平衡常数的值为
A(g) +B(g)的平衡常数的值为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】科学家利用氧化锆锌作催化剂,在一定温度下将 和
和 转化为重要有机原料甲醇
转化为重要有机原料甲醇 ,其原理为:
,其原理为:
 。在容积为
。在容积为 的恒温密闭容器中,充入
的恒温密闭容器中,充入 和
和 发生上述反应。
发生上述反应。 和
和 的物质的量随时间变化如图所示。回答下列问题:
的物质的量随时间变化如图所示。回答下列问题:
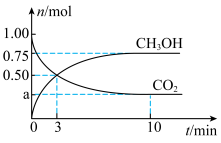
(1)图中
_____ ; 时,
时, 的转化率为
的转化率为_____ 。
(2)下列叙述正确的是_____ (填序号)。
a. 时
时 的生成速率等于其分解速率
的生成速率等于其分解速率
b.由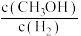 保持不变,可判断该反应达到平衡状态
保持不变,可判断该反应达到平衡状态
c.当 时,该反应一定达到平衡状态
时,该反应一定达到平衡状态
d.若改变催化剂,则反应达到平衡状态所需的时间一定小于
(3)该温度下达到平衡时,混合气体中 的体积分数为
的体积分数为_____ ,此时体系压强与开始时的压强之比为_____ 。
(4)其他条件不变时,下列措施不能使生成 的反应速率增大的是
的反应速率增大的是_____ (填序号)。
a.增大 的浓度
的浓度
b.将容器的容积变为
c.恒容条件下充入一定量
d.将恒温恒容容器改为绝热恒容容器
已知升高温度,平衡向吸热方向移动。降低温度,此反应再次达到平衡时体系中混合气体的平均摩尔质量_____ (填“增大”“减小”或“不变”)。
 和
和 转化为重要有机原料甲醇
转化为重要有机原料甲醇 ,其原理为:
,其原理为:
 。在容积为
。在容积为 的恒温密闭容器中,充入
的恒温密闭容器中,充入 和
和 发生上述反应。
发生上述反应。 和
和 的物质的量随时间变化如图所示。回答下列问题:
的物质的量随时间变化如图所示。回答下列问题:
(1)图中

 时,
时, 的转化率为
的转化率为(2)下列叙述正确的是
a.
 时
时 的生成速率等于其分解速率
的生成速率等于其分解速率b.由
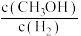 保持不变,可判断该反应达到平衡状态
保持不变,可判断该反应达到平衡状态c.当
 时,该反应一定达到平衡状态
时,该反应一定达到平衡状态d.若改变催化剂,则反应达到平衡状态所需的时间一定小于

(3)该温度下达到平衡时,混合气体中
 的体积分数为
的体积分数为(4)其他条件不变时,下列措施不能使生成
 的反应速率增大的是
的反应速率增大的是a.增大
 的浓度
的浓度b.将容器的容积变为

c.恒容条件下充入一定量

d.将恒温恒容容器改为绝热恒容容器
已知升高温度,平衡向吸热方向移动。降低温度,此反应再次达到平衡时体系中混合气体的平均摩尔质量
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】对碳及其氧化物的化学研究有助于人类充分利用化石燃料,消除碳氧化物对环境的负面影响。用 代替
代替 与燃料
与燃料 反应,既可以提高燃烧效率,又能得到高纯
反应,既可以提高燃烧效率,又能得到高纯 ,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
①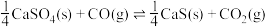
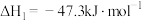
②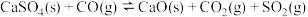
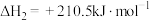
③
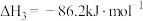
(1)反应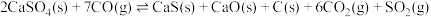 的
的
___________ (用 表示)。
表示)。
(2)向盛有 的真空恒容容器中充入
的真空恒容容器中充入 ,反应①于
,反应①于 达到平衡(
达到平衡( ),平衡时
),平衡时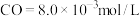 ,
, 的平衡转化率为
的平衡转化率为___________ 。(忽略副反应,结果保留2位有效数字)。
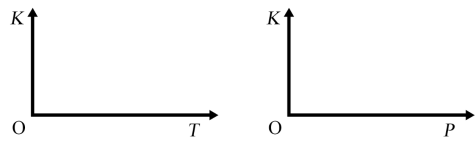
(3)其它条件不变时,升高温度戒缩小容器的体积,均能使反应②的平衡发生移动,请在下列坐标中作出该反应的平衡常数K随温度(T)、压强(P,缩小容器体积)变化而变化的示意图_______ :
(4)某温度下,测得 的
的 溶液的
溶液的 为11,将该温度下
为11,将该温度下 的
的 溶液
溶液 与
与 的
的 溶液,
溶液, 混合,通过计算填写以下不同情况时两溶液的体积比:
混合,通过计算填写以下不同情况时两溶液的体积比:
①若所得混合溶液为中性,且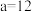 ,
,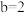 ,则
,则
___________ 。
②若所得混合溶液为中性,且 ,则
,则
___________ 。
③若所得混合溶液的 ,且
,且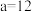 ,
,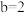 ,则
,则
___________ 。
 代替
代替 与燃料
与燃料 反应,既可以提高燃烧效率,又能得到高纯
反应,既可以提高燃烧效率,又能得到高纯 ,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。①
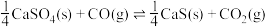
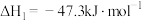
②
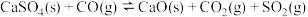
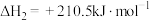
③

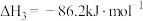
(1)反应
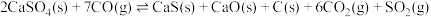 的
的
 表示)。
表示)。(2)向盛有
 的真空恒容容器中充入
的真空恒容容器中充入 ,反应①于
,反应①于 达到平衡(
达到平衡( ),平衡时
),平衡时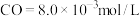 ,
, 的平衡转化率为
的平衡转化率为(3)其它条件不变时,升高温度戒缩小容器的体积,均能使反应②的平衡发生移动,请在下列坐标中作出该反应的平衡常数K随温度(T)、压强(P,缩小容器体积)变化而变化的示意图

(4)某温度下,测得
 的
的 溶液的
溶液的 为11,将该温度下
为11,将该温度下 的
的 溶液
溶液 与
与 的
的 溶液,
溶液, 混合,通过计算填写以下不同情况时两溶液的体积比:
混合,通过计算填写以下不同情况时两溶液的体积比:①若所得混合溶液为中性,且
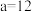 ,
,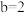 ,则
,则
②若所得混合溶液为中性,且
 ,则
,则
③若所得混合溶液的
 ,且
,且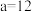 ,
,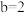 ,则
,则
您最近一年使用:0次
【推荐1】(1)某温度时,测得0.01mol﹒L-1的NaOH溶液的pH为11,则该温度下水的离子积常数Kw=___ 。
(2)在(1)所述温度下,将pH=a的NaOH溶液VaL与pH=b的硫酸VbL混合。若所得混合液的pH=10,且a=12,b=2,则Va:Vb=___ 。
(3)已知:25℃时,H2SO3Ka1=1.5×10-2Ka2=1.0×10-7;H2CO3Ka1=4.4×10-7Ka2=4.7×10-11;HNO2Ka=5.1×10-4;HClOKa=3.0×10-8下列离子反应正确的有:___ 。
A.2HCO +SO2=SO
+SO2=SO +2CO2+H2O
+2CO2+H2O
B.ClO-+CO2+H2O=HClO+HCO
C.ClO-+SO2+H2O=HClO+HSO
D.2ClO-+SO2+H2O=2HClO+SO
(4)已知:Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10。某实验小组采用K2CrO4作为指示剂,以AgNO3标准溶液滴定溶液中Cl-,利用Ag+与CrO 生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5mol/L)时,此时溶液中c(CrO
生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5mol/L)时,此时溶液中c(CrO )等于
)等于___ mol/L。
(5)已知:

①C(s)+H2O(g)=CO(g)+H2(g)ΔH=+131.3kJ﹒mol-1;
②CO2(g)+H2(g)=CO(g)+H2O(g)ΔH=+41.3kJ﹒mol-1。
则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为___ 。
(6)水煤气(主要成分CO、H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C(s)+H2O(g) CO(g)+H2(g);ΔH=+131.3kJ•mol-1。现有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0mol炭和1.0mol水蒸气(H216O),发生上述反应,达到平衡时,容器的体积变为原来的1.25倍。若再补充amol(a<3)水蒸气(H218O),最终容器中C16O和C18O的物质的量之比为
CO(g)+H2(g);ΔH=+131.3kJ•mol-1。现有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0mol炭和1.0mol水蒸气(H216O),发生上述反应,达到平衡时,容器的体积变为原来的1.25倍。若再补充amol(a<3)水蒸气(H218O),最终容器中C16O和C18O的物质的量之比为___ 。
(2)在(1)所述温度下,将pH=a的NaOH溶液VaL与pH=b的硫酸VbL混合。若所得混合液的pH=10,且a=12,b=2,则Va:Vb=
(3)已知:25℃时,H2SO3Ka1=1.5×10-2Ka2=1.0×10-7;H2CO3Ka1=4.4×10-7Ka2=4.7×10-11;HNO2Ka=5.1×10-4;HClOKa=3.0×10-8下列离子反应正确的有:
A.2HCO
 +SO2=SO
+SO2=SO +2CO2+H2O
+2CO2+H2OB.ClO-+CO2+H2O=HClO+HCO

C.ClO-+SO2+H2O=HClO+HSO

D.2ClO-+SO2+H2O=2HClO+SO

(4)已知:Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10。某实验小组采用K2CrO4作为指示剂,以AgNO3标准溶液滴定溶液中Cl-,利用Ag+与CrO
 生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5mol/L)时,此时溶液中c(CrO
生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5mol/L)时,此时溶液中c(CrO )等于
)等于(5)已知:

①C(s)+H2O(g)=CO(g)+H2(g)ΔH=+131.3kJ﹒mol-1;
②CO2(g)+H2(g)=CO(g)+H2O(g)ΔH=+41.3kJ﹒mol-1。
则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为
(6)水煤气(主要成分CO、H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C(s)+H2O(g)
 CO(g)+H2(g);ΔH=+131.3kJ•mol-1。现有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0mol炭和1.0mol水蒸气(H216O),发生上述反应,达到平衡时,容器的体积变为原来的1.25倍。若再补充amol(a<3)水蒸气(H218O),最终容器中C16O和C18O的物质的量之比为
CO(g)+H2(g);ΔH=+131.3kJ•mol-1。现有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0mol炭和1.0mol水蒸气(H216O),发生上述反应,达到平衡时,容器的体积变为原来的1.25倍。若再补充amol(a<3)水蒸气(H218O),最终容器中C16O和C18O的物质的量之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】完成下列各题。
(1)已知25℃时,AgI的饱和溶液中c(Ag+)为1.22×10-8 mol/L,AgCl的饱和溶液中c(Ag+)为1.25×10-5 mol/L。若在5 mL含KCl和KI各为0.01 mol/L的溶液中,加入8 mL0.01 mol/L AgNO3溶液,这时溶液中所含溶质的离子浓度由大到小的次序是_______ 。[已知:25℃时Ksp(AgC1)=1.6×10-10,Ksp(AgI)=8.5×10-17]
(2)如图所示,无摩擦、无质量的活塞1,2,3和4将反应器隔成甲、乙、丙和丁4部分,分别进行反应:A(g)+B(g)⇌C(g),起始时物质的量已标在图中。某温度和100 kPa下达到平衡时,各部分的体积分别为V甲、V乙、V丙和V丁。这时若抽掉活塞1或3均不会引起其它活塞移动。
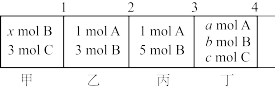
①据题意计算x=_______ 。
②a、b、c必须满足的一般条件是(请用含有a、b、c的方程表示):_______ 。
(1)已知25℃时,AgI的饱和溶液中c(Ag+)为1.22×10-8 mol/L,AgCl的饱和溶液中c(Ag+)为1.25×10-5 mol/L。若在5 mL含KCl和KI各为0.01 mol/L的溶液中,加入8 mL0.01 mol/L AgNO3溶液,这时溶液中所含溶质的离子浓度由大到小的次序是
(2)如图所示,无摩擦、无质量的活塞1,2,3和4将反应器隔成甲、乙、丙和丁4部分,分别进行反应:A(g)+B(g)⇌C(g),起始时物质的量已标在图中。某温度和100 kPa下达到平衡时,各部分的体积分别为V甲、V乙、V丙和V丁。这时若抽掉活塞1或3均不会引起其它活塞移动。
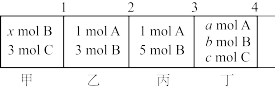
①据题意计算x=
②a、b、c必须满足的一般条件是(请用含有a、b、c的方程表示):
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】在100℃时,将0.200 mol的四氧化二氮气体充入2 L真空的密闭容器中,每隔一定的时间对该容器内的物质进行分析,得到如下表格:
试填空:
(1)该反应的化学方程式为N2O4 2NO2,达到平衡时,四氧化二氮的转化率为
2NO2,达到平衡时,四氧化二氮的转化率为__________ %,表中c2________ c3、a______ b(填“>”、“<”或“=”)。
(2) 20 s时四氧化二氮的浓度c1=________ mol/L,在0 s~20 s时间段内,四氧化二氮的平均反应速率为________ mol/(L·s)。
(3)若在相同情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度是________ mol/L。
时间s 浓度mol/L | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4) | 0.100 | c1 | 0.050 | c3 | a | b |
| c(NO2) | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
试填空:
(1)该反应的化学方程式为N2O4
 2NO2,达到平衡时,四氧化二氮的转化率为
2NO2,达到平衡时,四氧化二氮的转化率为(2) 20 s时四氧化二氮的浓度c1=
(3)若在相同情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度是
您最近一年使用:0次
【推荐1】I.已知在448℃时,反应H2(g)+I2(g)⇌2HI(g)的平衡常数K1为49,则该温度下反应2HI(g)⇌H2(g)+I2(g)的平衡常数K2为______ ;反应 H2(g)+
H2(g)+ I2(g)⇌HI(g)的平衡常数K3为
I2(g)⇌HI(g)的平衡常数K3为______ 。
II.在一定体积的密闭容器中进行如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
回答下列问题:
(1)该反应的逆反应为______ (填“吸热”或“放热”)反应。
(2)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为______ ℃,在此温度下,加入2 mol的CO和3 mol的H2O,达到平衡时,CO的转化率为______ 。
(3)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2 mol•L-1,c(H2)为1.5 mol•L-1,c(CO)为1 mol•L-1,c(H2O)为3 mol•L-1,则下一时刻,反应将______ (填“正向”或“逆向”)进行。
 H2(g)+
H2(g)+ I2(g)⇌HI(g)的平衡常数K3为
I2(g)⇌HI(g)的平衡常数K3为II.在一定体积的密闭容器中进行如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的逆反应为
(2)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为
(3)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2 mol•L-1,c(H2)为1.5 mol•L-1,c(CO)为1 mol•L-1,c(H2O)为3 mol•L-1,则下一时刻,反应将
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】在一个容积为2L的密闭容器内进行如下反应:A2(g)+3B2(g)=aX(g)。反应开始时,n(A2)=1.5mol,n(B2)= 4.0mol,2min后,n(B2)=0.4mol, n(X)=2.4mol。
请计算:
(1)a值_______ 。
(2)X的表示式(用A、B表示)_______ 。
(3)2min末A2的浓度________ 。
(4)B2的化学反应速率为_______ 。
(5)2min末B2的转化率为_______ 。
请计算:
(1)a值
(2)X的表示式(用A、B表示)
(3)2min末A2的浓度
(4)B2的化学反应速率为
(5)2min末B2的转化率为
您最近一年使用:0次




