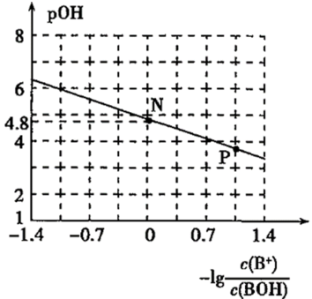
相同温度下,两种弱酸HA、HB的电离平衡常数Ka(HA)>Ka(HB)。下列有关说法正确的是
| A.浓度均为0.1 mol·L-1的HA、HB溶液中,其溶液的pH大小为:pH(HA)>pH(HB) |
| B.浓度均为0.1 mol·L-1的NaA、NaB溶液中,其溶液的pH大小为:pH(NaA)>pH(NaB) |
| C.等体积pH相同的HA、HB溶液,分别加入等浓度的NaOH溶液,恰好完全反应消耗的NaOH溶液体积HA比HB多 |
| D.在0.1 mol·L-1NaA溶液中各离子浓度关系为:c(Na+)>c(A一)>c(OH一)>c(H+) |
2011·江西新余·模拟预测 查看更多[2]
更新时间:2016-12-09 01:36:01
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列叙述正确的是
| A.稀醋酸中加入少量醋酸钠能增大醋酸的电离程度 |
| B.测得0.1mol·L-1的一元碱BOH溶液的pH=12,则BOH一定是一种弱电解质 |
| C.25℃时,pH=2的硫酸和pH=2的醋酸以体积比1:10混合后,溶液pH仍为2 |
D.室温下,向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中 减小 减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
| A.pH=6的溶液一定是酸性溶液 |
| B.c(H+)>c(OH-)一定是酸性溶液 |
| C.25℃时,水溶液中由水电离出的c(H+)和由水电离出的c(OH-)的乘积一定等于10−14 |
| D.HCl或NaOH溶于水,都会促进水的电离 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】室温下,下列说法正确的是
A.向水中加入少量 固体,促进水的电离, 固体,促进水的电离, 增大, 增大, 不变 不变 |
B.1 mol/L的 溶液中: 溶液中: |
C.在0.1mol•L-1NaHCO3溶液中:c(Na+)>c(HCO )>c(CO )>c(CO )>c(H2CO3) )>c(H2CO3) |
D.pH=8的 溶液中:由水电离出的c(H+)=1×10-6 mol·L-1 溶液中:由水电离出的c(H+)=1×10-6 mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】微电解技术处理高盐、难降解、高色度废水的一种工艺,其原理是在不通电的条件下,将酸性废水通过铁、碳构成的填料,利用电化学反应进行废水处理。下列叙述错误 的是
A.铁失电子产生的 可以还原废水中的 可以还原废水中的 |
B.碳表面的废水 降低 降低 |
C.若向装置内通入 ,则 ,则 在碳表面发生还原反应 在碳表面发生还原反应 |
D.溶液中产生的 ,能净化废水中悬浮的微小颗粒 ,能净化废水中悬浮的微小颗粒 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】设NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,2.24 L的CHCl3含有C-Cl键的数目为0.3 NA |
| B.1 L pH=1的盐酸中含有阴离子总数为0.1NA |
| C.1 mol NH4F固体中含有的共价键数目为5 NA |
| D.常温下,18 g水中含有的OH- 数目为10-7 NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,通过实验研究亚硫酸盐的性质,已知 ,
,
下列说法正确的是
 ,
,
| 实验 | 实验操作和现象 |
| 1 | 把SO2通入氨水,测得溶液pH=7 |
| 2 | 向0.1mol·L-1Na2SO3溶液中加入过量0.2mol·L-1CaCl2溶液,产生白色沉淀 |
| 3 | 向0.1mol·L-1NaHSO3溶液中滴入等浓度等体积的NaOH溶液 |
| 4 | 把少量氯气通入Na2SO3溶液中,测得溶液pH变小 |
A.实验1中,可计算出 |
B.实验2反应静置后的上层清液中有 |
C.实验3中: |
| D.实验4中说明氯气溶于水显酸性 |
您最近一年使用:0次

 )
) 为阿伏伽德罗常数的值。下列叙述正确的是
为阿伏伽德罗常数的值。下列叙述正确的是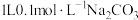 溶液中含
溶液中含 的数目小于
的数目小于
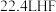 含有的分子数为
含有的分子数为 中含共价键的总数为
中含共价键的总数为
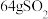 含有的氧原子数为
含有的氧原子数为