某温度(t ℃)时,水的离子积Kw=1×10-12
(1)将此温度下pH=11的NaOH溶液与pH=1的HCl溶液等体积混合,混合后溶液的pH=________ ,溶液中由水电离出的c(H+)=__________________
(2)将此温度下pH=11的NaOH溶液a L与pH=1的H2SO4溶液b L混合:若所得混合液的pH=2,则a∶b=_____________________ 。
(1)将此温度下pH=11的NaOH溶液与pH=1的HCl溶液等体积混合,混合后溶液的pH=
(2)将此温度下pH=11的NaOH溶液a L与pH=1的H2SO4溶液b L混合:若所得混合液的pH=2,则a∶b=
更新时间:2017-03-06 10:31:55
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)水是极弱的电解质,也是最重要的溶剂。常温下某电解质溶解在水中后,溶液中由水电离出的c(H+)=10-9mol·L-1,则该电解质可能是___________ (填序号)。
A.CuSO4 B.Na2CO3 C.HCl D.NaOH E.K2SO4
(2)常温下,将pH=3的盐酸aL分别与下列三种溶液混合,结果溶液均呈中性。
①c(OH-)=1.0×10-3mol·L-1的氨水bL;
②浓度为1.0×10-3mol·L-1的氨水cL;
③c(OH-)=1.0×10-3mol·L-1的氢氧化钡溶液dL。
则a、b、c、d之间的关系是___________ 。
(3)已知室温时,0.1mol·L-1的某一元酸HA在水中有0.1%发生电离,回答下列各问题:
①该溶液的pH=___________ 。
②升高温度时,K将______ (填“增大”、“减小”或“不变”),pH将_______ (填“增大”、“减小”或“不变”)。
③由HA电离出的c(H+)约为水电离出的c(H+)的_________ 倍。
(1)水是极弱的电解质,也是最重要的溶剂。常温下某电解质溶解在水中后,溶液中由水电离出的c(H+)=10-9mol·L-1,则该电解质可能是
A.CuSO4 B.Na2CO3 C.HCl D.NaOH E.K2SO4
(2)常温下,将pH=3的盐酸aL分别与下列三种溶液混合,结果溶液均呈中性。
①c(OH-)=1.0×10-3mol·L-1的氨水bL;
②浓度为1.0×10-3mol·L-1的氨水cL;
③c(OH-)=1.0×10-3mol·L-1的氢氧化钡溶液dL。
则a、b、c、d之间的关系是
(3)已知室温时,0.1mol·L-1的某一元酸HA在水中有0.1%发生电离,回答下列各问题:
①该溶液的pH=
②升高温度时,K将
③由HA电离出的c(H+)约为水电离出的c(H+)的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)现有下列物质:①熔融的NaCl;②稀硫酸;③液氯;④冰醋酸;⑤铜;⑥ ;⑦
;⑦ ;⑧液氨;⑨
;⑧液氨;⑨ ;⑩
;⑩ 固体。以上物质中属于弱电解质的是
固体。以上物质中属于弱电解质的是_______ (填数字序号,下同);属于非电解质的是_______ 。
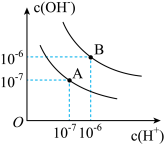
(2)水溶液存在离子平衡,水的电离平衡曲线如图所示。若以A点表示25℃时水在电离平衡时的离子浓度。当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积为_______ (不用写单位);在该温度时,pH为1的硫酸溶液中,硫酸的浓度为_______ ; 溶液pOH为
溶液pOH为_______ 。(已知 )
)
(3)一定温度下,向 溶液中加入
溶液中加入 固体,则醋酸的电离平衡向
固体,则醋酸的电离平衡向_______ (填“正”或“逆”)反应方向移动;水的电离程度将_______ (填“增大”、“减小”或“不变”)。
(1)现有下列物质:①熔融的NaCl;②稀硫酸;③液氯;④冰醋酸;⑤铜;⑥
 ;⑦
;⑦ ;⑧液氨;⑨
;⑧液氨;⑨ ;⑩
;⑩ 固体。以上物质中属于弱电解质的是
固体。以上物质中属于弱电解质的是(2)水溶液存在离子平衡,水的电离平衡曲线如图所示。若以A点表示25℃时水在电离平衡时的离子浓度。当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积为
 溶液pOH为
溶液pOH为 )
)
(3)一定温度下,向
 溶液中加入
溶液中加入 固体,则醋酸的电离平衡向
固体,则醋酸的电离平衡向
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】类别万千的酸碱溶液共同构筑了化学世界的丰富多彩。
(1)现有常温下pH=2的盐酸(甲)、pH=2的醋酸溶液(乙)和0.1mo1/L (丙),请根据下列操作回答:
(丙),请根据下列操作回答:
①常温下,将丙溶液加水稀释,下列数值一定变小的是___________ (填字母)。
A. B.
B. C.
C. D.
D.
②常温下,取甲、乙各1mL分别稀释至100mL,稀释后,水的电离程度:乙___________ 甲(填“>”“<”或“=”)。
(2)①某温度时,测得0.01mol/L NaOH溶液pH为11,则该温度___________ 25℃。(填“>”“<”或“=”)
②相同条件下,取等体积、等pH的 、NaOH和
、NaOH和 三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为
三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为 、
、 、
、 ,则三者的由大到小关系为
,则三者的由大到小关系为___________ 。
③某温度下,水的离子积常数 ,将
,将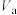 L pH=4的HCl溶液和
L pH=4的HCl溶液和 L pH=9的
L pH=9的 溶液混合均匀,测得溶液的pH=7,则
溶液混合均匀,测得溶液的pH=7,则
___________ 。
(3)已知:在25℃,有关弱电解质的电离平衡常数如下表有下表:
①将 通入氨水中,当
通入氨水中,当 降至
降至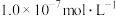 时,溶液中的
时,溶液中的
___________ 。
②下列微粒在溶液中不能大量共存的是___________ 。
A. 、
、 B.
B. 、
、 C.
C. 、
、 D.HClO、
D.HClO、
(1)现有常温下pH=2的盐酸(甲)、pH=2的醋酸溶液(乙)和0.1mo1/L
 (丙),请根据下列操作回答:
(丙),请根据下列操作回答:①常温下,将丙溶液加水稀释,下列数值一定变小的是
A.
 B.
B. C.
C. D.
D.
②常温下,取甲、乙各1mL分别稀释至100mL,稀释后,水的电离程度:乙
(2)①某温度时,测得0.01mol/L NaOH溶液pH为11,则该温度
②相同条件下,取等体积、等pH的
 、NaOH和
、NaOH和 三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为
三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为 、
、 、
、 ,则三者的由大到小关系为
,则三者的由大到小关系为③某温度下,水的离子积常数
 ,将
,将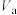 L pH=4的HCl溶液和
L pH=4的HCl溶液和 L pH=9的
L pH=9的 溶液混合均匀,测得溶液的pH=7,则
溶液混合均匀,测得溶液的pH=7,则
(3)已知:在25℃,有关弱电解质的电离平衡常数如下表有下表:
| 弱电解质 |  |  | HClO |  |
| 电离平衡常数 |   |   | 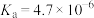 |  |
 通入氨水中,当
通入氨水中,当 降至
降至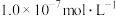 时,溶液中的
时,溶液中的
②下列微粒在溶液中不能大量共存的是
A.
 、
、 B.
B. 、
、 C.
C. 、
、 D.HClO、
D.HClO、
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.已知298K时, ,
, 。
。
(1)向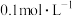 的CH3COONa溶液中逐滴滴加HNO2溶液,当溶液中
的CH3COONa溶液中逐滴滴加HNO2溶液,当溶液中 时,溶液的pH=
时,溶液的pH=___________ (保留2位小数);此时溶液中 为
为___________ (取整数)。
Ⅱ.25℃时,用Na2S沉淀Cu2+、Sn2+两种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如下图所示。
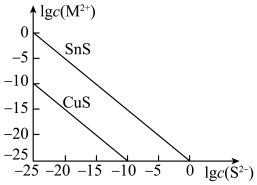
(2)25℃时Ksp(CuS)=___________。
(3)25℃时向50mL的Sn2+、Cu2+浓度均为0.01 的混合溶液中逐滴加入Na2S溶液。当Na2S溶液加到150mL时开始生成SnS沉淀,此时溶液中Cu2+浓度为
的混合溶液中逐滴加入Na2S溶液。当Na2S溶液加到150mL时开始生成SnS沉淀,此时溶液中Cu2+浓度为___________  。
。
 ,
, 。
。(1)向
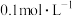 的CH3COONa溶液中逐滴滴加HNO2溶液,当溶液中
的CH3COONa溶液中逐滴滴加HNO2溶液,当溶液中 时,溶液的pH=
时,溶液的pH= 为
为Ⅱ.25℃时,用Na2S沉淀Cu2+、Sn2+两种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如下图所示。

(2)25℃时Ksp(CuS)=___________。
A. | B.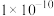 | C. | D. |
(3)25℃时向50mL的Sn2+、Cu2+浓度均为0.01
 的混合溶液中逐滴加入Na2S溶液。当Na2S溶液加到150mL时开始生成SnS沉淀,此时溶液中Cu2+浓度为
的混合溶液中逐滴加入Na2S溶液。当Na2S溶液加到150mL时开始生成SnS沉淀,此时溶液中Cu2+浓度为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.温度t℃时,某NaOH稀溶液中c(H+)=10-amol·L-1,c(OH-)=10-b mol·L-1,已知a+b=12,请回答下列问题:
(1)该NaOH溶液中NaOH的物质的量浓度为__________ ,该NaOH溶液中由水电离出的c(OH-)为__________ 。
(2)给该NaOH溶液加热时,pH________ (填“变大”、“变小”或“不变”)。
Ⅱ.现用盐酸标准溶液来测定NaOH溶液的浓度。有以下实验操作:
①向溶液中加入1~2滴指示剂
②取20.00 mL标准溶液放入锥形瓶中
③用氢氧化钠溶液滴定至终点
④重复以上操作
⑤配制250 mL盐酸标准溶液
⑥根据实验数据计算氢氧化钠的物质的量浓度
(3)实验过程中正确的操作顺序是______ (填序号),上述操作②中使用的仪器除锥形瓶外,还需要______ ,用______ 作指示剂。
(4)滴定并记录V(NaOH)的初、终读数。数据记录如表所示:
某同学在处理数据过程中计算得到平均消耗NaOH溶液的体积V(NaOH)=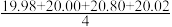 mL=20.20 mL。他的计算
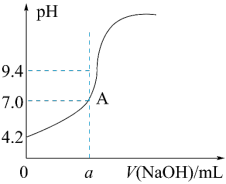
mL=20.20 mL。他的计算______ (填“合理”或“不合理”),理由是____________ 。通过仪器测得第4次滴定过程中溶液pH随加入氢氧化钠溶液体积的变化曲线如图所示,则a______ (填“>”“<”或“=”)20.02。
(1)该NaOH溶液中NaOH的物质的量浓度为
(2)给该NaOH溶液加热时,pH
Ⅱ.现用盐酸标准溶液来测定NaOH溶液的浓度。有以下实验操作:
①向溶液中加入1~2滴指示剂
②取20.00 mL标准溶液放入锥形瓶中
③用氢氧化钠溶液滴定至终点
④重复以上操作
⑤配制250 mL盐酸标准溶液
⑥根据实验数据计算氢氧化钠的物质的量浓度
(3)实验过程中正确的操作顺序是
(4)滴定并记录V(NaOH)的初、终读数。数据记录如表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| V(HCl)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)/mL(初读数) | 0.10 | 0.30 | 0.00 | 0.20 |
| V(NaOH)/mL(终读数) | 20.08 | 20.30 | 20.80 | 20.22 |
| V(NaOH)/mL(消耗) | 19.98 | 20.00 | 20.80 | 20.02 |
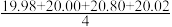 mL=20.20 mL。他的计算
mL=20.20 mL。他的计算
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列问题。
(1)写出 HClO的电离方程式___________ 。
(2)在常温下,0.1mol/LCH3COONa溶液的pH=9,则溶液中由水电离出来的从c(OH-)___________ 。
(3)Al、B、N的电负性由大到小的顺序排列的顺序为:___________ 。
(4)HCHO分子中碳原子轨道杂化类型是___________ 。
(5)根据甲醇在酸性电解质中与氧气作用生成二氧化碳和水的反应,设计一种燃料电池,该燃料电池工作时,正极的电极反应式是___________ 。
(1)写出 HClO的电离方程式
(2)在常温下,0.1mol/LCH3COONa溶液的pH=9,则溶液中由水电离出来的从c(OH-)
(3)Al、B、N的电负性由大到小的顺序排列的顺序为:
(4)HCHO分子中碳原子轨道杂化类型是
(5)根据甲醇在酸性电解质中与氧气作用生成二氧化碳和水的反应,设计一种燃料电池,该燃料电池工作时,正极的电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请按照下列要求回答问题:
(1)电解氯化钠溶液的化学方程式:__________________________________ 。
(2)0.1 mol/L 的碳酸钠溶液中离子浓度由大到小顺序为:__________________________ 。
(3)浓的 Al2(SO4)3 溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理__________________________ 。
(4)将25℃下 pH=12 的 Ba(OH)2 溶液aL与 pH=1的HCl溶液bL 混合,若所得混合液为中性,则 a:b=__________________________ 。(溶液体积变化忽略不计)。
(5)pH=3 的 NH4Cl 溶液,由水电离出的 c(H+)=__________________________ 。
(6)常温时,Fe(OH)3 的溶度积常数 Ksp=1×10-38,要使溶液中的 Fe3+沉淀完全(残留的 c(Fe3+)<10-5 mol·L-1),则 溶液的 pH 应大于____________________________ 。
(1)电解氯化钠溶液的化学方程式:
(2)0.1 mol/L 的碳酸钠溶液中离子浓度由大到小顺序为:
(3)浓的 Al2(SO4)3 溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理
(4)将25℃下 pH=12 的 Ba(OH)2 溶液aL与 pH=1的HCl溶液bL 混合,若所得混合液为中性,则 a:b=
(5)pH=3 的 NH4Cl 溶液,由水电离出的 c(H+)=
(6)常温时,Fe(OH)3 的溶度积常数 Ksp=1×10-38,要使溶液中的 Fe3+沉淀完全(残留的 c(Fe3+)<10-5 mol·L-1),则 溶液的 pH 应大于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】室温下,用0.1000mol·L−1NaOH滴定20.00mL0.1000mol·L−1HCl溶液过程中,溶液的pH随NaOH溶液体积的变化如下图所示。
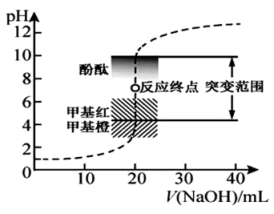
(1)酸碱式滴定管在加溶液滴定前,需要的操作是___________ 和___________ 。
(2)配制上述NaOH标准溶液时,下列仪器中不必要 用到的有___________ 。(用编号表示)。
①电子天平②烧杯③量筒④玻璃棒⑤容量瓶⑥胶头滴管⑦移液管
(3)当V(NaOH)=20.00mL时,溶液中所有离子的浓度存在的关系是___________ 。
(4)已知lg5=0.7.当加入的V(NaOH)=30.00mL时,溶液中pH=___________ 。
(5)在化学分析中,以AgNO3标准溶液滴定溶液中的Cl-时,采用K2CrO4为指示剂,利用Ag+和CrO 反应生成砖红色沉淀表示滴定终点。当溶液中的Cl-恰好完全沉淀时,溶液中的c(Ag+)=
反应生成砖红色沉淀表示滴定终点。当溶液中的Cl-恰好完全沉淀时,溶液中的c(Ag+)=___________ mol/L;c(CrO )=
)=___________ mol/L;
已知:①25℃时,Ksp(Ag2CrO4)=2.0×10-12,Ksp(AgCl)=1.8×10-10;

(1)酸碱式滴定管在加溶液滴定前,需要的操作是
(2)配制上述NaOH标准溶液时,下列仪器中
①电子天平②烧杯③量筒④玻璃棒⑤容量瓶⑥胶头滴管⑦移液管
(3)当V(NaOH)=20.00mL时,溶液中所有离子的浓度存在的关系是
(4)已知lg5=0.7.当加入的V(NaOH)=30.00mL时,溶液中pH=
(5)在化学分析中,以AgNO3标准溶液滴定溶液中的Cl-时,采用K2CrO4为指示剂,利用Ag+和CrO
 反应生成砖红色沉淀表示滴定终点。当溶液中的Cl-恰好完全沉淀时,溶液中的c(Ag+)=
反应生成砖红色沉淀表示滴定终点。当溶液中的Cl-恰好完全沉淀时,溶液中的c(Ag+)= )=
)=已知:①25℃时,Ksp(Ag2CrO4)=2.0×10-12,Ksp(AgCl)=1.8×10-10;
②当溶液中某种离子的浓度等于或小于1.0×10-5mol/L时,可认为已完全沉淀。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请根据信息回答下列问题。
(1)硒酸(H2SeO4)在水溶液中的电离方程式如下:H2SeO4=H++HSeO ,HSeO
,HSeO ⇌H++SeO
⇌H++SeO 。
。
①写出NaHSeO4在水溶液中的电离方程式_______ 。
②已知25℃时,1mol/L的H2SeO4溶液中,HSeO 的电离度为α,则其电离常数Ka=
的电离度为α,则其电离常数Ka=_______ (用含α的计算式表示,忽略水的电离)
(2)亚磷酸(H3PO3)是二元酸,25℃时,K a1=1×10-2、Ka2=2.6×10-7,HF的电离常数的值为Ka=3.6×10-4,将足量H3PO3溶液和NaF溶液反应,其离子方程式为_______ 。
(3)在常温下,有硫酸和盐酸的混合液20 mL,向该溶液中加入0.05 mol/L的Ba(OH)2时,生成的BaSO4沉淀的质量和混合溶液的pH有如图所示关系。
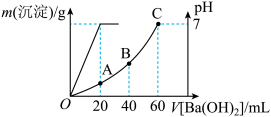
①C点溶液中的主要溶质是_______ (写化学式)。
②A、B、C三点中,水的电离程度最大的是_______
③当滴加Ba(OH)2的体积至80 mL时,溶液的pH值为_______ (已知lg2=0.3,混合后溶液体积变化忽略不计)
(1)硒酸(H2SeO4)在水溶液中的电离方程式如下:H2SeO4=H++HSeO
 ,HSeO
,HSeO ⇌H++SeO
⇌H++SeO 。
。①写出NaHSeO4在水溶液中的电离方程式
②已知25℃时,1mol/L的H2SeO4溶液中,HSeO
 的电离度为α,则其电离常数Ka=
的电离度为α,则其电离常数Ka=(2)亚磷酸(H3PO3)是二元酸,25℃时,K a1=1×10-2、Ka2=2.6×10-7,HF的电离常数的值为Ka=3.6×10-4,将足量H3PO3溶液和NaF溶液反应,其离子方程式为
(3)在常温下,有硫酸和盐酸的混合液20 mL,向该溶液中加入0.05 mol/L的Ba(OH)2时,生成的BaSO4沉淀的质量和混合溶液的pH有如图所示关系。

①C点溶液中的主要溶质是
②A、B、C三点中,水的电离程度最大的是
③当滴加Ba(OH)2的体积至80 mL时,溶液的pH值为
您最近一年使用:0次



