完成下列问题。
(1)写出 HClO的电离方程式___________ 。
(2)在常温下,0.1mol/LCH3COONa溶液的pH=9,则溶液中由水电离出来的从c(OH-)___________ 。
(3)Al、B、N的电负性由大到小的顺序排列的顺序为:___________ 。
(4)HCHO分子中碳原子轨道杂化类型是___________ 。
(5)根据甲醇在酸性电解质中与氧气作用生成二氧化碳和水的反应,设计一种燃料电池,该燃料电池工作时,正极的电极反应式是___________ 。
(1)写出 HClO的电离方程式
(2)在常温下,0.1mol/LCH3COONa溶液的pH=9,则溶液中由水电离出来的从c(OH-)
(3)Al、B、N的电负性由大到小的顺序排列的顺序为:
(4)HCHO分子中碳原子轨道杂化类型是
(5)根据甲醇在酸性电解质中与氧气作用生成二氧化碳和水的反应,设计一种燃料电池,该燃料电池工作时,正极的电极反应式是
更新时间:2023-09-23 17:32:49
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】25℃时,如图烧杯中各盛有20mL的溶液。
甲. 0.100mol/L盐酸 乙.
0.100mol/L盐酸 乙.  0.100mol/L氨水 丙.
0.100mol/L氨水 丙.  0.100mol/LNH4Cl
0.100mol/LNH4Cl
(1)甲溶液的pH=_____________ 。
(2)若将甲全部倒入乙中,所得溶液的pH_____________ 丙溶液的pH(填“>”、“=”或“<”)。
(3)若将一部分乙倒入丙中,所得的混合溶液呈中性,所得混合溶液中离子浓度大小关系是_____________ 。
甲.
 0.100mol/L盐酸 乙.
0.100mol/L盐酸 乙.  0.100mol/L氨水 丙.
0.100mol/L氨水 丙.  0.100mol/LNH4Cl
0.100mol/LNH4Cl(1)甲溶液的pH=
(2)若将甲全部倒入乙中,所得溶液的pH
(3)若将一部分乙倒入丙中,所得的混合溶液呈中性,所得混合溶液中离子浓度大小关系是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求回答下列问题:
(1)常温下向一定体积的0.1mol/L醋酸溶液中加水稀释后,下列说法正确的是___ 。
A.溶液中导电粒子的数目减少 B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中 不变 D.溶液中
不变 D.溶液中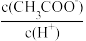 减小
减小
(2)常温下将0.15mol/L稀硫酸V1mL与0.1mol/L NaOH溶液V2mL混合,所得溶液的pH为1,则V1:V2=___ (溶液体积变化忽略不计)。
(3)常温下,某溶液中由水电离产生的c(H+)=1×10-11 mol·L-1,则该溶液的pH可能是___ 。
(4)常温下,在pH=9的CH3COONa溶液中,由水电离出的OH-浓度___ 。
(5)电解质水溶液中存在电离平衡、水解平衡,请回答下列问题。
已知部分弱酸的电离平衡常数如下表:
①同浓度HCOONa、NaCN、NaHCO3、Na2CO3这4种溶液中碱性最强的是__ ;
②体积相同、c(H+)相同的三种酸溶液a.HCOOH;b.HCN;c.HCl分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填字母)__ 。
(1)常温下向一定体积的0.1mol/L醋酸溶液中加水稀释后,下列说法正确的是
A.溶液中导电粒子的数目减少 B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中
 不变 D.溶液中
不变 D.溶液中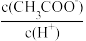 减小
减小(2)常温下将0.15mol/L稀硫酸V1mL与0.1mol/L NaOH溶液V2mL混合,所得溶液的pH为1,则V1:V2=
(3)常温下,某溶液中由水电离产生的c(H+)=1×10-11 mol·L-1,则该溶液的pH可能是
(4)常温下,在pH=9的CH3COONa溶液中,由水电离出的OH-浓度
(5)电解质水溶液中存在电离平衡、水解平衡,请回答下列问题。
已知部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
①同浓度HCOONa、NaCN、NaHCO3、Na2CO3这4种溶液中碱性最强的是
②体积相同、c(H+)相同的三种酸溶液a.HCOOH;b.HCN;c.HCl分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填字母)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】在不同温度下的水溶液中,c(H+)和c(OH-)的关系如图所示:
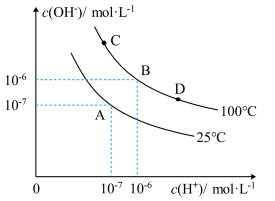
(1)A点水的离子积为________ ,C点水的离子积为_______ ,对纯水由25℃升高温度至100℃时水的离子积______ (填“增大”、“减小”或“不变”)。
(2)100℃时,若向B点溶液中滴加硫酸,体系将由B点移向_____ 点(填C或D),为什么_________ 。
(3)25℃时,0.001mol/L的盐酸溶液pH=_______ ;0.001mol/L的氢氧化钠溶液pH=_________ ;若将二者温度都升高至100℃,_________ (填“盐酸”、“氢氧化钠”、“盐酸和氢氧化钠”)的pH会改变。

(1)A点水的离子积为
(2)100℃时,若向B点溶液中滴加硫酸,体系将由B点移向
(3)25℃时,0.001mol/L的盐酸溶液pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】比亚迪双模电动汽车使用高铁电池供电。高铁电池的总反应为: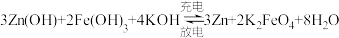 ,则放电时的负极反应式为
,则放电时的负极反应式为___________ 。
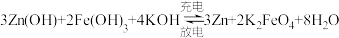 ,则放电时的负极反应式为
,则放电时的负极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有如下两个反应:A、NaOH+HCl=NaCl+H2O B、Cu+2Ag+=2Ag+Cu2+
(1)根据两反应本质,判断___________ 能设计成原电池。
(2)如果不能,说明其原因___________ 。
(3)如果可以,请选择正、负极材料(可供选择:铜片、锌片、石墨棒)、写出其电极反应式、反应类型(“氧化”或“还原”):
负极:___________ ,___________ ,___________ 反应。
正极:___________ ,___________ ,___________ 反应。
电解质溶液为___________ (填化学式),若导线上转移电子0.1 mol,则正极质量增加___________ g。
(1)根据两反应本质,判断
(2)如果不能,说明其原因
(3)如果可以,请选择正、负极材料(可供选择:铜片、锌片、石墨棒)、写出其电极反应式、反应类型(“氧化”或“还原”):
负极:
正极:
电解质溶液为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】高铁酸钾(K2FeO4)是一种可溶于水,具有极强氧化性的高效多功能水处理剂,也可作高容量电池材料。回答下列问题:
(1)高铁酸钾中铁元素的化合价为___________ 。
(2)工业上通常先用干法制备高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,析出高铁酸钾。干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2==2Na2FeO4+2Na2O+2Na2SO4+O2↑。该反应中还原剂为_______________ 。低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾,其原因是_________________ 。
(3)常温下,高铁酸钾能氧化浓盐酸生成氯气,该反应离子方程式为___ 。
(4)比亚迪双模电动汽车使用高铁电池供电,其电池反应为3Zn+2K2FeO4+8H2O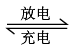 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为_______________________________________ ,正极附近溶液的pH变__________ (填“大”或“小”)。
(5)工业上可用K2FeO4溶液氧化废水中的还原性污染物M,为研究反应效果,设计如下所示的对比实验探究温度、浓度、pH对降解速率和反应效果的影响,实验测得M的浓度与时间关系如图所示。
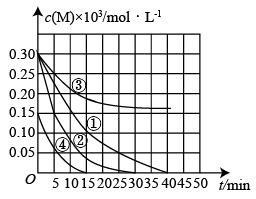
实验①中前25 min内M的反应速率为_____________________ ;其他条件相同时,实验①、②说明温度越高,M的反应速率越_________ (填“大”或“小”);其他条件相同时,实验①、③说明pH越大,M的反应速率越_________ (填“大”或“小”)。
(1)高铁酸钾中铁元素的化合价为
(2)工业上通常先用干法制备高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,析出高铁酸钾。干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2==2Na2FeO4+2Na2O+2Na2SO4+O2↑。该反应中还原剂为
(3)常温下,高铁酸钾能氧化浓盐酸生成氯气,该反应离子方程式为
(4)比亚迪双模电动汽车使用高铁电池供电,其电池反应为3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为
3Zn(OH)2+2Fe(OH)3+4KOH。放电时,负极反应式为(5)工业上可用K2FeO4溶液氧化废水中的还原性污染物M,为研究反应效果,设计如下所示的对比实验探究温度、浓度、pH对降解速率和反应效果的影响,实验测得M的浓度与时间关系如图所示。

实验编号 | 温度(℃) | pH |
① | 25 | 1 |
② | 45 | 1 |
③ | 25 | 7 |
④ | 25 | 1 |
您最近一年使用:0次
【推荐1】开发新型储氢材料是开发利用氢能的重要研究方向。
(1) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。
①基态Cl原子中,电子占据的最高电子层符号为______ ,该电子层具有的原子轨道数为 _______ 。
②Li、B、H元素的电负性由大到小的排列顺序为___________ 。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+___________ (填“>”“=”或“<”)H-。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如表所示:
则M是______________ (填元素名称)。
(1)
 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。①基态Cl原子中,电子占据的最高电子层符号为
②Li、B、H元素的电负性由大到小的排列顺序为
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如表所示:
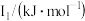 | 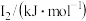 | 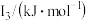 | 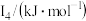 | 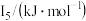 |
| 738 | 1451 | 7733 | 10540 | 13630 |
则M是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】X、Y、Z、W、Q 五种元素原子序数依次增大,X原子核外的L层电子数是K层的两倍,Z原子价电子排布式为nsnnp2n,W原子核外的M层中只有两对成对电子,Q的核电荷数是Z与W的核电荷数之和.请回答下列问题:
(1)Y、Q的元素符号依次为__ 、__ ;
(2)Y与Z的第一电离能大小关系是(用元素符号回答)__ ;
(3)X、Y、Z两两组合可形成很多等电子体,请任意写出两组等电子体__ 、__ ;
(4)Q在元素周期表 区,其价电子排布图为__ .
(5)X与W的电负性大小关系是(用元素符号回答)__ ,这两种元素组成的一种化合物是一种常见的溶剂,其电子式为__ .
(1)Y、Q的元素符号依次为
(2)Y与Z的第一电离能大小关系是(用元素符号回答)
(3)X、Y、Z两两组合可形成很多等电子体,请任意写出两组等电子体
(4)Q在元素周期表 区,其价电子排布图为
(5)X与W的电负性大小关系是(用元素符号回答)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】甲醇(CH3OH)空气氧化法是生产工业甲醛(HCHO)的常用方法。发生的反应为2CH3OH+O2 2
2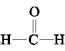 +2H2O
+2H2O
(1)C、H、O 三种元素的电负性由大到小的顺序为_______ 。
(2)H2O的中心原子上的孤电子对数为_______ 。
(3)HCHO分子内σ键与π键个数之比为_______ ,HCHO的空间结构为_______ 。
(4)CH3OH和HCHO分子中碳原子的杂化轨道类型分别为_______ 和_______ 。
(5)工业上利用甲醛易溶于水的性质吸收产品,解释甲醛易溶于水的原因:_______ 。
 2
2 +2H2O
+2H2O(1)C、H、O 三种元素的电负性由大到小的顺序为
(2)H2O的中心原子上的孤电子对数为
(3)HCHO分子内σ键与π键个数之比为
(4)CH3OH和HCHO分子中碳原子的杂化轨道类型分别为
(5)工业上利用甲醛易溶于水的性质吸收产品,解释甲醛易溶于水的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】完成下列问题。
(1)硅是重要的半导体材料,构成了现代电子工业的基础。碳和硅的有关化学键键能如表所示,简要分析和解释下列有关事实:
硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是___________ 。SiH4的稳定性小于CH4,更易生成氧化物,原因是___________ 。
(2)比较NH3和[Cu(NH3)4]2+中H−N−H键角的大小:NH3___________ [Cu(NH3)4]2+(填“>”或“<”),并说明理由:___________
(3)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为_______ ,下列对XeF2中心原子杂化方式推断合理的是_______ (填标号)。
A.sp B.sp2 C.sp3 D.sp3d
(4)苯胺( )与甲苯(
)与甲苯(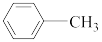 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是_______ 。
(5)硒的两种含氧酸的酸分别为 、
、 ,试比较其酸性强弱并说明原因:
,试比较其酸性强弱并说明原因:___________ 。
(6)在水中的溶解度,吡啶(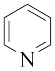 )远大于苯,主要原因是①
)远大于苯,主要原因是①_______ ,②_______ 。
(1)硅是重要的半导体材料,构成了现代电子工业的基础。碳和硅的有关化学键键能如表所示,简要分析和解释下列有关事实:
| 化学键 | C−C | C−H | C−O | Si−Si | Si−H | Si−O |
| 键能/ (kJ·mol-1) | 365 | 413 | 336 | 226 | 318 | 452 |
(2)比较NH3和[Cu(NH3)4]2+中H−N−H键角的大小:NH3
(3)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为
A.sp B.sp2 C.sp3 D.sp3d
(4)苯胺(
 )与甲苯(
)与甲苯(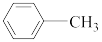 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是(5)硒的两种含氧酸的酸分别为
 、
、 ,试比较其酸性强弱并说明原因:
,试比较其酸性强弱并说明原因:(6)在水中的溶解度,吡啶(
 )远大于苯,主要原因是①
)远大于苯,主要原因是①
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇及其化合物可制成甘油、医药、农药、香料,合成维生素E和KI及天然抗癌药物紫杉醇中都含有关键的烯丙醇结构。丙烯醇的结构简式为CH2=CH-CH2OH。请回答下列问题:
①基态镍原子的价电子排布式为________ 。
②1 mol CH2=CH-CH2OH含___ molσ键,烯丙醇分子中碳原子的杂化类型为___ 。
③Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(CN)2]2- 和[Ni(SCN)2]- 等,与CN-互为等电子体的分子为_____ 。
(2)乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
①CaC2中C22-中碳与碳之间存在碳碳三键,C22-与O22+互为等电子体,O22+的电子式可表示为_______ 。
②乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是________ 。
①基态镍原子的价电子排布式为
②1 mol CH2=CH-CH2OH含
③Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(CN)2]2- 和[Ni(SCN)2]- 等,与CN-互为等电子体的分子为
(2)乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
①CaC2中C22-中碳与碳之间存在碳碳三键,C22-与O22+互为等电子体,O22+的电子式可表示为
②乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】我国科学家构建了新型催化剂“纳米片”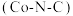 ,该“纳米片”可用于氧化
,该“纳米片”可用于氧化 和吸附
和吸附 。回答下列问题:
。回答下列问题:
(1)基态Co原子的价层电子排布式为_______ ,N、C、Co中第一电离能最大的是_______ (填元素符号)。
(2)在空气中 会被氧化成
会被氧化成 ,
, 中S原子采用
中S原子采用_______ 杂化。已知氧族元素氢化物的熔沸点高低顺序为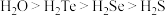 ,其原因是
,其原因是_______ 。
(3)氰 称为拟卤素,它的分子中每个原子最外层都达到8电子结构,则
称为拟卤素,它的分子中每个原子最外层都达到8电子结构,则 分子中σ键、π键个数之比为
分子中σ键、π键个数之比为_______ 。
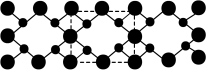
(4)氮和碳组成的一种新型材料,硬度超过金刚石,其部分结构如下图所示,它的化学式为_______ 。
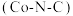 ,该“纳米片”可用于氧化
,该“纳米片”可用于氧化 和吸附
和吸附 。回答下列问题:
。回答下列问题:(1)基态Co原子的价层电子排布式为
(2)在空气中
 会被氧化成
会被氧化成 ,
, 中S原子采用
中S原子采用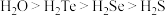 ,其原因是
,其原因是(3)氰
 称为拟卤素,它的分子中每个原子最外层都达到8电子结构,则
称为拟卤素,它的分子中每个原子最外层都达到8电子结构,则 分子中σ键、π键个数之比为
分子中σ键、π键个数之比为(4)氮和碳组成的一种新型材料,硬度超过金刚石,其部分结构如下图所示,它的化学式为

您最近一年使用:0次



