按要求回答下列问题:
(1)常温下向一定体积的0.1mol/L醋酸溶液中加水稀释后,下列说法正确的是___ 。
A.溶液中导电粒子的数目减少 B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中 不变 D.溶液中
不变 D.溶液中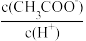 减小
减小
(2)常温下将0.15mol/L稀硫酸V1mL与0.1mol/L NaOH溶液V2mL混合,所得溶液的pH为1,则V1:V2=___ (溶液体积变化忽略不计)。
(3)常温下,某溶液中由水电离产生的c(H+)=1×10-11 mol·L-1,则该溶液的pH可能是___ 。
(4)常温下,在pH=9的CH3COONa溶液中,由水电离出的OH-浓度___ 。
(5)电解质水溶液中存在电离平衡、水解平衡,请回答下列问题。
已知部分弱酸的电离平衡常数如下表:
①同浓度HCOONa、NaCN、NaHCO3、Na2CO3这4种溶液中碱性最强的是__ ;
②体积相同、c(H+)相同的三种酸溶液a.HCOOH;b.HCN;c.HCl分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填字母)__ 。
(1)常温下向一定体积的0.1mol/L醋酸溶液中加水稀释后,下列说法正确的是
A.溶液中导电粒子的数目减少 B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中
 不变 D.溶液中
不变 D.溶液中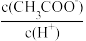 减小
减小(2)常温下将0.15mol/L稀硫酸V1mL与0.1mol/L NaOH溶液V2mL混合,所得溶液的pH为1,则V1:V2=
(3)常温下,某溶液中由水电离产生的c(H+)=1×10-11 mol·L-1,则该溶液的pH可能是
(4)常温下,在pH=9的CH3COONa溶液中,由水电离出的OH-浓度
(5)电解质水溶液中存在电离平衡、水解平衡,请回答下列问题。
已知部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ka=1.77×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
①同浓度HCOONa、NaCN、NaHCO3、Na2CO3这4种溶液中碱性最强的是
②体积相同、c(H+)相同的三种酸溶液a.HCOOH;b.HCN;c.HCl分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填字母)
更新时间:2019-11-26 19:21:41
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】25℃时,三种酸的电离平衡常数如下:
回答下列问题:
(1)物质的量浓度均为0.1mol/L的四种溶液;① ②NaClO③
②NaClO③ ④
④ ,溶液的pH由大到小的顺序是
,溶液的pH由大到小的顺序是___________ (填编号,下同);
(2)下列反应不能发生的是___________(填序号)。
(3)在25℃下, 的NaOH溶液中,水电离产生的
的NaOH溶液中,水电离产生的 浓度c(OH-)水=
浓度c(OH-)水=___________ ; 的
的 溶液中,水电离出来的c(OH-)水=
溶液中,水电离出来的c(OH-)水=___________ 。
(4)25℃下,将 的苛性钠溶液V1L与
的苛性钠溶液V1L与 的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则
,则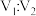 =
=___________ 。
| 化学式 |  |  | HClO |
| 电离平衡常数 | 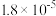 |  , ,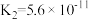 | 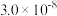 |
回答下列问题:
(1)物质的量浓度均为0.1mol/L的四种溶液;①
 ②NaClO③
②NaClO③ ④
④ ,溶液的pH由大到小的顺序是
,溶液的pH由大到小的顺序是(2)下列反应不能发生的是___________(填序号)。
A. |
B. |
C.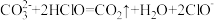 |
D.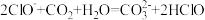 |
 的NaOH溶液中,水电离产生的
的NaOH溶液中,水电离产生的 浓度c(OH-)水=
浓度c(OH-)水= 的
的 溶液中,水电离出来的c(OH-)水=
溶液中,水电离出来的c(OH-)水=(4)25℃下,将
 的苛性钠溶液V1L与
的苛性钠溶液V1L与 的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则
,则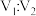 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)某温度下纯水中c(H+) = 2×10-7mol/L,则此时水中的c(OH-)=________ mol/L,若温度不变,向水中滴入稀盐酸使c(H+) = 5×10-6mol/L,则此时溶液中的c(OH-) = ________ mol/L,滴入盐酸后水的离子积_______ (填“变大”“变小”或“不变”,下同),水的电离度______ 。
(2)今有A.CH3COOH B.HCl C.H2SO4三种溶液
①当它们pH相同时,其物质的量浓度关系是_________ (用字母表示,下同);
②体积和物质的量浓度相同的三种溶液,分别与同浓度的烧碱溶液反应,要使反应后的溶液呈中性,所需烧碱溶液的体积关系为____________ ;
③当它们pH相同、体积相同时,分别加入足量锌,相同状况下产生气体体积关系为____________ 。
(2)今有A.CH3COOH B.HCl C.H2SO4三种溶液
①当它们pH相同时,其物质的量浓度关系是
②体积和物质的量浓度相同的三种溶液,分别与同浓度的烧碱溶液反应,要使反应后的溶液呈中性,所需烧碱溶液的体积关系为
③当它们pH相同、体积相同时,分别加入足量锌,相同状况下产生气体体积关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列有关水的电离及电解质溶液问题:
(1)某温度时,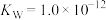 ,该条件下测出
,该条件下测出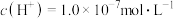 ,溶液呈
,溶液呈_______ (填“酸性”“碱性”或“中性”),若该溶液为碱溶液,则由 电离出来的
电离出来的 为
为_______  。
。
(2)将少量碳酸钠固体加入盐酸中,溶液中水的电离平衡_______ (填“向左”“向右”或“不”,下同)移动。在新制氯水中加入少量NaCl固体,水的电离平衡_______ 移动。
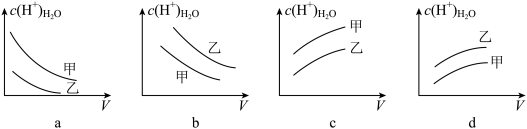
(3)将NaOH(甲)、 (乙)等物质的量浓度的水溶液加水稀释,下图水电离出的
(乙)等物质的量浓度的水溶液加水稀释,下图水电离出的 与加入水的体积
与加入水的体积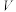 的关系正确的是
的关系正确的是_______ 。
(4)25℃时,pH=4的盐酸中水的电离程度_______ (填“大于”“小于”或“等于”)pH=10的 溶液中水的电离程度。
溶液中水的电离程度。
(1)某温度时,
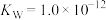 ,该条件下测出
,该条件下测出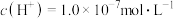 ,溶液呈
,溶液呈 电离出来的
电离出来的 为
为 。
。(2)将少量碳酸钠固体加入盐酸中,溶液中水的电离平衡
(3)将NaOH(甲)、
 (乙)等物质的量浓度的水溶液加水稀释,下图水电离出的
(乙)等物质的量浓度的水溶液加水稀释,下图水电离出的 与加入水的体积
与加入水的体积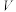 的关系正确的是
的关系正确的是
(4)25℃时,pH=4的盐酸中水的电离程度
 溶液中水的电离程度。
溶液中水的电离程度。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】溶液的pH
(1)定义:pH是c(H+)的负对数,其表达式是pH=___________ 。
(2)溶液的pH、c(H+)及酸碱性的关系(25 ℃):
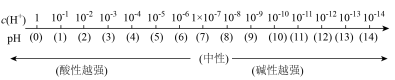
pH大小能反映出___________ ,即能表示溶液的酸碱性强弱。
(3)pH的适用范围:1×10-14 mol·L-1≤c(H+)≤1 mol·L-1,即___________≤pH≤__________,___________ 。
(1)定义:pH是c(H+)的负对数,其表达式是pH=
(2)溶液的pH、c(H+)及酸碱性的关系(25 ℃):
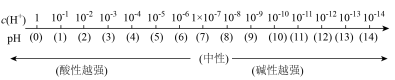
pH大小能反映出
(3)pH的适用范围:1×10-14 mol·L-1≤c(H+)≤1 mol·L-1,即___________≤pH≤__________,
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1) 时,
时,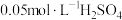 溶液的
溶液的
______
(2)完出下列电解质在水溶液中的水解离子方程式
 :
:______ ;
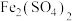 :
:______ 。
(3)资料出沶: 的电离常数
的电离常数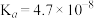 ;
; 的中离常数
的中离常数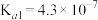 ,
,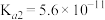 。浓度相同的
。浓度相同的 溶液和
溶液和 溶液比较,酸性较强的是
溶液比较,酸性较强的是______ (填化学式),向 溶液中通入少量
溶液中通入少量 气体,发生反应的离子方程式为
气体,发生反应的离子方程式为______ 。
(1)
 时,
时,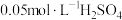 溶液的
溶液的
(2)完出下列电解质在水溶液中的水解离子方程式
 :
: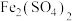 :
:(3)资料出沶:
 的电离常数
的电离常数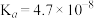 ;
; 的中离常数
的中离常数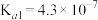 ,
,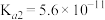 。浓度相同的
。浓度相同的 溶液和
溶液和 溶液比较,酸性较强的是
溶液比较,酸性较强的是 溶液中通入少量
溶液中通入少量 气体,发生反应的离子方程式为
气体,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)水是极弱的电解质,也是最重要的溶剂。常温下某电解质溶解在水中后,溶液中由水电离出的c(H+)=10-9mol·L-1,则该电解质可能是___________ (填序号)。
A.CuSO4 B.Na2CO3 C.HCl D.NaOH E.K2SO4
(2)常温下,将pH=3的盐酸aL分别与下列三种溶液混合,结果溶液均呈中性。
①c(OH-)=1.0×10-3mol·L-1的氨水bL;
②浓度为1.0×10-3mol·L-1的氨水cL;
③c(OH-)=1.0×10-3mol·L-1的氢氧化钡溶液dL。
则a、b、c、d之间的关系是___________ 。
(3)已知室温时,0.1mol·L-1的某一元酸HA在水中有0.1%发生电离,回答下列各问题:
①该溶液的pH=___________ 。
②升高温度时,K将______ (填“增大”、“减小”或“不变”),pH将_______ (填“增大”、“减小”或“不变”)。
③由HA电离出的c(H+)约为水电离出的c(H+)的_________ 倍。
(1)水是极弱的电解质,也是最重要的溶剂。常温下某电解质溶解在水中后,溶液中由水电离出的c(H+)=10-9mol·L-1,则该电解质可能是
A.CuSO4 B.Na2CO3 C.HCl D.NaOH E.K2SO4
(2)常温下,将pH=3的盐酸aL分别与下列三种溶液混合,结果溶液均呈中性。
①c(OH-)=1.0×10-3mol·L-1的氨水bL;
②浓度为1.0×10-3mol·L-1的氨水cL;
③c(OH-)=1.0×10-3mol·L-1的氢氧化钡溶液dL。
则a、b、c、d之间的关系是
(3)已知室温时,0.1mol·L-1的某一元酸HA在水中有0.1%发生电离,回答下列各问题:
①该溶液的pH=
②升高温度时,K将
③由HA电离出的c(H+)约为水电离出的c(H+)的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有下列五种溶液:盐酸、NH3·H2O、NH4HSO4、NaOH、CH3COOH。回答下列问题:
(1)将1LpH=2的HCl溶液分别与0.01mol·L-1的NH3· H2O溶液x L、0.01 mol·L-1的NaOH溶液yL充分反应至中性,x、y大小关系为:y___ x(填“>”“<”或“=”)。
(2)H+浓度相同的等体积的两份溶液:盐酸和CH3COOH,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,则下列说法正确的是____ (填写序号)。
①反应所需要的时间CH3COOH >HCl
②开始反应时的速率HCl>CH3COOH
③参加反应的锌粉物质的量HCl=CH3COOH
④反应过程的平均速率CH3COOH>HCl
⑤HCl溶液里有锌粉剩余
⑥CH3COOH溶液里有锌粉剩余
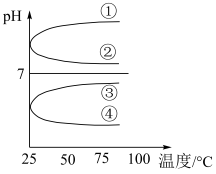
(3)将等体积、等物质的量浓度的NH3·H2O和NH4HSO4溶液混合后,升高温度(溶质不会分解)溶液pH随温度变化如图中的____ 曲线(填写序号)。
(4)室温下,向0.01mol·L-1NH4HSO4溶液中滴加0.01mol·L-1NaOH溶液至中性,得到的溶液中:c(Na+)+c(NH4+)___ 2c(SO42- )(填“>”“=”或“<”);用NH4HSO4与氢氧化钡溶液制取硫酸钡,若溶液中SO42-完全沉淀,则反应后溶液的pH___ 7(填“>”“=”或“<”)
(5)25℃时,将amolNH4NO3溶于水,溶液显酸性,原因是____ (用离子方程式表示)。向该溶液滴加b L氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将___ (填“正向”“不”或“逆向”)移动。
(1)将1LpH=2的HCl溶液分别与0.01mol·L-1的NH3· H2O溶液x L、0.01 mol·L-1的NaOH溶液yL充分反应至中性,x、y大小关系为:y
(2)H+浓度相同的等体积的两份溶液:盐酸和CH3COOH,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,则下列说法正确的是
①反应所需要的时间CH3COOH >HCl
②开始反应时的速率HCl>CH3COOH
③参加反应的锌粉物质的量HCl=CH3COOH
④反应过程的平均速率CH3COOH>HCl
⑤HCl溶液里有锌粉剩余
⑥CH3COOH溶液里有锌粉剩余
(3)将等体积、等物质的量浓度的NH3·H2O和NH4HSO4溶液混合后,升高温度(溶质不会分解)溶液pH随温度变化如图中的

(4)室温下,向0.01mol·L-1NH4HSO4溶液中滴加0.01mol·L-1NaOH溶液至中性,得到的溶液中:c(Na+)+c(NH4+)
(5)25℃时,将amolNH4NO3溶于水,溶液显酸性,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请按要求填空:
(1)下列物质:① 溶液 ②
溶液 ②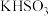 ③
③ ④冰醋酸 ⑤
④冰醋酸 ⑤ ⑥
⑥ ⑦
⑦ ,属于强电解质的是
,属于强电解质的是_______ (填标号),属于弱电解质的是_______ (填标号),写出⑤物质在水溶液中的电离方程式_______ 。
(2)①已知: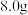 甲烷完全燃烧生成液态水放出的热量为445.15kJ(25℃、
甲烷完全燃烧生成液态水放出的热量为445.15kJ(25℃、 时测定)。写出该条件下表示甲烷燃烧热的热化学方程式
时测定)。写出该条件下表示甲烷燃烧热的热化学方程式_______ 。
②根据以下键能数据计算 的反应热
的反应热
_______  。
。
(3)已知常温下, 的电离平衡常数
的电离平衡常数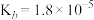 ,写出
,写出 的电离方程式
的电离方程式_______ ;若氨水的浓度为 ,则溶液中
,则溶液中 的浓度约为
的浓度约为_______  。
。
(4)常温下, 的
的 溶液与
溶液与 的硫酸混合,所得溶液的
的硫酸混合,所得溶液的 (近似认为酸碱总体积就是混合液体积),则
(近似认为酸碱总体积就是混合液体积),则 溶液与硫酸的体积比为
溶液与硫酸的体积比为_______ 。
(1)下列物质:①
 溶液 ②
溶液 ②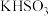 ③
③ ④冰醋酸 ⑤
④冰醋酸 ⑤ ⑥
⑥ ⑦
⑦ ,属于强电解质的是
,属于强电解质的是(2)①已知:
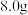 甲烷完全燃烧生成液态水放出的热量为445.15kJ(25℃、
甲烷完全燃烧生成液态水放出的热量为445.15kJ(25℃、 时测定)。写出该条件下表示甲烷燃烧热的热化学方程式
时测定)。写出该条件下表示甲烷燃烧热的热化学方程式②根据以下键能数据计算
 的反应热
的反应热
 。
。| 化学键 | C-H | C-F | H-F | F-F |
键能/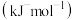 | 414 | 489 | 565 | 155 |
 的电离平衡常数
的电离平衡常数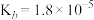 ,写出
,写出 的电离方程式
的电离方程式 ,则溶液中
,则溶液中 的浓度约为
的浓度约为 。
。(4)常温下,
 的
的 溶液与
溶液与 的硫酸混合,所得溶液的
的硫酸混合,所得溶液的 (近似认为酸碱总体积就是混合液体积),则
(近似认为酸碱总体积就是混合液体积),则 溶液与硫酸的体积比为
溶液与硫酸的体积比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有以下几种
①c(Cl-)>c(NH4+)>c(H+)>c(OH-)
②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+)
④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
(1)上述关系一定不正确的是_______________ (填序号);
(2)若溶液中只有一种溶质,则该溶质为__________ ,该溶液中离子浓度的大小关系为_______ (填序号);
(3)若关系③正确,则溶液中溶质为_________ ;
(4)若四种离子浓度关系有c(NH4+)=c(Cl-),则该溶液显_________ (填“酸性”、“碱性”、“中性”)。
(5)25℃,pH=a的盐酸VamL与pH=14-a的氨水VbmL混合,若溶液显中性,则Va__________ Vb(填>、<、=、无法确定)。
①c(Cl-)>c(NH4+)>c(H+)>c(OH-)
②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+)
④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
(1)上述关系一定不正确的是
(2)若溶液中只有一种溶质,则该溶质为
(3)若关系③正确,则溶液中溶质为
(4)若四种离子浓度关系有c(NH4+)=c(Cl-),则该溶液显
(5)25℃,pH=a的盐酸VamL与pH=14-a的氨水VbmL混合,若溶液显中性,则Va
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据要求填写:
(1)硅和氯两元素的单质反应生成1 mol Si的最高价化合物,恢复至室温,放热687 kJ,已知该化合物的熔、沸点分别为-69 ℃和58 ℃,写出该反应的热化学方程式_______ 。
(2)比较下列溶液中指定微粒浓度的大小:浓度均为0.1 mol·L-1的①H2S、②NaHS、③Na2S、④H2S和NaHS混合液,溶液pH从大到小的顺序是_______ 。(填序号)c(H2S)从大到小的顺序是_______ 。(填序号)
(3)已知Ksp[Cu(OH)2] = 1×10-20 。要使0.2 mol / L 的CuSO4溶液中Cu2+沉淀较为完全,则应向溶液里加入NaOH溶液,调整溶液的pH范围为_______ 。
(1)硅和氯两元素的单质反应生成1 mol Si的最高价化合物,恢复至室温,放热687 kJ,已知该化合物的熔、沸点分别为-69 ℃和58 ℃,写出该反应的热化学方程式
(2)比较下列溶液中指定微粒浓度的大小:浓度均为0.1 mol·L-1的①H2S、②NaHS、③Na2S、④H2S和NaHS混合液,溶液pH从大到小的顺序是
(3)已知Ksp[Cu(OH)2] = 1×10-20 。要使0.2 mol / L 的CuSO4溶液中Cu2+沉淀较为完全,则应向溶液里加入NaOH溶液,调整溶液的pH范围为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)CO2是温室气体,可用NaOH溶液吸收得到Na2CO3或NaHCO3。
①Na2CO3俗称纯碱,因 水解而使其水溶液呈碱性,试写出
水解而使其水溶液呈碱性,试写出 水解的离子方程式(忽略第二步水解):
水解的离子方程式(忽略第二步水解):____ 。
②已知25℃时, 的水解常数Kh=2×10-4,则当Na2CO3溶液中c(
的水解常数Kh=2×10-4,则当Na2CO3溶液中c( ):c(
):c( )=2:1时,试求该溶液的pH=
)=2:1时,试求该溶液的pH=____ 。
③0.1mol•L-1Na2CO3溶液中:c(OH-)-c(H+)=____ [用含c( )、c(H2CO3)的关系式表示]。
)、c(H2CO3)的关系式表示]。
④向Na2CO3溶液中加入明矾会产生沉淀和气体,请写出相关的离子方程式:____ 。
(2)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2molNaOH的水溶液与0.2molNO2恰好完全反应得1L溶液A,溶液B为0.1mol•L-1的CH3COONa溶液,则两溶液中c( )、c(
)、c( )和c(CH3COO-)由大到小的顺序为
)和c(CH3COO-)由大到小的顺序为____ (已知:HNO2的电离常数Ka=7.1×10-4mol•L-1,CH3COOH的电离常数Ka=1.7×10-5mol•L-1,可使溶液A和溶液B的pH相等的方法是____ (填选项字母)。
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
(1)CO2是温室气体,可用NaOH溶液吸收得到Na2CO3或NaHCO3。
①Na2CO3俗称纯碱,因
 水解而使其水溶液呈碱性,试写出
水解而使其水溶液呈碱性,试写出 水解的离子方程式(忽略第二步水解):
水解的离子方程式(忽略第二步水解):②已知25℃时,
 的水解常数Kh=2×10-4,则当Na2CO3溶液中c(
的水解常数Kh=2×10-4,则当Na2CO3溶液中c( ):c(
):c( )=2:1时,试求该溶液的pH=
)=2:1时,试求该溶液的pH=③0.1mol•L-1Na2CO3溶液中:c(OH-)-c(H+)=
 )、c(H2CO3)的关系式表示]。
)、c(H2CO3)的关系式表示]。④向Na2CO3溶液中加入明矾会产生沉淀和气体,请写出相关的离子方程式:
(2)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2molNaOH的水溶液与0.2molNO2恰好完全反应得1L溶液A,溶液B为0.1mol•L-1的CH3COONa溶液,则两溶液中c(
 )、c(
)、c( )和c(CH3COO-)由大到小的顺序为
)和c(CH3COO-)由大到小的顺序为a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】判断正误
1.温度一定时,水的电离常数与水的离子积常数相等_______ ;
2.100 ℃的纯水中c(H+)=1×10—6 mol·L—1,此时水呈酸性_______ ;
3.在蒸馏水中滴加浓H2SO4,Kw不变_______ ;
4.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同_______ ;
5.室温下,0.1 mol·L—1的HCl溶液与0.1 mol·L—1的NaOH溶液中水的电离程度相等_______ ;
6.任何水溶液中均存在H+和OH—,且水电离出的c(H+)和c(OH—)相等_______ ;
7.25 ℃时,0.1 mol·L—1的NaOH溶液中KW=1×10—13 mol2·L—2_______ ;
8.某温度下,纯水中的c(H+)=2×10—7mol·L—1,则c(OH—)=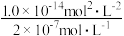
_______ ;
9.25 ℃时,0.01 mol·L—1的盐酸中,c(OH—)=1.0×10—12mol·L—1_______ 。
1.温度一定时,水的电离常数与水的离子积常数相等
2.100 ℃的纯水中c(H+)=1×10—6 mol·L—1,此时水呈酸性
3.在蒸馏水中滴加浓H2SO4,Kw不变
4.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同
5.室温下,0.1 mol·L—1的HCl溶液与0.1 mol·L—1的NaOH溶液中水的电离程度相等
6.任何水溶液中均存在H+和OH—,且水电离出的c(H+)和c(OH—)相等
7.25 ℃时,0.1 mol·L—1的NaOH溶液中KW=1×10—13 mol2·L—2
8.某温度下,纯水中的c(H+)=2×10—7mol·L—1,则c(OH—)=
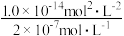
9.25 ℃时,0.01 mol·L—1的盐酸中,c(OH—)=1.0×10—12mol·L—1
您最近一年使用:0次



