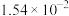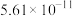根据要求填写:
(1)硅和氯两元素的单质反应生成1 mol Si的最高价化合物,恢复至室温,放热687 kJ,已知该化合物的熔、沸点分别为-69 ℃和58 ℃,写出该反应的热化学方程式_______ 。
(2)比较下列溶液中指定微粒浓度的大小:浓度均为0.1 mol·L-1的①H2S、②NaHS、③Na2S、④H2S和NaHS混合液,溶液pH从大到小的顺序是_______ 。(填序号)c(H2S)从大到小的顺序是_______ 。(填序号)
(3)已知Ksp[Cu(OH)2] = 1×10-20 。要使0.2 mol / L 的CuSO4溶液中Cu2+沉淀较为完全,则应向溶液里加入NaOH溶液,调整溶液的pH范围为_______ 。
(1)硅和氯两元素的单质反应生成1 mol Si的最高价化合物,恢复至室温,放热687 kJ,已知该化合物的熔、沸点分别为-69 ℃和58 ℃,写出该反应的热化学方程式
(2)比较下列溶液中指定微粒浓度的大小:浓度均为0.1 mol·L-1的①H2S、②NaHS、③Na2S、④H2S和NaHS混合液,溶液pH从大到小的顺序是
(3)已知Ksp[Cu(OH)2] = 1×10-20 。要使0.2 mol / L 的CuSO4溶液中Cu2+沉淀较为完全,则应向溶液里加入NaOH溶液,调整溶液的pH范围为
更新时间:2018-01-10 20:57:41
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氮是地球上含量较丰富的一种元素,氮及其化合物在工农业生产、日常生活中有着重要作用。

(1)右图是1mol NO2(g)和1mol CO(g)反应生成CO2(g)和NO(g)过程中能量变化示意图,请写出NO2和CO反应的热化学方程式____________ 。
(2)在一定体积的密闭容器中,进行如下化学反应:
N2(g)+3H2(g) 2NH3(g)
2NH3(g)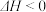
其化学平衡常数K与温度t的关系如下表:
完成下列问题:
①比较K1、K2的大小:K1____ K2(填“>”、“=”或“<”)。
②判断该反应达到化学平衡状态的依据是____ (填序号)。

(1)右图是1mol NO2(g)和1mol CO(g)反应生成CO2(g)和NO(g)过程中能量变化示意图,请写出NO2和CO反应的热化学方程式
(2)在一定体积的密闭容器中,进行如下化学反应:
N2(g)+3H2(g)
 2NH3(g)
2NH3(g)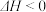
其化学平衡常数K与温度t的关系如下表:
| t/℃ | 25 | 125 | 225 | … |
| K/(mol·L-1)-2 | 4.1×106 | K1 | K2 | … |
完成下列问题:
①比较K1、K2的大小:K1
②判断该反应达到化学平衡状态的依据是
A.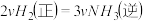 | B. |
| C.容器内压强保持不变 | D.混合气体的密度保持不变 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知由氢气和氧气反应生成1 mol水蒸气,放出241.8 kJ热量。
(1)写出该反应的热化学方程式_________ 。
(2)若1g水蒸气转化成液态水放热2.494kJ,则反应H2(g)+ O2(g)=H2O(l)的ΔH=
O2(g)=H2O(l)的ΔH=_____ kJ/mol。
(3)HCl和NaOH反应的中和热ΔH=-57.3 kJ/mol,则H2SO4和NaOH反应的中和热的热化学方程式为_________ 。
(1)写出该反应的热化学方程式
(2)若1g水蒸气转化成液态水放热2.494kJ,则反应H2(g)+
 O2(g)=H2O(l)的ΔH=
O2(g)=H2O(l)的ΔH=(3)HCl和NaOH反应的中和热ΔH=-57.3 kJ/mol,则H2SO4和NaOH反应的中和热的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)1mol碳与足量水蒸气反应生成CO和H2,需吸收131.3kJ热量,此反应的热化学方程式为______ 。
(2)已知以下的热化学反应方程式:
①2CO(g)+O2(g)=2CO2(g) ∆H=-566kJ/mol
②2H2(g)+O2(g)=2H2O(g) ∆H=-484kJ/mol
③CH4(g)+2O2(g)=CO2(g)+2H2O(g) ∆H=-890kJ/mol
则:CH4(g)+CO2(g)=2CO(g)+2H2(g) ∆H=____ kJ/mol。
(3)已知H2(g)+Br2(l)=2HBr(g) ∆H=-102kJ/mol,其他的相关数据如下表:
则表中a为_______ 。
(2)已知以下的热化学反应方程式:
①2CO(g)+O2(g)=2CO2(g) ∆H=-566kJ/mol
②2H2(g)+O2(g)=2H2O(g) ∆H=-484kJ/mol
③CH4(g)+2O2(g)=CO2(g)+2H2O(g) ∆H=-890kJ/mol
则:CH4(g)+CO2(g)=2CO(g)+2H2(g) ∆H=
(3)已知H2(g)+Br2(l)=2HBr(g) ∆H=-102kJ/mol,其他的相关数据如下表:
| H2(g) | Br2(l) | HBr(g) | |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 |
则表中a为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】填空。
(1)25℃时,浓度为0.1mol·L-1的6种溶液:①HCl,②CH3COOH,③Ba(OH)2,④Na2CO3,⑤KCl,⑥NH4Cl。溶液pH由小到大的顺序为_______ (填写编号)。
(2)25℃时,醋酸的电离常数Ka=2×10-5mol·L-1,则该温度下CH3COONa的水解平衡常数Kh=_______ 。
(3)25℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液呈_______ (填“酸性”“中性”或“碱性”),请写出溶液中离子 浓度间的一个等式:_______ 。
(4)25℃时,将mmol·L-1的醋酸和nmol·L-1的氢氧化钠溶液等体积混合后,溶液的pH=7,则溶液中c(CH3COO-)+c(CH3COOH)=_____ mol·L-1,m与n的大小关系是m______ n(填“>”“=”或“<”)。
(5)25℃时,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的pH=7,则NH3·H2O的电离常数Kb=_______ 。
(6)设计一个简单的实验,怎样证明醋酸是弱酸?_______ 。
(1)25℃时,浓度为0.1mol·L-1的6种溶液:①HCl,②CH3COOH,③Ba(OH)2,④Na2CO3,⑤KCl,⑥NH4Cl。溶液pH由小到大的顺序为
(2)25℃时,醋酸的电离常数Ka=2×10-5mol·L-1,则该温度下CH3COONa的水解平衡常数Kh=
(3)25℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液呈
(4)25℃时,将mmol·L-1的醋酸和nmol·L-1的氢氧化钠溶液等体积混合后,溶液的pH=7,则溶液中c(CH3COO-)+c(CH3COOH)=
(5)25℃时,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的pH=7,则NH3·H2O的电离常数Kb=
(6)设计一个简单的实验,怎样证明醋酸是弱酸?
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在氨水中存在下列电离平衡:NH3·H2O
 +OH-。
+OH-。
(1)下列情况能引起电离平衡正向移动的有___________ (填字母,下同)。
①加NH4Cl固体;②加NaOH溶液;③通入HCl;④加CH3COOH溶液;⑤加水;⑥加热至沸腾
(2)向含有酚酞的0.1 mol·L-1氨水中加入少量的NH4Cl晶体,则溶液颜色___________ 。
a.变蓝色 b.变深 c.变浅 d.不变
(3)向0.1 mol·L-1醋酸溶液中逐滴加入氨水至过量时,溶液的导电能力将发生相应的变化,其电流强度(I)随加入氨水的体积(V)变化的曲线关系是下图中的___________。

 +OH-。
+OH-。(1)下列情况能引起电离平衡正向移动的有
①加NH4Cl固体;②加NaOH溶液;③通入HCl;④加CH3COOH溶液;⑤加水;⑥加热至沸腾
(2)向含有酚酞的0.1 mol·L-1氨水中加入少量的NH4Cl晶体,则溶液颜色
a.变蓝色 b.变深 c.变浅 d.不变
(3)向0.1 mol·L-1醋酸溶液中逐滴加入氨水至过量时,溶液的导电能力将发生相应的变化,其电流强度(I)随加入氨水的体积(V)变化的曲线关系是下图中的___________。
A.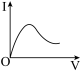 | B. | C.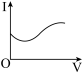 | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据所学知识,完成下列问题。
(1).次磷酸(H3PO2)是一种精细化工产品,向10mLH3PO2溶液中加入30mL等物质的量浓度的NaOH溶液后,所得的溶液中只有 和
和 两种阴离子。
两种阴离子。
①H3PO2中磷元素的化合价为_____________ 。
②写出次磷酸的电离方程式________________________________________________ 。
③H3PO2溶液加水稀释过程中,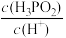 的数值
的数值__________ (填“变大”“变小”或“不变”
(2).联氨(N2H4)是一种应用广泛的化工原料,可用作火箭燃料。N2H4性质与NH3类似。
①在水中,N2H4是一种二元弱碱,请写出其第一步电离方程式_________________________
②等物质的量N2H4与硫酸反应生成的盐的化学式为_________________ 。
(3).已知碳酸、亚硫酸、次氯酸的电离平衡常数如下表。
①试比较 、
、 和HClO的酸性强弱:
和HClO的酸性强弱:_____________ 。
②写出H2SO3与过量NaClO反应的离子方程式_________________________________________________ 。
(1).次磷酸(H3PO2)是一种精细化工产品,向10mLH3PO2溶液中加入30mL等物质的量浓度的NaOH溶液后,所得的溶液中只有
 和
和 两种阴离子。
两种阴离子。
①H3PO2中磷元素的化合价为
②写出次磷酸的电离方程式
③H3PO2溶液加水稀释过程中,
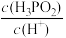 的数值
的数值(2).联氨(N2H4)是一种应用广泛的化工原料,可用作火箭燃料。N2H4性质与NH3类似。
①在水中,N2H4是一种二元弱碱,请写出其第一步电离方程式
②等物质的量N2H4与硫酸反应生成的盐的化学式为
(3).已知碳酸、亚硫酸、次氯酸的电离平衡常数如下表。
物质 | H2CO3 | H2SO3 | HClO | |
电离平衡常数 | Ka1 |
|
|
|
Ka2 |
|
| — | |
 、
、 和HClO的酸性强弱:
和HClO的酸性强弱:②写出H2SO3与过量NaClO反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】常温下,关于下列两个反应:
a、0.1 mol/L 醋酸溶液:CH3COOH CH3COO-+H+
CH3COO-+H+
b、0.1 mol/L 醋酸钠溶液:CH3COO-+H2O CH3COOH+OH-
CH3COOH+OH-
(1)两式到达平衡后,加入一定量的水后,平衡向右移动的是________ ,溶液的pH增大的是________________ 。
(2)向b反应中加入少量的醋酸钠固体,溶液的pH将________ ,若加入同浓度的醋酸钠溶液,溶液的pH将________ (填“增大”、“减小”、“不变”)。
(3)若向a反应中加入少量的醋酸钠固体,溶液的pH将________ ,电离程度将________ ,溶液的导电性将________ (填“增大”、“减小”、“不变”)
a、0.1 mol/L 醋酸溶液:CH3COOH
 CH3COO-+H+
CH3COO-+H+b、0.1 mol/L 醋酸钠溶液:CH3COO-+H2O
 CH3COOH+OH-
CH3COOH+OH-(1)两式到达平衡后,加入一定量的水后,平衡向右移动的是
(2)向b反应中加入少量的醋酸钠固体,溶液的pH将
(3)若向a反应中加入少量的醋酸钠固体,溶液的pH将
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)已知常温时,a mol/L醋酸在水中有0.1 mol/L NaOH等体积混合,溶液为中性,则醋酸钠的水解平衡常数Kh=___________________ (用含a的代数式表示)。
(2)向冰醋酸中逐滴加水,溶液导电性随加入水的体积变化如下图所示:
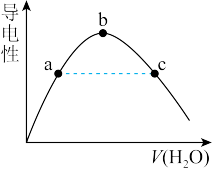
a、b、c三点溶液中CH3COOH的电离程度由大到小的顺序是______________ 。
(3)已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
①物质的量浓度均为0.1 mol/L的四种溶液:pH由小到大排列的顺序是____________ (用编号填写)
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
②写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:_____________________________ 。
(2)向冰醋酸中逐滴加水,溶液导电性随加入水的体积变化如下图所示:

a、b、c三点溶液中CH3COOH的电离程度由大到小的顺序是
(3)已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
②写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知常温下部分弱电解质的电离平衡常数如下表:
(1)常温下,物质的量浓度相同的三种溶液①NaF溶液、②NaClO溶液、③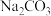 溶液,其pH由大到小的顺序是
溶液,其pH由大到小的顺序是_______ (填标号)。
(2)NaClO溶液显碱性的原因是_______ (用离子方程式表示)。
(3)常温下,将0.1 的氨水和0.1
的氨水和0.1  的
的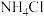 溶液等体积混合,所得混合溶液显
溶液等体积混合,所得混合溶液显_______ (填“酸性”“碱性”或“中性”)。
(4)25℃时,将a 的氨水与0.01
的氨水与0.01  的盐酸等体积混合,反应后所得溶液中
的盐酸等体积混合,反应后所得溶液中 ,用含a的代数式表示
,用含a的代数式表示 的电离平衡常数
的电离平衡常数
_______ 。
| 化学式 | HF | HClO |  |  |
| 电离常数 | 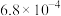 | 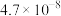 | 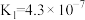 、 、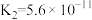 | 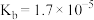 |
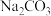 溶液,其pH由大到小的顺序是
溶液,其pH由大到小的顺序是(2)NaClO溶液显碱性的原因是
(3)常温下,将0.1
 的氨水和0.1
的氨水和0.1  的
的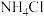 溶液等体积混合,所得混合溶液显
溶液等体积混合,所得混合溶液显(4)25℃时,将a
 的氨水与0.01
的氨水与0.01  的盐酸等体积混合,反应后所得溶液中
的盐酸等体积混合,反应后所得溶液中 ,用含a的代数式表示
,用含a的代数式表示 的电离平衡常数
的电离平衡常数
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】草酸即乙二酸,是一种有机二元酸,在工业上有重要的应用。草酸在100℃时开始升华,157℃时大量升华,并开始分解。常温下,相关数据如表所示:
(1)常温下,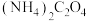 ,溶液的pH
,溶液的pH__________ 7(填“>”“<”或“=”)。
(2)用惰性电极电解饱和草酸溶液可制得乙醛酸( ),阴极的电极反应式为
),阴极的电极反应式为_______ 。
(3)草酸钠是一种重要的还原剂。合成草酸钠的操作如下:草酸 草酸钠晶体
草酸钠晶体
①75%酒精的作用是____________________________________ 。
②将草酸与碳酸钠按物质的量之比为2∶1充分溶解在足量的水中,所得溶液的 。请将所得溶液中离子浓度按由大到小的顺序排列:
。请将所得溶液中离子浓度按由大到小的顺序排列:____________________________________________ 。
(4)已知某温度下 的
的 为
为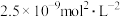 。将
。将 的
的 溶液和
溶液和 的
的 溶液等体积混合后,所得溶液中
溶液等体积混合后,所得溶液中 的物质的量浓度为
的物质的量浓度为__________ 。
| 电离方程式 | 电离常数 |
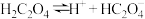 |  |
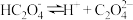 | 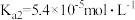 |
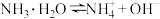 | 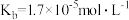 |
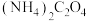 ,溶液的pH
,溶液的pH(2)用惰性电极电解饱和草酸溶液可制得乙醛酸(
 ),阴极的电极反应式为
),阴极的电极反应式为(3)草酸钠是一种重要的还原剂。合成草酸钠的操作如下:草酸
 草酸钠晶体
草酸钠晶体①75%酒精的作用是
②将草酸与碳酸钠按物质的量之比为2∶1充分溶解在足量的水中,所得溶液的
 。请将所得溶液中离子浓度按由大到小的顺序排列:
。请将所得溶液中离子浓度按由大到小的顺序排列:(4)已知某温度下
 的
的 为
为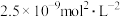 。将
。将 的
的 溶液和
溶液和 的
的 溶液等体积混合后,所得溶液中
溶液等体积混合后,所得溶液中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某工厂采用如下工艺处理镍钴矿硫酸浸取液含(Ni2+、Co2+、Fe2+、Fe3+、Mg2+和Mn2+)。实现镍、钴、镁元素的回收。
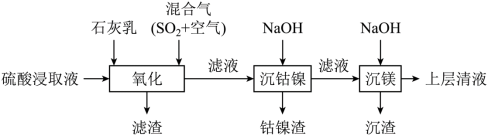
已知:
(1)“氧化”中,用石灰乳调节pH=4,Mn2+被H2SO5氧化为MnO2,该反应的离子方程式为___________ ( H2SO5的电离第一步完全,第二步微弱);滤渣的成分为MnO2、___________ (填化学式)。
(2)“沉镁”中为使Mg2+沉淀完全(25℃),需控制pH不低于___________ (精确至0.1)。

已知:
| 物质 | Fe(OH)3 | Co(OH)2 | Ni(OH)2 | Mg(OH)2 |
| Ksp | 10-37.4 | 10-14.7 | 10-14.7 | 10-10.8 |
(2)“沉镁”中为使Mg2+沉淀完全(25℃),需控制pH不低于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题
(1)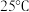 时,
时, 的电离平衡常数为:
的电离平衡常数为: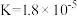 ,
, 的电离平衡常数为:
的电离平衡常数为: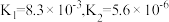 ;则:
;则:
①写出 的电离方程式:
的电离方程式:_______
②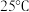 时,
时,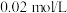 的
的 溶液的电离度约为
溶液的电离度约为_______  。
。
③往 溶液中滴加足量
溶液中滴加足量 溶液的离子反应方程式为:
溶液的离子反应方程式为:_______
(2)①某课外活动小组为了探究 的溶解度,分别将足量
的溶解度,分别将足量 加入下列物质中:
加入下列物质中:
a.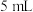 水 b.
水 b.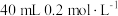 的
的 溶液
溶液
c.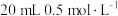 的
的 溶液 d.
溶液 d.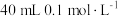 的
的 溶液中
溶液中
溶解 后形成的溶液中,
后形成的溶液中, 的浓度由大到小的顺序为
的浓度由大到小的顺序为_______ (填字母)。
A.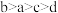 B.
B.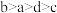 C.
C.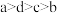 D.
D.
②已知 时,
时,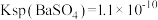 ,此时,溶液b中加入
,此时,溶液b中加入 后,
后, 为
为_______  。
。
(3)新型高效的乙烷燃料电池采用铂为电极材料,两电极上分别通入 和
和 ,电解质溶液为
,电解质溶液为 溶液。请写出乙烷燃料电池的负极反应式:
溶液。请写出乙烷燃料电池的负极反应式:_______ 。
(1)
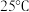 时,
时, 的电离平衡常数为:
的电离平衡常数为: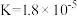 ,
, 的电离平衡常数为:
的电离平衡常数为: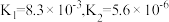 ;则:
;则:①写出
 的电离方程式:
的电离方程式:②
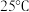 时,
时,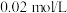 的
的 溶液的电离度约为
溶液的电离度约为 。
。③往
 溶液中滴加足量
溶液中滴加足量 溶液的离子反应方程式为:
溶液的离子反应方程式为:(2)①某课外活动小组为了探究
 的溶解度,分别将足量
的溶解度,分别将足量 加入下列物质中:
加入下列物质中:a.
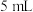 水 b.
水 b.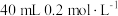 的
的 溶液
溶液c.
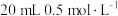 的
的 溶液 d.
溶液 d.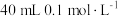 的
的 溶液中
溶液中溶解
 后形成的溶液中,
后形成的溶液中, 的浓度由大到小的顺序为
的浓度由大到小的顺序为A.
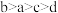 B.
B.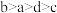 C.
C.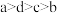 D.
D.
②已知
 时,
时,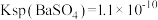 ,此时,溶液b中加入
,此时,溶液b中加入 后,
后, 为
为 。
。(3)新型高效的乙烷燃料电池采用铂为电极材料,两电极上分别通入
 和
和 ,电解质溶液为
,电解质溶液为 溶液。请写出乙烷燃料电池的负极反应式:
溶液。请写出乙烷燃料电池的负极反应式:
您最近一年使用:0次