A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)元素名称:A___ 、B___ 、C___ 、D___
(2)D元素的最高价氧化物的水化物是(化学式)__________ ,A、B两元素形成化合物属 _______ (选填“离子”或“共价”)化合物。
(3)写出A、B的化合物与E反应的化学方程式:____________________ 。
(1)元素名称:A
(2)D元素的最高价氧化物的水化物是(化学式)
(3)写出A、B的化合物与E反应的化学方程式:
更新时间:2017-05-05 15:56:05
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。

(1)若A 是一种淡黄色固体单质.则C与H2O反应的生成物为______ (填化学式)。
(2)Na2O2也是一种淡黄色固体,Na2O2与CO2反应生成O2和_______ (填化学式)。
(3)写出在催化剂作用下N2与H2合成氨的化学方程式:_______________________________ 。

(1)若A 是一种淡黄色固体单质.则C与H2O反应的生成物为
(2)Na2O2也是一种淡黄色固体,Na2O2与CO2反应生成O2和
(3)写出在催化剂作用下N2与H2合成氨的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】下图中每一方框中表示一种反应物或生成物,其中A、C、D、E在通常情况下均为气体,B为液体,(图中有些反应的产物和反应条件没有标出)。试回答:
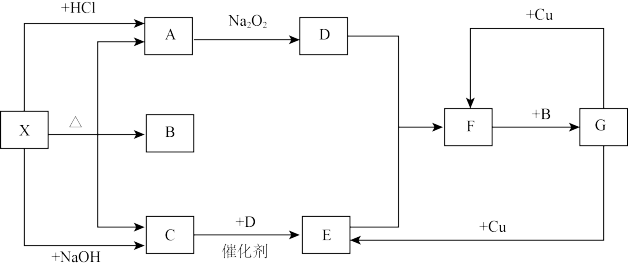
(1)X是_____ ,C是______ ,F是______ 。
(2)写出A→D反应的化学方程式___________ 。
(3)写出G→E反应的化学方程式___________ 。
(4)写出C→E反应的化学方程式____________ 。

(1)X是
(2)写出A→D反应的化学方程式
(3)写出G→E反应的化学方程式
(4)写出C→E反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐3】下表为元素周期表的一部分,请参照元素①~⑩在表中的位置,回答下列问题(填元素符号或化学式):
(1)元素⑪的原子结构示意图为________________ 。
(2)④、⑤、⑥的简单离子半径由大到小的顺序为______________ (用离子符号和“>”表示)。
(3)④⑨⑩的气态氢化物中,最稳定的是__________ (用化学式表示),最高价氧化物对应水化物中,酸性最强的是_________ (用化学式表示)。
(4)⑥的最高价氧化物对应的水化物与⑧的最高价氧化物对应的水化物发生反应的离子方程式____________________________________ 。
(5)⑥的单质在空气中燃烧可生成淡黄色粉末X,X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和下图所示实验装置证明X有提供氧气的作用。回答下列问题:

①装置A使用石灰石与浓盐酸反应制取CO2,装置B中饱和NaHCO3溶液的作用是_____________________________________________ ;
②装置C中X与CO2反应的化学方程式是_________________________________ ,装置D盛放NaOH溶液的作用是除去____________________________________ ;
③为检验试管F收集的气体,操作为________________________ ,出现_____________________ 现象,即证明X可作供氧剂。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ||||||||||||||
| ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||||||||||||
| ⑪ | |||||||||||||||||
(2)④、⑤、⑥的简单离子半径由大到小的顺序为
(3)④⑨⑩的气态氢化物中,最稳定的是
(4)⑥的最高价氧化物对应的水化物与⑧的最高价氧化物对应的水化物发生反应的离子方程式
(5)⑥的单质在空气中燃烧可生成淡黄色粉末X,X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和下图所示实验装置证明X有提供氧气的作用。回答下列问题:

①装置A使用石灰石与浓盐酸反应制取CO2,装置B中饱和NaHCO3溶液的作用是
②装置C中X与CO2反应的化学方程式是
③为检验试管F收集的气体,操作为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】下表中的实线表示元素周期表的部分边界,a-j分别表示周期表中对应位置的元素。回答下列问题:
(1)请在上表中用实线补全元素周期表边界_______ 。
(2)元素b在元素周期表中的位置是_______ ;元素a与d形成的4核18电子物质的分子式_______ 。
(3)元素e、g、h的简单离子半径由小到大的顺序为______ 。(用离子符号表示)
(4)元素e的气态氢化物比元素i的气态氢化物稳定性______ 。(填“强”或“弱”)。
(5)元素d与f形成的化合物中,原子个数1:1的化合物所含化学键类型为______ 。
(6)用电子式表示元素i、j形成化合物的过程______________________ 。
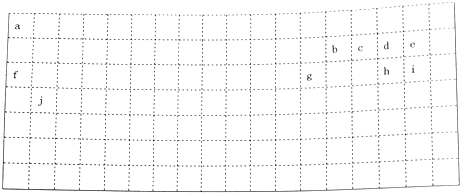
(1)请在上表中用实线补全元素周期表边界
(2)元素b在元素周期表中的位置是
(3)元素e、g、h的简单离子半径由小到大的顺序为
(4)元素e的气态氢化物比元素i的气态氢化物稳定性
(5)元素d与f形成的化合物中,原子个数1:1的化合物所含化学键类型为
(6)用电子式表示元素i、j形成化合物的过程
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期。自然界存在多种A的化合物,B原子核外电子由6种不同的运动状态,B与C可形成正四面体形分子,D的M能层没有空轨道且只有2个未成对电子。请回答下列问题:
(1)A与B元素形成的B2A2种含有的σ键、π键数目之比为________ 。
(2)B元素的一种单质晶体结构如图1所示,理论上12g该晶体中有________ 个六元环;图2位在元素周期表中与B相邻的元素位置关系,B、G形成的晶胞结构如图3所示(其中“●”为B元素原子,“〇”为G元素原子),图中“●”点构成的堆积方式与图4中_____ (填序号)所表示的堆积方式相同;图3的结构中,设晶胞边长为a cm,B原子直径为bcm,G原子直径为c cm,则该晶胞的空间利用率为_______ (用含a、b、c的式子表示)。

(3)请说出E的氟化物(EF3)和F的氢化物(FH3)能发生反应的原因,并写出反应的化学方程式_____ (用化学式表示)。
(4)元素C的含氧酸中,酸性最强的是_________ (写化学式),该酸根离子的立体构型为________ 。
(5)基态D原子的核外电子排布式为[Ar]_______ ;D形成的配合物D(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=______ ;由D一铝合金为原料可制得一种历史悠久、应用广泛的催化剂,其催化的i实例为: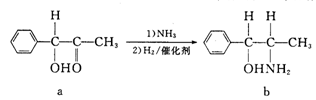 化合物b中进行sp3杂化的原子有
化合物b中进行sp3杂化的原子有__________ (填元素符号)。
(1)A与B元素形成的B2A2种含有的σ键、π键数目之比为
(2)B元素的一种单质晶体结构如图1所示,理论上12g该晶体中有

(3)请说出E的氟化物(EF3)和F的氢化物(FH3)能发生反应的原因,并写出反应的化学方程式
(4)元素C的含氧酸中,酸性最强的是
(5)基态D原子的核外电子排布式为[Ar]
 化合物b中进行sp3杂化的原子有
化合物b中进行sp3杂化的原子有
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】W、X、Y、Z为原子序数依次递增的短周期主族元素,W的单质是同条件下密度最小的气体,X、Y、Z为同一周期紧邻元素,M、R为同一主族的元素,M的单质常温为液态,R的单质常温为固态,且易升华。回答下列问题:
(1)写出下列元素的名称:W___ ;M____ 。
(2)若X为形成化合物种类最多的元素,XZ(YW2)2为一种有机物,是目前使用量较大的化学肥料。XZ(YW2)2在碱性条件下能被MZ−氧化成单质Q(空气中的主要成分之一),X以酸根的形式存在。
①写出Q的化学式:___ ;X、Y、Z的简单氢化物的沸点由高到低的顺序为__ (写化学式)。
②上述反应的离子方程式为___ 。
(3)若Z为本周期中半径最小的元素,其最高价氧化物对应的水化物为强酸。
①请判断R2+ZO3-→RO3-+Z2是否能发生,__ (填“能”或“不能”)发生,其原因是____ 。
②请写出R2与含YO32-溶液反应的离子方程式为____ 。
(1)写出下列元素的名称:W
(2)若X为形成化合物种类最多的元素,XZ(YW2)2为一种有机物,是目前使用量较大的化学肥料。XZ(YW2)2在碱性条件下能被MZ−氧化成单质Q(空气中的主要成分之一),X以酸根的形式存在。
①写出Q的化学式:
②上述反应的离子方程式为
(3)若Z为本周期中半径最小的元素,其最高价氧化物对应的水化物为强酸。
①请判断R2+ZO3-→RO3-+Z2是否能发生,
②请写出R2与含YO32-溶液反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
真题
解题方法
【推荐1】 是生产多晶硅的副产物。利用
是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下:
(1)Co位于元素周期表第_______ 周期,第_______ 族。
(2)烧渣是LiCl、 和
和 的混合物,“500℃焙烧”后剩余的
的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因
应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因_______ 。
(3)鉴别洗净的“滤饼3”和固体 常用方法的名称是
常用方法的名称是_______ 。
(4)已知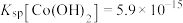 ,若“沉钴过滤”的pH控制为10.0,则溶液中
,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
浓度为_______  。“850℃煅烧”时的化学方程式为
。“850℃煅烧”时的化学方程式为_______ 。
(5)导致 比
比 易水解的因素有
易水解的因素有_______ (填标号)。
a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
 是生产多晶硅的副产物。利用
是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下: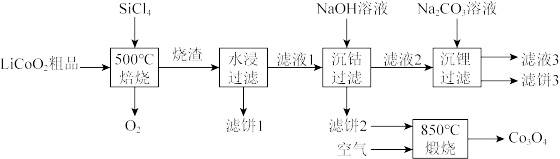
(1)Co位于元素周期表第
(2)烧渣是LiCl、
 和
和 的混合物,“500℃焙烧”后剩余的
的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因
应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因(3)鉴别洗净的“滤饼3”和固体
 常用方法的名称是
常用方法的名称是(4)已知
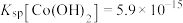 ,若“沉钴过滤”的pH控制为10.0,则溶液中
,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
浓度为 。“850℃煅烧”时的化学方程式为
。“850℃煅烧”时的化学方程式为(5)导致
 比
比 易水解的因素有
易水解的因素有a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】下列表格是元素周期表的一部分。请按要求填空(用化学用语填写)
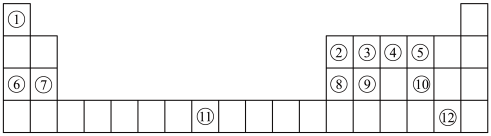
(1)元素①和⑥形成的化合物中存在的化学键类型为_______ 。
(2)用化学方程式表示④的简单氢化物的工业制法_______ 。
(3)写出由③④⑥形成的化合物的电子式_______ 。
(4)列举元素⑨形成的氧化物的一种用途_______ ,元素⑪在周期表中的位置_______ 。
(5)①⑤⑦⑧的简单离子半径由大到小的顺序为_______ 。
(6)写出⑧⑫的最高价氧化物的水化物发生反应的化学方程式为_______ 。
(7)X是由①④⑤⑧⑩形成的复盐,向含0.01 mol X的溶液中加入0.024 mol ,生成沉淀的物质的量的总和为
,生成沉淀的物质的量的总和为_______ 。

(1)元素①和⑥形成的化合物中存在的化学键类型为
(2)用化学方程式表示④的简单氢化物的工业制法
(3)写出由③④⑥形成的化合物的电子式
(4)列举元素⑨形成的氧化物的一种用途
(5)①⑤⑦⑧的简单离子半径由大到小的顺序为
(6)写出⑧⑫的最高价氧化物的水化物发生反应的化学方程式为
(7)X是由①④⑤⑧⑩形成的复盐,向含0.01 mol X的溶液中加入0.024 mol
 ,生成沉淀的物质的量的总和为
,生成沉淀的物质的量的总和为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】已知A、B、C、D四种元素分别为短周期元素,表示中三个不同短周期的主族元素,且原子序数依次增
大。D原子的质子数是B原子质子数的2倍,A原子与D原子的最外层电子数之和是B原子与C原子质子
数之和的1/3。A与B可形成BA3型化合物,该化合物与C的单质在一定条件下反应,能生成化合物BC,请按要求填写下列空白:
(1)D元素的名称____________ ,C元素在元素周期表中的位置_____________ 。
(2)写出BA3的电子式____________ ,BA3跟C的单质在一定条件下反应,能生成化合物BC的化学方程式________________________________ 。
(3)D单质在工业上最重要的用途是_________ ,写出工业上制取D单质的化学方程式__________ 。
(4)在实验室中B的最高价氧化物的水化物的浓溶液应如何保存__________________ ,用化学方程
式说明理由____________________________________ 。
大。D原子的质子数是B原子质子数的2倍,A原子与D原子的最外层电子数之和是B原子与C原子质子
数之和的1/3。A与B可形成BA3型化合物,该化合物与C的单质在一定条件下反应,能生成化合物BC,请按要求填写下列空白:
(1)D元素的名称
(2)写出BA3的电子式
(3)D单质在工业上最重要的用途是
(4)在实验室中B的最高价氧化物的水化物的浓溶液应如何保存
式说明理由
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】铝酸铋[Bi(AlO2)3]主要用作抗酸药及抗溃疡药,具有中和胃酸和收敛作用。以辉铋矿(主要成分为Bi2S3,含有SiO2、Cu2S、FeS2杂质)为原料制备铝酸铋的一种工艺流程如图所示:

已知:①常温下,Cu(OH)2、Fe(OH)2、Fe(OH)3和Bi(OH)3的Ksp分别为2.0×10-20、4.0×10-16、.4.0×10-38和8.0×10-31,lg2=0.3。
②Cu(OH)2能溶于氨水生成[Cu(NH3)4]2+。
③Sn2+和Sn4+在碱性溶液中分别以[Sn(OH)4]2-和[Sn(OH)6]2-的形式存在。
请回答下列问题:
(1)铋与氮同主族,铋元素在元素周期表中的位置是___________ 。
(2)滤渣1中除了硫单质,还含另一种物质,30g该物质中含共价键的数目是___________ ,FeCl3与Cu2S反应中氧化剂与还原剂的物质的量之比为___________ 。
(3)“还原”时,加入铋的目的是___________ 。
(4)“沉淀”前,若滤液中Cu2+浓度为0.005mol·L-1,Fe2+浓度为0.01mol·L-1,则“沉淀”时调pH的最大值应小于___________ 。
(5)在碱性溶液中,可用[Sn(OH)4]2-鉴定Bi3+存在,Bi3+被还原为Bi写出该反应的离子方程式:___________ 。
(6)在氢氧化钠溶液中,次氯酸钠能将Bi(OH)3氧化为NaBiO3,写出该反应的化学方程式:___________ 。

已知:①常温下,Cu(OH)2、Fe(OH)2、Fe(OH)3和Bi(OH)3的Ksp分别为2.0×10-20、4.0×10-16、.4.0×10-38和8.0×10-31,lg2=0.3。
②Cu(OH)2能溶于氨水生成[Cu(NH3)4]2+。
③Sn2+和Sn4+在碱性溶液中分别以[Sn(OH)4]2-和[Sn(OH)6]2-的形式存在。
请回答下列问题:
(1)铋与氮同主族,铋元素在元素周期表中的位置是
(2)滤渣1中除了硫单质,还含另一种物质,30g该物质中含共价键的数目是
(3)“还原”时,加入铋的目的是
(4)“沉淀”前,若滤液中Cu2+浓度为0.005mol·L-1,Fe2+浓度为0.01mol·L-1,则“沉淀”时调pH的最大值应小于
(5)在碱性溶液中,可用[Sn(OH)4]2-鉴定Bi3+存在,Bi3+被还原为Bi写出该反应的离子方程式:
(6)在氢氧化钠溶液中,次氯酸钠能将Bi(OH)3氧化为NaBiO3,写出该反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】有7种短周期主族元素,其中元素A、B、C、D原子序数依次减小,该四种元素原子K层电子总数为7,L层电子中总数为22,M层电子总数为12,E与B同主族,F与C同主族,短周期中G的原子半径最大。用化学用语或文字回答下列问题。
(1)A、C、F、G简单离子半径由大到小顺序___________ 。
(2)G、C按1∶1形成的化合物含化学键类型___________ 。
(3)下列事实能说明A元素的非金属性比F元素的非金属性强的是___________ 。
a.A单质与 溶液反应溶液变混浊
溶液反应溶液变混浊
b.F氢化物的酸性比A的氢化物酸性弱
c.A和F两元素的简单氢化物受热分解,前者的分解温度高
(4)举例说明最高价氧化物对应的水化物碱性强弱:___________ >G的最高价氧化物对应的水化物>___________ 。
(5)在微电子工业中,E的简单气态氢化物的水溶液可作刻蚀剂 的清除剂,所发生反应的产物不污染环境,其化学方程式为
的清除剂,所发生反应的产物不污染环境,其化学方程式为___________ 。
(1)A、C、F、G简单离子半径由大到小顺序
(2)G、C按1∶1形成的化合物含化学键类型
(3)下列事实能说明A元素的非金属性比F元素的非金属性强的是
a.A单质与
 溶液反应溶液变混浊
溶液反应溶液变混浊b.F氢化物的酸性比A的氢化物酸性弱
c.A和F两元素的简单氢化物受热分解,前者的分解温度高
(4)举例说明最高价氧化物对应的水化物碱性强弱:
(5)在微电子工业中,E的简单气态氢化物的水溶液可作刻蚀剂
 的清除剂,所发生反应的产物不污染环境,其化学方程式为
的清除剂,所发生反应的产物不污染环境,其化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】Ⅰ:实验室通过简单的“试管实验”,即可探究元素金属性、非金属性的递变规律。
(1)甲同学为证明Mg的金属性比Al强,进行简单“试管实验”时,需要实验室提供的化学试剂分别是_______________________________________ ;能够说明Mg的金属性比Al强的实验现象是_____________________________________ 。
(2)乙同学为探究Cl与Br的非金属性强弱,设计实验方案中依据的化学反应原理是_______________________________ (用化学反应方程式表示);要使可观察到的实验现象明显,需向反应后的试管中加入的一种试剂是__________________________ 。
Ⅱ:有关资料表明:①将氯化铝加热,在180℃时开始升华;②在2.02×105Pa条件下,氯化铝的熔点为190℃;
(3)根据资料信息推理,你认为氯化铝是离子化合物还是共价化合物?___________ ;理由是______________________________________________________________ 。
(4) 请你设计一实验方案,证明氯化铝是离子化合物还是共价化合物。简要写出实验内容、现象和结论。___________________________________________________ 。
(1)甲同学为证明Mg的金属性比Al强,进行简单“试管实验”时,需要实验室提供的化学试剂分别是
(2)乙同学为探究Cl与Br的非金属性强弱,设计实验方案中依据的化学反应原理是
Ⅱ:有关资料表明:①将氯化铝加热,在180℃时开始升华;②在2.02×105Pa条件下,氯化铝的熔点为190℃;
(3)根据资料信息推理,你认为氯化铝是离子化合物还是共价化合物?
(4) 请你设计一实验方案,证明氯化铝是离子化合物还是共价化合物。简要写出实验内容、现象和结论。
您最近一年使用:0次



