 是生产多晶硅的副产物。利用
是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下: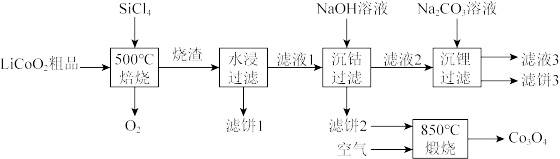
(1)Co位于元素周期表第
(2)烧渣是LiCl、
 和
和 的混合物,“500℃焙烧”后剩余的
的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因
应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因(3)鉴别洗净的“滤饼3”和固体
 常用方法的名称是
常用方法的名称是(4)已知
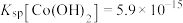 ,若“沉钴过滤”的pH控制为10.0,则溶液中
,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
浓度为 。“850℃煅烧”时的化学方程式为
。“850℃煅烧”时的化学方程式为(5)导致
 比
比 易水解的因素有
易水解的因素有a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
2023·湖北·高考真题 查看更多[13]
2023年高考湖北卷化学真题(已下线)专题18 工艺流程题(已下线)T16-工业流程题(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题(已下线)第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第32讲难溶电解质的溶解平衡(已下线)题型06 化工微流程-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)专题06 沉淀溶解平衡-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)(已下线)题型四 无机化工流程题解题策略-备战2024年高考化学答题技巧与模板构建
更新时间:2023-06-14 16:08:23
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
【推荐1】正盐A、B均含三种元素,且所含元素种类相同。A在加热条件下发生如下变化。已知,气体D能使带火星的木条复燃。透过蓝色钴玻璃,A、B、C的焰色反应均为紫色。往C的溶液中加入AgNO3溶液,出现白色沉淀,再加入稀硝酸,沉淀不溶解,且沉淀质量为14.35克。请回答:

(1)C的化学式为___________ 。
(2)写出 A分解的化学方程式___________ 。
(3)将A与C混合,再加入稀硫酸,有气体产生,用离子方程式表示发生的反应___________ 。

(1)C的化学式为
(2)写出 A分解的化学方程式
(3)将A与C混合,再加入稀硫酸,有气体产生,用离子方程式表示发生的反应
您最近一年使用:0次
【推荐2】I.A是一种重要的化工原料,可以制备多种物质。下图所列物质中,C、D、E均为单原,其中D是一种黄绿色气体,C在D中燃烧时发出苍白色火焰,B是一种强碱,焰色试验火焰呈黄色,H是一种混合物,其水溶液具有漂白性。

(1)A是_______ 、B是_______ 、E是_______ 、F是_______ (以上均写化学式)。
(2)写出图中D生成H的化学方程式_______ ,当反应中消耗21.3gD时,转移的电子数是_______ 。
(3)高温时,将金红石(主要成分是 )、焦炭和D混合反应,得到一种可燃性气体和另一种化合物(由:元素和D所含元素组成,其中
)、焦炭和D混合反应,得到一种可燃性气体和另一种化合物(由:元素和D所含元素组成,其中 为+4价,相对分子质量为190)。写出上述反应的化学方程式
为+4价,相对分子质量为190)。写出上述反应的化学方程式_______ 。
II.栲胶法脱除煤气中硫化氢的工艺流程示意如下:

“吸收”步骤除了生成 外,还生成了
外,还生成了 ,“脱硫”步骤的中间产物可与“吸收”步骤中生成的
,“脱硫”步骤的中间产物可与“吸收”步骤中生成的 反应,实现
反应,实现 的再生。
的再生。
“氧化I”发生反应的化学方程式为: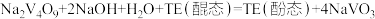
(4) 中V的化合价是
中V的化合价是_______ ;
(5)“氧化I”步骤的作用是_______ 。
(6)该流程总反应的化学方程式为_______ 。

(1)A是
(2)写出图中D生成H的化学方程式
(3)高温时,将金红石(主要成分是
 )、焦炭和D混合反应,得到一种可燃性气体和另一种化合物(由:元素和D所含元素组成,其中
)、焦炭和D混合反应,得到一种可燃性气体和另一种化合物(由:元素和D所含元素组成,其中 为+4价,相对分子质量为190)。写出上述反应的化学方程式
为+4价,相对分子质量为190)。写出上述反应的化学方程式II.栲胶法脱除煤气中硫化氢的工艺流程示意如下:

“吸收”步骤除了生成
 外,还生成了
外,还生成了 ,“脱硫”步骤的中间产物可与“吸收”步骤中生成的
,“脱硫”步骤的中间产物可与“吸收”步骤中生成的 反应,实现
反应,实现 的再生。
的再生。“氧化I”发生反应的化学方程式为:
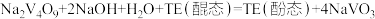
(4)
 中V的化合价是
中V的化合价是(5)“氧化I”步骤的作用是
(6)该流程总反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】2019年诺贝尔化学奖颁给了日本吉野彰等三人,以表彰他们对锂离子电池研发的卓越贡献。
(1)自然界中主要的锂矿物为锂辉石、锂云母、透锂长石和磷锂铝石等。为鉴定某矿石中是否含有锂元素,可以采用焰色反应来进行鉴定,当观察到火焰呈________ ,可以认为存在锂元素。
A.紫红色 B.紫色 C.黄色
(2)工业中利用锂辉石(主要成分为LiAlSi2O6,还含有FeO、CaO、MgO等)制备钴酸锂(LiCoO2)的流程如下:
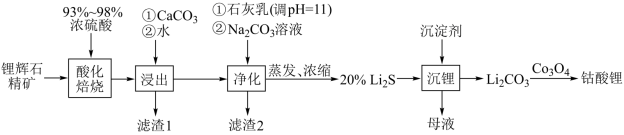
已知:部分金属氢氧化物的pKsp(pKsp=-lgKsp)的柱状图如图1。
回答下列问题:
①锂辉石的主要成分为LiAlSi2O6,其氧化物的形式为________ 。
②为提高“酸化焙烧”效率,常采取的措施是________ 。
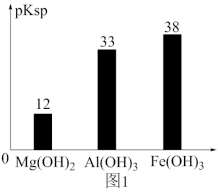
③向“浸出液”中加入CaCO3,其目的是除去“酸化焙烧”中过量的硫酸,控制pH使Fe3+、A13+完全沉淀,则pH至少为_______ 。(已知:完全沉淀后离子浓度低于1×l0-5)mol/L)
④“沉锂”过程所获得的“母液”中仍含有大量的Li+,可将其加入到“___________ ”步骤中。
⑤Li2CO3与Co3O4在敞口容器中高温下焙烧生成钴酸锂的化学方程式为__________
(3)利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LiCoO2+C6 LixC6+Li1-xCoO2 ,其工作原理如图2。
LixC6+Li1-xCoO2 ,其工作原理如图2。

下列关于该电池的说法正确的是___________ (填字母)。
A.电池反应式中过程1为放电过程
B.该电池若用隔膜可选用质子交换膜
C.石墨烯电池的优点是提高电池的储锂容量进而提高能量密度
D.充电时,LiCoO2极发生的电极反应为LiCoO2-xe-=xLi++Li1-xCoO2
E.对废旧的该电池进行“放电处理”让Li+嵌入石墨烯中而有利于回收
(1)自然界中主要的锂矿物为锂辉石、锂云母、透锂长石和磷锂铝石等。为鉴定某矿石中是否含有锂元素,可以采用焰色反应来进行鉴定,当观察到火焰呈
A.紫红色 B.紫色 C.黄色
(2)工业中利用锂辉石(主要成分为LiAlSi2O6,还含有FeO、CaO、MgO等)制备钴酸锂(LiCoO2)的流程如下:

已知:部分金属氢氧化物的pKsp(pKsp=-lgKsp)的柱状图如图1。

回答下列问题:
①锂辉石的主要成分为LiAlSi2O6,其氧化物的形式为
②为提高“酸化焙烧”效率,常采取的措施是
③向“浸出液”中加入CaCO3,其目的是除去“酸化焙烧”中过量的硫酸,控制pH使Fe3+、A13+完全沉淀,则pH至少为
④“沉锂”过程所获得的“母液”中仍含有大量的Li+,可将其加入到“
⑤Li2CO3与Co3O4在敞口容器中高温下焙烧生成钴酸锂的化学方程式为
(3)利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LiCoO2+C6
 LixC6+Li1-xCoO2 ,其工作原理如图2。
LixC6+Li1-xCoO2 ,其工作原理如图2。
下列关于该电池的说法正确的是
A.电池反应式中过程1为放电过程
B.该电池若用隔膜可选用质子交换膜
C.石墨烯电池的优点是提高电池的储锂容量进而提高能量密度
D.充电时,LiCoO2极发生的电极反应为LiCoO2-xe-=xLi++Li1-xCoO2
E.对废旧的该电池进行“放电处理”让Li+嵌入石墨烯中而有利于回收
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】水是生命之源,生产和生活都离不开水。请回答有关问题:
(1)置于密闭容器中的纯水(如图一所示,存在平衡: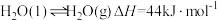 。一定温度下达到平衡时,
。一定温度下达到平衡时,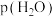 (水蒸气产生的压强)为一定值,该压强称为相应温度下的饱和蒸气压。若将水置于敞口容器中,当水的饱和蒸气压与外界气压相同时,水就会沸腾。
(水蒸气产生的压强)为一定值,该压强称为相应温度下的饱和蒸气压。若将水置于敞口容器中,当水的饱和蒸气压与外界气压相同时,水就会沸腾。

①从过程的自发性角度分析,常温下水能够挥发的原因是_______ 。
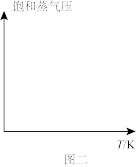
②已知一定物质的量的气体产生的压强与温度成正比。请在图二中画出水的饱和蒸气压随温度的变化曲线,标注为纯水。当水中溶有非挥发性溶质时,水的沸点会升高,请再在图二中画出水中加入非挥发性溶质时,饱和蒸气压与温度的变化曲线,标注为溶液_______ 。
(2)水是很好的溶剂,通常所讲的沉淀在水中也有一定的溶解度,它们在水中存在溶解平衡。已知常温时:
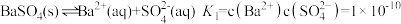
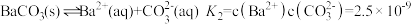
工业上常用碳酸钠溶液处理 ,使之转化成
,使之转化成 后再转化成可溶性钡盐。若用体积为
后再转化成可溶性钡盐。若用体积为 ,物质的量浓度为c的碳酸钠溶液一次性处理
,物质的量浓度为c的碳酸钠溶液一次性处理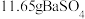 ,使之完全转化为
,使之完全转化为 ,则c应满足的条件是(反应过程中溶液体积不变)
,则c应满足的条件是(反应过程中溶液体积不变)_______ 。
(3)水蒸气和沼气(含 )的催化重整反应可用于制氢气,相关反应如下:
)的催化重整反应可用于制氢气,相关反应如下:
Ⅰ: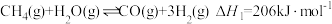
Ⅱ: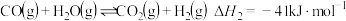
Ⅲ: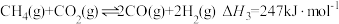
其他:甲烷高温分解等原因造成的积碳反应。
①工业生产中常采用700℃左右的高温,原因是_______ 。
②一定温度下,某密闭容器中充入一定量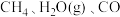 和
和 发生反应Ⅰ,下列有关说法正确的是
发生反应Ⅰ,下列有关说法正确的是_______ 。
A.若反应在恒压容器中进行,容器体积不再发生变化时,反应达到平衡状态
B.若反应在恒容容器中进行,达到平衡后再向容器中充入一定量 ,达到新平衡后,与原平衡相比,正反应速率增大,逆反应速率减小
,达到新平衡后,与原平衡相比,正反应速率增大,逆反应速率减小
C.若反应在恒容容器中进行,达到平衡后,降低体系温度,达新平衡时, 体积分数一定减小
体积分数一定减小
D.若反应在恒压容器中进行,达到平衡后再向容器中充入一定量 ,达新平衡时,
,达新平衡时, 比原平衡大
比原平衡大
③在催化剂作用下,反应Ⅰ机理涉及如下过程(*代表催化剂吸附中心位点,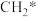 代表吸附态的
代表吸附态的 )
)
(a):
(b):
(c):_______
(d):_______
(e)
分别写出过程(c)、(d)的反应式:
(c)_______
(d)_______
(1)置于密闭容器中的纯水(如图一所示,存在平衡:
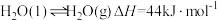 。一定温度下达到平衡时,
。一定温度下达到平衡时,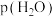 (水蒸气产生的压强)为一定值,该压强称为相应温度下的饱和蒸气压。若将水置于敞口容器中,当水的饱和蒸气压与外界气压相同时,水就会沸腾。
(水蒸气产生的压强)为一定值,该压强称为相应温度下的饱和蒸气压。若将水置于敞口容器中,当水的饱和蒸气压与外界气压相同时,水就会沸腾。
①从过程的自发性角度分析,常温下水能够挥发的原因是
②已知一定物质的量的气体产生的压强与温度成正比。请在图二中画出水的饱和蒸气压随温度的变化曲线,标注为纯水。当水中溶有非挥发性溶质时,水的沸点会升高,请再在图二中画出水中加入非挥发性溶质时,饱和蒸气压与温度的变化曲线,标注为溶液

(2)水是很好的溶剂,通常所讲的沉淀在水中也有一定的溶解度,它们在水中存在溶解平衡。已知常温时:
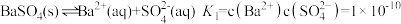
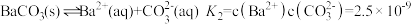
工业上常用碳酸钠溶液处理
 ,使之转化成
,使之转化成 后再转化成可溶性钡盐。若用体积为
后再转化成可溶性钡盐。若用体积为 ,物质的量浓度为c的碳酸钠溶液一次性处理
,物质的量浓度为c的碳酸钠溶液一次性处理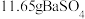 ,使之完全转化为
,使之完全转化为 ,则c应满足的条件是(反应过程中溶液体积不变)
,则c应满足的条件是(反应过程中溶液体积不变)(3)水蒸气和沼气(含
 )的催化重整反应可用于制氢气,相关反应如下:
)的催化重整反应可用于制氢气,相关反应如下:Ⅰ:
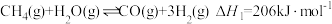
Ⅱ:
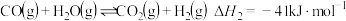
Ⅲ:
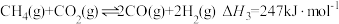
其他:甲烷高温分解等原因造成的积碳反应。
①工业生产中常采用700℃左右的高温,原因是
②一定温度下,某密闭容器中充入一定量
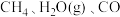 和
和 发生反应Ⅰ,下列有关说法正确的是
发生反应Ⅰ,下列有关说法正确的是A.若反应在恒压容器中进行,容器体积不再发生变化时,反应达到平衡状态
B.若反应在恒容容器中进行,达到平衡后再向容器中充入一定量
 ,达到新平衡后,与原平衡相比,正反应速率增大,逆反应速率减小
,达到新平衡后,与原平衡相比,正反应速率增大,逆反应速率减小C.若反应在恒容容器中进行,达到平衡后,降低体系温度,达新平衡时,
 体积分数一定减小
体积分数一定减小D.若反应在恒压容器中进行,达到平衡后再向容器中充入一定量
 ,达新平衡时,
,达新平衡时, 比原平衡大
比原平衡大③在催化剂作用下,反应Ⅰ机理涉及如下过程(*代表催化剂吸附中心位点,
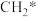 代表吸附态的
代表吸附态的 )
)(a):

(b):

(c):_______
(d):_______
(e)

分别写出过程(c)、(d)的反应式:
(c)
(d)
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】硫酸锌是制造锌钡白和锌盐的主要原料,也可用作木材的防腐剂等。用氧化锌烟尘(主要成分为 ZnO, 还含有少量 PbO、CuO、Fe2O3、FeO等)生产ZnSO4•7H2O的流程如下:
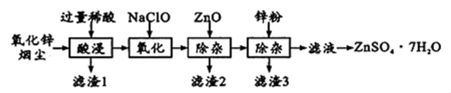
有关金属离子[ c( Mn+)=0.1mol / L ]形成氢氧化物沉淀的pH范围如下:
(1)“酸浸”时用的稀酸是_________ ;滤渣1的主要成分是______ 。
(2)“氧化”时的离子方程式为______ ;加入ZnO除杂时溶液的pH控制范围是___ ~5.0。
(3)滤渣3含有锌和___ 。
(4)取14.35gZnSO4•7H2O加热至不同温度,剩余固体的质量如下表:
则680°C时剩余固体的化学式为____ (填序号)。
A ZnO B Zn3O( SO4)2 C ZnSO4 D ZnSO4•H2O

有关金属离子[ c( Mn+)=0.1mol / L ]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cu2+ |
| 开始沉淀的pH | 1.5 | 6. 3 | 6.2 | 4.7 |
| 沉淀完全的pH | 2.8 | 8. 3 | 8.2 | 6.7 |
(1)“酸浸”时用的稀酸是
(2)“氧化”时的离子方程式为
(3)滤渣3含有锌和
(4)取14.35gZnSO4•7H2O加热至不同温度,剩余固体的质量如下表:
| 温度/℃ | 100 | 250 | 680 | 930 |
| 质量/g | 8.95 | 8.05 | 6.72 | 4.05 |
则680°C时剩余固体的化学式为
A ZnO B Zn3O( SO4)2 C ZnSO4 D ZnSO4•H2O
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】三氯化锑(SbCl3)用于红外光谱分析以及显像管生产等。工业生产中,以辉锑矿(主要成分为Sb2S3,还含有As2S3、PbS、CuO和SiO2等)为原料制备SbCl3的工艺流程如图:

已知:① 具有强氧化性,“浸出液”主要含盐酸和:
具有强氧化性,“浸出液”主要含盐酸和: ,还含
,还含 、
、 、
、 和
和 等杂质;
等杂质;
②常温下, ,
,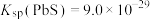 ;
;
③溶液中离子浓度小于或等于 时,认为该离子沉淀完全。
时,认为该离子沉淀完全。
回答下列问题:
(1)Cu位于元素周期表第
(2)“滤渣1”的主要成分有S和
(3)“浸出液”中加入适量Sb的目的是
(4)当
 、
、 共沉淀时,溶液中
共沉淀时,溶液中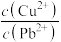 =
=(5)“除砷”时,氧化产物为
 ,则
,则 (可溶于水)与
(可溶于水)与 反应的离子方程式为
反应的离子方程式为(6)已知:“电解”
 溶液时有
溶液时有 生成。则上述流程中可循环利用的物质有
生成。则上述流程中可循环利用的物质有
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】几种主族元素在周期表中的位置如下:
根据上表回答下列问题:
(1)画出⑩的原子结构示意图:_______ 。
(2)④和⑨两种元素形成的化合物的电子式是_______ 。
(3)②、⑦、⑧三种元素离子半径由大到小的顺序是_______ (用离子符号表示)。
(4)由⑥、⑨组成的化合物分子中,⑥、⑨原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物和一种碱性气体,试写出该反应的化学方程式:_______ 。
(5)对于元素②与④,能说明②的金属性比④强的是_______(填标号)。
(6)由①、③、⑦组成的化合物中含有的化学键有_______ 。
(7)在含有①、④、⑤简单阳离子的 溶液中,逐滴滴加
溶液中,逐滴滴加 的
的 溶液到过量,生成沉淀的质量与加入的
溶液到过量,生成沉淀的质量与加入的 溶液的体积关系如图所示。由图中数据分析计算:
溶液的体积关系如图所示。由图中数据分析计算:
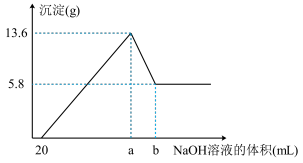
i.沉淀减少时发生的离子方程式:_______ 。
ii.a点的数值为_______  。
。
| 族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ② | ④ | ⑤ | ⑧ | ⑨ | |||
| 4 | ③ | ⑩ | ||||||
(1)画出⑩的原子结构示意图:
(2)④和⑨两种元素形成的化合物的电子式是
(3)②、⑦、⑧三种元素离子半径由大到小的顺序是
(4)由⑥、⑨组成的化合物分子中,⑥、⑨原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物和一种碱性气体,试写出该反应的化学方程式:
(5)对于元素②与④,能说明②的金属性比④强的是_______(填标号)。
A.②与 反应比④与 反应比④与 反应剧烈 反应剧烈 |
| B.②单质的熔、沸点比④的低 |
| C.②的最高价氧化物对应的水化物的碱性比④的最高价氧化物对应的水化物的碱性强 |
| D.与非金属单质反应时,②原子失电子数目比④原子失电子数目少 |
(7)在含有①、④、⑤简单阳离子的
 溶液中,逐滴滴加
溶液中,逐滴滴加 的
的 溶液到过量,生成沉淀的质量与加入的
溶液到过量,生成沉淀的质量与加入的 溶液的体积关系如图所示。由图中数据分析计算:
溶液的体积关系如图所示。由图中数据分析计算:
i.沉淀减少时发生的离子方程式:
ii.a点的数值为
 。
。
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】某固态结晶水合物 X 由 5 种元素组成。某学习小组进行了如下实验:
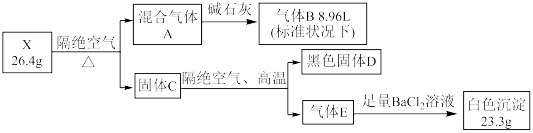
已知气体B能与 AgNO3 溶液反应, D中两种元素质量比为4:1 ,请回答:
(1)上述五种元素中,写出原子序数最大的元素在周期表中的位置___________
(2)气体 B 的实验方法是___________
(3)写出 X 在隔绝空气条件下加热,生成 A 、D 、E 的化学方程式:___________
(4)已知气体B和固体D加热时会发生反应,产物中有两种单质,当参加反应的 D 质量是1.2g时,所生成的两种单质的质量差为___________ g

已知气体B能与 AgNO3 溶液反应, D中两种元素质量比为4:1 ,请回答:
(1)上述五种元素中,写出原子序数最大的元素在周期表中的位置
(2)气体 B 的实验方法是
(3)写出 X 在隔绝空气条件下加热,生成 A 、D 、E 的化学方程式:
(4)已知气体B和固体D加热时会发生反应,产物中有两种单质,当参加反应的 D 质量是1.2g时,所生成的两种单质的质量差为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】已知A、B、C、D四种元素分别为短周期元素,表示中三个不同短周期的主族元素,且原子序数依次增
大。D原子的质子数是B原子质子数的2倍,A原子与D原子的最外层电子数之和是B原子与C原子质子
数之和的1/3。A与B可形成BA3型化合物,该化合物与C的单质在一定条件下反应,能生成化合物BC,请按要求填写下列空白:
(1)D元素的名称____________ ,C元素在元素周期表中的位置_____________ 。
(2)写出BA3的电子式____________ ,BA3跟C的单质在一定条件下反应,能生成化合物BC的化学方程式________________________________ 。
(3)D单质在工业上最重要的用途是_________ ,写出工业上制取D单质的化学方程式__________ 。
(4)在实验室中B的最高价氧化物的水化物的浓溶液应如何保存__________________ ,用化学方程
式说明理由____________________________________ 。
大。D原子的质子数是B原子质子数的2倍,A原子与D原子的最外层电子数之和是B原子与C原子质子
数之和的1/3。A与B可形成BA3型化合物,该化合物与C的单质在一定条件下反应,能生成化合物BC,请按要求填写下列空白:
(1)D元素的名称
(2)写出BA3的电子式
(3)D单质在工业上最重要的用途是
(4)在实验室中B的最高价氧化物的水化物的浓溶液应如何保存
式说明理由
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】非金属在生产、生活和科研中应用广泛。回答下列问题:
(1)基态 F 原子的电子排布式为_______ 。
(2)N2F2(二氟氮烯)分子中,氮原子的杂化类型为 sp2,则 N2F2 的结构式为_______ 。
(3)OF2 主要用于火箭工程液体助燃剂,其分子的空间构型为_______ ;OF2 的熔、沸点_______ Cl2O (填“高于”或“低于”),原因是_______ 。
(4)NO 、NO
、NO 、NO
、NO 的键角由大到小的顺序是
的键角由大到小的顺序是_______ 。
(5)碳酸亚乙酯( )是某锂离子电池电解液的添加剂,该物质能溶于水,请解释原因
)是某锂离子电池电解液的添加剂,该物质能溶于水,请解释原因_______ 。
(6)FeS2 晶体的晶胞结构如图所示。在晶胞中,Fe2+位于S 所形成的
所形成的_______ (填“正四面体”或 “正八面体”)空隙;若晶胞参数为 a nm,密度为ρg·cm −3 ,阿伏加德罗常数的值为NA ,则FeS2 的摩尔质量 M=_______  (用含 a、ρ、NA 的代数式表示)。
(用含 a、ρ、NA 的代数式表示)。

(1)基态 F 原子的电子排布式为
(2)N2F2(二氟氮烯)分子中,氮原子的杂化类型为 sp2,则 N2F2 的结构式为
(3)OF2 主要用于火箭工程液体助燃剂,其分子的空间构型为
(4)NO
 、NO
、NO 、NO
、NO 的键角由大到小的顺序是
的键角由大到小的顺序是(5)碳酸亚乙酯(
 )是某锂离子电池电解液的添加剂,该物质能溶于水,请解释原因
)是某锂离子电池电解液的添加剂,该物质能溶于水,请解释原因(6)FeS2 晶体的晶胞结构如图所示。在晶胞中,Fe2+位于S
 所形成的
所形成的 (用含 a、ρ、NA 的代数式表示)。
(用含 a、ρ、NA 的代数式表示)。 
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】点击化学的代表反应为铜催化的叠氮-炔基Husigen环加成反应,NaN3、SO2F2、FSO2N2等均是点击化学中常用无机试剂。回答下列问题:
(1)基态Cu原子价电子排布式为___________ ;基态N原子未成对电子有___________ 个。
(2)F、O、N的电负性从小到大的顺序是___________ 。
(3)SO2F2中硫原子价层电子对数目为___________ ;SO2F2的沸点比FSO2N3的低,其主要原因是___________ 。
(4)NaN3是HN3的钠盐,下列有关HN3说法正确的是___________ (填字母)。
a.HN3分子呈直线型 b.HN3分子间存在氢键
c.HN3中氮原子杂化方式只有sp d.HN3与HOCN互为等电子体
(5)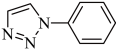 是一种叠氮-炔基Husigen环加成反应产物,每个该分子中含有
是一种叠氮-炔基Husigen环加成反应产物,每个该分子中含有___________ 个σ键。
(6)CuBr是点击化学常用的催化剂,其晶胞结构如图所示,晶胞参数为a pm。
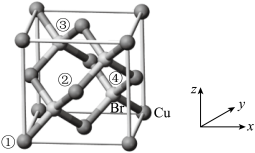
已知①、②号铜原子坐标依次为(0,0,0)、( ,0,
,0, ),则③号溴原子的坐标为
),则③号溴原子的坐标为___________ ;设NA为阿伏加德罗常数的值,CuBr的密度为___________ g·cm-3(列出计算式)。
(1)基态Cu原子价电子排布式为
(2)F、O、N的电负性从小到大的顺序是
(3)SO2F2中硫原子价层电子对数目为
(4)NaN3是HN3的钠盐,下列有关HN3说法正确的是
a.HN3分子呈直线型 b.HN3分子间存在氢键
c.HN3中氮原子杂化方式只有sp d.HN3与HOCN互为等电子体
(5)
 是一种叠氮-炔基Husigen环加成反应产物,每个该分子中含有
是一种叠氮-炔基Husigen环加成反应产物,每个该分子中含有(6)CuBr是点击化学常用的催化剂,其晶胞结构如图所示,晶胞参数为a pm。

已知①、②号铜原子坐标依次为(0,0,0)、(
 ,0,
,0, ),则③号溴原子的坐标为
),则③号溴原子的坐标为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素。M基态原子L层中p轨道电子数是s电子的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满。请回答下列问题:
(1)X原子的结构示意图为:___________ ,其核外电子运动状态共有___________ 种,Z的基态原子的价电子排布式为___________ 。
(2)写出M与R形成含有非极性键的离子化合物的电子式___________ 。
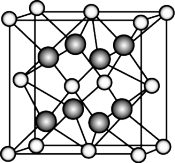
(3)M和R所形成的一种离子化合物晶体的晶胞如图所示,则该离子化合物的化学式是___________ ,该物质与水反应的化学方程式为:___________ 。
(4)在稀硫酸中,Z的最高价含氧酸的钾盐(K2Z2O7橙色)氧化M的一种氢化物,Z被还原为+3价,该反应的离子方程式是___________ 。
(1)X原子的结构示意图为:
(2)写出M与R形成含有非极性键的离子化合物的电子式
(3)M和R所形成的一种离子化合物晶体的晶胞如图所示,则该离子化合物的化学式是

(4)在稀硫酸中,Z的最高价含氧酸的钾盐(K2Z2O7橙色)氧化M的一种氢化物,Z被还原为+3价,该反应的离子方程式是
您最近一年使用:0次



