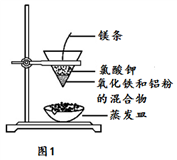

(1)按如图装置进行实验,可观察到反应剧烈,火星四射,漏斗下方有红热熔融物“铁块”流出。
该反应的化学方程式为

(2)某校化学兴趣小组同学,为了测定铝热反应后得到“铁块”混合物中铝的含量。取“铁块”样品研碎称得质量为x g,加入如图装置,再滴入足量NaOH溶液充分反应,测量生成气体体积为a ml(标况)。
①仪器A的名称为
②写出样品中Al与NaOH反应的化学方程式
③该小组同学改进实验,用恒压漏斗(如图)代替仪器A,其优点有
④该样品中铝的含量为
相似题推荐

(1)PAFC中铁元素的化合价为
(2)废料与稀盐酸混合后发生了多个化学反应,在发生的这些反应中,请写出一个是氧化还原反应但不属于四大基本反应类型的反应的离子方程式
(3)所得酸性溶液中,不能确定是否一定存在的阳离子是
(4)试剂X最好是下列中的
A.Fe B.HNO3 C.氯水 D.高锰酸钾溶液
(5)水解形成的聚合物分散在水中的粒子直径在1nm~100nm之间,请用简单的实验操作验证该分散系
Ⅱ.为检测PAFC中Al和Fe含量,采用如图所示流程进行。
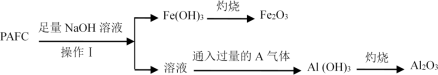
回答下列问题:
(6)操作I的名称
(7)通入过量的A气体的离子方程式为
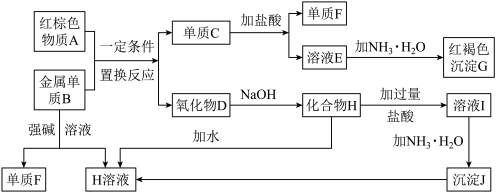
请回答下列问题:
(1)物质A的化学式为
(2)写出单质B与强碱溶液反应的离子方程式
(3)溶液E中加入氨水时,先生成白色沉淀L,L最终变为红褐色沉淀G,写出L变为G的化学反应方程式
(4)溶液E敞口放置容易变质,为了防止溶液E的变质,可往溶液中加入
(5)溶液I中所含金属离子是
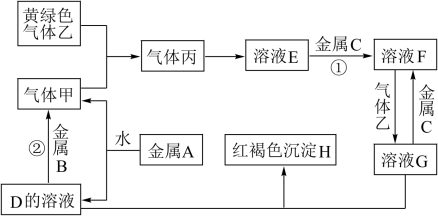
请根据以上信息回答下列问题
(1)写出下列物质的化学式:A
(2)写出下列反应的化学方程式:
反应①
反应②
(3)检测溶液G中金属离子的常用方法是:
(1)氨的催化氧化是制备硝酸的重要反应,实验中先用酒精喷灯加热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到
 以上。下列图示中,能够正确表示该反应过程能量变化的是
以上。下列图示中,能够正确表示该反应过程能量变化的是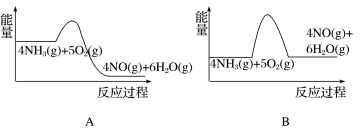
(2)在2L的温恒容密闭容器中,发生反应
 ,通入等物质的量的NO和O2气体,
,通入等物质的量的NO和O2气体,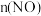 随时间的变化如下表:
随时间的变化如下表: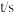 | 0 | 1 | 2 | 3 | 4 | 5 |
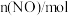 | 0.020 | 0.012 | 0.008 | 0.005 | 0.004 | 0.004 |
 内,
内,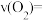
 。
。②某同学由数据推测,反应在第4s时恰好达到平衡状态。该推测
③在第5s时,O2的转化率为
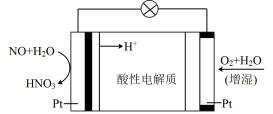
(3)一氧化氮-空气燃料电池将化学能转化为电能的同时,实现了制硝酸、发电、环保三位一体的结合,其工作原理如图所示,写出放电过程中正极的电极反应式:
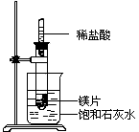
(1)实验中观察到的现象是
(2)写出有关反应的离子方程式
(3)由实验推知,MgCl2溶液和H2的总能量
II.(1)若将上述反应设计成原电池,用用稀盐酸作电解质溶液,铜为原电池的某一电极材料,则铜为原电池的
(2)将铁棒和锌片连接后浸入CuCl2溶液里,当电池中有0.2 mol电子通过时,正极电极反应式:
(3)氢氧燃料电池是常见的燃料电池,在电解质溶液是KOH溶液的负极反应为
(1)已知CH3OH(g)+
 O2(g) ⇌CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是
O2(g) ⇌CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是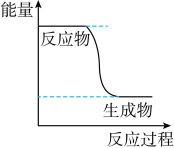
a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学变化不仅有新物质生成,同时也一定有能量变化
d.1 mol H—O键断裂的同时2 mol C=O键断裂,则反应达最大限度
(2)某温度下,将5 mol CH3OH和2 mol O2充入2 L的密闭容器中,经过4 min反应达到平衡,测得c(O2)=0.2 mol·L-1,4 min内平均反应速率v(H2)=
(3)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。则下列说法正确的是
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4 g CH3OH转移1.2 mol电子
(4)写出CH3OH燃料电池在酸性条件下负极的反应式
【推荐1】I、硼酸(H3BO3)大量应用于玻璃制造行业,以硼镁矿(2MgO·B2O3·H2O、SiO2及少量Fe3O4、CaCO3、Al2O3)为原料生产硼酸的工艺流程如下:

已知: H3BO3在20°C、40°C、60°C、100°C时溶解度依次为5.0g、8.7g、14.8g、40.2 g。
(1)浸出渣除了CaSO4外,还有
(2)“浸出液”显酸性,含H3BO3和Mg2+、SO , 还含有Fe3+、Fe2+、Ca2+、Al3+等杂质。“除杂”时向浸出液中依次加入适量H2O2和MgO, 除去的杂质离子是
, 还含有Fe3+、Fe2+、Ca2+、Al3+等杂质。“除杂”时向浸出液中依次加入适量H2O2和MgO, 除去的杂质离子是
(3)“浸取”后,采用“热过滤”的目的是
(4)以硼酸为原料可制得硼氢化钠(NaBH4)它是有机合成中的重要还原剂,其电子式为
II、为了分析矿石中铁元素的含量,先将浸出液处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式:5Fe2+ + MnO + 8H+= 5Fe3+ + Mn2+ + 4H2O
+ 8H+= 5Fe3+ + Mn2+ + 4H2O
(5)滴定前是否要滴加指示剂?
(6)达到滴定终点的标志是
(7)某同学称取4.000g样品,经处理后在容量瓶中配制成100mL溶液,移取25.00mL试样溶液,用1.000×10-2mol/L KMnO4标准溶液滴定。达到滴定终点时消耗标准溶液20.00 mL, 则样品中铁元素的质量分数是
 ,在有氧、光照的条件下易被氧化,维生素C含量的测定就是利用其较强的还原性,可以与具有氧化性的物质如,发生化学反应,把维生素C氧化生成去氢抗坏血酸。维生素C与碘单质的化学反应如下:
,在有氧、光照的条件下易被氧化,维生素C含量的测定就是利用其较强的还原性,可以与具有氧化性的物质如,发生化学反应,把维生素C氧化生成去氢抗坏血酸。维生素C与碘单质的化学反应如下: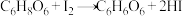 。
。某实验小组准确量取稀释过的市售饮料
 ,用已经标定的
,用已经标定的 的
的 溶液进行滴定,记录所用体积,平行滴定三次。消耗
溶液进行滴定,记录所用体积,平行滴定三次。消耗 溶液体积如下表所示:
溶液体积如下表所示:| 实验编号 | 待测溶液的体积( ) ) | 滴定前 溶液读数( 溶液读数( ) ) | 滴定后 溶液读数( 溶液读数( ) ) |
| 1 | 10.00 | 1.20 | 13.22 |
| 2 | 10.00 | 1.21 | 13.19 |
| 3 | 10.00 | 2.00 | 14.00 |
(1)标准
 溶液应装入
溶液应装入(2)如图表示某次放液后
 滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积___________(填字母)。
滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积___________(填字母)。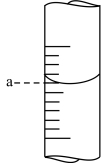
A. | B.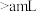 | C.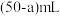 | D.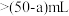 |
(4)该市售饮料维生素C的浓度为
 。
。(5)其他操作均正确,下列操作会导致维生素C测定结果偏低的是
A.锥形瓶中有少量水
B.盛装标准液的滴定管用蒸馏水清洗后未用标准液润洗
C.滴定结束时仰视刻度线读数
D.量取待测液的滴定管没有润洗
E.滴定后盛装标准液的滴定管中有气泡
(2) 由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是
(3)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I―发生反应的氧化性质杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL(已知:I2+2
 =
= +2I―)
+2I―)①可选用
②CuCl2溶液与KI反应的离子方程式为
③该试样中CuCl2•2H2O的质量百分数为
④如果试样是液体,用移液管移取时,下列使用正确的是