氯及其化合物在生活和生产中应用广泛。
(1)已知:900 K时,4HCl(g)+O2(g) 2Cl2(g)+2H2O(g),反应自发。
2Cl2(g)+2H2O(g),反应自发。
①该反应是放热还是吸热,判断并说明理由___________________________ 。
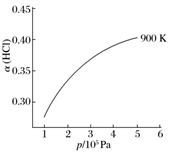
②900 K时,体积比为4∶1的HCl和O2在恒温恒容的密闭容器中发生反应,HCl的平衡转化率α(HCl)随压强(p)变化曲线如图。保持其他条件不变,升温到T K(假定反应历程不变),请画出压强在1.5×105~4.5 ×105Pa范围内,HCl的平衡转化率α(HCl)随压强(p)变化曲线示意图。
×105Pa范围内,HCl的平衡转化率α(HCl)随压强(p)变化曲线示意图。_____________________
(2)已知:Cl2(g)+2NaOH(aq)===NaCl(aq)+NaClO(aq)+H2O(l) ΔHl=-102 kJ·mol-1
3Cl2(g)+6NaOH(aq)===5NaCl(aq)+NaClO3(aq)+3H2O(l) ΔH2=-422 kJ·mol-1
①写出在溶液中NaClO分解生成NaClO3的热化学方程式:________________________________ 。
②用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不含NaClO3),此时ClO-的浓度为c0 mol·L-1;加热时NaClO转化为NaClO3,测得t时刻溶液中ClO-浓度为ct mol·L-1,写出该时刻溶液中Cl-浓度的表达式:c(Cl-)=________________ (用c0、ct表示)mol·L-1。
③有研究表明,生成NaClO3的反应分两步进行:
Ⅰ.2ClO-===ClO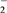 + Cl-
+ Cl-
Ⅱ.ClO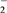 +ClO-===ClO
+ClO-===ClO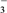 +Cl-
+Cl-
常温下,反应Ⅱ能快速进行,但氯气与NaOH溶液反应很难得到NaClO3,试用碰撞理论解释其原因:______________________________________________________ 。
(1)已知:900 K时,4HCl(g)+O2(g)
 2Cl2(g)+2H2O(g),反应自发。
2Cl2(g)+2H2O(g),反应自发。①该反应是放热还是吸热,判断并说明理由
②900 K时,体积比为4∶1的HCl和O2在恒温恒容的密闭容器中发生反应,HCl的平衡转化率α(HCl)随压强(p)变化曲线如图。保持其他条件不变,升温到T K(假定反应历程不变),请画出压强在1.5×105~4.5
 ×105Pa范围内,HCl的平衡转化率α(HCl)随压强(p)变化曲线示意图。
×105Pa范围内,HCl的平衡转化率α(HCl)随压强(p)变化曲线示意图。
(2)已知:Cl2(g)+2NaOH(aq)===NaCl(aq)+NaClO(aq)+H2O(l) ΔHl=-102 kJ·mol-1
3Cl2(g)+6NaOH(aq)===5NaCl(aq)+NaClO3(aq)+3H2O(l) ΔH2=-422 kJ·mol-1
①写出在溶液中NaClO分解生成NaClO3的热化学方程式:
②用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不含NaClO3),此时ClO-的浓度为c0 mol·L-1;加热时NaClO转化为NaClO3,测得t时刻溶液中ClO-浓度为ct mol·L-1,写出该时刻溶液中Cl-浓度的表达式:c(Cl-)=
③有研究表明,生成NaClO3的反应分两步进行:
Ⅰ.2ClO-===ClO
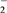 + Cl-
+ Cl-Ⅱ.ClO
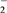 +ClO-===ClO
+ClO-===ClO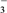 +Cl-
+Cl-常温下,反应Ⅱ能快速进行,但氯气与NaOH溶液反应很难得到NaClO3,试用碰撞理论解释其原因:
更新时间:2017-08-13 07:40:43
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】研究氮氧化物(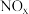 )的还原处理方法是环保领域的主要方向之一,回答下列问题:
)的还原处理方法是环保领域的主要方向之一,回答下列问题:
(1)CO还原NO的反应机理及相对能量如图(TS表示过渡态):
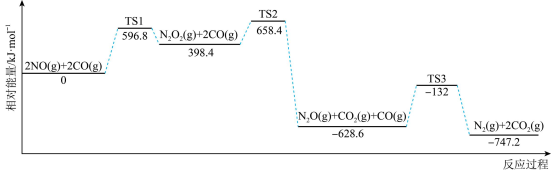
①反应过程中速率最慢步骤的热化学方程式为_______ ,活化能最小
_______  。
。
②为提高NO的平衡转化率可采用的措施为_______ (填标号)。
A.升高温度 B.增大压强 C.增大NO浓度 D.使用催化剂
(2)用 还原NO的反应为
还原NO的反应为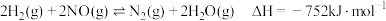 。为研究
。为研究 和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为a L的刚性密闭容器中加入一定量
和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为a L的刚性密闭容器中加入一定量 和NO发生反应,实验结果如图。
和NO发生反应,实验结果如图。
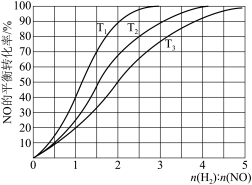
①应温度 、
、 、
、 从大到小的关系为
从大到小的关系为_______ 。
② 温度下,充入
温度下,充入 、NO分别为3mol、3mol,容器内的压强为w Pa,反应进行到10min时达平衡,0~10min内
、NO分别为3mol、3mol,容器内的压强为w Pa,反应进行到10min时达平衡,0~10min内 的平均反应速率为
的平均反应速率为_______ 。该反应的平衡常数
_______ 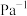 (写出计算表达式,以分压表示的平衡常数为
(写出计算表达式,以分压表示的平衡常数为 ,分压=总压×物质的量分数)。
,分压=总压×物质的量分数)。
③该反应的正反应速率方程可表示为 ,
, 下测得有关数据如下表:
下测得有关数据如下表:
则
_______ ,
_______ 。
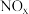 )的还原处理方法是环保领域的主要方向之一,回答下列问题:
)的还原处理方法是环保领域的主要方向之一,回答下列问题:(1)CO还原NO的反应机理及相对能量如图(TS表示过渡态):

①反应过程中速率最慢步骤的热化学方程式为

 。
。②为提高NO的平衡转化率可采用的措施为
A.升高温度 B.增大压强 C.增大NO浓度 D.使用催化剂
(2)用
 还原NO的反应为
还原NO的反应为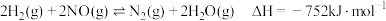 。为研究
。为研究 和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为a L的刚性密闭容器中加入一定量
和NO的起始投料比对NO平衡转化率的影响,分别在不同温度下,向三个体积均为a L的刚性密闭容器中加入一定量 和NO发生反应,实验结果如图。
和NO发生反应,实验结果如图。
①应温度
 、
、 、
、 从大到小的关系为
从大到小的关系为②
 温度下,充入
温度下,充入 、NO分别为3mol、3mol,容器内的压强为w Pa,反应进行到10min时达平衡,0~10min内
、NO分别为3mol、3mol,容器内的压强为w Pa,反应进行到10min时达平衡,0~10min内 的平均反应速率为
的平均反应速率为
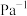 (写出计算表达式,以分压表示的平衡常数为
(写出计算表达式,以分压表示的平衡常数为 ,分压=总压×物质的量分数)。
,分压=总压×物质的量分数)。③该反应的正反应速率方程可表示为
 ,
, 下测得有关数据如下表:
下测得有关数据如下表:| NO/mol | 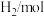 | v正/mol·L-1·min-1 |
| 1 | 1 | 4.14k |
| 1 | 4 | 16.56k |
| 2 | 1 | 16.56k |


您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】二氧化锰是化学工业中常用的氧化剂和催化剂。我国主要以贫菱锰矿(有效成分为 )为原料,通过热解法进行生产。
)为原料,通过热解法进行生产。
(1)碳酸锰热解制二氧化锰分两步进行:
i.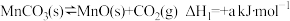
ii.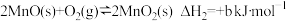
①反应i的化学平衡常数表达式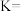
___________ 。
②焙烧 制取
制取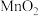 的热化学方程式是
的热化学方程式是_________________ 。
(2)焙烧(装置如图1)时持续通入空气,并不断抽气的目的是________________ 。
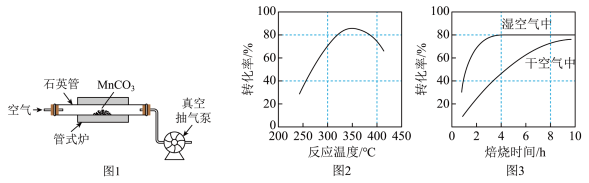
(3)在其他条件不变时,某科研团队对影响 转化率的生产条件进行了研究,结果如图2、图3所示。
转化率的生产条件进行了研究,结果如图2、图3所示。
①图2是在常压(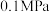 )下的研究结果,请在图2中用虚线画出
)下的研究结果,请在图2中用虚线画出 下
下 转化率与反应温度的关系图
转化率与反应温度的关系图______ 。
②常压下,要提高 的转化率,应选择的生产条件是
的转化率,应选择的生产条件是____________ 焙烧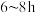 。
。
③图3中,焙烧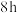 时,
时, 的转化率:干空气<湿空气,原因是
的转化率:干空气<湿空气,原因是______________ 。
 )为原料,通过热解法进行生产。
)为原料,通过热解法进行生产。(1)碳酸锰热解制二氧化锰分两步进行:
i.
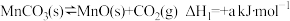
ii.
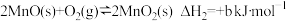
①反应i的化学平衡常数表达式
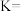
②焙烧
 制取
制取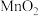 的热化学方程式是
的热化学方程式是(2)焙烧(装置如图1)时持续通入空气,并不断抽气的目的是

(3)在其他条件不变时,某科研团队对影响
 转化率的生产条件进行了研究,结果如图2、图3所示。
转化率的生产条件进行了研究,结果如图2、图3所示。①图2是在常压(
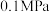 )下的研究结果,请在图2中用虚线画出
)下的研究结果,请在图2中用虚线画出 下
下 转化率与反应温度的关系图
转化率与反应温度的关系图②常压下,要提高
 的转化率,应选择的生产条件是
的转化率,应选择的生产条件是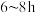 。
。③图3中,焙烧
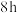 时,
时, 的转化率:干空气<湿空气,原因是
的转化率:干空气<湿空气,原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】氨气在工农业生产和国防科技中有着重要应用,科研工作者对其进行者广泛研究。回答:
(1)某课题组实现了在常湿常压下,以氮气和液态水为原料制备氨气同时有氧气生成。
已知,在一定温度和压强下,由最稳定的单质生成1mol纯物质的热效应,称为该物质的生成热(△H)。常温常压下、相关物质的生成热如下表所示:
上述合成氨反应的热化学方程式为______________________ 。
(2)利用生物电池,以H2、N2为原料合成氨的装置如下图所示。
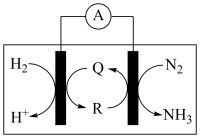
Q、R均为催化剂,据到示判断,负极反应的催化剂为___ (填“Q”或“R”);正极的电极反应式为_______________ 。
(3)氨气是工业制硝酸的主要原料之一,催化氧化步骤中发生的主要反应如下:
I.4NH3(g)+5O2(g) 4NO(g)+6H2O(g)△H=-906kJ/mol
4NO(g)+6H2O(g)△H=-906kJ/mol
II.4NH3(g)+3O2(g) 2N2(g)+ 6H2O(g)△H=-126kJ/mol
2N2(g)+ 6H2O(g)△H=-126kJ/mol
将固定比例NH3和O2的混合气体以一定流速通过填充有催化剂的反应器,反应产率与温度的关系如图1所示。
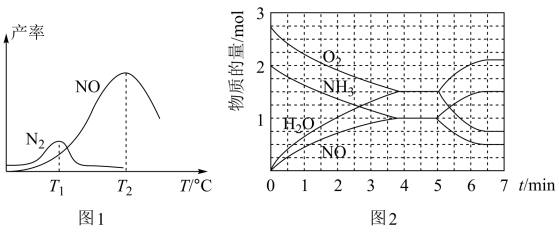
①催化氧化步骤中,最适宜的温度为____ (填“T1”或“T2”)。
②低于T1℃时,NO的产率较低的原因为_____ 。
③高于T2℃时,NO的产率降低的可能原因为_____ (填选项字母)
A.催化剂活性降低 B.平衡常数减小 C.反应活化能增大 D.氨气溶于水
④T2℃(T1>T2)时,向20L恒容密闭容器中充入2molNH3和2.75molO2,发生反应I.反应过程中各物质的物质的量的随时间(t)变化关系如图2所示。T2℃时,该反应的平衡常数K=_____ ;5min时,改变了某一外界条件,所改变的条件可能为__________ 。
(1)某课题组实现了在常湿常压下,以氮气和液态水为原料制备氨气同时有氧气生成。
已知,在一定温度和压强下,由最稳定的单质生成1mol纯物质的热效应,称为该物质的生成热(△H)。常温常压下、相关物质的生成热如下表所示:
| 物质 | NH3(s) | H20(1) |
| △H/ kJ·mol-1 | -46 | -242 |
上述合成氨反应的热化学方程式为
(2)利用生物电池,以H2、N2为原料合成氨的装置如下图所示。

Q、R均为催化剂,据到示判断,负极反应的催化剂为
(3)氨气是工业制硝酸的主要原料之一,催化氧化步骤中发生的主要反应如下:
I.4NH3(g)+5O2(g)
 4NO(g)+6H2O(g)△H=-906kJ/mol
4NO(g)+6H2O(g)△H=-906kJ/molII.4NH3(g)+3O2(g)
 2N2(g)+ 6H2O(g)△H=-126kJ/mol
2N2(g)+ 6H2O(g)△H=-126kJ/mol将固定比例NH3和O2的混合气体以一定流速通过填充有催化剂的反应器,反应产率与温度的关系如图1所示。

①催化氧化步骤中,最适宜的温度为
②低于T1℃时,NO的产率较低的原因为
③高于T2℃时,NO的产率降低的可能原因为
A.催化剂活性降低 B.平衡常数减小 C.反应活化能增大 D.氨气溶于水
④T2℃(T1>T2)时,向20L恒容密闭容器中充入2molNH3和2.75molO2,发生反应I.反应过程中各物质的物质的量的随时间(t)变化关系如图2所示。T2℃时,该反应的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】二十大报告提出坚决深入推进环境污染防治。氮氧化物是大气污染物之一,消除氮氧化物的污染是重要的科研目的之一。
(1)NH3可用于消除氮氧化物污染,反应原理为6NO(g)+4NH3(g) 6H2O(g)+5N2(g) ΔH1
6H2O(g)+5N2(g) ΔH1
已知:N2(g)+O2(g) 2NO(g) ΔH2=+180.4kJ·mol-1
2NO(g) ΔH2=+180.4kJ·mol-1
4NH3(g)+5O2(g) 6H2O(g)+4NO(g) ΔH3=-905.8kJ·mol-1则
6H2O(g)+4NO(g) ΔH3=-905.8kJ·mol-1则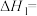
_______ kJ·mol-1
(2)对比研究活性炭、负载钙、镧氧化物的反应活性。在三个反应器中分别加入C、CaO/C、La2O3/C,通入相同浓度的NO,不同温度下测得反应2h时NO去除率如图1所示。
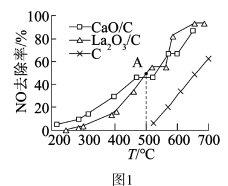
据图分析,温度在500°C以内,三种情况下反应的活化能最小的是_______ (填“C”、“CaO/C”或“La2O3/C”)。A点_______ (填“是”或“不是”)平衡点,原因是_______ 。
(3)在一定条件下,可用CO还原NO消除氮氧化物造成的污染。某温度下,若向2L体积恒定的密闭容器中充入1molCO和9mol汽车尾气(主要成分为NO和N2,其中NO的体积分数为10%)发生反应:2NO(g)+2CO(g) 2CO2(g)+N2(g),10min时反应达到平衡,此时CO的转化率为50%。
2CO2(g)+N2(g),10min时反应达到平衡,此时CO的转化率为50%。
①0~10min内,v(NO)=_______ mol·L-1·min-l。
②平衡时,体系压强为9.75MPa,则Kp=_______ (保留一位小数)。
(4)T°C时,2NO2(g) N2O4(g),该反应正、逆反应速率与浓度的关系为v正=k正c2(NO2),v逆=k逆c(N2O4)(k正、k逆为速率常数),lgv与lgc的关系如图2所示。
N2O4(g),该反应正、逆反应速率与浓度的关系为v正=k正c2(NO2),v逆=k逆c(N2O4)(k正、k逆为速率常数),lgv与lgc的关系如图2所示。

①图2中表示lgv正~lgc(NO2)的线是_______ (填“m”或“n”)。
②T°C时,向刚性容器中充入一定量NO2气体,平衡后测得c(N2O4)为1mol·L-1,则平衡时,v正=_______ (用含a的表达式表示)。
③T°C时,向2L的容器中充入5molN2O4气体和1molNO2气体,此时v正_______ (填“<”“<”或“=”)v逆。
(1)NH3可用于消除氮氧化物污染,反应原理为6NO(g)+4NH3(g)
 6H2O(g)+5N2(g) ΔH1
6H2O(g)+5N2(g) ΔH1已知:N2(g)+O2(g)
 2NO(g) ΔH2=+180.4kJ·mol-1
2NO(g) ΔH2=+180.4kJ·mol-14NH3(g)+5O2(g)
 6H2O(g)+4NO(g) ΔH3=-905.8kJ·mol-1则
6H2O(g)+4NO(g) ΔH3=-905.8kJ·mol-1则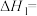
(2)对比研究活性炭、负载钙、镧氧化物的反应活性。在三个反应器中分别加入C、CaO/C、La2O3/C,通入相同浓度的NO,不同温度下测得反应2h时NO去除率如图1所示。

据图分析,温度在500°C以内,三种情况下反应的活化能最小的是
(3)在一定条件下,可用CO还原NO消除氮氧化物造成的污染。某温度下,若向2L体积恒定的密闭容器中充入1molCO和9mol汽车尾气(主要成分为NO和N2,其中NO的体积分数为10%)发生反应:2NO(g)+2CO(g)
 2CO2(g)+N2(g),10min时反应达到平衡,此时CO的转化率为50%。
2CO2(g)+N2(g),10min时反应达到平衡,此时CO的转化率为50%。①0~10min内,v(NO)=
②平衡时,体系压强为9.75MPa,则Kp=
(4)T°C时,2NO2(g)
 N2O4(g),该反应正、逆反应速率与浓度的关系为v正=k正c2(NO2),v逆=k逆c(N2O4)(k正、k逆为速率常数),lgv与lgc的关系如图2所示。
N2O4(g),该反应正、逆反应速率与浓度的关系为v正=k正c2(NO2),v逆=k逆c(N2O4)(k正、k逆为速率常数),lgv与lgc的关系如图2所示。
①图2中表示lgv正~lgc(NO2)的线是
②T°C时,向刚性容器中充入一定量NO2气体,平衡后测得c(N2O4)为1mol·L-1,则平衡时,v正=
③T°C时,向2L的容器中充入5molN2O4气体和1molNO2气体,此时v正
您最近一年使用:0次
【推荐2】氯及其化合物在生产、生活中广泛应用。
(1)三氯乙醛常用于制造农药。化学反应原理是4Cl2(g)+C2H5OH(g) CCl3CHO(g)+5HCl(g)。一定温度下,在某恒容密闭容器中充入4molCl2和2molC2H5OH(g),发生上述反应。下列叙述正确的是_____
CCl3CHO(g)+5HCl(g)。一定温度下,在某恒容密闭容器中充入4molCl2和2molC2H5OH(g),发生上述反应。下列叙述正确的是_____
(2)SCl4是一种化工产品。已知有关反应如下:
①2S(1)+Cl2(g)=S2Cl2(1) ΔH1=akJ·mol-1
②S2C12(1)+Cl2(g)=2SCl2(1) ΔH2=bkJ·mol-1
③SC12(1)+Cl2(g)=SCl4(1) ΔH3=ckJ·mol-1
④S(1)+2Cl2(g)=SCl4(l) ΔH4=_____ kJ·mol-1(用含a、b和c的式子表示)。
(3)工业上,曾用催化氧化氯化氢法(俗称地康法)制备氯气:
4HCl(g)+O2(g)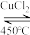 2Cl2(g)+2H2O(g) ΔH
2Cl2(g)+2H2O(g) ΔH
从化学反应原理角度分析,一定条件下,投料比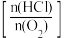 是提高HCl平衡转化率和反应速率以及提纯氯气的关键条件。若投料比太小,有利的是
是提高HCl平衡转化率和反应速率以及提纯氯气的关键条件。若投料比太小,有利的是_____ ;不利的是_____ 。
(4)已知Arrhenius经验公式为Rlnk=- +C(Ea为活化能,k为速率常数,R和C为常数,活化能不随温度变化)。为了探究催化剂对地康法制氯气的影响,某小组选择ZnCl2、CuCl2为催化剂,探究其对氯化氢催化氧化反应的影响,实验结果如图1所示。
+C(Ea为活化能,k为速率常数,R和C为常数,活化能不随温度变化)。为了探究催化剂对地康法制氯气的影响,某小组选择ZnCl2、CuCl2为催化剂,探究其对氯化氢催化氧化反应的影响,实验结果如图1所示。
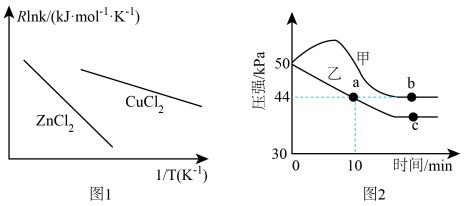
从图1中信息获知催化效能较低的催化剂是_____ (填化学式),其理由是_____ 。
(5)在体积相同的甲、乙两个密闭容器中充入4molHCl(g)和1molO2(g),分别在恒容恒温、恒容绝热条件下发生反应:4HCl(g)+O2(g)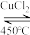 2Cl2(g)+2H2O(g)ΔH,测得气体压强变化与时间关系如图2所示。
2Cl2(g)+2H2O(g)ΔH,测得气体压强变化与时间关系如图2所示。
①气体总物质的量:n(a)______ n(b)(填“>”“<”或“=”,下同)。
②a点Qp=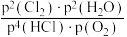 =
=_____ (kPa)-1(结果保留2位小数)。b点Kp_____ a点Qp。
(1)三氯乙醛常用于制造农药。化学反应原理是4Cl2(g)+C2H5OH(g)
 CCl3CHO(g)+5HCl(g)。一定温度下,在某恒容密闭容器中充入4molCl2和2molC2H5OH(g),发生上述反应。下列叙述正确的是_____
CCl3CHO(g)+5HCl(g)。一定温度下,在某恒容密闭容器中充入4molCl2和2molC2H5OH(g),发生上述反应。下列叙述正确的是_____| A.混合气体平均摩尔质量不变时达到平衡状态 |
| B.平衡后再充入少量Cl2反应正向进行 |
| C.加入高效催化剂,能提高氯气的平衡产率 |
| D.平衡时三氯乙醛体积分数可能等于15% |
①2S(1)+Cl2(g)=S2Cl2(1) ΔH1=akJ·mol-1
②S2C12(1)+Cl2(g)=2SCl2(1) ΔH2=bkJ·mol-1
③SC12(1)+Cl2(g)=SCl4(1) ΔH3=ckJ·mol-1
④S(1)+2Cl2(g)=SCl4(l) ΔH4=
(3)工业上,曾用催化氧化氯化氢法(俗称地康法)制备氯气:
4HCl(g)+O2(g)
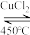 2Cl2(g)+2H2O(g) ΔH
2Cl2(g)+2H2O(g) ΔH从化学反应原理角度分析,一定条件下,投料比
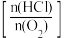 是提高HCl平衡转化率和反应速率以及提纯氯气的关键条件。若投料比太小,有利的是
是提高HCl平衡转化率和反应速率以及提纯氯气的关键条件。若投料比太小,有利的是(4)已知Arrhenius经验公式为Rlnk=-
 +C(Ea为活化能,k为速率常数,R和C为常数,活化能不随温度变化)。为了探究催化剂对地康法制氯气的影响,某小组选择ZnCl2、CuCl2为催化剂,探究其对氯化氢催化氧化反应的影响,实验结果如图1所示。
+C(Ea为活化能,k为速率常数,R和C为常数,活化能不随温度变化)。为了探究催化剂对地康法制氯气的影响,某小组选择ZnCl2、CuCl2为催化剂,探究其对氯化氢催化氧化反应的影响,实验结果如图1所示。
从图1中信息获知催化效能较低的催化剂是
(5)在体积相同的甲、乙两个密闭容器中充入4molHCl(g)和1molO2(g),分别在恒容恒温、恒容绝热条件下发生反应:4HCl(g)+O2(g)
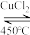 2Cl2(g)+2H2O(g)ΔH,测得气体压强变化与时间关系如图2所示。
2Cl2(g)+2H2O(g)ΔH,测得气体压强变化与时间关系如图2所示。①气体总物质的量:n(a)_
②a点Qp=
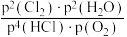 =
=
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如图:

(1)反应I:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551kJ/mol
反应III:S(s)+O2(g)=SO2(g) ΔH2=-297kJ/mol
写出反应II的热化学方程式:____ 。
(2)I-可作为水溶液中SO2歧化反应的催化剂(可能的催化过程如下。写出反应ii的离子方程式:i.SO2+4I-+4H+=S↓+2I2+2H2O;ii.____ 。
(3)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18mLSO2饱和溶液加入到2mL下列试剂中,密闭放置观察现象。已知:I2易溶解在KI溶液中。
①A是B的对照实验,则a=____ 。
②比较A、B、C实验现象可知:H+____ (填“是”或“不是”)SO2歧化反应的催化剂。
③实验表明,SO2的歧化反应速率D>A,结合i、ii的反应速率解释原因____ 。

(1)反应I:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551kJ/mol
反应III:S(s)+O2(g)=SO2(g) ΔH2=-297kJ/mol
写出反应II的热化学方程式:
(2)I-可作为水溶液中SO2歧化反应的催化剂(可能的催化过程如下。写出反应ii的离子方程式:i.SO2+4I-+4H+=S↓+2I2+2H2O;ii.
(3)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18mLSO2饱和溶液加入到2mL下列试剂中,密闭放置观察现象。已知:I2易溶解在KI溶液中。
| A | B | C | D | |
| 试剂组成 | 0.4mol·L-1KI | amol·L-1KI 0.2mol·L-1H2SO4 | 0.2mol·L-1H2SO4 | 0.2mol·L-1KI 0.0002molI2 |
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
②比较A、B、C实验现象可知:H+
③实验表明,SO2的歧化反应速率D>A,结合i、ii的反应速率解释原因
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】十九大报告提出要对环境问题进行全面、系统的可持续治理,绿色能源是实施可持续发展的重要途径,利用生物乙醇来制取绿色能源氢气的部分反应过程如图所示:

(1)已知反应Ⅰ.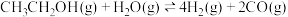
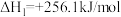
反应Ⅱ.
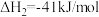
写出反应Ⅲ的热化学方程式_______ 。
(2)反应Ⅱ,在进气比 不同时,测得相应的
不同时,测得相应的 平衡转化率见图(各点对应的反应温度可能相同,也可能不同;各点对应的其他反应条件都相同)。
平衡转化率见图(各点对应的反应温度可能相同,也可能不同;各点对应的其他反应条件都相同)。

①A、E和G三点对应的反应温度相同,反应在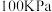 的压强下进行,则G点的
的压强下进行,则G点的
_______ (填数值),图中温度最高的点是_______ 。
②C、D两点对应的正反应速率: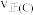
_______ 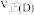 (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。已知反应速率
”)。已知反应速率 ,k为反应速率常数,x为物质的量分数,计算在达到平衡状态为C点的反应过程中,当
,k为反应速率常数,x为物质的量分数,计算在达到平衡状态为C点的反应过程中,当 转化率刚好达到20%时,
转化率刚好达到20%时,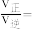
_______ 。
(3)工业上采用催化乙烯水合制乙醇,该反应过程中能量变化如图所示:
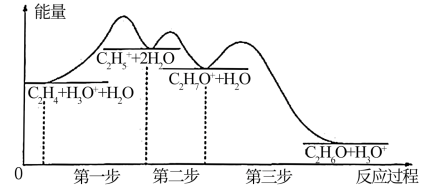
①反应过程中的控制总反应速率的步骤是_______ ,理由为_______ 。
②反应物分子有效碰撞几率最大的步骤是_______ ,对应的基元反应为_______ 。

(1)已知反应Ⅰ.
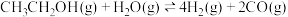
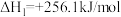
反应Ⅱ.

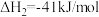
写出反应Ⅲ的热化学方程式
(2)反应Ⅱ,在进气比
 不同时,测得相应的
不同时,测得相应的 平衡转化率见图(各点对应的反应温度可能相同,也可能不同;各点对应的其他反应条件都相同)。
平衡转化率见图(各点对应的反应温度可能相同,也可能不同;各点对应的其他反应条件都相同)。
①A、E和G三点对应的反应温度相同,反应在
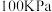 的压强下进行,则G点的
的压强下进行,则G点的
②C、D两点对应的正反应速率:
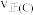
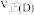 (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。已知反应速率
”)。已知反应速率 ,k为反应速率常数,x为物质的量分数,计算在达到平衡状态为C点的反应过程中,当
,k为反应速率常数,x为物质的量分数,计算在达到平衡状态为C点的反应过程中,当 转化率刚好达到20%时,
转化率刚好达到20%时,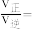
(3)工业上采用催化乙烯水合制乙醇,该反应过程中能量变化如图所示:

①反应过程中的控制总反应速率的步骤是
②反应物分子有效碰撞几率最大的步骤是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】乙酸是基本的有机化工原料,乙酸制氢具有重要意义,制氢过程发生如下反应:
热裂解反应Ⅰ: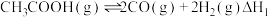
脱羧基反应Ⅱ: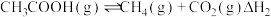
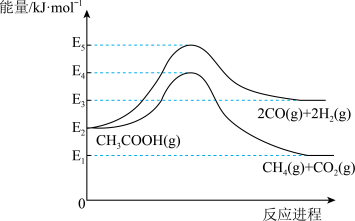
(1)由图可知,
_____  '(用有关E的代数式表示);反应Ⅰ的活化能
'(用有关E的代数式表示);反应Ⅰ的活化能_____ (填“>”或“<”)反应Ⅱ的活化能。
(2)在恒容密闭容器中,加入一定量乙酸蒸气制氢,在相同时间测得温度与气体产率的关系如图:
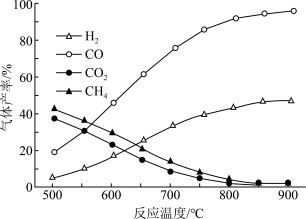
①约650℃之前,氢气产率低于甲烷的原因是_____ 。
②分析图像知该容器中还发生了其他的副反应,理由是_____ 。
③若保持其他条件不变,在乙酸蒸气中掺杂一定量水,氢气的产率显著提高,而CO的产率下降,请用化学方程式表示可能发生的反应:_____ 。
(3)若利用合适的催化剂发生热裂解反应Ⅰ和脱羧基反应Ⅱ,温度为TK时达到平衡,总压强为 ,乙酸体积分数为20%,其中热裂解反应Ⅰ消耗的乙酸占投入量的20%,脱羧基反应Ⅱ的平衡常数
,乙酸体积分数为20%,其中热裂解反应Ⅰ消耗的乙酸占投入量的20%,脱羧基反应Ⅱ的平衡常数 为
为_____  (
( 为以分压表示的平衡常数)。
为以分压表示的平衡常数)。
(4)工业上通常用甲醇与CO反应来制备乙酸,反应如下: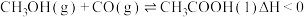 ,在恒压密闭容器中通入
,在恒压密闭容器中通入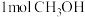 气体和
气体和 CO气体,
CO气体, 时测得甲醇的转化率随温度的变化如图:
时测得甲醇的转化率随温度的变化如图:
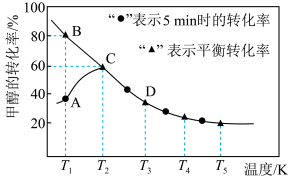
①温度为 时,
时,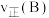
_____ (填“>”“=”或“<”)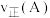 。
。
②温度为 时,上述反应已达平衡后,保持压强不变,再通入
时,上述反应已达平衡后,保持压强不变,再通入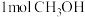 和
和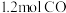 的混合气体,再次达到平衡时,CO的转化率
的混合气体,再次达到平衡时,CO的转化率_____ (填“>”“=”或“<”)60%。
热裂解反应Ⅰ:
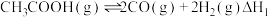
脱羧基反应Ⅱ:
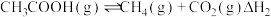
(1)由图可知,

 '(用有关E的代数式表示);反应Ⅰ的活化能
'(用有关E的代数式表示);反应Ⅰ的活化能
(2)在恒容密闭容器中,加入一定量乙酸蒸气制氢,在相同时间测得温度与气体产率的关系如图:

①约650℃之前,氢气产率低于甲烷的原因是
②分析图像知该容器中还发生了其他的副反应,理由是
③若保持其他条件不变,在乙酸蒸气中掺杂一定量水,氢气的产率显著提高,而CO的产率下降,请用化学方程式表示可能发生的反应:
(3)若利用合适的催化剂发生热裂解反应Ⅰ和脱羧基反应Ⅱ,温度为TK时达到平衡,总压强为
 ,乙酸体积分数为20%,其中热裂解反应Ⅰ消耗的乙酸占投入量的20%,脱羧基反应Ⅱ的平衡常数
,乙酸体积分数为20%,其中热裂解反应Ⅰ消耗的乙酸占投入量的20%,脱羧基反应Ⅱ的平衡常数 为
为 (
( 为以分压表示的平衡常数)。
为以分压表示的平衡常数)。(4)工业上通常用甲醇与CO反应来制备乙酸,反应如下:
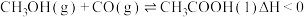 ,在恒压密闭容器中通入
,在恒压密闭容器中通入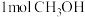 气体和
气体和 CO气体,
CO气体, 时测得甲醇的转化率随温度的变化如图:
时测得甲醇的转化率随温度的变化如图:
①温度为
 时,
时,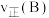
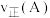 。
。②温度为
 时,上述反应已达平衡后,保持压强不变,再通入
时,上述反应已达平衡后,保持压强不变,再通入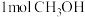 和
和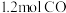 的混合气体,再次达到平衡时,CO的转化率
的混合气体,再次达到平衡时,CO的转化率
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】工业合成氨是人类科学技术的重大突破,其反应为
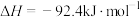 。合成氨原料中的
。合成氨原料中的 一般由分馏液态空气得到,
一般由分馏液态空气得到, 可来源于水煤气,相关反应如下:
可来源于水煤气,相关反应如下:
a.
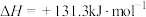
b.
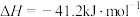
回答下列问题:
(1)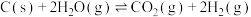 的反应物总能量
的反应物总能量_______ 生成物总能量(填“高于”或“低于”)。
(2)在密闭容器中同时发生反应 ,下列说法正确的是_______。
,下列说法正确的是_______。
(3)实验室模拟合成水煤气,一定温度下在 的密闭容器中加入
的密闭容器中加入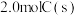 与
与 发生反应
发生反应 ,在
,在 达到平衡时,
达到平衡时, 的转化率是
的转化率是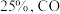 的物质的量是
的物质的量是 ,反应开始到平衡时生成
,反应开始到平衡时生成 的平均反应速率为
的平均反应速率为_______ ,计算反应 的平衡常数
的平衡常数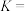
_____ (写出计算过程)。
(4)合成氨总反应在起始反应物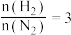 时,在不同条件下达到平衡,设体系中
时,在不同条件下达到平衡,设体系中 的体积分数为
的体积分数为 ,在
,在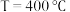 下的
下的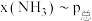 、
、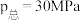 下的
下的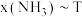 如图所示,图中对应等压过程的曲线是
如图所示,图中对应等压过程的曲线是______ (填“Ⅰ”或“Ⅱ”),当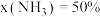 时氨气的分压
时氨气的分压
______  (分压=气体的物质的量分数×总压)。
(分压=气体的物质的量分数×总压)。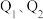 均大于0):
均大于0):________ 。
②合成尿素过程中会积聚一定浓度的氨基甲酸铵( ),为减少氨基甲酸铵的积聚,提高尿素的产率,可控制
),为减少氨基甲酸铵的积聚,提高尿素的产率,可控制 与
与 的通入比例
的通入比例_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。

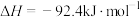 。合成氨原料中的
。合成氨原料中的 一般由分馏液态空气得到,
一般由分馏液态空气得到, 可来源于水煤气,相关反应如下:
可来源于水煤气,相关反应如下:a.

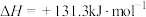
b.

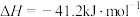
回答下列问题:
(1)
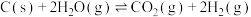 的反应物总能量
的反应物总能量(2)在密闭容器中同时发生反应
 ,下列说法正确的是_______。
,下列说法正确的是_______。A.增大压强,反应 平衡不移动 平衡不移动 | B.使用催化剂提高 平衡转化率 平衡转化率 |
C.升高温度,反应a的 增大, 增大, 减小 减小 | D.反应a有非极性键的断裂与形成 |
(3)实验室模拟合成水煤气,一定温度下在
 的密闭容器中加入
的密闭容器中加入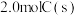 与
与 发生反应
发生反应 ,在
,在 达到平衡时,
达到平衡时, 的转化率是
的转化率是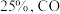 的物质的量是
的物质的量是 ,反应开始到平衡时生成
,反应开始到平衡时生成 的平均反应速率为
的平均反应速率为 的平衡常数
的平衡常数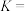
(4)合成氨总反应在起始反应物
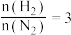 时,在不同条件下达到平衡,设体系中
时,在不同条件下达到平衡,设体系中 的体积分数为
的体积分数为 ,在
,在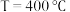 下的
下的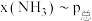 、
、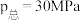 下的
下的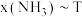 如图所示,图中对应等压过程的曲线是
如图所示,图中对应等压过程的曲线是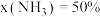 时氨气的分压
时氨气的分压
 (分压=气体的物质的量分数×总压)。
(分压=气体的物质的量分数×总压)。
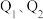 均大于0):
均大于0):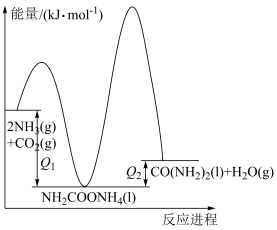
②合成尿素过程中会积聚一定浓度的氨基甲酸铵(
 ),为减少氨基甲酸铵的积聚,提高尿素的产率,可控制
),为减少氨基甲酸铵的积聚,提高尿素的产率,可控制 与
与 的通入比例
的通入比例 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】反应 。在进气比
。在进气比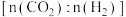 不同时,测得相应的
不同时,测得相应的 平衡转化率如图(各点对应的反应温度可能相同,也可能不同;各点对应的其他反应条件都相同)。
平衡转化率如图(各点对应的反应温度可能相同,也可能不同;各点对应的其他反应条件都相同)。 的平衡转化率与进气比、反应温度之间的关系是
的平衡转化率与进气比、反应温度之间的关系是_______ 。
(2)图中E和G两点对应的反应温度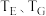 的关系是
的关系是_______ ,其原因是_______ 。
(3)A、B两点对应的反应速率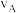
_______ (填“<”“=”或“>”) 。已知反应速率
。已知反应速率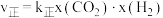 ,
,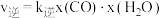 ,k为反应速率常数,x为物质的量分数,在达到平衡状态为C点的反应过程(此过程为恒温)中,当
,k为反应速率常数,x为物质的量分数,在达到平衡状态为C点的反应过程(此过程为恒温)中,当 的转化率刚好达到60%时,
的转化率刚好达到60%时,
_______ 。
 。在进气比
。在进气比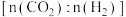 不同时,测得相应的
不同时,测得相应的 平衡转化率如图(各点对应的反应温度可能相同,也可能不同;各点对应的其他反应条件都相同)。
平衡转化率如图(各点对应的反应温度可能相同,也可能不同;各点对应的其他反应条件都相同)。
 的平衡转化率与进气比、反应温度之间的关系是
的平衡转化率与进气比、反应温度之间的关系是(2)图中E和G两点对应的反应温度
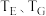 的关系是
的关系是(3)A、B两点对应的反应速率
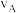
 。已知反应速率
。已知反应速率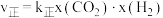 ,
,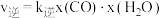 ,k为反应速率常数,x为物质的量分数,在达到平衡状态为C点的反应过程(此过程为恒温)中,当
,k为反应速率常数,x为物质的量分数,在达到平衡状态为C点的反应过程(此过程为恒温)中,当 的转化率刚好达到60%时,
的转化率刚好达到60%时,
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】硫化氢为易燃危化品,与空'气混合能形成爆炸性混合物,遇明火、高热能引起燃烧爆炸,并且硫化氢有剧毒。油开气采、石油化工、煤化工等行业废气普遍含有硫化氢,需要回收处理并加以利用。
回答下列问题:
(1)已知下列反应的热化学方程式:
①2H2S(g) S2(g) +2H2(g) ΔH1= + 180kJ·mol-1 Kp1=a
S2(g) +2H2(g) ΔH1= + 180kJ·mol-1 Kp1=a
②CS2(g)+2H2(g) CH4(g) +S2(g) ΔH2=-81kJ·mol-1 Kp2= b
CH4(g) +S2(g) ΔH2=-81kJ·mol-1 Kp2= b
则反应③CH4(g) +2H2S(g) CS2(g) +4H2(g) 的 ΔH3=
CS2(g) +4H2(g) 的 ΔH3=___________ kJ·mol-1,Kp3=________ (不写单位)。
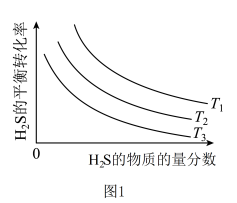
(2)在不同温度、反应压强为100kPn,进料H2S的摩尔分数(可看成体积分数)为0.1%~20% (其余为N2)的条件下,对于反应①,H2S 分解平衡转化率的结果如图1所示。则T1、T2和T3由大到小的顺序为___________ ,同温同压下H2S的摩尔分数越大,H2S 分解平衡转化率越小的原因是______________________ 。
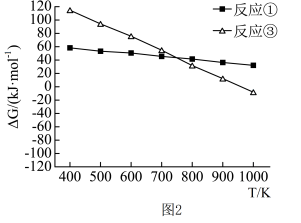
(3)反应①和③的 ΔG随温度的影响如图2所示,已知ΔG =-RTlnK (R为常数,T为温度,K为平衡常数),则在1000°C时,反应的自发趋势①___________ ③(填“>”、“<”或“=”)。在1000°C、100kPa反应条件下,将一定量的H2S和CH4混合进行反应(不考虑反应②),达到平衡时n(CS2):n(H2)约为1:4, n(S2)微乎其微,其原因是___________ 。
(4)在1000°C、100kPa反应条件下,将H2S、CH4、N2摩尔分数比为3:3:2的混合气进行反应③,达到平衡时,CS2分压与H2S的分压相同。则反应③的Kp=___________ (不写单位)。
回答下列问题:
(1)已知下列反应的热化学方程式:
①2H2S(g)
 S2(g) +2H2(g) ΔH1= + 180kJ·mol-1 Kp1=a
S2(g) +2H2(g) ΔH1= + 180kJ·mol-1 Kp1=a②CS2(g)+2H2(g)
 CH4(g) +S2(g) ΔH2=-81kJ·mol-1 Kp2= b
CH4(g) +S2(g) ΔH2=-81kJ·mol-1 Kp2= b 则反应③CH4(g) +2H2S(g)
 CS2(g) +4H2(g) 的 ΔH3=
CS2(g) +4H2(g) 的 ΔH3=(2)在不同温度、反应压强为100kPn,进料H2S的摩尔分数(可看成体积分数)为0.1%~20% (其余为N2)的条件下,对于反应①,H2S 分解平衡转化率的结果如图1所示。则T1、T2和T3由大到小的顺序为

(3)反应①和③的 ΔG随温度的影响如图2所示,已知ΔG =-RTlnK (R为常数,T为温度,K为平衡常数),则在1000°C时,反应的自发趋势①

(4)在1000°C、100kPa反应条件下,将H2S、CH4、N2摩尔分数比为3:3:2的混合气进行反应③,达到平衡时,CS2分压与H2S的分压相同。则反应③的Kp=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈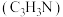 和副产物丙烯醛
和副产物丙烯醛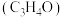 的热化学方程式如下:
的热化学方程式如下:
Ⅰ.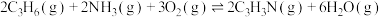

Ⅱ.

回答下列问题:
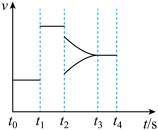
(1)如图表示在某一时间段密闭体系中反应Ⅰ的反应速率与反应进程的曲线关系。由图可知,正反应速率最快的时间段是_______ , 时刻表示体系改变的反应条件是
时刻表示体系改变的反应条件是_______ , 时刻表示体系改变的另一反应条件是
时刻表示体系改变的另一反应条件是_______ 。
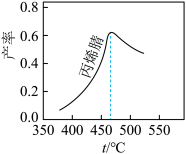
(2)在不同温度下反应进行相同时间,丙烯腈产率与反应温度的关系曲线如图,最高产率对应的温度为460℃。高于460℃时,丙烯腈产率下降的原因是_______ (答出两点即可)。
(3)一定条件下,在容积为V L的密闭容器中充入 、
、 、
、 各1mol发生反应,达到平衡时,容器内压强为
各1mol发生反应,达到平衡时,容器内压强为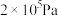 ,容器中
,容器中 和
和 的物质的量分别为0.3mol和1.5mol,此时
的物质的量分别为0.3mol和1.5mol,此时 的浓度为
的浓度为_______  ,反应Ⅱ的标准平衡常数
,反应Ⅱ的标准平衡常数
_______ 。(已知:分压=总压×该组分物质的量分数,对于反应: ,
,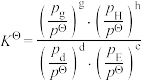 ,其中
,其中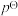 为标准压强
为标准压强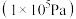 ,
,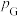 、
、 、
、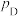 、
、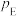 为各组分的平衡分压。)
为各组分的平衡分压。)
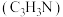 和副产物丙烯醛
和副产物丙烯醛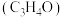 的热化学方程式如下:
的热化学方程式如下:Ⅰ.
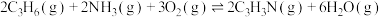

Ⅱ.


回答下列问题:
(1)如图表示在某一时间段密闭体系中反应Ⅰ的反应速率与反应进程的曲线关系。由图可知,正反应速率最快的时间段是
 时刻表示体系改变的反应条件是
时刻表示体系改变的反应条件是 时刻表示体系改变的另一反应条件是
时刻表示体系改变的另一反应条件是
(2)在不同温度下反应进行相同时间,丙烯腈产率与反应温度的关系曲线如图,最高产率对应的温度为460℃。高于460℃时,丙烯腈产率下降的原因是

(3)一定条件下,在容积为V L的密闭容器中充入
 、
、 、
、 各1mol发生反应,达到平衡时,容器内压强为
各1mol发生反应,达到平衡时,容器内压强为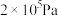 ,容器中
,容器中 和
和 的物质的量分别为0.3mol和1.5mol,此时
的物质的量分别为0.3mol和1.5mol,此时 的浓度为
的浓度为 ,反应Ⅱ的标准平衡常数
,反应Ⅱ的标准平衡常数
 ,
, ,其中
,其中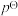 为标准压强
为标准压强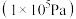 ,
,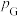 、
、 、
、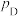 、
、 为各组分的平衡分压。)
为各组分的平衡分压。)
您最近一年使用:0次



