氯及其化合物在生产、生活中广泛应用。
(1)三氯乙醛常用于制造农药。化学反应原理是4Cl2(g)+C2H5OH(g) CCl3CHO(g)+5HCl(g)。一定温度下,在某恒容密闭容器中充入4molCl2和2molC2H5OH(g),发生上述反应。下列叙述正确的是_____
CCl3CHO(g)+5HCl(g)。一定温度下,在某恒容密闭容器中充入4molCl2和2molC2H5OH(g),发生上述反应。下列叙述正确的是_____
(2)SCl4是一种化工产品。已知有关反应如下:
①2S(1)+Cl2(g)=S2Cl2(1) ΔH1=akJ·mol-1
②S2C12(1)+Cl2(g)=2SCl2(1) ΔH2=bkJ·mol-1
③SC12(1)+Cl2(g)=SCl4(1) ΔH3=ckJ·mol-1
④S(1)+2Cl2(g)=SCl4(l) ΔH4=_____ kJ·mol-1(用含a、b和c的式子表示)。
(3)工业上,曾用催化氧化氯化氢法(俗称地康法)制备氯气:
4HCl(g)+O2(g)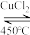 2Cl2(g)+2H2O(g) ΔH
2Cl2(g)+2H2O(g) ΔH
从化学反应原理角度分析,一定条件下,投料比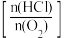 是提高HCl平衡转化率和反应速率以及提纯氯气的关键条件。若投料比太小,有利的是
是提高HCl平衡转化率和反应速率以及提纯氯气的关键条件。若投料比太小,有利的是_____ ;不利的是_____ 。
(4)已知Arrhenius经验公式为Rlnk=- +C(Ea为活化能,k为速率常数,R和C为常数,活化能不随温度变化)。为了探究催化剂对地康法制氯气的影响,某小组选择ZnCl2、CuCl2为催化剂,探究其对氯化氢催化氧化反应的影响,实验结果如图1所示。
+C(Ea为活化能,k为速率常数,R和C为常数,活化能不随温度变化)。为了探究催化剂对地康法制氯气的影响,某小组选择ZnCl2、CuCl2为催化剂,探究其对氯化氢催化氧化反应的影响,实验结果如图1所示。
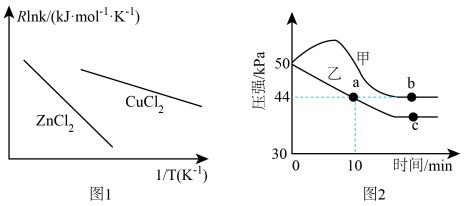
从图1中信息获知催化效能较低的催化剂是_____ (填化学式),其理由是_____ 。
(5)在体积相同的甲、乙两个密闭容器中充入4molHCl(g)和1molO2(g),分别在恒容恒温、恒容绝热条件下发生反应:4HCl(g)+O2(g)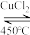 2Cl2(g)+2H2O(g)ΔH,测得气体压强变化与时间关系如图2所示。
2Cl2(g)+2H2O(g)ΔH,测得气体压强变化与时间关系如图2所示。
①气体总物质的量:n(a)______ n(b)(填“>”“<”或“=”,下同)。
②a点Qp=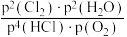 =
=_____ (kPa)-1(结果保留2位小数)。b点Kp_____ a点Qp。
(1)三氯乙醛常用于制造农药。化学反应原理是4Cl2(g)+C2H5OH(g)
 CCl3CHO(g)+5HCl(g)。一定温度下,在某恒容密闭容器中充入4molCl2和2molC2H5OH(g),发生上述反应。下列叙述正确的是_____
CCl3CHO(g)+5HCl(g)。一定温度下,在某恒容密闭容器中充入4molCl2和2molC2H5OH(g),发生上述反应。下列叙述正确的是_____| A.混合气体平均摩尔质量不变时达到平衡状态 |
| B.平衡后再充入少量Cl2反应正向进行 |
| C.加入高效催化剂,能提高氯气的平衡产率 |
| D.平衡时三氯乙醛体积分数可能等于15% |
①2S(1)+Cl2(g)=S2Cl2(1) ΔH1=akJ·mol-1
②S2C12(1)+Cl2(g)=2SCl2(1) ΔH2=bkJ·mol-1
③SC12(1)+Cl2(g)=SCl4(1) ΔH3=ckJ·mol-1
④S(1)+2Cl2(g)=SCl4(l) ΔH4=
(3)工业上,曾用催化氧化氯化氢法(俗称地康法)制备氯气:
4HCl(g)+O2(g)
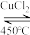 2Cl2(g)+2H2O(g) ΔH
2Cl2(g)+2H2O(g) ΔH从化学反应原理角度分析,一定条件下,投料比
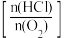 是提高HCl平衡转化率和反应速率以及提纯氯气的关键条件。若投料比太小,有利的是
是提高HCl平衡转化率和反应速率以及提纯氯气的关键条件。若投料比太小,有利的是(4)已知Arrhenius经验公式为Rlnk=-
 +C(Ea为活化能,k为速率常数,R和C为常数,活化能不随温度变化)。为了探究催化剂对地康法制氯气的影响,某小组选择ZnCl2、CuCl2为催化剂,探究其对氯化氢催化氧化反应的影响,实验结果如图1所示。
+C(Ea为活化能,k为速率常数,R和C为常数,活化能不随温度变化)。为了探究催化剂对地康法制氯气的影响,某小组选择ZnCl2、CuCl2为催化剂,探究其对氯化氢催化氧化反应的影响,实验结果如图1所示。
从图1中信息获知催化效能较低的催化剂是
(5)在体积相同的甲、乙两个密闭容器中充入4molHCl(g)和1molO2(g),分别在恒容恒温、恒容绝热条件下发生反应:4HCl(g)+O2(g)
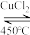 2Cl2(g)+2H2O(g)ΔH,测得气体压强变化与时间关系如图2所示。
2Cl2(g)+2H2O(g)ΔH,测得气体压强变化与时间关系如图2所示。①气体总物质的量:n(a)_
②a点Qp=
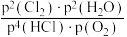 =
=
更新时间:2023-06-04 07:24:53
|
相似题推荐
【推荐1】金属铁盐或其氧化物在生产生活和科学实验中应用广泛。
(1)一定条件下Fe2O3与甲烷反应制取纳米级铁,同时生成CO和H2。
已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-27.6kJ/mol
CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.4kJ/mol
CO(g)+H2O(g)=CO2(g)+H2(g) △H=-41.0kJ/mol
①反应Fe2O3(s)+3 CH4(g) 2Fe(s)+3CO(g) +6H2(g)的△H
2Fe(s)+3CO(g) +6H2(g)的△H______ 0(填“>”、“<”或“=”)
②若该反应在5L的密闭容器中进行,1min后达到平衡,测得体系中固体质量减少0.96g。则该段时间内CO的平均反应速率为__________ 。
③若该反应在恒温恒压容器中进行,能表明该反应达到平衡状态的是______ (选填序号)
a.c(CH4)=c(CO)
b.固体的总质量不变
c.v(CO)与v(H2)的比值不变
d.混合气体的平均相对分子质量不变
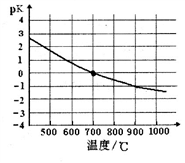
④该反应的化学平衡常数的负对数pK随反应温度T的变化曲线如下图。试用平衡移动原理解释该曲线的变化规律:______________________ 。若700℃时测得c平衡(H2)=1.0mol·L-1,则CH4的转化率为_________ 。
(2)菱铁矿的主要成分是:FeCO3,实验室中可以通过FeSO4与NaHCO3溶液混合制得FeCO3,有关反应的离子方程式为:____________________ 。已知Ksp[FeCO3]=3.2×10-11,H2CO3的Ka1=4.30×10-7,Ka2=5.61×10-11。试通过以上数据简要计算说明该反应能进行的原因_____________________ 。
(3)Na2FeO4是一种高效净水剂,工业上以Fe为阳极,NaOH为电解质溶液进行电解制备, 写出阳极电极反应式:_____________________ 。
(1)一定条件下Fe2O3与甲烷反应制取纳米级铁,同时生成CO和H2。
已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-27.6kJ/mol
CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.4kJ/mol
CO(g)+H2O(g)=CO2(g)+H2(g) △H=-41.0kJ/mol
①反应Fe2O3(s)+3 CH4(g)
 2Fe(s)+3CO(g) +6H2(g)的△H
2Fe(s)+3CO(g) +6H2(g)的△H②若该反应在5L的密闭容器中进行,1min后达到平衡,测得体系中固体质量减少0.96g。则该段时间内CO的平均反应速率为
③若该反应在恒温恒压容器中进行,能表明该反应达到平衡状态的是
a.c(CH4)=c(CO)
b.固体的总质量不变
c.v(CO)与v(H2)的比值不变
d.混合气体的平均相对分子质量不变
④该反应的化学平衡常数的负对数pK随反应温度T的变化曲线如下图。试用平衡移动原理解释该曲线的变化规律:
(2)菱铁矿的主要成分是:FeCO3,实验室中可以通过FeSO4与NaHCO3溶液混合制得FeCO3,有关反应的离子方程式为:
(3)Na2FeO4是一种高效净水剂,工业上以Fe为阳极,NaOH为电解质溶液进行电解制备, 写出阳极电极反应式:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】以氧化铝为原料,通过碳热还原法可合成氮化铝(AlN);通过电解法可制取铝。电解铝时阳极产生的CO2可通过二氧化碳甲烷化再利用。请回答:
(1)已知:2Al2O3(s)=4Al(g)+3O2(g) ΔH1=+3351 kJ·molˉ1
2C(s)+O2(g)=2CO(g) ΔH2=-221 kJ·molˉ1
2Al(g)+N2(g)=2AlN(s) ΔH3=-318 kJ·molˉ1
则反应Al2O3(s)+ 3C(s)+ N2(g)=3CO(g)+ 2AlN(s)的ΔH=_______ ,该反应自发进行的条件是:_______ 。
(2)在常压、Ru/TiO2催化下,CO2和H2混和气体(体积比1∶4,总物质的量a mol)进行反应,测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比)。
反应ⅠCO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH4
CH4(g)+2H2O(g) ΔH4
反应ⅡCO2(g)+H2(g) CO(g)+H2O(g) ΔH5
CO(g)+H2O(g) ΔH5

①下列说法不正确的是_______ 。
a.ΔH 4小于零
B.温度可影响产物的选择性
C.CO2平衡转化率随温度升高先增大后减少
D.其他条件不变,将CO2和H2的初始体积比改变为1∶3,可提高CO2平衡转化率
②350℃时,反应Ⅰ在t1时刻达到平衡,平衡时容器体积为V L,该温度下反应Ⅰ的平衡常数K=_______ (用a、V表示)。
③350℃下CH4物质的量随时间的变化曲线如图3所示。画出400℃下0~t1时刻CH4物质的量随时间的变化曲线。___________

(1)已知:2Al2O3(s)=4Al(g)+3O2(g) ΔH1=+3351 kJ·molˉ1
2C(s)+O2(g)=2CO(g) ΔH2=-221 kJ·molˉ1
2Al(g)+N2(g)=2AlN(s) ΔH3=-318 kJ·molˉ1
则反应Al2O3(s)+ 3C(s)+ N2(g)=3CO(g)+ 2AlN(s)的ΔH=
(2)在常压、Ru/TiO2催化下,CO2和H2混和气体(体积比1∶4,总物质的量a mol)进行反应,测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比)。
反应ⅠCO2(g)+4H2(g)
 CH4(g)+2H2O(g) ΔH4
CH4(g)+2H2O(g) ΔH4反应ⅡCO2(g)+H2(g)
 CO(g)+H2O(g) ΔH5
CO(g)+H2O(g) ΔH5
①下列说法不正确的是
a.ΔH 4小于零
B.温度可影响产物的选择性
C.CO2平衡转化率随温度升高先增大后减少
D.其他条件不变,将CO2和H2的初始体积比改变为1∶3,可提高CO2平衡转化率
②350℃时,反应Ⅰ在t1时刻达到平衡,平衡时容器体积为V L,该温度下反应Ⅰ的平衡常数K=
③350℃下CH4物质的量随时间的变化曲线如图3所示。画出400℃下0~t1时刻CH4物质的量随时间的变化曲线。

您最近一年使用:0次
【推荐3】二氧化碳的吸收和利用是实现“碳中和”的重要途径。
Ⅰ.工业生产中,利用 和
和 制取尿素,通常认为该反应分为两步:
制取尿素,通常认为该反应分为两步:
ⅰ.
 kJ⋅mol-1
kJ⋅mol-1
ⅱ.
 kJ⋅mol-1
kJ⋅mol-1
(1) 和
和 制取尿素的总反应的热化学方程式为
制取尿素的总反应的热化学方程式为___________ 。
(2)尿素易溶于水,从微观角度解释其主要原因为___________ 。
Ⅱ.以 为原料合成甲醇,可以实现碳的循环利用。
为原料合成甲醇,可以实现碳的循环利用。
(3)一种铜基催化剂催化 转化成甲醇的催化机理如图所示,该反应的副产物是
转化成甲醇的催化机理如图所示,该反应的副产物是___________ 。

(4)①合成甲醇的另一途径可表示为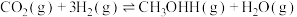
 。在恒容绝热的密闭容器中,一定说明该反应已达到化学平衡状态的是
。在恒容绝热的密闭容器中,一定说明该反应已达到化学平衡状态的是___________ (填标号)。
A. B.气体的压强保持不变
B.气体的压强保持不变
C.气体的密度保持不变 D.体系的温度保持不变
②某甲醇燃料电池的工作原理如图所示,铂电极(a)上的电极反应式为___________ 。

(5)甲醇在一定条件下脱水可制得二甲醚,该反应可表示为
 。
。
实验测得: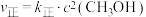 ,
, ,
, 、
、 为速率常数。T₁温度下。向2L恒容密闭容器中加入0.4 mol
为速率常数。T₁温度下。向2L恒容密闭容器中加入0.4 mol  ,达到平衡时测得
,达到平衡时测得 的体积分数为60%,则平衡时
的体积分数为60%,则平衡时 的产率
的产率
___________ ,反应的平衡常数
___________ 。当温度改变为 时,
时,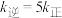 ,则
,则
___________  (填“<”“>”或“=”)。
(填“<”“>”或“=”)。
Ⅰ.工业生产中,利用
 和
和 制取尿素,通常认为该反应分为两步:
制取尿素,通常认为该反应分为两步:ⅰ.

 kJ⋅mol-1
kJ⋅mol-1ⅱ.

 kJ⋅mol-1
kJ⋅mol-1(1)
 和
和 制取尿素的总反应的热化学方程式为
制取尿素的总反应的热化学方程式为(2)尿素易溶于水,从微观角度解释其主要原因为
Ⅱ.以
 为原料合成甲醇,可以实现碳的循环利用。
为原料合成甲醇,可以实现碳的循环利用。(3)一种铜基催化剂催化
 转化成甲醇的催化机理如图所示,该反应的副产物是
转化成甲醇的催化机理如图所示,该反应的副产物是
(4)①合成甲醇的另一途径可表示为
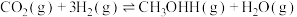
 。在恒容绝热的密闭容器中,一定说明该反应已达到化学平衡状态的是
。在恒容绝热的密闭容器中,一定说明该反应已达到化学平衡状态的是A.
 B.气体的压强保持不变
B.气体的压强保持不变C.气体的密度保持不变 D.体系的温度保持不变
②某甲醇燃料电池的工作原理如图所示,铂电极(a)上的电极反应式为

(5)甲醇在一定条件下脱水可制得二甲醚,该反应可表示为

 。
。实验测得:
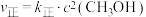 ,
, ,
, 、
、 为速率常数。T₁温度下。向2L恒容密闭容器中加入0.4 mol
为速率常数。T₁温度下。向2L恒容密闭容器中加入0.4 mol  ,达到平衡时测得
,达到平衡时测得 的体积分数为60%,则平衡时
的体积分数为60%,则平衡时 的产率
的产率

 时,
时,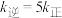 ,则
,则
 (填“<”“>”或“=”)。
(填“<”“>”或“=”)。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】二甲醚 是无色气体,可作为一种新型能源,同时也是重要的化工原料,采用
是无色气体,可作为一种新型能源,同时也是重要的化工原料,采用 催化加氢可合成二甲醚,发生的反应如下:
催化加氢可合成二甲醚,发生的反应如下:
I.

Ⅱ.
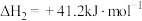
回答下列问题:
(1)已知反应: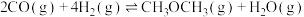
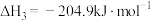 ,则
,则
______ ;
(2)在恒温恒容密闭容器中充入一定量的 和
和 ,发生上述反应。下列能说明反应I达到平衡状态的是
,发生上述反应。下列能说明反应I达到平衡状态的是______ 。
a.容器内气体的密度不再发生变化
b.容器内的压强不再发生变化
c.
d.容器内气体平均相对分子质量不再变化
(3)在压强、 和
和 的起始投料一定的条件下,发生反应I、Ⅱ,实验测得(
的起始投料一定的条件下,发生反应I、Ⅱ,实验测得( 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图所示。(已知:
的选择性随温度的变化如图所示。(已知: 的选择性
的选择性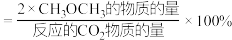 )
)

其中表示平衡时 的选择性的曲线是
的选择性的曲线是______ (填“①”或“②”);温度高于300℃时,曲线②随温度升高而升高的原因是______ 。
(4)对于反应Ⅱ的反应速率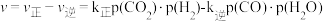 其中
其中 、
、 分别为正、逆反应速率常数,p为气体的分压(分压
分别为正、逆反应速率常数,p为气体的分压(分压 总压
总压 物质的量分数)。
物质的量分数)。
a.达到平衡后,降低温度,
______ (填“增大”、“减小”或”不变”);
b.在一定温度和压强下的反应Ⅱ,按照n(CO2):n(H2)=6:7投料,当CO2转化率为50%时,用气体分压表示的平衡常数
(5)二甲醚—氧气燃料电池具有启动快,效率高等优点,若电解质溶液为NaOH溶液时,燃料电池的负极反应式为______ 。
 是无色气体,可作为一种新型能源,同时也是重要的化工原料,采用
是无色气体,可作为一种新型能源,同时也是重要的化工原料,采用 催化加氢可合成二甲醚,发生的反应如下:
催化加氢可合成二甲醚,发生的反应如下:I.


Ⅱ.

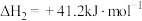
回答下列问题:
(1)已知反应:
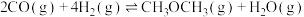
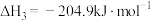 ,则
,则
(2)在恒温恒容密闭容器中充入一定量的
 和
和 ,发生上述反应。下列能说明反应I达到平衡状态的是
,发生上述反应。下列能说明反应I达到平衡状态的是a.容器内气体的密度不再发生变化
b.容器内的压强不再发生变化
c.

d.容器内气体平均相对分子质量不再变化
(3)在压强、
 和
和 的起始投料一定的条件下,发生反应I、Ⅱ,实验测得(
的起始投料一定的条件下,发生反应I、Ⅱ,实验测得( 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图所示。(已知:
的选择性随温度的变化如图所示。(已知: 的选择性
的选择性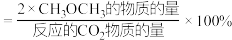 )
)
其中表示平衡时
 的选择性的曲线是
的选择性的曲线是(4)对于反应Ⅱ的反应速率
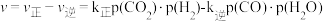 其中
其中 、
、 分别为正、逆反应速率常数,p为气体的分压(分压
分别为正、逆反应速率常数,p为气体的分压(分压 总压
总压 物质的量分数)。
物质的量分数)。a.达到平衡后,降低温度,

b.在一定温度和压强下的反应Ⅱ,按照n(CO2):n(H2)=6:7投料,当CO2转化率为50%时,用气体分压表示的平衡常数
(5)二甲醚—氧气燃料电池具有启动快,效率高等优点,若电解质溶液为NaOH溶液时,燃料电池的负极反应式为
您最近一年使用:0次
【推荐2】甲醇是重要的化工原料之一,也可用作燃料,利用合成气(主要成分为CO、CO2和H2)可以合成甲醇,涉及的反应如下:
反应ⅰ: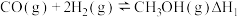
反应ⅱ:
反应ⅲ:
请回答下列问题:
(1)在某催化剂作用下,反应ⅰ的反应历程如图所示(图中数据表示微粒数目以及微粒的相对总能量,*表示吸附在催化剂上):___________ (填“较低”或“较高”)温度下才能自发进行。
②结合反应历程,写出反应ⅰ中生成甲醇的决速步骤的反应方程式:___________ 。
③
___________ (计算结果保留两位有效数字,已知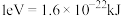 )。
)。
(2)反应ⅰ的Arrhenius经验公式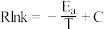 (
( 为活化能,
为活化能, 为速率常数,
为速率常数, 和
和 均为常数,
均为常数, 为温度),实验数据如图中曲线
为温度),实验数据如图中曲线 所示。当改变外界条件时,实验数据如图中曲线
所示。当改变外界条件时,实验数据如图中曲线 所示,则实验可能改变的外界条件是
所示,则实验可能改变的外界条件是___________ 。 和
和 充入密闭容器中并加入合适的催化剂,只发生反应ⅱ和ⅲ。相同温度下,在不同压强下测得
充入密闭容器中并加入合适的催化剂,只发生反应ⅱ和ⅲ。相同温度下,在不同压强下测得 的平衡转化率、
的平衡转化率、 的选择性[
的选择性[ ]和
]和 的选择性[
的选择性[ ]随压强的变化曲线如图所示。
]随压强的变化曲线如图所示。___________ (填“m”“n”或“p”),简述判断方法:___________ 。
(4)有研究认为,在某催化剂作用下反应ⅱ先后通过反应ⅲ、ⅰ来实现。保持温度 不变,向一恒容密闭容器中充入4molCO2和8molH2,在该催化剂作用下发生反应,经5min达到平衡,测得H2O(g)的物质的量为3mol,起始及达平衡时容器的总压强分别为
不变,向一恒容密闭容器中充入4molCO2和8molH2,在该催化剂作用下发生反应,经5min达到平衡,测得H2O(g)的物质的量为3mol,起始及达平衡时容器的总压强分别为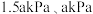 ,则从开始到平衡用H2分压表示的平均反应速率为
,则从开始到平衡用H2分压表示的平均反应速率为___________ kPa•min-1(用含 的式子表示,下同,分压
的式子表示,下同,分压 总压
总压 物质的量分数);反应ⅱ的压强平衡常数
物质的量分数);反应ⅱ的压强平衡常数
___________ 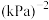 (
( 为用分压代替浓度计算的平衡常数)。
为用分压代替浓度计算的平衡常数)。
(5)光催化CO2制甲醇技术也是研究热点。铜基纳米光催化材料还原CO2的机理如图所示,光照时,低能价带失去电子并产生空穴( ,具有强氧化性)。在低能价带上,H2O直接转化为O2的电极反应式为
,具有强氧化性)。在低能价带上,H2O直接转化为O2的电极反应式为___________ 。
反应ⅰ:
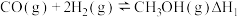
反应ⅱ:

反应ⅲ:

请回答下列问题:
(1)在某催化剂作用下,反应ⅰ的反应历程如图所示(图中数据表示微粒数目以及微粒的相对总能量,*表示吸附在催化剂上):

②结合反应历程,写出反应ⅰ中生成甲醇的决速步骤的反应方程式:
③

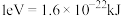 )。
)。(2)反应ⅰ的Arrhenius经验公式
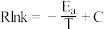 (
( 为活化能,
为活化能, 为速率常数,
为速率常数, 和
和 均为常数,
均为常数, 为温度),实验数据如图中曲线
为温度),实验数据如图中曲线 所示。当改变外界条件时,实验数据如图中曲线
所示。当改变外界条件时,实验数据如图中曲线 所示,则实验可能改变的外界条件是
所示,则实验可能改变的外界条件是
 和
和 充入密闭容器中并加入合适的催化剂,只发生反应ⅱ和ⅲ。相同温度下,在不同压强下测得
充入密闭容器中并加入合适的催化剂,只发生反应ⅱ和ⅲ。相同温度下,在不同压强下测得 的平衡转化率、
的平衡转化率、 的选择性[
的选择性[ ]和
]和 的选择性[
的选择性[ ]随压强的变化曲线如图所示。
]随压强的变化曲线如图所示。
(4)有研究认为,在某催化剂作用下反应ⅱ先后通过反应ⅲ、ⅰ来实现。保持温度
 不变,向一恒容密闭容器中充入4molCO2和8molH2,在该催化剂作用下发生反应,经5min达到平衡,测得H2O(g)的物质的量为3mol,起始及达平衡时容器的总压强分别为
不变,向一恒容密闭容器中充入4molCO2和8molH2,在该催化剂作用下发生反应,经5min达到平衡,测得H2O(g)的物质的量为3mol,起始及达平衡时容器的总压强分别为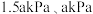 ,则从开始到平衡用H2分压表示的平均反应速率为
,则从开始到平衡用H2分压表示的平均反应速率为 的式子表示,下同,分压
的式子表示,下同,分压 总压
总压 物质的量分数);反应ⅱ的压强平衡常数
物质的量分数);反应ⅱ的压强平衡常数
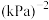 (
( 为用分压代替浓度计算的平衡常数)。
为用分压代替浓度计算的平衡常数)。(5)光催化CO2制甲醇技术也是研究热点。铜基纳米光催化材料还原CO2的机理如图所示,光照时,低能价带失去电子并产生空穴(
 ,具有强氧化性)。在低能价带上,H2O直接转化为O2的电极反应式为
,具有强氧化性)。在低能价带上,H2O直接转化为O2的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】综合利用CO2和CO是科学家研究的热点课题。
(1)CO用于处理大气污染物N2O所发生的反应为:CO(g)+N2O(g)⇌ CO2(g)+N2(g) 。几种物质的相对能量如表:
。几种物质的相对能量如表:
①
_______  。
。
②有人提出上述反应可以用“Fe+”作催化剂。其总反应分两步进行:
第一步: ;
;
第二步:_______ (写化学方程式)。
第二步反应不影响总反应达到平衡所用时间,由此推知,第二步反应活化能_______ 第一步反应活化能(填“大于”“小于”或“等于”)。
(2)在实验室采用 测定空气中CO的含量。在密闭容器中充入足量的
测定空气中CO的含量。在密闭容器中充入足量的 粉末和一定量的CO,发生反应:I2O5(s)+5CO(g)⇌ 5CO2(g)+I2(s)。测得CO的转化率如图所示:
粉末和一定量的CO,发生反应:I2O5(s)+5CO(g)⇌ 5CO2(g)+I2(s)。测得CO的转化率如图所示:

①相对曲线a,曲线b仅改变一个条件,改变的条件可能是_______ 。
②在此温度下,该可逆反应的平衡常数
_______ (用含x的代数式表示)。
(3)CH4超干重整CO2技术可得到富含CO的化工原料。反应为CH4(g)+CO2(g)⇌ 2CO(g)+2H2(g) =−49.0 kJ·mol−1
=−49.0 kJ·mol−1
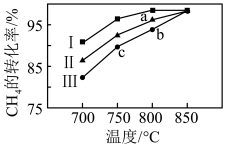
其他条件不变,在不同催化剂(I、II、III)作用下,反应进行相同时间后,CH4的转化率随反应温度的变化如图所示。a点所代表的状态_______ (填“是”或“不是”)平衡状态;b点CH4的转化率高于c点,原因是_______ 。
(1)CO用于处理大气污染物N2O所发生的反应为:CO(g)+N2O(g)⇌ CO2(g)+N2(g)
 。几种物质的相对能量如表:
。几种物质的相对能量如表:| 物质 |  | 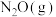 |  |  |
相对能量( ) ) | 283 | 475.5 | 0 | 393.5 |

 。
。②有人提出上述反应可以用“Fe+”作催化剂。其总反应分两步进行:
第一步:
 ;
;第二步:
第二步反应不影响总反应达到平衡所用时间,由此推知,第二步反应活化能
(2)在实验室采用
 测定空气中CO的含量。在密闭容器中充入足量的
测定空气中CO的含量。在密闭容器中充入足量的 粉末和一定量的CO,发生反应:I2O5(s)+5CO(g)⇌ 5CO2(g)+I2(s)。测得CO的转化率如图所示:
粉末和一定量的CO,发生反应:I2O5(s)+5CO(g)⇌ 5CO2(g)+I2(s)。测得CO的转化率如图所示:
①相对曲线a,曲线b仅改变一个条件,改变的条件可能是
②在此温度下,该可逆反应的平衡常数

(3)CH4超干重整CO2技术可得到富含CO的化工原料。反应为CH4(g)+CO2(g)⇌ 2CO(g)+2H2(g)
 =−49.0 kJ·mol−1
=−49.0 kJ·mol−1其他条件不变,在不同催化剂(I、II、III)作用下,反应进行相同时间后,CH4的转化率随反应温度的变化如图所示。a点所代表的状态

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】乙醇-水催化重整可获得 。主要发生以下反应:
。主要发生以下反应:
反应Ⅰ:
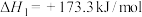
反应Ⅱ:
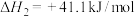
(1)反应Ⅰ自发进行的条件是_______。
(2)500℃时,向体积为VL的恒容密闭容器中充入1mol (g)和3mol
(g)和3mol  (g)发生上述反应。初始时体系压强为100kPa,平衡时,CO的选择性为50%,
(g)发生上述反应。初始时体系压强为100kPa,平衡时,CO的选择性为50%, 的转化率为80%。(CO的选择性=
的转化率为80%。(CO的选择性= )
)
①反应Ⅰ的
_______ (列出计算式即可)。反应Ⅰ的标准平衡常数 ,其中
,其中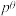 为标准压强100kPa,p(X)为气体X的平衡分压,分压=总压×该气体的物质的量分数。
为标准压强100kPa,p(X)为气体X的平衡分压,分压=总压×该气体的物质的量分数。
②在下图中画出500℃时,乙醇平衡转化率随[ ]变化而变化的情况
]变化而变化的情况_______ 。 的平衡产率与温度、起始时
的平衡产率与温度、起始时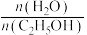 关系如图所示,每条曲线表示
关系如图所示,每条曲线表示 相同的平衡产率。
相同的平衡产率。 的平衡产率:Q点
的平衡产率:Q点_______ N点(填“>”、“=”或“<”);
②M、N两点 的平衡产率相等的原因是
的平衡产率相等的原因是_______ 。
(4)氢气的应用:氢气熔融碳酸盐燃料电池工作原理如图所示。 和
和 经催化重整生成CO和
经催化重整生成CO和 ,CO和
,CO和 全部进入电极A发生反应,写出负极的电极反应式(用一个总方程式表示)
全部进入电极A发生反应,写出负极的电极反应式(用一个总方程式表示)_______ 。
②理论上负极生成的 与正极消耗的
与正极消耗的 的物质的量之比是
的物质的量之比是_______ 。
 。主要发生以下反应:
。主要发生以下反应:反应Ⅰ:

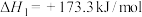
反应Ⅱ:

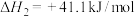
(1)反应Ⅰ自发进行的条件是_______。
| A.低温 | B.高温 | C.低压 | D.高压 |
(2)500℃时,向体积为VL的恒容密闭容器中充入1mol
 (g)和3mol
(g)和3mol  (g)发生上述反应。初始时体系压强为100kPa,平衡时,CO的选择性为50%,
(g)发生上述反应。初始时体系压强为100kPa,平衡时,CO的选择性为50%, 的转化率为80%。(CO的选择性=
的转化率为80%。(CO的选择性= )
)①反应Ⅰ的

 ,其中
,其中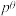 为标准压强100kPa,p(X)为气体X的平衡分压,分压=总压×该气体的物质的量分数。
为标准压强100kPa,p(X)为气体X的平衡分压,分压=总压×该气体的物质的量分数。②在下图中画出500℃时,乙醇平衡转化率随[
 ]变化而变化的情况
]变化而变化的情况
 的平衡产率与温度、起始时
的平衡产率与温度、起始时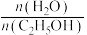 关系如图所示,每条曲线表示
关系如图所示,每条曲线表示 相同的平衡产率。
相同的平衡产率。
 的平衡产率:Q点
的平衡产率:Q点②M、N两点
 的平衡产率相等的原因是
的平衡产率相等的原因是(4)氢气的应用:氢气熔融碳酸盐燃料电池工作原理如图所示。

 和
和 经催化重整生成CO和
经催化重整生成CO和 ,CO和
,CO和 全部进入电极A发生反应,写出负极的电极反应式(用一个总方程式表示)
全部进入电极A发生反应,写出负极的电极反应式(用一个总方程式表示)②理论上负极生成的
 与正极消耗的
与正极消耗的 的物质的量之比是
的物质的量之比是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】甲醛(HCHO)是一种重要的化工产品,工业上可用甲醇脱氢法制备,相关反应方程式为:CH3OH(g)  HCHO(g)+H2(g) △H=+akJ/mol回答下列问题:
HCHO(g)+H2(g) △H=+akJ/mol回答下列问题:
(1)反应过程中需要向体系中通入空气,通过以下反应提供上述反应所需要的热量:H2(g)+ O2(g)=H2O(g) △H=-bkJ/mol
O2(g)=H2O(g) △H=-bkJ/mol
要使反应温度维持在650℃,则进料时,甲醇和空气的体积比应为___ (已知空气中氧气的体积分数为20%,b>a)。
(2)Na2CO3是甲醇脱氢制甲醛的催化剂,有研究指出,催化反应的部分机理如下:
历程i:CH30H→・H+・CH2OH(・H叫做氢自由基,实际上就是H原子,有很高的反应活性,
“・”代表有一个单电子可以参与配对成键)
历程ii:・CH2OH→・H+HCHO
历程iii:・CH2OH→3•H+CO
历程iv:自由基发生碰撞形成新化学键而湮灭
如图1所示为在体积为2L的恒容容器中,投入1molCH3OH(g),在碳酸钠催化剂作用下开始反应,20min后,测得甲醇的转化率(X)与甲醛的选择性(S)与温度的关系(副反应仅考虑CH3OH CO+2H2):
CO+2H2):

①请在图2所给坐标中,画出历程iv的反应过程一能量变化示意图___ 。
②下列说法合理的是__ 。
a.升高温度,甲醇转化率提高,平衡常数变大
b.当体系气体密度保持不变时,达到平衡状态
c.及时分离产品有利于提高甲醇生成甲醛的转化率
③600℃时,前20min甲醇的平均反应速率为__ ,此时生成甲醛的反应的Qp=___ (Qp的表达式与平衡常数Kp相同,p为物质的分压,分压=总压×物质的量分数,体系初始压强为P0)
④650℃以后,甲醛的选择性降低,而甲醇的转化率升高的可能原因是___ 。
(3)氧化剂可处理甲醛污染,结合以下图象分析夏季(水温约20℃)应急处理甲醛污染的水源最好应选择的试剂为____ 。

 HCHO(g)+H2(g) △H=+akJ/mol回答下列问题:
HCHO(g)+H2(g) △H=+akJ/mol回答下列问题:(1)反应过程中需要向体系中通入空气,通过以下反应提供上述反应所需要的热量:H2(g)+
 O2(g)=H2O(g) △H=-bkJ/mol
O2(g)=H2O(g) △H=-bkJ/mol要使反应温度维持在650℃,则进料时,甲醇和空气的体积比应为
(2)Na2CO3是甲醇脱氢制甲醛的催化剂,有研究指出,催化反应的部分机理如下:
历程i:CH30H→・H+・CH2OH(・H叫做氢自由基,实际上就是H原子,有很高的反应活性,
“・”代表有一个单电子可以参与配对成键)
历程ii:・CH2OH→・H+HCHO
历程iii:・CH2OH→3•H+CO
历程iv:自由基发生碰撞形成新化学键而湮灭
如图1所示为在体积为2L的恒容容器中,投入1molCH3OH(g),在碳酸钠催化剂作用下开始反应,20min后,测得甲醇的转化率(X)与甲醛的选择性(S)与温度的关系(副反应仅考虑CH3OH
 CO+2H2):
CO+2H2):
①请在图2所给坐标中,画出历程iv的反应过程一能量变化示意图
②下列说法合理的是
a.升高温度,甲醇转化率提高,平衡常数变大
b.当体系气体密度保持不变时,达到平衡状态
c.及时分离产品有利于提高甲醇生成甲醛的转化率
③600℃时,前20min甲醇的平均反应速率为
④650℃以后,甲醛的选择性降低,而甲醇的转化率升高的可能原因是
(3)氧化剂可处理甲醛污染,结合以下图象分析夏季(水温约20℃)应急处理甲醛污染的水源最好应选择的试剂为

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
真题
解题方法
【推荐3】主要成分为 的工业废气的回收利用有重要意义。
的工业废气的回收利用有重要意义。
(1)回收单质硫。将三分之一的 燃烧,产生的
燃烧,产生的 与其余
与其余 混合后反应:
混合后反应: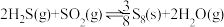 。在某温度下达到平衡,测得密闭系统中各组分浓度分别为
。在某温度下达到平衡,测得密闭系统中各组分浓度分别为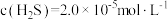 、
、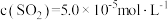 、
、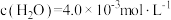 ,计算该温度下的平衡常数
,计算该温度下的平衡常数
_______ 。
(2)热解 制
制 。根据文献,将
。根据文献,将 和
和 的混合气体导入石英管反应器热解(一边进料,另一边出料),发生如下反应:
的混合气体导入石英管反应器热解(一边进料,另一边出料),发生如下反应:
Ⅰ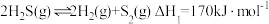
Ⅱ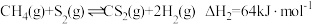
总反应:
Ⅲ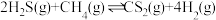
投料按体积之比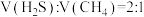 ,并用
,并用 稀释;常压,不同温度下反应相同时间后,测得
稀释;常压,不同温度下反应相同时间后,测得 和
和 体积分数如下表:
体积分数如下表:
请回答:
①反应Ⅲ能自发进行的条件是_______ 。
②下列说法正确的是_______ 。
A.其他条件不变时,用Ar替代 作稀释气体,对实验结果几乎无影响
作稀释气体,对实验结果几乎无影响
B.其他条件不变时,温度越高, 的转化率越高
的转化率越高
C.由实验数据推出 中的
中的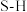 键强于
键强于 中的
中的 键
键
D.恒温恒压下,增加 的体积分数,
的体积分数, 的浓度升高
的浓度升高
③若将反应Ⅲ看成由反应Ⅰ和反应Ⅱ两步进行,画出由反应原料经两步生成产物的反应过程能量示意图_______ 。

④在 ,常压下,保持通入的
,常压下,保持通入的 体积分数不变,提高投料比
体积分数不变,提高投料比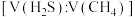 ,
, 的转化率不变,原因是
的转化率不变,原因是_______ 。
⑤在 范围内(其他条件不变),
范围内(其他条件不变), 的体积分数随温度升高发生变化,写出该变化规律并分析原因
的体积分数随温度升高发生变化,写出该变化规律并分析原因_______ 。
 的工业废气的回收利用有重要意义。
的工业废气的回收利用有重要意义。(1)回收单质硫。将三分之一的
 燃烧,产生的
燃烧,产生的 与其余
与其余 混合后反应:
混合后反应: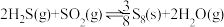 。在某温度下达到平衡,测得密闭系统中各组分浓度分别为
。在某温度下达到平衡,测得密闭系统中各组分浓度分别为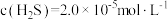 、
、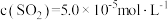 、
、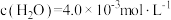 ,计算该温度下的平衡常数
,计算该温度下的平衡常数
(2)热解
 制
制 。根据文献,将
。根据文献,将 和
和 的混合气体导入石英管反应器热解(一边进料,另一边出料),发生如下反应:
的混合气体导入石英管反应器热解(一边进料,另一边出料),发生如下反应:Ⅰ
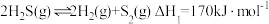
Ⅱ
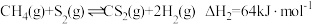
总反应:
Ⅲ
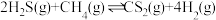
投料按体积之比
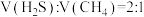 ,并用
,并用 稀释;常压,不同温度下反应相同时间后,测得
稀释;常压,不同温度下反应相同时间后,测得 和
和 体积分数如下表:
体积分数如下表:温度/ | 950 | 1000 | 1050 | 1100 | 1150 |
 | 0.5 | 1.5 | 3.6 | 5.5 | 8.5 |
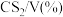 | 0.0 | 0.0 | 0.1 | 0.4 | 1.8 |
①反应Ⅲ能自发进行的条件是
②下列说法正确的是
A.其他条件不变时,用Ar替代
 作稀释气体,对实验结果几乎无影响
作稀释气体,对实验结果几乎无影响B.其他条件不变时,温度越高,
 的转化率越高
的转化率越高C.由实验数据推出
 中的
中的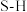 键强于
键强于 中的
中的 键
键D.恒温恒压下,增加
 的体积分数,
的体积分数, 的浓度升高
的浓度升高③若将反应Ⅲ看成由反应Ⅰ和反应Ⅱ两步进行,画出由反应原料经两步生成产物的反应过程能量示意图

④在
 ,常压下,保持通入的
,常压下,保持通入的 体积分数不变,提高投料比
体积分数不变,提高投料比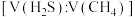 ,
, 的转化率不变,原因是
的转化率不变,原因是⑤在
 范围内(其他条件不变),
范围内(其他条件不变), 的体积分数随温度升高发生变化,写出该变化规律并分析原因
的体积分数随温度升高发生变化,写出该变化规律并分析原因
您最近一年使用:0次
【推荐1】氢能作为公认的清洁能源正在脱颖而出,我国在氢能的开发和利用上处于世界领先水平。回答下列问题:
Ⅰ.已知:① C(s) + H2O(g) CO(g) + H2(g) ΔH1= +131.4 kJ/mol
CO(g) + H2(g) ΔH1= +131.4 kJ/mol
② CO(g) + H2O(g) CO2(g) + H2(g) ΔH2= - 41.2 kJ/ mol
CO2(g) + H2(g) ΔH2= - 41.2 kJ/ mol
(1)写出C与CO2反应的热化学方程式___________ ;
(2)一定温度下,向恒容密闭容器中加入适量焦炭和水蒸气发生反应①,下列事实能说明其一定达到平衡状态的是___________ ;
a.容器内气体密度不再改变
b.CO与H2的物质的量之比不再改变
c.消耗0.1 mol H2O同时生成0.1 mol CO
d. 容器内气体的平均摩尔质量不再改变
(3)一定温度下,向10 L恒容密闭容器中充入1 mol CO和1 mol H2O(g)发生反应②,5 min达到平衡。用CO表示的正反应速率与时间的变化关系如图所示。

5min时,反应放出热量___________ , 平衡体系中H2的体积分数为___________ , CO的平衡转化率为___________ 。
Ⅱ.氢氧碱性燃料电池在航天、汽车等领域成功应用,其装置示意图如图所示。

(4)正极的电极反应式为___________ ;
(5)若放电后电池中KOH溶液的密度为ρ1 g·cm-3、质量分数为w。取55.0 mL该溶液与50.0 mL等浓度的盐酸混合,所得混合溶液的密度为ρ2g·cm-3、比热容为c J·(kg·℃)-1,混合后溶液温度升高了t ℃。假设溶液体积可以相加,则由此计算出反应的中和热ΔH=___________ kJ/mol(用代数式表示)。
Ⅰ.已知:① C(s) + H2O(g)
 CO(g) + H2(g) ΔH1= +131.4 kJ/mol
CO(g) + H2(g) ΔH1= +131.4 kJ/mol② CO(g) + H2O(g)
 CO2(g) + H2(g) ΔH2= - 41.2 kJ/ mol
CO2(g) + H2(g) ΔH2= - 41.2 kJ/ mol(1)写出C与CO2反应的热化学方程式
(2)一定温度下,向恒容密闭容器中加入适量焦炭和水蒸气发生反应①,下列事实能说明其一定达到平衡状态的是
a.容器内气体密度不再改变
b.CO与H2的物质的量之比不再改变
c.消耗0.1 mol H2O同时生成0.1 mol CO
d. 容器内气体的平均摩尔质量不再改变
(3)一定温度下,向10 L恒容密闭容器中充入1 mol CO和1 mol H2O(g)发生反应②,5 min达到平衡。用CO表示的正反应速率与时间的变化关系如图所示。

5min时,反应放出热量
Ⅱ.氢氧碱性燃料电池在航天、汽车等领域成功应用,其装置示意图如图所示。

(4)正极的电极反应式为
(5)若放电后电池中KOH溶液的密度为ρ1 g·cm-3、质量分数为w。取55.0 mL该溶液与50.0 mL等浓度的盐酸混合,所得混合溶液的密度为ρ2g·cm-3、比热容为c J·(kg·℃)-1,混合后溶液温度升高了t ℃。假设溶液体积可以相加,则由此计算出反应的中和热ΔH=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】研究 的利用对促进低碳社会的构建具有重要意义。工业上利用废气中的
的利用对促进低碳社会的构建具有重要意义。工业上利用废气中的 合成
合成 ,主要有以下反应:
,主要有以下反应:
反应Ⅰ:
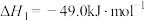

反应Ⅱ:


反应Ⅲ: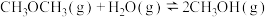

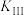
(1)已知某些化学键的键能数据如下:
氢气中的 键比甲醇中的
键比甲醇中的 键
键_______ (填“强”或“弱”)。用盖斯定律计算反应Ⅱ中的
_______  。
。
(2)同一温度下,反应Ⅱ的平衡常数
_______ (用含 、
、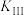 的代数式表示)。
的代数式表示)。
(3)在T℃时,甲、乙、丙三个2L的恒容密闭容器中,按不同方式投入反应物发生反应Ⅰ,测得平衡时有关数据如下:
①甲容器10s达到平衡时测得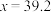 ,则0~10s时间段内甲中
,则0~10s时间段内甲中 的平均反应速率为
的平均反应速率为_______ 。
②下列说法正确的是_______ (填标号)。
A. B.
B. C.
C.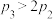 D.
D.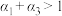
(4)在 ℃下,将
℃下,将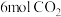 和
和 充入3L的恒容密闭容器中发生反应Ⅰ、Ⅱ,5min后反应达到平衡状态,此时
充入3L的恒容密闭容器中发生反应Ⅰ、Ⅱ,5min后反应达到平衡状态,此时 的物质的量为2mol,
的物质的量为2mol, 的物质的量为0.5mol;则
的物质的量为0.5mol;则 ℃时反应Ⅰ的平衡常数
℃时反应Ⅰ的平衡常数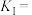
_______ (保留三位有效数字)。
(5)在恒容、 ℃下,发生反应
℃下,发生反应 ,下列物理量不再发生变化时,能说明反应达到平衡状态的是_______(填标号)。
,下列物理量不再发生变化时,能说明反应达到平衡状态的是_______(填标号)。
(6)一种碱性“二甲醚 燃料电池”具有启动快、能量密度高、效率高等优点;其电池负极反应式为
燃料电池”具有启动快、能量密度高、效率高等优点;其电池负极反应式为_______ 。
 的利用对促进低碳社会的构建具有重要意义。工业上利用废气中的
的利用对促进低碳社会的构建具有重要意义。工业上利用废气中的 合成
合成 ,主要有以下反应:
,主要有以下反应:反应Ⅰ:

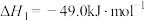

反应Ⅱ:



反应Ⅲ:
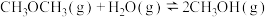

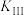
(1)已知某些化学键的键能数据如下:
| 化学键 |  |  |  |
键能 | 750 | 343 | 465 |
氢气中的
 键比甲醇中的
键比甲醇中的 键
键
 。
。(2)同一温度下,反应Ⅱ的平衡常数

 、
、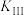 的代数式表示)。
的代数式表示)。(3)在T℃时,甲、乙、丙三个2L的恒容密闭容器中,按不同方式投入反应物发生反应Ⅰ,测得平衡时有关数据如下:
| 容器 | 甲 | 乙 | 丙 | |
| 起始反应物投入量 |  、 、 | 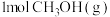 、 、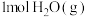 |  、 、 | |
| 平衡数据 |  |  |  | 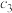 |
| 反应的能量变化/kJ | x | y | z | |
| 体系压强/Pa |  |  |  | |
| 反应物转化率 |  |  |  | |
①甲容器10s达到平衡时测得
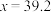 ,则0~10s时间段内甲中
,则0~10s时间段内甲中 的平均反应速率为
的平均反应速率为②下列说法正确的是
A.
 B.
B. C.
C.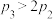 D.
D.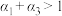
(4)在
 ℃下,将
℃下,将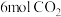 和
和 充入3L的恒容密闭容器中发生反应Ⅰ、Ⅱ,5min后反应达到平衡状态,此时
充入3L的恒容密闭容器中发生反应Ⅰ、Ⅱ,5min后反应达到平衡状态,此时 的物质的量为2mol,
的物质的量为2mol, 的物质的量为0.5mol;则
的物质的量为0.5mol;则 ℃时反应Ⅰ的平衡常数
℃时反应Ⅰ的平衡常数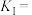
(5)在恒容、
 ℃下,发生反应
℃下,发生反应 ,下列物理量不再发生变化时,能说明反应达到平衡状态的是_______(填标号)。
,下列物理量不再发生变化时,能说明反应达到平衡状态的是_______(填标号)。| A.二氧化碳的浓度 | B.容器中的压强 |
| C.气体的密度 | D. 与 与 的物质的量之比 的物质的量之比 |
 燃料电池”具有启动快、能量密度高、效率高等优点;其电池负极反应式为
燃料电池”具有启动快、能量密度高、效率高等优点;其电池负极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】热解耦合化学链制氢工艺是一种将生物质废物转变为高纯H2的环境友好型技术路线,如图1。

(1)在燃料反应器中,研究人员对纯CO作为燃料气与铁基载氧体(Fe2O3)的还原反应进行了理论研究,得到了还原阶段CO平衡浓度和固体成分随温度变化的图象,如图2(m、n、p、q均为正值)。

已知:a.3Fe2O3(s)+CO(g) 2Fe3O4(s)+CO2(g) △H1=-mkJ/mol
2Fe3O4(s)+CO2(g) △H1=-mkJ/mol
b.Fe3O4(s)+CO(g) 3FeO(s)+CO2(g) △H2=+nkJ/mol
3FeO(s)+CO2(g) △H2=+nkJ/mol
c.FeO(s)+CO(g) Fe(s)+CO2(g) △H3=-qkJ/mol
Fe(s)+CO2(g) △H3=-qkJ/mol
d.Fe3O4(s)+4CO(g) 3Fe(s)+4CO2(g) △H4=-pkJ/mol
3Fe(s)+4CO2(g) △H4=-pkJ/mol
①反应 Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)的△H=
2Fe(s)+3CO2(g)的△H= _______ kJ/mol(用 m、n、q表示)。
②当温度低于300℃时,燃料还原阶段得到的固体主要是Fe和_______ 。
③曲线L3代表的反应为_______ (填“b”或“c”),曲线L2随温度升高而降低的原因是_______ 。
(2)在蒸汽反应器中,研究表明:压强对出口气体百分含量的影响不大,其原因是_______ 。
(3)纯CO作燃料气反应时发生歧化反应[2CO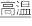 C(s)+CO2]使铁基载氧体的固定床内大量积碳。对CO歧化反应进行独立研究:t℃时,标准压强下进行该反应,标准平衡常数
C(s)+CO2]使铁基载氧体的固定床内大量积碳。对CO歧化反应进行独立研究:t℃时,标准压强下进行该反应,标准平衡常数 ,其中标准压强(P)=100kPa,分压(P)=总压(Pθ)×物质的量分数。向一恒温恒压容器中通入2molCO,测得平衡后CO2的物质的量为为0.5mol,该条件下的Kpθ=
,其中标准压强(P)=100kPa,分压(P)=总压(Pθ)×物质的量分数。向一恒温恒压容器中通入2molCO,测得平衡后CO2的物质的量为为0.5mol,该条件下的Kpθ=_______ 。对于反应2CO(g) C(s)+CO2(g),下列物理量或说法不能用来判断反应达到平衡的是
C(s)+CO2(g),下列物理量或说法不能用来判断反应达到平衡的是 _______ 。(填标号)。
A.气体平均相对分子质量 B.气体的密度(恒温恒压)
C.CO的消耗速率等于2倍的CO2生成速率 D.C(s)的质量
(4)CO深度还原Fe2O3的过程为:Fe2O3 Fe2O2.55
Fe2O2.55 Fe2O2
Fe2O2 Fe2O1.5
Fe2O1.5 Fe2O。该过程中,在不同铁基载氧体(FexOy)表面的能垒变化如下图所示:CO在各表面稳定吸附为初始状态(IS),CO2从各表面脱附进入气相为最终状态(FS)。
Fe2O。该过程中,在不同铁基载氧体(FexOy)表面的能垒变化如下图所示:CO在各表面稳定吸附为初始状态(IS),CO2从各表面脱附进入气相为最终状态(FS)。

①在I表面上CO转化成CO2的反应路径分三步:
i)*+CO→CO*;(*为活性点位);
ii)CO*+O*→*COO*;
iii)_______ 。
②CO在_______ 表面反应释放CO2的速率最快(填“I”、“II”、“III”或“IV”);释放等量CO2时,在_______ 表面反应放出能量最多(填"I”、“II”、“III”或“IV”)。

(1)在燃料反应器中,研究人员对纯CO作为燃料气与铁基载氧体(Fe2O3)的还原反应进行了理论研究,得到了还原阶段CO平衡浓度和固体成分随温度变化的图象,如图2(m、n、p、q均为正值)。

已知:a.3Fe2O3(s)+CO(g)
 2Fe3O4(s)+CO2(g) △H1=-mkJ/mol
2Fe3O4(s)+CO2(g) △H1=-mkJ/molb.Fe3O4(s)+CO(g)
 3FeO(s)+CO2(g) △H2=+nkJ/mol
3FeO(s)+CO2(g) △H2=+nkJ/molc.FeO(s)+CO(g)
 Fe(s)+CO2(g) △H3=-qkJ/mol
Fe(s)+CO2(g) △H3=-qkJ/mold.Fe3O4(s)+4CO(g)
 3Fe(s)+4CO2(g) △H4=-pkJ/mol
3Fe(s)+4CO2(g) △H4=-pkJ/mol①反应 Fe2O3(s)+3CO(g)
 2Fe(s)+3CO2(g)的△H=
2Fe(s)+3CO2(g)的△H= ②当温度低于300℃时,燃料还原阶段得到的固体主要是Fe和
③曲线L3代表的反应为
(2)在蒸汽反应器中,研究表明:压强对出口气体百分含量的影响不大,其原因是
(3)纯CO作燃料气反应时发生歧化反应[2CO
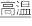 C(s)+CO2]使铁基载氧体的固定床内大量积碳。对CO歧化反应进行独立研究:t℃时,标准压强下进行该反应,标准平衡常数
C(s)+CO2]使铁基载氧体的固定床内大量积碳。对CO歧化反应进行独立研究:t℃时,标准压强下进行该反应,标准平衡常数 ,其中标准压强(P)=100kPa,分压(P)=总压(Pθ)×物质的量分数。向一恒温恒压容器中通入2molCO,测得平衡后CO2的物质的量为为0.5mol,该条件下的Kpθ=
,其中标准压强(P)=100kPa,分压(P)=总压(Pθ)×物质的量分数。向一恒温恒压容器中通入2molCO,测得平衡后CO2的物质的量为为0.5mol,该条件下的Kpθ= C(s)+CO2(g),下列物理量或说法不能用来判断反应达到平衡的是
C(s)+CO2(g),下列物理量或说法不能用来判断反应达到平衡的是 A.气体平均相对分子质量 B.气体的密度(恒温恒压)
C.CO的消耗速率等于2倍的CO2生成速率 D.C(s)的质量
(4)CO深度还原Fe2O3的过程为:Fe2O3
 Fe2O2.55
Fe2O2.55 Fe2O2
Fe2O2 Fe2O1.5
Fe2O1.5 Fe2O。该过程中,在不同铁基载氧体(FexOy)表面的能垒变化如下图所示:CO在各表面稳定吸附为初始状态(IS),CO2从各表面脱附进入气相为最终状态(FS)。
Fe2O。该过程中,在不同铁基载氧体(FexOy)表面的能垒变化如下图所示:CO在各表面稳定吸附为初始状态(IS),CO2从各表面脱附进入气相为最终状态(FS)。
①在I表面上CO转化成CO2的反应路径分三步:
i)*+CO→CO*;(*为活性点位);
ii)CO*+O*→*COO*;
iii)
②CO在
您最近一年使用:0次



