可逆反应A(g)+B(g) 2C(g)在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示。
2C(g)在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示。
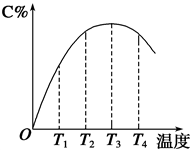
(1)由T1向T2变化时,正反应速率_______ 逆反应速率(填“>”“<”或“=”)。
(2)由T3向T4变化时,正反应速率_______ 逆反应速率(填“>”“<”或“=”)。
(3)反应在_________ 温度下达到平衡。
(4)此反应的正反应为_______ 热反应。
 2C(g)在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示。
2C(g)在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示。
(1)由T1向T2变化时,正反应速率
(2)由T3向T4变化时,正反应速率
(3)反应在
(4)此反应的正反应为
更新时间:2017-11-02 15:23:52
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】汽车让人们的生活越来越便捷。请回答以下问题:
(1)汽车尾气主要含有CO2、CO、SO2、NO等物质,是造成城市空气污染的主要因素之一,N2和O2反应生成NO的能量变化如图所示,则由该反应生成1mol NO时,应___________ (填“释放”或“吸收”)___________ kJ能量。
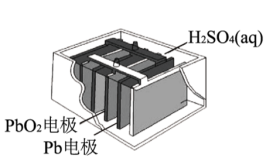
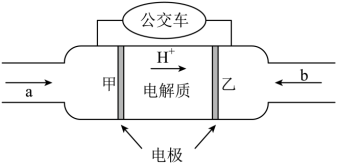
(3)近年来广州首批15辆氢燃料电池公交车已经投入运营,标志着广州公交进入氢能产业时代,如图是某种氢氧燃料电池的内部结构示意图,该电池工作时,氢气从___________ (填“a”或“b”)处通入,正极反应方程式为___________ ,标况下消耗11.2L空气,整个电路中转移的电子数约为___________ NA。___________ ,负极电极反应式为___________ 。
(1)汽车尾气主要含有CO2、CO、SO2、NO等物质,是造成城市空气污染的主要因素之一,N2和O2反应生成NO的能量变化如图所示,则由该反应生成1mol NO时,应




| A.NaN3属于离子化合物 |
| B.NaN3的分解反应属于吸热反应 |
| C.E1表示2mol NaN3固体的能量 |
| D.NaN3作为安全气囊的气体发生剂,具有产气快、产气量大等优点 |
(3)近年来广州首批15辆氢燃料电池公交车已经投入运营,标志着广州公交进入氢能产业时代,如图是某种氢氧燃料电池的内部结构示意图,该电池工作时,氢气从
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学使我们的生活更加美好。使用自热材料的暖贴、自热食品极大的方便了人们的生活。
(1)自热材料是利用化学反应原理,将_____ 能转化为热能供人们使用。一般利用原电池原理来_____ (“加快”或“减慢”)放热速度。
(2)暖贴中自热材料的主要化学成分有:铁粉、炭粉、氯化钠固体、其他辅助成分及保温材料等,并用可控制氧气透过速率的无纺布包装。在工作时,铁粉与炭粉形成原电池反应,该反应过程中的能量变化关系图中,正确的是______ 。

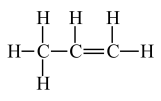
(3)控制适当的氧气透过速率,使暖贴保持一个适合人体的温度,无纺布非常重要。制作无纺布的原料为丙烯,丙烯结构如图。关于丙烯分子内 的相互作用有______ 。
A.共价键 B.离子键 C.范德华力 D.氢键
(4)自热食品的自热材料中,除有暖贴当中的成分外,还有生石灰、铝粉、碳酸钠等,仍用无纺布包装。使用时先加适量的水。开始时有放热的非氧化还原反应发生,其化学方程式为_____ 。然后会形成强碱性溶液,并进一步发生剧烈反应,并产生一种易燃易爆的气体,大量放热,将食品煮熟。该反应的离子方程式为:_______ 。商家为保证迅速放热,采取了以下哪些加速反应的措施:_____ 。
①形成原电池反应 ②将铝粒制成铝粉 ③增大压强 ④使用催化剂
(1)自热材料是利用化学反应原理,将
(2)暖贴中自热材料的主要化学成分有:铁粉、炭粉、氯化钠固体、其他辅助成分及保温材料等,并用可控制氧气透过速率的无纺布包装。在工作时,铁粉与炭粉形成原电池反应,该反应过程中的能量变化关系图中,正确的是

(3)控制适当的氧气透过速率,使暖贴保持一个适合人体的温度,无纺布非常重要。制作无纺布的原料为丙烯,丙烯结构如图。关于丙烯分子

A.共价键 B.离子键 C.范德华力 D.氢键
(4)自热食品的自热材料中,除有暖贴当中的成分外,还有生石灰、铝粉、碳酸钠等,仍用无纺布包装。使用时先加适量的水。开始时有放热的非氧化还原反应发生,其化学方程式为
①形成原电池反应 ②将铝粒制成铝粉 ③增大压强 ④使用催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)在一定条件下,氢气在氯气中燃烧的热化学方程式:H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6kJ·mol-1;该反应属于___________ (填“热吸”或“放热”)反应。
(2)常温常压下,1mol乙醇(C2H5OH)完全燃烧生成CO2气体和液态水放出的热量为1367kJ,写出表示乙醇燃烧热的热化学方程式:___________ 。
(3)根据盖斯定律计算:
P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ·mol-1 ①
P(红磷,s)+ O2(g)=
O2(g)= P4O10(s) ΔH=-738.5kJ·mol-1 ②
P4O10(s) ΔH=-738.5kJ·mol-1 ②
则白磷转化为红磷的热化学方程式为___________ 。
(4)已知破坏1mol H−H键、1mol I−I键、1 mol H−I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘单质反应生成2 mol HI需要放出___________ kJ的热量。
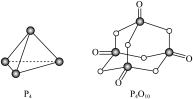
(5)白磷与氧可发生如下反应:P4+5O2=P4O10,已知断裂下列化学键需要吸收的能量分别为:P−P键 a kJ·mol-1、P−O键bkJ·mol-1、P=O键ckJ·mol-1、O=O键dkJ·mol-1。根据图示的分子结构和有关数据计算该反应的反应热为___________ 。
(1)在一定条件下,氢气在氯气中燃烧的热化学方程式:H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6kJ·mol-1;该反应属于
(2)常温常压下,1mol乙醇(C2H5OH)完全燃烧生成CO2气体和液态水放出的热量为1367kJ,写出表示乙醇燃烧热的热化学方程式:
(3)根据盖斯定律计算:
P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ·mol-1 ①
P(红磷,s)+
 O2(g)=
O2(g)= P4O10(s) ΔH=-738.5kJ·mol-1 ②
P4O10(s) ΔH=-738.5kJ·mol-1 ②则白磷转化为红磷的热化学方程式为
(4)已知破坏1mol H−H键、1mol I−I键、1 mol H−I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘单质反应生成2 mol HI需要放出
(5)白磷与氧可发生如下反应:P4+5O2=P4O10,已知断裂下列化学键需要吸收的能量分别为:P−P键 a kJ·mol-1、P−O键bkJ·mol-1、P=O键ckJ·mol-1、O=O键dkJ·mol-1。根据图示的分子结构和有关数据计算该反应的反应热为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】工业制硫酸,利用催化氧化反应将SO2转化为SO3是一个关键步骤。请回答:
(1)某温度下,SO2(g)+ O2(g)
O2(g) SO3(g) ΔH=-98kJ·mol-1。开始时在100L的密闭容器中加入4.00molSO2(g)和10.00molO2(g),当反应达到平衡时共放出热量196.00kJ,该温度下平衡常数K=
SO3(g) ΔH=-98kJ·mol-1。开始时在100L的密闭容器中加入4.00molSO2(g)和10.00molO2(g),当反应达到平衡时共放出热量196.00kJ,该温度下平衡常数K=__ (精确到小数点后2位)。
(2)一定条件下,向一带活塞的密闭容器中充入2molSO2和1molO2,发生下列反应:2SO2(g)+O2(g) 2SO3(g),达到平衡后改变下述条件,SO2、O2、SO3气体平衡浓度都比原来增大的是
2SO3(g),达到平衡后改变下述条件,SO2、O2、SO3气体平衡浓度都比原来增大的是___ (填字母)。
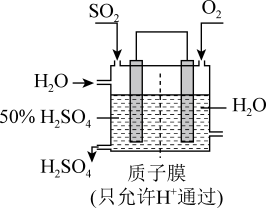
(3)某人设想以如图所示装置用电化学原理生产硫酸,写出通入SO2的电极的电极反应式:___ 。
(4)下列关于2SO2(g)+O2(g) 2SO3(g)反应的图象中,一定正确的是
2SO3(g)反应的图象中,一定正确的是___ (填序号)。
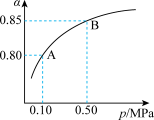
(5)①某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如图所示。当平衡状态由A变到B时,平衡常数K(A)__ K(B)(填“>”、“<"或“=”)。
②将一定量的SO2(g)和O2(g)充入某固定体积的密闭容器中,在一定条件下,c(SO3)的变化如图所示。若在第5分钟将容器的体积缩小一半后,在第8分钟达到新的平衡(此时SO3的浓度为0.25mol·L-1)。请在图中画出第5分钟至第9分钟SO3(g)浓度的变化曲线___ 。

(1)某温度下,SO2(g)+
 O2(g)
O2(g) SO3(g) ΔH=-98kJ·mol-1。开始时在100L的密闭容器中加入4.00molSO2(g)和10.00molO2(g),当反应达到平衡时共放出热量196.00kJ,该温度下平衡常数K=
SO3(g) ΔH=-98kJ·mol-1。开始时在100L的密闭容器中加入4.00molSO2(g)和10.00molO2(g),当反应达到平衡时共放出热量196.00kJ,该温度下平衡常数K=(2)一定条件下,向一带活塞的密闭容器中充入2molSO2和1molO2,发生下列反应:2SO2(g)+O2(g)
 2SO3(g),达到平衡后改变下述条件,SO2、O2、SO3气体平衡浓度都比原来增大的是
2SO3(g),达到平衡后改变下述条件,SO2、O2、SO3气体平衡浓度都比原来增大的是| A.保持温度和容器体积不变,充入2molSO3 |
| B.保持温度和容器体积不变,充入2molN2 |
| C.移动活塞压缩气体 |
| D.保持温度和容器内压强不变,充入1molSO3 |

(4)下列关于2SO2(g)+O2(g)
 2SO3(g)反应的图象中,一定正确的是
2SO3(g)反应的图象中,一定正确的是A.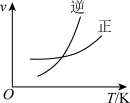 | B.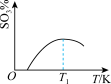 |
C.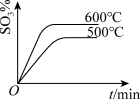 | D.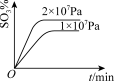 |

②将一定量的SO2(g)和O2(g)充入某固定体积的密闭容器中,在一定条件下,c(SO3)的变化如图所示。若在第5分钟将容器的体积缩小一半后,在第8分钟达到新的平衡(此时SO3的浓度为0.25mol·L-1)。请在图中画出第5分钟至第9分钟SO3(g)浓度的变化曲线

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知可逆反应为:CO(g)+H2O(g)⇌H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表:
(1)从表中的数据可以推断:此反应是___ (填“吸”或“放”)热反应。在830℃下开始时向恒容密闭容器中充入1molCO和2molH2O达到平衡后CO的转化率为_____ .
(2)在500℃,按照下表的物质的量(按照CO、H2O、H2、CO2的顺序)投入恒容密闭容器中进行上述反应,达到平衡后下列关系正确的是_____ .
A.2c1=c2=c3 B.2Q1=Q2=Q3 C.α1=α2=α3 D.α1+α2=1
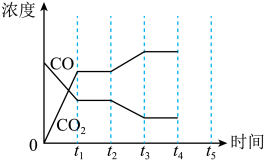
(3)如图表示此反应,在t1时刻达到平衡、在t2时刻因改变某个条件使浓度发生变化的情况:图中t2时刻发生改变的条件是__ (任写一种)
(1)从表中的数据可以推断:此反应是
| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
(2)在500℃,按照下表的物质的量(按照CO、H2O、H2、CO2的顺序)投入恒容密闭容器中进行上述反应,达到平衡后下列关系正确的是
| 实验编号 | 反应物投入量 | 平衡时H2浓度 | 吸收或放出的热量 | 反应物转化率 |
| 1 | 1、1、0、0 | c1 | Q1 | α1 |
| 2 | 0、0、2、2 | c2 | Q2 | α2 |
| 3 | 2、2、0、0 | c3 | Q3 | α3 |
(3)如图表示此反应,在t1时刻达到平衡、在t2时刻因改变某个条件使浓度发生变化的情况:图中t2时刻发生改变的条件是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】硫及其化合物在工农业生产中有着重要作用.回答下列问题
(1)工业制硫酸,接触室中发生反应的化学方程式为___________ 。下列可提高SO2平衡转化率的措施是___________ 。(填标号)
A.降低温度 B.减小压强 C.延长反应时间 D.增大O2的投料
(2)工业上可用Fe2(SO4)3溶液吸收SO2,该过程的离子方程式为________ 。为实现吸收液的再生,可通入_________ 。
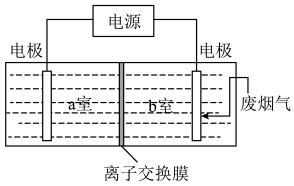
(3)用如图装置脱除废烟气中的SO2和废水中的Cu2+,该方法总反应的化学方程式为___________ 。含Cu2+的废水应置于___________ 室(填“a”或“b”)。
(1)工业制硫酸,接触室中发生反应的化学方程式为
A.降低温度 B.减小压强 C.延长反应时间 D.增大O2的投料
(2)工业上可用Fe2(SO4)3溶液吸收SO2,该过程的离子方程式为
(3)用如图装置脱除废烟气中的SO2和废水中的Cu2+,该方法总反应的化学方程式为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】汽车使用乙醇汽油并不能减少 的排放,某研究小组在实验室以耐高温试剂
的排放,某研究小组在实验室以耐高温试剂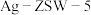 催化,测得
催化,测得 转化为
转化为 的转化率随温度变化情况如下图所示。
的转化率随温度变化情况如下图所示。
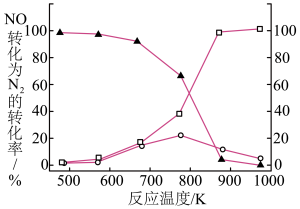
○无 时
时 直接分解为
直接分解为 的产率
的产率
▲ 剩余的百分率
剩余的百分率
□ 条件下,
条件下, 还原为
还原为 转化率
转化率
(1)在 条件下,最佳温度应控制在
条件下,最佳温度应控制在_______ 左右。
(2)若不使用 ,温度超过
,温度超过 ,发现
,发现 的分解率降低,其可能的原因为
的分解率降低,其可能的原因为_______ 。
(3)用平衡移动原理解释为什么加入 后
后 转化为
转化为 的转化率增大:
的转化率增大:_______ 。
 的排放,某研究小组在实验室以耐高温试剂
的排放,某研究小组在实验室以耐高温试剂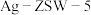 催化,测得
催化,测得 转化为
转化为 的转化率随温度变化情况如下图所示。
的转化率随温度变化情况如下图所示。
○无
 时
时 直接分解为
直接分解为 的产率
的产率▲
 剩余的百分率
剩余的百分率□
 条件下,
条件下, 还原为
还原为 转化率
转化率(1)在
 条件下,最佳温度应控制在
条件下,最佳温度应控制在(2)若不使用
 ,温度超过
,温度超过 ,发现
,发现 的分解率降低,其可能的原因为
的分解率降低,其可能的原因为(3)用平衡移动原理解释为什么加入
 后
后 转化为
转化为 的转化率增大:
的转化率增大:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮是大气中含量最多的气体,研究氮及其化合物对人类有重要的意义。
(1)合成氨的原理为:N2(g)+3H2 2NH3△H=-92.4kJ/mol
2NH3△H=-92.4kJ/mol
①将一定量的N2(g)和H2(g)放入1L的密闭容器中,在500℃、2×107Pa下达到平衡,平衡时测得N2为0.1 mol,H2为0.3 mol,NH3为0.1 mol。该条件下H2的转化率为______ 。
此温度下该反应的平衡常数K=__________ 。
②欲提高H2的转化率,下列措施可行的是___________ 。
a.向容器中按原比例再充入原料气
b.向容器中再充入惰性气体
c.改变反应的催化剂
d.液化生成物分离出氨
(2)在2L密闭容器中,800℃时反应2NO(g)+O2(g) 2NO2(g) △H<0体系中,各成分浓度随时间的变化如图:
2NO2(g) △H<0体系中,各成分浓度随时间的变化如图:
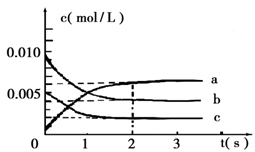
①用O2表示从0~2s内该反应的平均速率υ=___________ 。
②能说明该反应已经达到平衡状态的是_________ 。
a.υ(NO2)=2υ(O2)
b.容器内压强保持不变
c.υ逆(NO)=2υ正(O2)
d.容器内的密度保持不变
③为使该反应的反应速率增大,且平衡向正反应方向移动的是_________ 。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效的催化剂
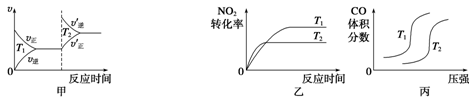
(3)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。4CO(g)+2NO2(g) 4CO2(g)+N2(g) ΔH=-1 200 kJ·mol-1对于该反应,温度不同(T2>T1)、其他条件相同时,下列图象正确的是
4CO2(g)+N2(g) ΔH=-1 200 kJ·mol-1对于该反应,温度不同(T2>T1)、其他条件相同时,下列图象正确的是______ (填代号)。
(1)合成氨的原理为:N2(g)+3H2
 2NH3△H=-92.4kJ/mol
2NH3△H=-92.4kJ/mol①将一定量的N2(g)和H2(g)放入1L的密闭容器中,在500℃、2×107Pa下达到平衡,平衡时测得N2为0.1 mol,H2为0.3 mol,NH3为0.1 mol。该条件下H2的转化率为
此温度下该反应的平衡常数K=
②欲提高H2的转化率,下列措施可行的是
a.向容器中按原比例再充入原料气
b.向容器中再充入惰性气体
c.改变反应的催化剂
d.液化生成物分离出氨
(2)在2L密闭容器中,800℃时反应2NO(g)+O2(g)
 2NO2(g) △H<0体系中,各成分浓度随时间的变化如图:
2NO2(g) △H<0体系中,各成分浓度随时间的变化如图:
①用O2表示从0~2s内该反应的平均速率υ=
②能说明该反应已经达到平衡状态的是
a.υ(NO2)=2υ(O2)
b.容器内压强保持不变
c.υ逆(NO)=2υ正(O2)
d.容器内的密度保持不变
③为使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效的催化剂
(3)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。4CO(g)+2NO2(g)
 4CO2(g)+N2(g) ΔH=-1 200 kJ·mol-1对于该反应,温度不同(T2>T1)、其他条件相同时,下列图象正确的是
4CO2(g)+N2(g) ΔH=-1 200 kJ·mol-1对于该反应,温度不同(T2>T1)、其他条件相同时,下列图象正确的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】环戊二烯(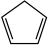 )是重要的有机化工原料,可通过反应
)是重要的有机化工原料,可通过反应 (g)+I2(g)
(g)+I2(g)
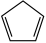 (g)+2HI(g)制得。回答下列问题。
(g)+2HI(g)制得。回答下列问题。
(1)某温度下,在固定容积的密闭容器中发生该反应,该反应达到平衡的标志是_______。
(2)1mol碘和1mol环戊烯( )在10L恒容容器内发生反应。
)在10L恒容容器内发生反应。
①不同温度下环戊烯的物质的量与反应时间的关系如图所示。
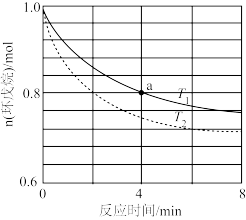
计算a点时,0-4分钟内HI的生成速率v=_______ mol·L-1·min-1。根据上图可得出 的理由是
的理由是_______ 。
②某温度下,若起始压强为 ,平衡时总压强增加了15%,环戊烯的转化率为
,平衡时总压强增加了15%,环戊烯的转化率为_______ ,该反应的平衡常数
_______ (列出计算表达式)。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
③欲增加环戊烯的平衡转化率,但K值不变,可采取的措施有_______ (填标号)。
A.通入惰性气体 B.增加碘浓度 C.增加环戊烯浓度 D.提高温度
 )是重要的有机化工原料,可通过反应
)是重要的有机化工原料,可通过反应 (g)+I2(g)
(g)+I2(g)
 (g)+2HI(g)制得。回答下列问题。
(g)+2HI(g)制得。回答下列问题。(1)某温度下,在固定容积的密闭容器中发生该反应,该反应达到平衡的标志是_______。
| A.容器内总压不变 | B.容器内气体颜色不变 |
| C.容器内气体密度不变 | D.生成1molC=C双键的同时生成2molH-I键 |
 )在10L恒容容器内发生反应。
)在10L恒容容器内发生反应。①不同温度下环戊烯的物质的量与反应时间的关系如图所示。

计算a点时,0-4分钟内HI的生成速率v=
 的理由是
的理由是②某温度下,若起始压强为
 ,平衡时总压强增加了15%,环戊烯的转化率为
,平衡时总压强增加了15%,环戊烯的转化率为
③欲增加环戊烯的平衡转化率,但K值不变,可采取的措施有
A.通入惰性气体 B.增加碘浓度 C.增加环戊烯浓度 D.提高温度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某温度时,在2L的密闭容器中,A、B、C三种气体的物质的量随时间的变化曲线如图所示。由图中数据分析
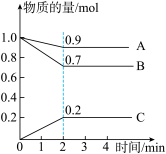
(1)该反应的反应物是_______ 。
(2)该反应_______ (填“是”或“不是”)可逆反应,原因是______________ 。写出该反应的化学方程式:_______ 。
(3)反应开始至2min时,用C表示的平均反应速率为_______ 。

(1)该反应的反应物是
(2)该反应
(3)反应开始至2min时,用C表示的平均反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有可逆反应.2NO2(g) N2O4(g),△H<0,试根据下列图像,判断t2、t3、t4时刻采取的措施。
N2O4(g),△H<0,试根据下列图像,判断t2、t3、t4时刻采取的措施。
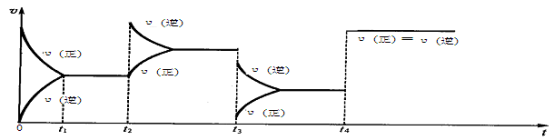
t2:_______________________________________________ ;
t3:_______________________________________________ ;
t4:_______________________________________________ 。
 N2O4(g),△H<0,试根据下列图像,判断t2、t3、t4时刻采取的措施。
N2O4(g),△H<0,试根据下列图像,判断t2、t3、t4时刻采取的措施。
t2:
t3:
t4:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知NO2和N2O4可以相互转化: 2NO2(g) N2O4(g) △H<0。现将一定量NO2和N2O4的混合气体通入一体积为2 L的恒温密闭容器中,物质浓度随时间变化关系如图所示,回答下列问题:
N2O4(g) △H<0。现将一定量NO2和N2O4的混合气体通入一体积为2 L的恒温密闭容器中,物质浓度随时间变化关系如图所示,回答下列问题:
(1)图中共有两条曲线X和Y,其中曲线________ 表示NO2浓度随时间的变化;a、b、c、d四个点中,表示化学反应处于平衡状态的点是________ 。
(2)反应进行至25 min时,曲线发生变化的原因是__________ ;前10 min内用NO2表示的化学反应速率 (NO2)=
(NO2)=______ mol/(L·min);d点的平衡常数的数值是___ (计算结果保留一位小数或分数表示)。
(3)恒温恒容条件下,下列选项一定可以判断反应2NO2(g) N2O4(g)达到平衡状态的依据有
N2O4(g)达到平衡状态的依据有______ ;
a.混合气体颜色不变 b.混合气体的密度保持不变
c. (NO2)=2
(NO2)=2 (N2O4) d.混合气体的平均相对分子质量保持不变
(N2O4) d.混合气体的平均相对分子质量保持不变
达到平衡状态后,恒温恒容条件下再充入一定量NO2,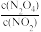 比值
比值_____ 选填“增大”、“减小”、“不变”)。
 N2O4(g) △H<0。现将一定量NO2和N2O4的混合气体通入一体积为2 L的恒温密闭容器中,物质浓度随时间变化关系如图所示,回答下列问题:
N2O4(g) △H<0。现将一定量NO2和N2O4的混合气体通入一体积为2 L的恒温密闭容器中,物质浓度随时间变化关系如图所示,回答下列问题: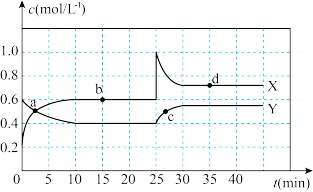
(1)图中共有两条曲线X和Y,其中曲线
(2)反应进行至25 min时,曲线发生变化的原因是
 (NO2)=
(NO2)=(3)恒温恒容条件下,下列选项一定可以判断反应2NO2(g)
 N2O4(g)达到平衡状态的依据有
N2O4(g)达到平衡状态的依据有a.混合气体颜色不变 b.混合气体的密度保持不变
c.
 (NO2)=2
(NO2)=2 (N2O4) d.混合气体的平均相对分子质量保持不变
(N2O4) d.混合气体的平均相对分子质量保持不变达到平衡状态后,恒温恒容条件下再充入一定量NO2,
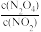 比值
比值
您最近一年使用:0次



