碘水溶液中存在下列平衡:I2(aq)+I-(aq)=I3-(aq)。测得不同温度下该反应的平衡常数K如表所示,下列说法正确的是
| t/℃ | 5 | 15 | 25 | 35 | 50 |
| K | 1100 | 841 | 689 | 533 | 409 |
A.反应I2(aq)+I-(aq) I3-(aq)的ΔH>0 I3-(aq)的ΔH>0 |
| B.25℃时,向溶液中加入少量KI固体,平衡常数K小于689 |
| C.其他条件不变,升高温度,溶液中c( I3-)减小 |
| D.该反应的平衡常数表达式为K=c(I-)/c(I3-) |
更新时间:2017-11-11 18:42:12
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知:2SO2 (g)+ O2(g)  2SO3(g) ΔH,有关数据如下:
2SO3(g) ΔH,有关数据如下:
下列说法不正确 的是
 2SO3(g) ΔH,有关数据如下:
2SO3(g) ΔH,有关数据如下:T(℃) | 527 | 627 | 727 | 827 | 927 |
| 平衡常数K | 910 | 42 | 3.2 | 0.39 | 0.12 |
| A.根据平衡常数随温度的变化关系,判断出ΔH<0 |
| B.保持其他条件不变,SO2的平衡转化率α(727℃)<α(927℃) |
| C.增大压强、降低温度能提高SO2的转化率 |
| D.SO3的稳定性随温度的升高而降低 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】可逆反应 符合以下两图。则下列叙述正确的是
符合以下两图。则下列叙述正确的是
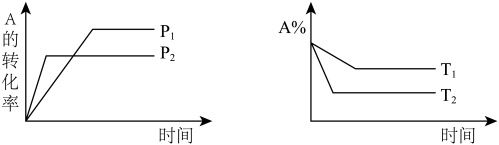
 符合以下两图。则下列叙述正确的是
符合以下两图。则下列叙述正确的是
A. ;正反应吸热 ;正反应吸热 | B. ;正反应吸热 ;正反应吸热 |
C. ;正反应放热 ;正反应放热 | D. ;正反应吸热 ;正反应吸热 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】某小组利用不同膜反应器(可选择性地让某些气体通过而离开体系)研究 的分解率,工作原理如下图所示.图a、b和c反应区温度维持恒定且相等,仅发生
的分解率,工作原理如下图所示.图a、b和c反应区温度维持恒定且相等,仅发生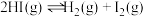 且在反应区内进行。投料均为
且在反应区内进行。投料均为 的
的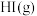 ,反应同时开始,
,反应同时开始, 时图b反应区处于瞬时平衡状态,其化学平衡常数
时图b反应区处于瞬时平衡状态,其化学平衡常数 。
。
下列说法正确的是
 的分解率,工作原理如下图所示.图a、b和c反应区温度维持恒定且相等,仅发生
的分解率,工作原理如下图所示.图a、b和c反应区温度维持恒定且相等,仅发生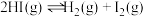 且在反应区内进行。投料均为
且在反应区内进行。投料均为 的
的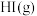 ,反应同时开始,
,反应同时开始, 时图b反应区处于瞬时平衡状态,其化学平衡常数
时图b反应区处于瞬时平衡状态,其化学平衡常数 。
。 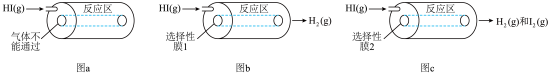
图a装置 | 图b装置 | 图c装置 | |
| 0.10 | 0.30 | x |
A.图a装置的化学平衡常数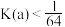 |
| B.图a装置中,HI(g)分解率为10% |
C.图b装置中,前 内 内 的平均渗透速率约为 的平均渗透速率约为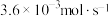 |
| D.图c装置中,x一定大于0.3 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】利用I2O5可消除CO污染,反应为5CO(g)+I2O5(s)⇌5CO2(g)+I2(s);∆H不同温度(T1、T2)下,向装有足量I2O5固体的2L恒容密闭容器中通入2mol CO,测得CO2气体体积分数φ(CO2)随时间t变化曲线如图所示。下列说法正确的是
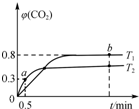

| A.T1<T2,∆H>0 |
| B.T1温度下,该反应的平衡常数为1024 |
| C.T2温度下,0-0.5min内,CO的平均反应速率为0.3mol·L-1·min-1 |
| D.T1温度下,若向装有足量I2固体的2L恒容密闭容器中通入10molCO2,达到平衡时,φ(CO2)大于0.8 |
您最近半年使用:0次


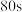 时反应区
时反应区 的物质的量/
的物质的量/
 时刻后改变反应条件,该平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知图乙中的
时刻后改变反应条件,该平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知图乙中的 ~
~ 阶段为使用催化剂;图甲中
阶段为使用催化剂;图甲中 ~
~ 阶段c(B)未画出。下列说法不正确的是
阶段c(B)未画出。下列说法不正确的是
 阶段改变的条件为减小压强
阶段改变的条件为减小压强


