在 1.0 L 密闭容器中放入 0.10molA(g),在一定温度进行如下反应:A(g) 2B(g)+C(g)+D(s) △H= +85.1kJ·mol-1。容器内气体总压强(P)与起始压强 P0 的比值随反应时间(t)数据见下表:
2B(g)+C(g)+D(s) △H= +85.1kJ·mol-1。容器内气体总压强(P)与起始压强 P0 的比值随反应时间(t)数据见下表:
回答下列问题:
(1)该平衡常数的表达式为_____________ 。
(2)下列能提高 A 的转化率的是________ 。
A.升高温度 B.体系中通入 A 气体 C.将 D 的浓度减小
D.通入稀有气体 He,使体系压强增大到原来的 5 倍
E.若体系中的 C 为 HCl,其它物质均难溶于水,滴入少许水
(3)前 2小时 C 的反应速率是___________ mol.L-1.h-1;
(4)平衡时 A 的转化率___________ C 的体积分数_________ (均保留两位有效数字)
 2B(g)+C(g)+D(s) △H= +85.1kJ·mol-1。容器内气体总压强(P)与起始压强 P0 的比值随反应时间(t)数据见下表:
2B(g)+C(g)+D(s) △H= +85.1kJ·mol-1。容器内气体总压强(P)与起始压强 P0 的比值随反应时间(t)数据见下表:| 时间 t/ h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 |
| P /P0 | 1.00 | 1.50 | 1.80 | 2.20 | 2.30 | 2.38 | 2.40 | 2.40 |
(1)该平衡常数的表达式为
(2)下列能提高 A 的转化率的是
A.升高温度 B.体系中通入 A 气体 C.将 D 的浓度减小
D.通入稀有气体 He,使体系压强增大到原来的 5 倍
E.若体系中的 C 为 HCl,其它物质均难溶于水,滴入少许水
(3)前 2小时 C 的反应速率是
(4)平衡时 A 的转化率
更新时间:2017-12-30 18:25:41
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氮化硅(Si3N4)是一种重要的陶瓷材料,可用石英与焦炭在1400~1450℃的氮气气氛下合成:3SiO2(s)+6C(s)+2N2(g) Si3N4(s)+6CO(g)﹣Q(Q>0),在反应条件下,向10L密闭容器中加入反应物,10min后达到平衡。完成下列填空:
Si3N4(s)+6CO(g)﹣Q(Q>0),在反应条件下,向10L密闭容器中加入反应物,10min后达到平衡。完成下列填空:
(1)上述反应所涉及的元素,原子半径由大到小的顺序是______ 。其中一种元素的原子核外s电子数与p电子数相等,写出它的最外层电子排布的轨道表示式______ 。比较碳、硅两种元素的非金属性强弱,可以通过比较______ (填:化合物性质的差异)来判断
(2)上述反应混合物中的极性分子是______ ,写出非极性分子的电子式______ 。从晶体类型的角度分析用氮化硅制造发动机中耐热部件的原因是______
(3)下列措施可以提高二氧化硅转化率的是______ (选填编号)
a.增加二氧化硅用量b.升高反应温度
c.增大气体压强 d.向反应容器中多充入氮气
(4)下列描述中能说明反应已达平衡的是______ (选填编号)
a.c(CO)=3c(N2)
b.v (CO)=3v(N2)
c.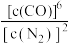 保持不变
保持不变
d.气体的压强保持不变
(5)测得平衡时固体质量减少了11.2g,则用氮气表示的平均反应速率为______
 Si3N4(s)+6CO(g)﹣Q(Q>0),在反应条件下,向10L密闭容器中加入反应物,10min后达到平衡。完成下列填空:
Si3N4(s)+6CO(g)﹣Q(Q>0),在反应条件下,向10L密闭容器中加入反应物,10min后达到平衡。完成下列填空:(1)上述反应所涉及的元素,原子半径由大到小的顺序是
(2)上述反应混合物中的极性分子是
(3)下列措施可以提高二氧化硅转化率的是
a.增加二氧化硅用量b.升高反应温度
c.增大气体压强 d.向反应容器中多充入氮气
(4)下列描述中能说明反应已达平衡的是
a.c(CO)=3c(N2)
b.v (CO)=3v(N2)
c.
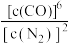 保持不变
保持不变d.气体的压强保持不变
(5)测得平衡时固体质量减少了11.2g,则用氮气表示的平均反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知NO2和N2O4可以相互转化:2NO2(g) N2O4(g)(正反应为放热反应)。现将一定量NO2和N2O4的混合气体通入一体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图所示,回答下列问题:
N2O4(g)(正反应为放热反应)。现将一定量NO2和N2O4的混合气体通入一体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图所示,回答下列问题:
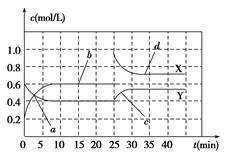
(1)图中共有两条曲线X和Y,其中曲线______ 表示NO2浓度随时间的变化;a、b、c、d四个点中,表示化学反应处于平衡状态的点是______ 。
(2)前10 min内用NO2表示的化学反应速率v(NO2)=______ mol/(L·min);反应进行至25 min时,曲线发生变化的原因是______ 。
(3)若要达到与最后相同的化学平衡状态,在25 min时还可以采取的措施是______。
 N2O4(g)(正反应为放热反应)。现将一定量NO2和N2O4的混合气体通入一体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图所示,回答下列问题:
N2O4(g)(正反应为放热反应)。现将一定量NO2和N2O4的混合气体通入一体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图所示,回答下列问题:
(1)图中共有两条曲线X和Y,其中曲线
(2)前10 min内用NO2表示的化学反应速率v(NO2)=
(3)若要达到与最后相同的化学平衡状态,在25 min时还可以采取的措施是______。
| A.加入催化剂 | B.缩小容器体积 |
| C.升高温度 | D.加入一定量的N2O4 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】煤中的氮元素在煤燃烧过程中的转化如图所示:完成下列填空:
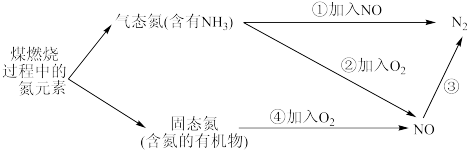
(1)氮原子最外层电子中两种自旋状态的电子数之比为:_______ ;氮原子最外层电子的能量_______ 磷原子。(选填“ ”“
”“ ”“
”“ ”或“无法比较”)
”或“无法比较”)
(2)固态氮中有一种含氮有机物: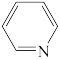 ,和碳原子相比,氨原子吸引电子能力更
,和碳原子相比,氨原子吸引电子能力更_______ (填“强”或“弱”),吸引电子能力差异的原因是:_______ 。
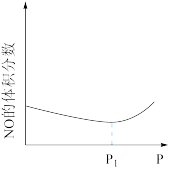
(3)过程②处理氨: ,一定温度下的密闭容器中发生该反应,平衡后NO的体积分数与压强的关系如图所示。NO的体积分数先减小后增大的原因可能是:
,一定温度下的密闭容器中发生该反应,平衡后NO的体积分数与压强的关系如图所示。NO的体积分数先减小后增大的原因可能是:_______ 。
(4)过程①有时会产生笑气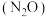 ,用同位素示踪法研究发现,在有氧气时,
,用同位素示踪法研究发现,在有氧气时,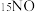 与
与 以一定比例反应,得到的笑气几乎都是
以一定比例反应,得到的笑气几乎都是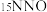 。配平化学方程式:
。配平化学方程式:_____
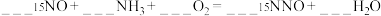
(5)氨可以转化为氮肥,含氮量是衡量肥效的指标之一,常见氮肥: (尿素)、
(尿素)、 和
和
①等物质的量 和
和 的混合物,与足量氢氧化钠加热,产生气体10.08L(标准状况下,固体混合物质量为
的混合物,与足量氢氧化钠加热,产生气体10.08L(标准状况下,固体混合物质量为_______ g。
②目前氮肥中 使用量最多,可能的原因是
使用量最多,可能的原因是_______ 、_______ (任写2条)。

(1)氮原子最外层电子中两种自旋状态的电子数之比为:
 ”“
”“ ”“
”“ ”或“无法比较”)
”或“无法比较”)(2)固态氮中有一种含氮有机物:
 ,和碳原子相比,氨原子吸引电子能力更
,和碳原子相比,氨原子吸引电子能力更(3)过程②处理氨:
 ,一定温度下的密闭容器中发生该反应,平衡后NO的体积分数与压强的关系如图所示。NO的体积分数先减小后增大的原因可能是:
,一定温度下的密闭容器中发生该反应,平衡后NO的体积分数与压强的关系如图所示。NO的体积分数先减小后增大的原因可能是:
(4)过程①有时会产生笑气
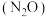 ,用同位素示踪法研究发现,在有氧气时,
,用同位素示踪法研究发现,在有氧气时,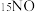 与
与 以一定比例反应,得到的笑气几乎都是
以一定比例反应,得到的笑气几乎都是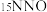 。配平化学方程式:
。配平化学方程式: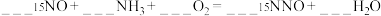
(5)氨可以转化为氮肥,含氮量是衡量肥效的指标之一,常见氮肥:
 (尿素)、
(尿素)、 和
和
①等物质的量
 和
和 的混合物,与足量氢氧化钠加热,产生气体10.08L(标准状况下,固体混合物质量为
的混合物,与足量氢氧化钠加热,产生气体10.08L(标准状况下,固体混合物质量为②目前氮肥中
 使用量最多,可能的原因是
使用量最多,可能的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】向某密闭容器中充入等物质的量的气体M和N,一定条件下发生反应,达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间的变化如图1、图2所示。
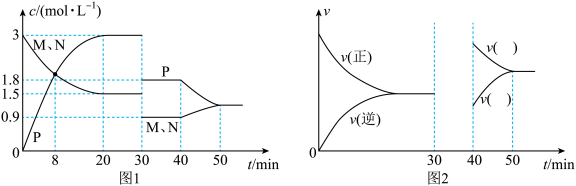
回答下列问题:
(1)该反应的化学方程式为_______ ,其
_______ (填“>”、“<”或“=”)0。
(2)30min时改变的条件是____ ,40min时改变的条件是____ ,请在图2中画出30min~40min的正逆反应速率变化曲线以及标出40min~50min内 、
、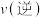 对应的曲线
对应的曲线_____ 。
(3)0~8min内,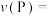
_______ ;50min后,M的转化率为_______ (保留三位有效数字)。
(4)20min~30min内,反应平衡时的平衡常数K=_______ 。

回答下列问题:
(1)该反应的化学方程式为

(2)30min时改变的条件是
 、
、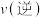 对应的曲线
对应的曲线(3)0~8min内,
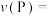
(4)20min~30min内,反应平衡时的平衡常数K=
您最近一年使用:0次
【推荐2】在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极而增大电解能耗。可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl-。已知:Cu+Cu2+ 2Cu+ K=7.6×10-7;Ksp(CuCl)=2.0×10-6。
2Cu+ K=7.6×10-7;Ksp(CuCl)=2.0×10-6。
(1)通过计算说明上述除Cl-的反应能完全进行的原因为___________ 。
(2)若用Zn替换Cu可加快除Cl-的速率,但需控制溶液的pH,若pH过低,除Cl-效果下降的原因是___________ 。
 2Cu+ K=7.6×10-7;Ksp(CuCl)=2.0×10-6。
2Cu+ K=7.6×10-7;Ksp(CuCl)=2.0×10-6。(1)通过计算说明上述除Cl-的反应能完全进行的原因为
(2)若用Zn替换Cu可加快除Cl-的速率,但需控制溶液的pH,若pH过低,除Cl-效果下降的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)反应m A+n B  p C在某温度下达到平衡。
p C在某温度下达到平衡。
①若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关系__________ 。
②若A、B、C都是气体,且m + n < p,而加压或升温平衡移动方向相同,则△H______ 0
(2)将1molN2和4molH2充入容积为2L的密闭容器中发生:N2(g)+ 3H2(g) 2NH3(g) ,2分钟后反应达平衡后,N2的浓度为0.25 mol/L,完成:
2NH3(g) ,2分钟后反应达平衡后,N2的浓度为0.25 mol/L,完成:
①N2转化率是____________
②用NH3 表达的化学反应速率为:___________
③平衡常数值是________________
 p C在某温度下达到平衡。
p C在某温度下达到平衡。①若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关系
②若A、B、C都是气体,且m + n < p,而加压或升温平衡移动方向相同,则△H
(2)将1molN2和4molH2充入容积为2L的密闭容器中发生:N2(g)+ 3H2(g)
 2NH3(g) ,2分钟后反应达平衡后,N2的浓度为0.25 mol/L,完成:
2NH3(g) ,2分钟后反应达平衡后,N2的浓度为0.25 mol/L,完成:①N2转化率是
②用NH3 表达的化学反应速率为:
③平衡常数值是
您最近一年使用:0次



