氧元素与多种元素具有亲和力,所形成化合物的种类很多。
(1)氮、氧、氟元素的第一电离能从大到小的顺序为__________ 。氧元素与氟元素能形成OF2分子,该分子的空间构型为__________ 。
(2)根据等电子体原理,在 中氮原子轨道杂化类型是
中氮原子轨道杂化类型是__________ ;1 mol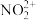 中含有的π键数目为
中含有的π键数目为__________ 个。
(3)氧元素和过渡元素可形成多种价态的金属氧化物,如和铬可生成Cr2O3、CrO3、CrO5等。Cr3+基态核外电子排布式为__________ 。
(4)下列物质的分子与O3分子的结构最相似的是__________ 。
A.H2O B.CO2 C.SO2 D.BeCl2
(5)O3分子是否为极性分子?__________ 。
(1)氮、氧、氟元素的第一电离能从大到小的顺序为
(2)根据等电子体原理,在
 中氮原子轨道杂化类型是
中氮原子轨道杂化类型是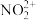 中含有的π键数目为
中含有的π键数目为(3)氧元素和过渡元素可形成多种价态的金属氧化物,如和铬可生成Cr2O3、CrO3、CrO5等。Cr3+基态核外电子排布式为
(4)下列物质的分子与O3分子的结构最相似的是
A.H2O B.CO2 C.SO2 D.BeCl2
(5)O3分子是否为极性分子?
14-15高二下·吉林·期中 查看更多[4]
(已下线)模块同步卷07 第二章综合检测-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)山西省平遥中学校2018-2019学年高二下学期第二次月考化学试题河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第二章 综合检测22014-2015吉林省吉林市第五十五中学高二下学期期中考试化学试卷
更新时间:2018-02-12 22:24:29
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)若某原子在处于能最最低状态时,外围电子排布为4d15s2,则下列说法正确的是___ (填标号)
A.该元戴原子处于能量最低状态时,原子中共有3个未成对电子
B.该元载原子核外共有5个电子层
C.该元素原子的M能层共有8个电子
D.该元素原子最外层其有3个电子
(2)下列说法正确的是_______ (填标号)
A.共价键的键能越大,共价键越牢固,由该键形成的分子越稳定
B.H2O是一种非常稳定的化合物,这是由于氢键所致
C.H2O分子中两个O-H键的键角为180°
D.所有分子中都含有共价键
(3)根据价层电子对互斥理论及原子的杂化理论判断NF3分子的空间构型和中心原子的杂化方式为____ (填标号)
A.直线形 sp杂化 B.三角形 sp2杂化
C.三角锥形 sp2杂化 D.三角锥形 sp3杂化
A.该元戴原子处于能量最低状态时,原子中共有3个未成对电子
B.该元载原子核外共有5个电子层
C.该元素原子的M能层共有8个电子
D.该元素原子最外层其有3个电子
(2)下列说法正确的是
A.共价键的键能越大,共价键越牢固,由该键形成的分子越稳定
B.H2O是一种非常稳定的化合物,这是由于氢键所致
C.H2O分子中两个O-H键的键角为180°
D.所有分子中都含有共价键
(3)根据价层电子对互斥理论及原子的杂化理论判断NF3分子的空间构型和中心原子的杂化方式为
A.直线形 sp杂化 B.三角形 sp2杂化
C.三角锥形 sp2杂化 D.三角锥形 sp3杂化
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)现有5种元素A、B、C、D、E,其中有3种金属元素,1种稀有气体元素,其I1~I3分别如下表。
根据表中数据判断其中的金属元素为___________ ,稀有气体元素为___________ ,显正二价的金属元素是___________ 。(填字母)
(2)水分子是H2O而不是H3O,是因为共价键具有___________ 性;水分子的键角为105°,是因为共价键具有___________ 性。
(3)1mol乙酸分子CH3COOH中含有的π键与σ键的数目之比为___________ 。
(4)已知NH5为离子化合物,则1molNH5晶体中含有的共价键数目为___________ 。
(1)现有5种元素A、B、C、D、E,其中有3种金属元素,1种稀有气体元素,其I1~I3分别如下表。
| 元素 | I1/eV | I2/eV | I3/eV |
| A | 13.0 | 23.9 | 40.0 |
| B | 4.3 | 31.9 | 47.8 |
| C | 5.7 | 47.4 | 71.8 |
| D | 7.7 | 15.1 | 80.3 |
| E | 21.6 | 41.1 | 65.2 |
(2)水分子是H2O而不是H3O,是因为共价键具有
(3)1mol乙酸分子CH3COOH中含有的π键与σ键的数目之比为
(4)已知NH5为离子化合物,则1molNH5晶体中含有的共价键数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)用“>”或“<”填写下表。
(2)一种制取NH2OH的反应为2NO2-+4SO2 + 6H2O+ 6NH3 = 4SO +6NH4++2NH2OH。
+6NH4++2NH2OH。
①N、H、O的电负性从小 到大 的顺序为____ 。
②NH3分子的空间构型为____ 。
③NH2OH极易溶于H2O,除因为它们都是极性分子外,还因为____ 。
(3)配合物K[PtCl3(NH3)]中[PtCl3(NH3)]-的结构可用示意图表示为____ (不考虑空间构型)。
(1)用“>”或“<”填写下表。
| 第一电离能 | 熔点 | 沸点(同压) | 键能 |
| P | MgO | CF4 | H-Cl |
(2)一种制取NH2OH的反应为2NO2-+4SO2 + 6H2O+ 6NH3 = 4SO
 +6NH4++2NH2OH。
+6NH4++2NH2OH。①N、H、O的电负性从
②NH3分子的空间构型为
③NH2OH极易溶于H2O,除因为它们都是极性分子外,还因为
(3)配合物K[PtCl3(NH3)]中[PtCl3(NH3)]-的结构可用示意图表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】硒化锌是一种半导体材料,回答下列问题。
(1)锌在周期表中的位置___________________ ;Se基态原子价电子排布图为_____________ 。元素锌、硫和硒第一电离能较大的是________ (填元素符号)。
(2)Na2SeO3分子中Se原子的杂化类型为_______ ;H2SeO4的酸性比H2SeO3强,原因是_______ 。
(3)气态SeO3分子的立体构型为_______ ;下列与SeO3互为等电子体的有_________ (填序号)。
A.CO32- B.NO3- C.NCl3 D.SO32-
(4)硒化锌的晶胞结构如图所示,图中X和Y点所堆积的原子均为______ (填元素符号);该晶胞中硒原子所处空隙类型为_____ (填“立方体”“正四面体”或“正八面体”);若该晶胞密度为ρg/cm3,硒化锌的摩尔质量为Mg/mol。用NA代表阿伏伽德罗常数的数值,则晶胞参数a为_______ nm。

(1)锌在周期表中的位置
(2)Na2SeO3分子中Se原子的杂化类型为
(3)气态SeO3分子的立体构型为
A.CO32- B.NO3- C.NCl3 D.SO32-
(4)硒化锌的晶胞结构如图所示,图中X和Y点所堆积的原子均为

您最近一年使用:0次
【推荐2】(1)橙红色晶体羰基钴 的熔点为52℃,可溶于多数有机溶剂。该晶体中三种元素电负性由大到小的顺序为
的熔点为52℃,可溶于多数有机溶剂。该晶体中三种元素电负性由大到小的顺序为_______ (填元素符号)。配体 中
中 键与
键与 键数目之比是
键数目之比是_______ 。
(2) 中键与键之间的夹角为180°,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为
中键与键之间的夹角为180°,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为_______ ,1个分子中含有_______ 个 键。
键。
 的熔点为52℃,可溶于多数有机溶剂。该晶体中三种元素电负性由大到小的顺序为
的熔点为52℃,可溶于多数有机溶剂。该晶体中三种元素电负性由大到小的顺序为 中
中 键与
键与 键数目之比是
键数目之比是(2)
 中键与键之间的夹角为180°,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为
中键与键之间的夹角为180°,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为 键。
键。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1) 分子中,C原子的杂化轨道类型是
分子中,C原子的杂化轨道类型是_______ 。
(2)将
 通入稀
通入稀 溶液中可生成
溶液中可生成 ,
, 分子空间结构为
分子空间结构为_______ ,其中氧原子的杂化方式为_______ 。
(3) 中C原子的杂化轨道类型为
中C原子的杂化轨道类型为_______ 。
(1)
 分子中,C原子的杂化轨道类型是
分子中,C原子的杂化轨道类型是(2)将

 通入稀
通入稀 溶液中可生成
溶液中可生成 ,
, 分子空间结构为
分子空间结构为(3)
 中C原子的杂化轨道类型为
中C原子的杂化轨道类型为
您最近一年使用:0次
填空题
|
适中
(0.65)
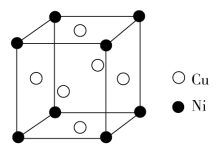
【推荐2】镍是一种银白色金属,具有良好的机械强度和延展性,常用来制造货币等,镀在其他金属上可以防止生锈。回答下列问题:铜镍合金主要用于造币,亦可用于制作仿银饰品。其立方晶胞结构如图所示,则该晶体的化学式为_______ ,铜原子构成的空间构型为_______ ,铜原子距离最近的Ni有_______ 个;已知该晶体的密度为ρg·cm-3,则晶胞中距离最近的Ni原子和Cu原子的核间距为 _______ pm(用NA表示阿伏加德罗常数的值,列出计算式即可)。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知下列微粒:①CH4 ②CH2=CH2③CH≡ CH④NH3 ⑤NH4+ ⑥BF3 ⑦H2O ⑧H2O2。试回答下列问题。
(1)分子空间构型为正四面体形的是__________ (填序号,下同)。
(2)中心原子为sp3杂化的是__________ ,中心原子为sp2杂化的是__________ ,中心原子为sp1杂化的是__________ 。
(3)所有原子共平面(含共直线)的是__________ ,共直线的是__________ 。
(1)分子空间构型为正四面体形的是
(2)中心原子为sp3杂化的是
(3)所有原子共平面(含共直线)的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】二草酸根合铜(II)酸钾 可用于无机合成、功能材料制备。回答下列有关问题:
可用于无机合成、功能材料制备。回答下列有关问题:
(1)基态氧原子的电子排布式为_______ ,以下氧原子的激发态中能量最高的是_______ (填字母)。
a.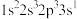 b.
b. c.
c.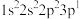
(2)二草酸根合铜(II)酸钾是一种配合物。
①其中配位体的化学式是_______ ,配位原子是氧而不是碳的原因是_______ 。
②草酸分子的结构为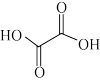 ,其中碳原子的杂化轨道类型为
,其中碳原子的杂化轨道类型为_______ , 草酸分子中含有的
草酸分子中含有的 键数目为
键数目为_______ (阿伏加德罗常数的值为 ),
), 键能大于
键能大于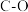 键能的判断依据是
键能的判断依据是_______ 。
 可用于无机合成、功能材料制备。回答下列有关问题:
可用于无机合成、功能材料制备。回答下列有关问题:(1)基态氧原子的电子排布式为
a.
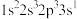 b.
b. c.
c.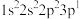
(2)二草酸根合铜(II)酸钾是一种配合物。
①其中配位体的化学式是
②草酸分子的结构为
 ,其中碳原子的杂化轨道类型为
,其中碳原子的杂化轨道类型为 草酸分子中含有的
草酸分子中含有的 键数目为
键数目为 ),
), 键能大于
键能大于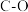 键能的判断依据是
键能的判断依据是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下列问题。
(1)3-氯-2-丁氨酸的结构简式为 ,1个该有机物分子中含有
,1个该有机物分子中含有_______ 个手性碳原子,其中-NH2中N原子的杂化轨道类型是_______ 。
(2)青蒿素是从黄花蒿中提取得到的一种无色针状晶体,分子结构如下图所示,则青蒿素分子中含有_______ 个手性碳原子。
(1)3-氯-2-丁氨酸的结构简式为
 ,1个该有机物分子中含有
,1个该有机物分子中含有(2)青蒿素是从黄花蒿中提取得到的一种无色针状晶体,分子结构如下图所示,则青蒿素分子中含有

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】材料是人类文明进步的阶梯,主族非金属元素是组成特殊材料的重要元素。请回答下列问题:
(1)氮氧共掺杂多孔碳材料是一种新型高效的能源存储材料,其中的三种主要元素C、N、O,电负性从小到大的顺序是_____ ,第一电离能从大到小的顺序是_____ 。
(2)根据杂化轨道理论的相关知识,在NH3、BF3、SO 、H3O+几种微粒中,中心原子杂化方式与其他三个不同的是
、H3O+几种微粒中,中心原子杂化方式与其他三个不同的是______ (填化学式);已知等电子体具有相同的空间构型,结合价电子对互斥理论可知N2O分子为______ 形。
(3)有一种配合物组成为[M(NH3)5(H2O)]Cl3,该配合物中提供孤电子对的原子是_____ (填符号);配合物T与[M(NH3)5(H2O)]Cl3组成所含微粒种类和数目相同,中心离子的配位数相同且T中也只有两种配体,若1molT溶于水,加入足量AgNO3溶液只生成2molAgCl,则T的配合物可表示为_____ 。
(4)最近发现一种由Ti原子和C原子构成的气态团簇分子如图所示,其化学式为_____ 。

(1)氮氧共掺杂多孔碳材料是一种新型高效的能源存储材料,其中的三种主要元素C、N、O,电负性从小到大的顺序是
(2)根据杂化轨道理论的相关知识,在NH3、BF3、SO
 、H3O+几种微粒中,中心原子杂化方式与其他三个不同的是
、H3O+几种微粒中,中心原子杂化方式与其他三个不同的是(3)有一种配合物组成为[M(NH3)5(H2O)]Cl3,该配合物中提供孤电子对的原子是
(4)最近发现一种由Ti原子和C原子构成的气态团簇分子如图所示,其化学式为

您最近一年使用:0次



