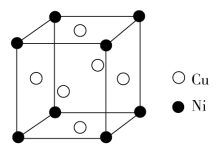
镍是一种银白色金属,具有良好的机械强度和延展性,常用来制造货币等,镀在其他金属上可以防止生锈。回答下列问题:铜镍合金主要用于造币,亦可用于制作仿银饰品。其立方晶胞结构如图所示,则该晶体的化学式为_______ ,铜原子构成的空间构型为_______ ,铜原子距离最近的Ni有_______ 个;已知该晶体的密度为ρg·cm-3,则晶胞中距离最近的Ni原子和Cu原子的核间距为 _______ pm(用NA表示阿伏加德罗常数的值,列出计算式即可)。
2022高三·全国·专题练习 查看更多[2]
更新时间:2022-04-26 10:36:46
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】硅和卤素单质反应可以得到SiX4。SiX4的熔、沸点见下表:
0℃时,SiF4、SiCl4、SiBr4、SiI4呈液态的是___________ (填化学式),沸点依次升高的原因是___________ ,气态SiX4分子的空间结构是___________ 。
| SiF4 | SiCl4 | SiBr4 | SiI4 | |
| 熔点/K | 183.0 | 203.2 | 278.6 | 393.7 |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】臭氧有强氧化性能在一定条件下将烟气中的SO2、NOx分别氧化为SO42- 和NO3 -。臭氧可用于净化空气,饮用水消毒,处理工业废物和作为漂白剂。
(1)NO3-中心原子轨道的杂化类型为___________ ;SO42- 的空间构型为_____________ (用文字描述)。
(2)Fe3+基态核外外层电子排布式为__________________ 。
(3)臭氧可用于含CN一碱性电镀废水的处理。第i步:CN一转化为OCN-;第ii步: OCN一继续转化为CO32一及两种单质气体。若第ii步转化时,O3与OCN-物质的质量之比为3∶2,该步反应的离子方程式为_______ 。
(4)为测定大气中臭氧(O3)含量,将0℃、1.01×105Pa的空气VL慢慢通过足量KI溶液,使臭氧完全反应;然后将所得溶液用amL cmol/L的Na2S2O3溶液进行滴定恰好到达终点。
(已知:2Na2S2O3+I2=Na2S4O6+2NaI)
①O3与KI溶液反应生成两种单质,则反应的化学方程式__________________________ 。
②该滴定实验中除烧杯、锥形瓶外,还需要的玻璃仪器是_____________ ;
③该实验中可选用_______ (填物质名称)作指示剂。空气中臭氧的体积分数为_______ 。
④甲同学认为在滴定前应微热溶液,以排除溶液中溶解的O3和O2,不然会使滴定结果偏_____ (填“低”或“高”)。
(1)NO3-中心原子轨道的杂化类型为
(2)Fe3+基态核外外层电子排布式为
(3)臭氧可用于含CN一碱性电镀废水的处理。第i步:CN一转化为OCN-;第ii步: OCN一继续转化为CO32一及两种单质气体。若第ii步转化时,O3与OCN-物质的质量之比为3∶2,该步反应的离子方程式为
(4)为测定大气中臭氧(O3)含量,将0℃、1.01×105Pa的空气VL慢慢通过足量KI溶液,使臭氧完全反应;然后将所得溶液用amL cmol/L的Na2S2O3溶液进行滴定恰好到达终点。
(已知:2Na2S2O3+I2=Na2S4O6+2NaI)
①O3与KI溶液反应生成两种单质,则反应的化学方程式
②该滴定实验中除烧杯、锥形瓶外,还需要的玻璃仪器是
③该实验中可选用
④甲同学认为在滴定前应微热溶液,以排除溶液中溶解的O3和O2,不然会使滴定结果偏
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在建国70周年阅兵仪式上,“歼20”、“东风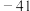 核导弹”等国之重器相继亮相,它们采用了大量合金材料.回答下列问题:
核导弹”等国之重器相继亮相,它们采用了大量合金材料.回答下列问题:
(1)早期战斗机主要采用铝合金,其中超硬铝属于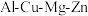 系。
系。
①第一电离能
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②已知金属锌晶体的堆积方式为六方最密堆积,则金属锌的配位数是_______ 。
③基态铜原子的价层电子排布式为_______ 。
(2)中期战斗机主要采用钛合金.按电子排布,钛元素位于元素周期表的____ 区。
(3)钛镍合金可用于战斗机的油压系统,该合金溶于热的硫酸生成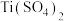 、
、 ,其中阴离子的立体构型为
,其中阴离子的立体构型为_______ ,S原子的_______ 杂化轨道与O原子的 轨道形成
轨道形成_______ 键(填“ ”或“
”或“ ”)。
”)。
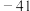 核导弹”等国之重器相继亮相,它们采用了大量合金材料.回答下列问题:
核导弹”等国之重器相继亮相,它们采用了大量合金材料.回答下列问题:(1)早期战斗机主要采用铝合金,其中超硬铝属于
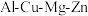 系。
系。①第一电离能

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②已知金属锌晶体的堆积方式为六方最密堆积,则金属锌的配位数是
③基态铜原子的价层电子排布式为
(2)中期战斗机主要采用钛合金.按电子排布,钛元素位于元素周期表的
(3)钛镍合金可用于战斗机的油压系统,该合金溶于热的硫酸生成
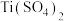 、
、 ,其中阴离子的立体构型为
,其中阴离子的立体构型为 轨道形成
轨道形成 ”或“
”或“ ”)。
”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】钙钛矿型太阳能光伏电池常用有机半导材料作为光敏层材料,其结构如图所示,其中A为正离子 ,另两种离子为
,另两种离子为 和
和 ,已知Pb为碳族元素。
,已知Pb为碳族元素。
(2)每个 周围距离相等且最近的X微粒有______。
周围距离相等且最近的X微粒有______。
 ,另两种离子为
,另两种离子为 和
和 ,已知Pb为碳族元素。
,已知Pb为碳族元素。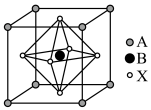
| A.N、I、Pb均属于p区元素 |
B.B微粒是 |
C.该物质化学式为 |
D. 中H-N-H键角小于 中H-N-H键角小于 中H-N-H键角 中H-N-H键角 |
(2)每个
 周围距离相等且最近的X微粒有______。
周围距离相等且最近的X微粒有______。| A.3个 | B.6个 | C.12个 | D.24个 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】 (1)如图所示为二维平面晶体结构示意图,化学式为 的晶体是
的晶体是______ 。(填序号)。

(2)如图为金属铜的晶胞,请完成下列各题。

①该晶胞“实际”拥有的铜原子数是______ 。
②设该晶胞立方体的边长为 ,Cu的相对原子质量为64,金属铜的密度为
,Cu的相对原子质量为64,金属铜的密度为 ,
, 为阿伏加德罗常数的值,则
为阿伏加德罗常数的值,则
______ (用a、ρ表示)。
 的晶体是
的晶体是
(2)如图为金属铜的晶胞,请完成下列各题。

①该晶胞“实际”拥有的铜原子数是
②设该晶胞立方体的边长为
 ,Cu的相对原子质量为64,金属铜的密度为
,Cu的相对原子质量为64,金属铜的密度为 ,
, 为阿伏加德罗常数的值,则
为阿伏加德罗常数的值,则
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】平行六面体晶胞中粒子个数的计算。
(1)晶胞的顶角原子是_______ 个晶胞共用的,晶胞棱上的原子是_______ 个晶胞共用的,晶胞面上的原子是_______ 个晶胞共用的。
(2)晶胞中微粒数目的确定。
“均摊法”是计算每个晶胞平均拥有的粒子数目的常用方法。其基本理念是每个粒子被n个晶胞所共用,则该粒子有1/n属于这个晶胞。

晶胞中微粒数目的确定
①金属铜晶胞中原子个数的计算。

金属铜的一个晶胞中,位于晶胞_______ 的铜原子有_______ 个,位于_______ 的铜原有_______ 个,金属铜晶胞中所含的铜原子数为_______ 。
②氯化钠晶胞中所含的Na+、Cl-数。

氯化钠晶胞如图所示,其中体积较小的为_______ 离子(填“Na+”或“Cl-”下同),体积较大的为_______ 离子,则晶胞中含_______ 个Na+(提示:晶胞中心还有一个Na+)和_______ 个Cl-。
③试计算钠、锌、碘、金刚石晶胞中含有原子的数目

金属钠的一个晶胞的原子数=_______
金属锌的一个晶胞的原子数=_______
碘的一个晶胞的原子数=_______
金刚石的一个晶胞的原子数=_______
(1)晶胞的顶角原子是
(2)晶胞中微粒数目的确定。
“均摊法”是计算每个晶胞平均拥有的粒子数目的常用方法。其基本理念是每个粒子被n个晶胞所共用,则该粒子有1/n属于这个晶胞。

晶胞中微粒数目的确定
①金属铜晶胞中原子个数的计算。

金属铜的一个晶胞中,位于晶胞
②氯化钠晶胞中所含的Na+、Cl-数。

氯化钠晶胞如图所示,其中体积较小的为
③试计算钠、锌、碘、金刚石晶胞中含有原子的数目

金属钠的一个晶胞的原子数=
金属锌的一个晶胞的原子数=
碘的一个晶胞的原子数=
金刚石的一个晶胞的原子数=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】石墨的片层结构如图所示,试回答:

(1)每个正六边形占有的碳原子数为___________ 。
(2)石墨晶体每一层内碳原子数与C-C键数之比是___________ 。
(3)ng碳原子可构成___________ 个正六边形。

(1)每个正六边形占有的碳原子数为
(2)石墨晶体每一层内碳原子数与C-C键数之比是
(3)ng碳原子可构成
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图是氯化钠的晶胞示意图,回答如下问题:

(1)在NaCl晶体中,与每个Cl-距离等同且距离最近的几个Na+所围成的空间几何构型为__________ 。
A.正四面体 B.正六面体 C.正八面体 D.正十二面体
(2)NaCl晶体中不存在分子,但是当温度达到1686 K时,NaCl晶体形成气体,并以分子形式存在。现有29.25 g NaCl晶体,强热使其气化,测的气体体积为5.6 L(已折算成标准状况)则此时氯化钠气体的化学式为_____________ 。
(3)随着科学技术的发展,阿伏加德罗常数的测定手段越来越多,测定的精确度也越来越高。现有一种简单可行的测定方法,具体步骤为:
①将固体NaCl细粒干燥后,准确称取ag NaCl固体并转移到定容容器A中;
②用滴定管向A仪器中加苯,不断振荡,继续加苯至A仪器的刻度,计算出NaCl固体的体积为V cm3。步骤①中A仪器最好使用_______________ 。
A.量筒 B.烧杯 C.容量瓶 D.试管
(4)已知NaCl晶体中,距离最近的Na+与Cl-间的平均距离为bcm,用上述测定方法测得的阿伏加德罗常数NA的表达式为______________________ 。(用含V、a、b的代数式表示)

(1)在NaCl晶体中,与每个Cl-距离等同且距离最近的几个Na+所围成的空间几何构型为
A.正四面体 B.正六面体 C.正八面体 D.正十二面体
(2)NaCl晶体中不存在分子,但是当温度达到1686 K时,NaCl晶体形成气体,并以分子形式存在。现有29.25 g NaCl晶体,强热使其气化,测的气体体积为5.6 L(已折算成标准状况)则此时氯化钠气体的化学式为
(3)随着科学技术的发展,阿伏加德罗常数的测定手段越来越多,测定的精确度也越来越高。现有一种简单可行的测定方法,具体步骤为:
①将固体NaCl细粒干燥后,准确称取ag NaCl固体并转移到定容容器A中;
②用滴定管向A仪器中加苯,不断振荡,继续加苯至A仪器的刻度,计算出NaCl固体的体积为V cm3。步骤①中A仪器最好使用
A.量筒 B.烧杯 C.容量瓶 D.试管
(4)已知NaCl晶体中,距离最近的Na+与Cl-间的平均距离为bcm,用上述测定方法测得的阿伏加德罗常数NA的表达式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】物质的微观结构对于生命科学的发展有着重要的作用。
(1)磷化铝(AlP)通常作为一种广谱熏蒸杀虫剂,其晶胞如图甲所示
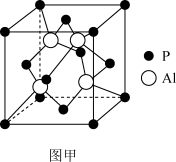
①P的配位数为_______ ;
②其中与P的含氧酸根PO 互为等电子体的非极性分子是
互为等电子体的非极性分子是_______ 。
(2)图乙所示是一种超分子,其中Mo处于第五周期第ⅥB族,核外电子排布与Cr相似,它的基态价电子排布式是_______ 。

(3)①如图丙所示,钙钛矿晶胞的Ti4+处于6个O2-组成的_______ 空隙中(填几何空间构型)。其中A的坐标参数为(0,0,0),则B的坐标参数为_______ 。
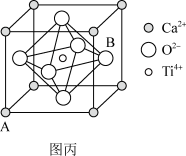
②与Ti相关化合物性质如下表:
TiC的熔沸点明显高于TiCl4的原因为_______ 。
(1)磷化铝(AlP)通常作为一种广谱熏蒸杀虫剂,其晶胞如图甲所示

①P的配位数为
②其中与P的含氧酸根PO
 互为等电子体的非极性分子是
互为等电子体的非极性分子是(2)图乙所示是一种超分子,其中Mo处于第五周期第ⅥB族,核外电子排布与Cr相似,它的基态价电子排布式是

(3)①如图丙所示,钙钛矿晶胞的Ti4+处于6个O2-组成的


②与Ti相关化合物性质如下表:
| 物质 | 性质 |
| TiC | 质硬,熔点:3140℃,沸点:4820℃ |
| TiCl4 | 熔点:-25℃,沸点:136.4℃,具有挥发性 |
您最近一年使用:0次



