室温下,0.1mol/L的Na2CO3溶液中,下列粒子浓度关系式不正确的是
| A.c(Na+)= 2[c(CO32-)+ c(HCO3-)+ c(H2CO3)] |
| B.c(Na+)+ c(H+)= 2c(CO32-)+ c(HCO3-)+ c(OH—) |
| C.c(H+)= c(OH-)—c(HCO3-)—c(H2CO3) |
| D.c(Na+)>c(CO32-)> c(OH—)> c(HCO3-)> c(H+) |
更新时间:2018-10-31 16:11:56
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,利用NaOH调节 溶液pH时,维持溶液中含磷微粒的物质的量浓度之和始终为0.1mol/L,得到溶液中各种含磷微粒的物质的量分数(δ)与溶液pH的关系如图所示。下列说法正确的是
溶液pH时,维持溶液中含磷微粒的物质的量浓度之和始终为0.1mol/L,得到溶液中各种含磷微粒的物质的量分数(δ)与溶液pH的关系如图所示。下列说法正确的是

 溶液pH时,维持溶液中含磷微粒的物质的量浓度之和始终为0.1mol/L,得到溶液中各种含磷微粒的物质的量分数(δ)与溶液pH的关系如图所示。下列说法正确的是
溶液pH时,维持溶液中含磷微粒的物质的量浓度之和始终为0.1mol/L,得到溶液中各种含磷微粒的物质的量分数(δ)与溶液pH的关系如图所示。下列说法正确的是
A.H3PO4的电离方程式为:H3PO4  3H++PO 3H++PO |
B.M点时,溶液中c(Na+)>c(H2PO )=c(HPO )=c(HPO )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
C.pH=5时,溶液c(Na+)=c(H2PO )+2c(HPO )+2c(HPO )+3(PO )+3(PO ) ) |
| D.pH=10时,溶液中水的电离程度比纯水小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】NA为阿伏加德罗常数的值。下列说法正确的是
| A.4.6g甲苯和甘油的混合物中含有氢原子数目为0.4NA |
B.1L 0.1mol/L  溶液中,所含阴离子数目为0.1NA 溶液中,所含阴离子数目为0.1NA |
C.标准状况下,2.24L  含有的中子数为1.1NA 含有的中子数为1.1NA |
D.酸性 溶液与1mol 溶液与1mol  完全反应,转移电子数为NA 完全反应,转移电子数为NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某温度下,部分电解质的电离平衡常数数据如下。
下列说法正确的是
 |  |  |
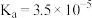 | 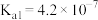  | 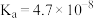 |
A.该温度下,等物质的量浓度的三种溶液的 大小关系: 大小关系: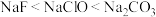 |
B. 的电离方程式为 的电离方程式为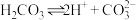 |
C.向 溶液中通入少量 溶液中通入少量 ,漂白性增强的原因是 ,漂白性增强的原因是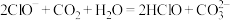 |
D.等浓度的 和 和 混合溶液中存在 混合溶液中存在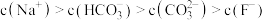 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.0.020 mol·L-1的HCN(aq)与0.020 mol·L-1 NaCN(aq)等体积混合得到的碱性混合溶液中:c(Na+)>c(CN-) |
| B.某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(A2-)=c(OH-)+c(H2A) |
| C.在物质的量浓度均为0.01 mol·L-1的CH3COOH和CH3COONa的混合溶液中:c(CH3COOH)+c(CH3COO-)=0.01 mol·L-1 |
D.c( )相等的(NH4)2SO4溶液、NH4HCO3溶液、NH4Cl溶液:c[(NH4)2SO4]>c(NH4HCO3)>c(NH4Cl) )相等的(NH4)2SO4溶液、NH4HCO3溶液、NH4Cl溶液:c[(NH4)2SO4]>c(NH4HCO3)>c(NH4Cl) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】25℃时,下列说法不正确 的是
| A.pH=3的硫酸溶液中,由水电离出的H+浓度为1.0 × 10−11 mol·L−1 |
| B.pH相等的盐酸和醋酸溶液中,c(Cl−)>c(CH3COO−) |
| C.NaHS溶液呈碱性,说明H2S是弱电解质 |
| D.pH=10的氨水中加入氯化铵固体,溶液pH减小 |
您最近一年使用:0次

 为阿伏加德罗常数值,下列说法正确的是
为阿伏加德罗常数值,下列说法正确的是 离子数为
离子数为

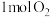 充分反应,产物的分子数为
充分反应,产物的分子数为
 和
和 微粒数之和为
微粒数之和为

