化工生产中含Cu2+的废水常用MnS(s)作沉淀剂,其反应原理为Cu2+(aq)+MnS(s) CuS(s)+Mn2+(aq)。一定温度下,下列有关该反应的推理正确的是
CuS(s)+Mn2+(aq)。一定温度下,下列有关该反应的推理正确的是
 CuS(s)+Mn2+(aq)。一定温度下,下列有关该反应的推理正确的是
CuS(s)+Mn2+(aq)。一定温度下,下列有关该反应的推理正确的是| A.该反应达到平衡时:c(Cu2+)=c(Mn2+) |
| B.平衡体系中加入少量CuS(s)后,c(Mn2+)变小 |
| C.平衡体系中加入少量Cu(NO3)2(s)后,c(Mn2+)变大 |
| D.该反应平衡常数表达式:K=Ksp(CuS)/Ksp(MnS) |
2018高二上·全国·专题练习 查看更多[5]
(已下线)2018年11月17日 《每日一题》人教选修4-周末培优黑龙江省哈尔滨市第六中学2020-2021学年高二上学期期末考试化学试题广东省省名校联盟2021届高三下学期开学考试(新高考)化学试题黑龙江省龙西北地区八校2020-2021学年高二下学期3月联考化学试题(已下线)专题22 沉淀溶解平衡及图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
更新时间:2018-11-22 20:47:52
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】25℃时,用Na2S沉淀Cu2+、Zn2+两种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示,下列说法不正确的是( )
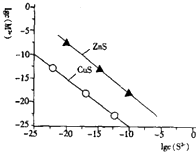

| A.向Cu2+浓度为10-5mol•L-1的工业废水中加入ZnS粉末,会有CuS沉淀析出 |
| B.25℃时K甲(CuS)约为1×10-35 |
| C.向100mLZn2+、Cu2+浓度均为10-5mol•L-1的混合溶液中逐滴加入10-4 mol•L-1的Na2S溶液,Cu2+先沉淀 |
| D.Na2S溶液中:c(S2-)+c(HS-)+c(H2S)═2c(Na+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下,t1时刻向两个盛有50mL蒸馏水的烧杯中分别加入①1gCaCO3、②1g蔗糖,搅拌,最终分别得到悬浊液和澄清溶液,溶解过程中分散系的导电能力变化如图。
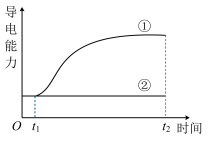
下列分析不正确 的是

下列分析
| A.该实验可证明蔗糖不是电解质 |
| B.该实验可证明碳酸钙是强电解质 |
C.当①中导电能力不变时,CaCO3(s) Ca2+(aq)+CO Ca2+(aq)+CO (aq)达到平衡 (aq)达到平衡 |
| D.t2时刻,①中再加1gCaCO3,导电能力不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】沉淀物并非绝对不溶。已知常温下: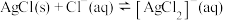
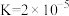 ,
, 的
的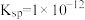 。下列说法不正确的是
。下列说法不正确的是
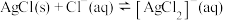
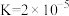 ,
, 的
的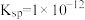 。下列说法不正确的是
。下列说法不正确的是| A.相同温度下,AgCl在NaCl溶液中的Ksp和其在AgNO3溶液中的Ksp相等 |
| B.欲将AgNO3溶液中的Ag+完全沉淀,可向溶液中加入过量的NaCl固体 |
| C.向饱和NaCl溶液中滴加少量AgNO3溶液和向AgNO3溶液中滴加饱和NaCl溶液的现象不同 |
D.1L0.1 NaCl溶液中AgCl溶解的质量约为 NaCl溶液中AgCl溶解的质量约为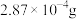 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法不正确的是
A.含 与 与 共1mol的溶液中, 共1mol的溶液中,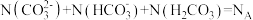 |
B.25℃时, 溶液的 溶液的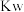 大于 大于 溶液的 溶液的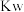 |
C.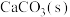 受热分解为 受热分解为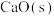 和 和 , , |
D.误将钡盐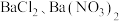 当作食盐食用后,常用0.5%的 当作食盐食用后,常用0.5%的 溶液解毒 溶液解毒 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】根据以下实验操作及现象能得出正确结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向溶有SO2的BaCl2溶液中通入气体X | 有白色沉淀产生 | 气体X一定有强氧化性 |
| B | 向等浓度等体积的H2O2中分别加入等浓度等体积的KMnO4溶液和CuSO4溶液 | 前者产生气泡速率快 | KMnO4的催化效果比CuSO4好 |
| C | 将银粉加到HI溶液中 | 产生无色气体和黄色沉淀 | I-和Ag+形成沉淀,促进Ag和H+反应 |
| D | 用铂电极电解等物质的量浓度的Fe(NO3)3和Cu(NO3)2混合溶液 | 开始时阴极无红色物质析出 | 氧化性:Cu2+<Fe2+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐1】某实验小组向1mL 0.lmol·L-l FeCl2溶液中依次加入下列试剂,记录的实验现象如下:
下列说法正确的是
| 试剂次序 | 试剂 | 现象 |
| ① | KSCN溶液 | 无明显现象 |
| ② | 足量氯水 | 溶液先变红色,后红色逐渐消失 |
| ③ | 足量盐酸酸化的BaCl2溶液 | 产生白色沉淀 |
| ④ | 再加入KSCN溶液 | 溶液变红色 |
| A.实验①说明Fe2+与KSCN溶液一定不发生反应 |
| B.实验②体现了氯水具有漂白性 |
C.实验③所得的上层清液中存在c(Ba2+)·c(SO )<Ksp(BaSO4) )<Ksp(BaSO4) |
| D.实验④说明过量氯水能与KSCN发生氧化还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关Ksp的叙述中正确的是()
| A.Ksp越大说明电解质的溶解度越大 |
| B.Ksp只与电解质的本性有关,而与外界条件无关 |
| C.Ksp表示难溶强电解质在水中达到沉淀溶解平衡时,溶液中离子浓度幂之积 |
| D.Ksp的数值只与温度有关 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列有关实验操作和结论均正确的是
选项 | 操作 | 结论 |
A | 配制Fe(NO3)2溶液时加入适量的硝酸 | 抑制Fe2+水解 |
B | 浓硫酸和蔗糖反应产生的气体通过足量的KMnO4溶液,气体全部被吸收且溶液紫红色褪去 | “黑面包实验”产生的气体具有还原性 |
C | 往溶液中滴加NaOH溶液,将湿润红色石蕊试纸置于试管口试纸不变蓝 | 原溶液中无NH4+ |
D | 幼儿使用含NaF的牙膏,可以使牙齿上的Ca5(PO4)3OH转化为Ca5(PO4)3F,防止蛀牙 | Ksp[Ca5(PO4)3F]<Ksp[Ca5(PO4)3OH] |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】温度25℃时,用Na2S、(NH4)2S等沉淀Cu2+、Zn2+两种金属离子(M2+),所需S2-最低浓度的对数值1gc(S2-)与1gc(M2+)关系如右图所示。下列说法不正确的是


| A.Na2S溶液中:c(S2-)+c(HS-)+c(H2S)=2c(Na+) |
| B.25℃时,Ksp(CuS)约为1×10-35 |
| C.向100mL浓度均为1×10-5 mol/L Zn2+、Cu2+的混合溶液中逐滴加入1×10-4mol/L的Na2S溶液,Cu2+先沉淀 |
| D.(NH4)2S溶液中: c(NH4+)+c(H+)=c(OH-)+2c(S2-)+c(HS-) |
您最近一年使用:0次
【推荐2】常温下,用AgNO3溶液分别滴定浓度均为0.01mol·L-1的KCl、K2C2O4溶液,所得的沉淀溶解平衡图像如图所示(不考虑 的水解)。下列叙述正确的是
的水解)。下列叙述正确的是
 的水解)。下列叙述正确的是
的水解)。下列叙述正确的是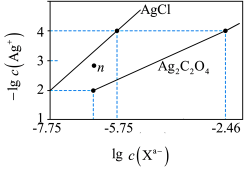
| A.Ksp(Ag2C2O4)的数量级等于10-7 |
| B.n点表示AgCl的过饱和溶液 |
C.向c(Cl-)=c( )的混合溶液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀 )的混合溶液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀 |
D.Ag2C2O4(s)+2Cl-(aq)⇌2AgCl(s)+ (aq)的平衡常数为1011.09 (aq)的平衡常数为1011.09 |
您最近一年使用:0次

 标准溶液滴定溶液中的
标准溶液滴定溶液中的 时,采用
时,采用 为指示剂。已知
为指示剂。已知 时,AgCl和
时,AgCl和 (砖红色)的沉淀溶解平衡曲线如下图所示,其中
(砖红色)的沉淀溶解平衡曲线如下图所示,其中 。下列叙述错误的是
。下列叙述错误的是

 、
、 不同温度下
不同温度下 在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是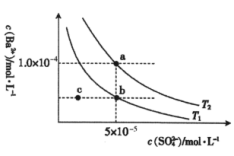

 时
时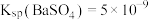
 曲线下方区域(不含曲线)任意一点时,均有
曲线下方区域(不含曲线)任意一点时,均有

