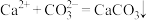某温度时,Ag2SO4在水中的沉淀溶解平衡曲线如图所示。该温度下,下列说法正确的是

| A.含有大量SO42-的溶液中肯定不存在Ag+ |
| B.Ag2SO4的溶度积常数(Ksp)为1×10-3 |
| C.0.02 mol·L-1的AgNO3溶液与0.02 mol·L-1的Na2SO4溶液等体积混合不会生成沉淀 |
| D.a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点 |
2010·广东汕头·一模 查看更多[17]
作业(二十一) 沉淀溶解平衡与溶度积(已下线)题型27 沉淀溶解平衡常数及其应用图象吉林省大安市第一中学校2021-2022学年高二上学期第三次月考化学试题云南省通海县一中2020-2021学年高二下学期期中考试化学试题吉林省榆树市实验高级中学2020-2021学年高二下学期第二次月考化学试题(已下线)第03章 水溶液中的离子反应与平衡(A卷基础强化篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)安徽省肥东县高级中学2020-2021学年高二上学期期中考试化学试题(已下线)山东省邹城市2018-2019学年高二上学期12月月考化学试卷安徽省合肥市六校2019-2020学年高二上学期期末考试化学试题云南省文山马关实验高级中学2019-2020学年高二期末考试化学试题广东省惠来县葵潭中学2019-2020学年高二上学期第二次月考化学试题【全国百强校】河北省石家庄市第一中学2018-2019学年高二上学期期中考试化学试题河南省安阳县第一高级中学2017-2018学年高二上学期第三次月考化学试卷辽宁省辽阳2017-2018学年高二化学上学期期末考试题(已下线)2010年广东省汕头市潮阳一中理综化学考前押题卷2014-2015辽宁省沈阳二中高二上学期12月月考化学试卷2016-2017学年黑龙江省哈尔滨市第六中学高二3月月考化学试卷
更新时间:2018-12-05 09:56:48
|
相似题推荐
单选题
|
适中
(0.65)
名校
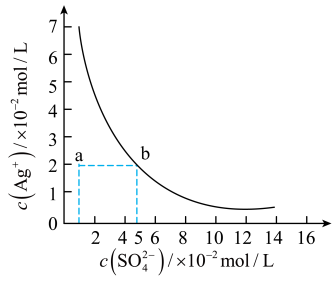
【推荐1】常温下,用0.100mol•L-1的NH4SCN溶液滴定25.00mL0.100mol•L-1AgNO3溶液,以NH4Fe(SO4)2•12H2O为指示剂,测得溶液中pSCN=‒lgc(SCN-)、pAg=‒lgc(Ag+)随加入NH4SCN溶液的体积变化如图所示。已知:Ag++SCN-⇌AgSCN↓,Ksp(Ag2SO4)=1.4×10-5。下列说法错误的是( )


| A.滴定至终点时溶液颜色变为红色,且振荡后不褪色 |
| B.该温度下AgSCN的溶度积常数Ksp=1.0×10-12 |
| C.为防止指示剂失效,溶液应维持酸性 |
| D.当加入15.00mLNH4SCN溶液时,溶液中c(SO42-)=0.14mol•L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃时,已知AgCl的Ksp=1.8×10-10,Ag2CO3在水中的沉淀溶解平衡曲线如图所示,下列说法错误的是
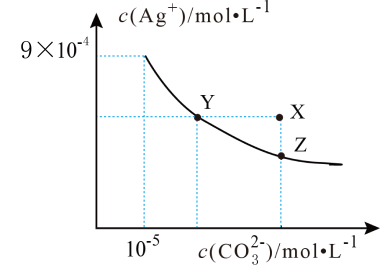

| A.Ag2CO3的Ksp为8.1×10-12 |
B.Ag2CO3(s)+2Cl-(aq)⇌2AgCl(s)+ (aq)的平衡常数K=2.5×108 (aq)的平衡常数K=2.5×108 |
C.在Ag2CO3的饱和溶液中加入K2CO3(s)可使c( )增大(由Y点到Z点) )增大(由Y点到Z点) |
D.在0.001mol•L-1AgNO3溶液中滴入同浓度的KCl和K2CO3的混合溶液, 先沉淀 先沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列有关离子浓度大小比较正确的是
| A.物质的量浓度均为0.1mol·L-1的三种物质的溶液:①NaAlO2,②CH3COONa,③NaHCO3,pH由大到小的顺序是①>③>② |
B.等pH的①(NH4)2SO4,②NH4HSO4,③NH4Cl,c(NH )由大到小的顺序是①>③>② )由大到小的顺序是①>③>② |
C.等浓度的①NH4Al(SO4)2,②(NH4)2CO3,③(NH4)2Fe(SO4)2,c(NH )由大到小的顺序是②>③>① )由大到小的顺序是②>③>① |
| D.相同温度下,将足量AgCl固体分别放入相同体积的①0.1mol·L-1盐酸,②0.1mol·L-1MgCl2溶液,③0.1mol·L-1AgNO3溶液中,c(Ag+)由大到小的顺序是③>②>① |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】 常用于锰盐制备,也用作氧化剂、催化剂等。由富锰废料(含
常用于锰盐制备,也用作氧化剂、催化剂等。由富锰废料(含 和少量
和少量 、
、 、
、 )进行废气脱硫并制备
)进行废气脱硫并制备 的工艺流程如下:
的工艺流程如下:

下列叙述正确的是
 常用于锰盐制备,也用作氧化剂、催化剂等。由富锰废料(含
常用于锰盐制备,也用作氧化剂、催化剂等。由富锰废料(含 和少量
和少量 、
、 、
、 )进行废气脱硫并制备
)进行废气脱硫并制备 的工艺流程如下:
的工艺流程如下:
下列叙述正确的是
A.“化浆”所得浆液中的锰元素均为 |
B.吸收 的主要反应为 的主要反应为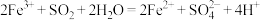 |
C.滤渣1中含有大量 ,应回收再利用 ,应回收再利用 |
| D.转化反应中氧化剂与还原剂物质的量之比为2:3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向2mL0.01mol/LNa2S溶液中先滴入几滴0.01mol∙L-1CuSO4溶液有黑色沉淀生成,再滴入0.01mol/LZnSO4溶液,又有白色沉淀生成 | Ksp(ZnS)<Ksp(CuS) |
| B | 室温下,用pH计测得0.1mol/LCH3COONH4溶液的pH小于0.1mol/LNaHCO3溶液 | 水解平衡常数:Kh(CH3COO-)<Kh( ) ) |
| C | 常温下,测得0.1mol/LNaA溶液的pH小于0.1mol/LNa2B溶液的pH | 酸性:HA>H2B |
| D | 向5mL0.005mol/LFeCl3溶液中加入5mL0.015mol/LKSCN溶液,溶液变红,再加入少量铁粉,溶液颜色变浅 | 加入铁粉后,Fe3++3SCN-⇌Fe(SCN)3向逆反应方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐1】铅蓄电池的拆解、回收和利用可以减少其对环境的污染,具有重要的可持续发展意义。利用废铅蓄电池的铅膏(主要成分为PbSO4、PbO2,还有少量Pb、Fe2O3、Al2O3)制取红丹(Pb3O4)的工艺流程如图:

已知:① 、
、 、
、 ;
;
②醋酸铅是弱电解质;
③当金属离子浓度低于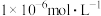 时,被认为沉淀完全。
时,被认为沉淀完全。
下列说法正确的是

已知:①
 、
、 、
、 ;
;②醋酸铅是弱电解质;
③当金属离子浓度低于
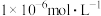 时,被认为沉淀完全。
时,被认为沉淀完全。下列说法正确的是
| A.“浸出”过程中将废铅膏研磨、使用高温条件均可以提高浸出率 |
| B.“调pH”步骤中调至pH约为5,可将铁铝杂质除尽 |
C.“沉铅”时主要发生的离子反应为: |
| D.反应过程中,H2O2和NaClO溶液均只作氧化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下,向10mL0.1mol·L-1CuCl2溶液中滴入0.1mol·L-l的Na2S溶液,溶液中-lgc(Cu2+)随滴入的Na2S溶液体积的变化如图所示。下列叙述正确的是
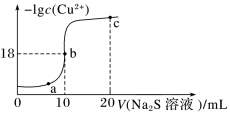

| A.Na2S溶液中:c(S2-)+c(HS-)+c(H2S)=2c(Na+) |
| B.Ksp(CuS)的数量级为10-36 |
| C.a、b、c三点对应溶液中,b点水的电离程度最大 |
| D.c点对应溶液成分只有Na2S |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列实验操作的目的或解释正确的是
| 实验设计或操作 | 实验目的或解释 | |
| A | 化学分析中,以 标准溶液滴定溶液中的 标准溶液滴定溶液中的 时,采用 时,采用 做指示剂,利用 做指示剂,利用 与 与 反应生成砖红色沉淀指示滴定终点 反应生成砖红色沉淀指示滴定终点 | 使用 做指示剂,因为相同温度下 做指示剂,因为相同温度下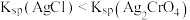 |
| B | 在某工业废水中加入 ,以除去废水中的 ,以除去废水中的 |  和 和 发生氧化还原反应生成 发生氧化还原反应生成 沉淀从而达到除杂的目的 沉淀从而达到除杂的目的 |
| C | 取5mL 0.1 KI溶液于试管中,加入1mL 0.1 KI溶液于试管中,加入1mL 0.1  溶液,充分反应后滴入5滴15%KSCN溶液 溶液,充分反应后滴入5滴15%KSCN溶液 | 若溶液变血红色,则KI与 的反应有一定限度 的反应有一定限度 |
| D | 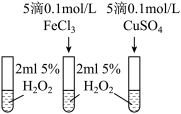 | 通过三支试管中气泡出现的快慢,比较 和 和 对 对 分解的催化效果 分解的催化效果 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】次磷酸钠( )广泛应用于化学镀镍,在生产
)广泛应用于化学镀镍,在生产 的过程中会产生大量废渣[主要含
的过程中会产生大量废渣[主要含 和
和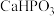 ,还含有少量
,还含有少量 ],一种回收次磷酸钠以及化学镀镍过程的工艺流程如图所示。
],一种回收次磷酸钠以及化学镀镍过程的工艺流程如图所示。
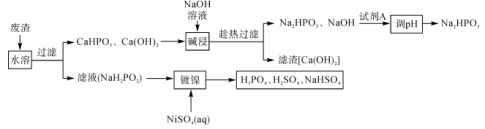
已知:①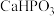 和
和 的
的 分别为
分别为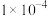 和
和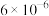 ;
;
② 为一元弱酸,
为一元弱酸, 为二元弱酸;
为二元弱酸;
③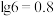 。
。
下列叙述错误的是
 )广泛应用于化学镀镍,在生产
)广泛应用于化学镀镍,在生产 的过程中会产生大量废渣[主要含
的过程中会产生大量废渣[主要含 和
和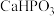 ,还含有少量
,还含有少量 ],一种回收次磷酸钠以及化学镀镍过程的工艺流程如图所示。
],一种回收次磷酸钠以及化学镀镍过程的工艺流程如图所示。
已知:①
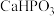 和
和 的
的 分别为
分别为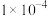 和
和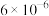 ;
;②
 为一元弱酸,
为一元弱酸, 为二元弱酸;
为二元弱酸;③
 。
。下列叙述错误的是
A.“趁热过滤”的目的是防止滤渣中的 溶解 溶解 |
B.“趁热过滤”后,要使滤液中 的浓度不小于0.01 mol⋅L 的浓度不小于0.01 mol⋅L ,则滤液的pH应不低于11.6 ,则滤液的pH应不低于11.6 |
C.试剂A可以是 , , 是正盐 是正盐 |
D.“镀镍”时,发生反应的离子方程式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】水体中的重金属离子如 、
、 等可以通过转化为
等可以通过转化为 、
、 沉淀除去。已知:室温下
沉淀除去。已知:室温下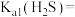
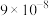 ,
,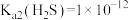 。下列说法正确的是
。下列说法正确的是
 、
、 等可以通过转化为
等可以通过转化为 、
、 沉淀除去。已知:室温下
沉淀除去。已知:室温下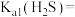
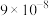 ,
,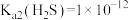 。下列说法正确的是
。下列说法正确的是A.0.1  溶液中: 溶液中: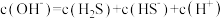 |
B.0.1  溶液中: 溶液中: |
C.向10 0.001 0.001  溶液中加入10 溶液中加入10 0.001 0.001  溶液,有沉淀析出。忽略混合时溶液体积的变化,说明 溶液,有沉淀析出。忽略混合时溶液体积的变化,说明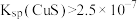 |
D.室温时,向0.001  粉末中加入10 粉末中加入10 0.1 0.1  溶液,充分浸出后所得溶液中 溶液,充分浸出后所得溶液中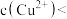 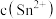 ,则 ,则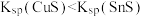 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知:对于含 Fe2(SO4)3、FeSO4和CuSO4各0.5 mol 的1 L 混合溶液,根据上表数据判断,下列说法错误的是
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp(25℃ ) | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| A.FeCl3 溶液溶解部分 Cu(OH)2 沉淀,主要是因为 Fe3+结合 Cu(OH)2 溶解的 OH— |
| B.向溶液中加入双氧水,并用CuO 粉末调节 pH,过滤后可获得溶质主要为CuSO4 的溶液 |
| C.若要完全除去其中的 Fe3+,可以加热搅拌,促进水解,从而产生 Fe(OH)3 沉淀 |
| D.将少量 FeCl3 粉末加入含 Cu(OH)2 的悬浊液中,其中 c(Cu2+)增大 |
您最近一年使用:0次

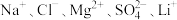 ,一种以该卤水为原料制备
,一种以该卤水为原料制备 的工艺流程如图:
的工艺流程如图: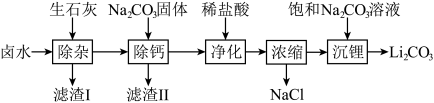
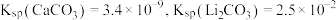 ,下列说法错误的是
,下列说法错误的是 和
和