下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 向盛有1 mL浓硫酸的试管中加入5 mL 0 .1 mol/L的K2Cr2O7溶液 | 溶液橙 色变深 | 增大生成物浓度,平衡Cr2O +H2O +H2O 2CrO 2CrO +2H逆向移动 +2H逆向移动 |
| B | 向Mg(OH)2悬浊液中加入少量醋酸铵晶体 | 沉淀溶解,溶液变澄清 | 说明反应Mg2++2NH3·H2O Mg(OH)2+2NH Mg(OH)2+2NH ,具有可逆性 ,具有可逆性 |
| C | 相同温度下,同时向①4mL0.1 mol/L. KMnO4),酸性溶液和②4 mL 0.2 mol/LKMnO4,酸性溶液中,分别加入4mL 1 mol/L. H2C2O4溶液 | ①中溶液先褪色 | 该实验条件下,KMnO4浓度越小,反应速率越快 |
| D | 向煤炉中灼热的煤炭上洒少量水 | 产生淡蓝色火焰煤炭燃烧更旺 | 加少量水后,可使煤炭燃烧放出更多的热量 |
| A.A | B.B | C.C | D.D |
更新时间:2019-01-01 18:28:23
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
| A.已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ·mol-1,氢气燃烧热为241.8kJ·mol-1 |
| B.C(石墨,s)=C(金刚石,s) ΔH=+1.9kJ/mol,则金刚石比石墨稳定 |
| C.某反应ΔH<0,ΔS>0,则该反应在任意条件下均可自发进行 |
D.Na2CO3在水溶液中的水解离子方程式:CO +2H2O⇌H2CO3+2OH− +2H2O⇌H2CO3+2OH− |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是:
| A.同温同压下H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件的ΔH都相同 |
| B.已知2H2(g)+O2(g)===2H2O(g) ΔH= -483.6 kJ/mol,则氢气的燃烧热为-241.8kJ/mol |
| C.CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2 ,所以CO的燃烧反应一定是吸热反应 |
| D.一定条件下2SO2(g)+O2(g)⇌2SO3(g) △H1 ,2SO2(g)+O2(g)⇌2SO3(l) △H2 则△H1<△H2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列有关热化学方程式的叙述正确的是
| A.已知C(石墨,s) = C(金刚石,s) ΔH>0,则金刚石比石墨稳定 |
| B.2CO(g)+O2(g)=2CO2(g) ΔH=﹣566 kJ·mol−1,则CO的摩尔燃烧焓为283 kJ∙mol−1 |
| C.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq) = CH3COONa(aq) + H2O(l) ΔH=−57.4 kJ∙mol−1 |
| D.已知2C(s)+2O2(g) =2CO2(g) ΔH1;2C(s)+O2(g) =2CO(g) ΔH2,则ΔH1>ΔH2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验方案能达到实验目的的是
| 选项 | 实验方案 | 实验目的 |
| A | 向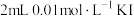 溶液中加入 溶液中加入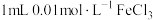 溶液,再滴加KSCN溶液,观察现象 溶液,再滴加KSCN溶液,观察现象 | 证明 与 与 的反应是有限度的 的反应是有限度的 |
| B | 量取同体积不同浓度的 溶液,分别加入等体积等浓度的 溶液,分别加入等体积等浓度的 溶液,对比现象 溶液,对比现象 | 探究浓度对化学反应速率的影响 |
| C | 用盛有酸性高锰酸钾溶液的洗气瓶洗气 | 除去甲烷中少量乙烯杂质 |
| D | 取少量样品于试管中,加入硝酸酸化,再加入 溶液,观察现象 溶液,观察现象 | 检验 是否变质 是否变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验方案设计不正确 的是
| 编号 | 目的 | 方案设计 |
| A | 探究Fe2+的还原性 | 在试管中加入少量酸性KMnO4溶液,然后向试管中逐滴加入FeSO4溶液,观察溶液颜色变化 |
| B | 探究Mg与Al的金属性强弱 | 两支试管中分别放入已除去氧化膜且大小相同的镁条和铝条,再各加入2mL2mol/L盐酸,比较实验现象 |
| C | 探究浓度对化学反应速率的影响 | 向两支试管分别加入2mL和1mL 0.1mol/LNa2S2O3溶液,向盛有1mL Na2S2O3溶液试管中加入1mL蒸馏水,再同时向两支试管中加2mL0.1mol/LH2SO4,振荡,比较溶液出现浑浊的快慢 |
| D | 探究淀粉是否完全水解 | 在0.5g淀粉中加入4mL2mol/L的硫酸溶液,加热一段时间,冷却后加入NaOH溶液调至碱性,再加入少量新制Cu(OH)2悬浊液加热,观察实验现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列生产或实验事实引出的结论不正确的是
| 选项 | 事实 | 结论 |
| A | 室温下,分别向2支试管中加入相同体积、相同浓度的 溶液,再分别加入相同体积不同浓度的稀硫酸,比较析出沉淀所需时间 溶液,再分别加入相同体积不同浓度的稀硫酸,比较析出沉淀所需时间 | 当其他条件不变时,反应物浓度增大,化学反应速率加快 |
| B | 向含有少量I2的淀粉溶液中加入NaOH溶液并加热,蓝色褪去 | NaOH是淀粉水解的催化剂 |
| C | 往黄色固体难溶物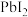 中加水,振荡,静置。取上层清液,然后加入NaI固体,产生黄色沉淀 中加水,振荡,静置。取上层清液,然后加入NaI固体,产生黄色沉淀 | 难溶物存在沉淀溶解平衡 |
| D | A、B两支试管中分别加入等体积5%的 溶液,在B中加入2~3滴 溶液,在B中加入2~3滴 溶液,B试管中产生气泡快 溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关物质变化蕴藏的反应原理正确的是
A.浓 需用棕色试剂瓶盛装且久置呈黄色,说明浓 需用棕色试剂瓶盛装且久置呈黄色,说明浓 见光分解 见光分解 |
B. 在高温下可以与 在高温下可以与 反应生成 反应生成 ,说明 ,说明 酸性强于 酸性强于 |
C.向石蕊试液中通入 ,石蕊变红且不褪色,说明 ,石蕊变红且不褪色,说明 水溶液呈酸性且无漂白性 水溶液呈酸性且无漂白性 |
D. 溶液滴入 溶液滴入 后变为黄色,说明 后变为黄色,说明 在碱性条件下被还原为 在碱性条件下被还原为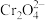 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2+O2 2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是
2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是
 2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是
2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是| A.使用催化剂是为了加快反应速率,提高生产效率 |
| B.在上述条件下,SO2不可能100%地转化为SO3 |
| C.为了提高SO2的转化率,应适当提高O2的浓度 |
| D.达到平衡时,SO2的浓度与SO3的浓度相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】在恒压、NO和O2的起始浓度一定的条件下, 催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是


| A.反应2NO(g)+O2(g)⇌2NO2(g)的△H<0 |
| B.图中X点所示条件下,延长反应时间能提高NO转化率 |
| C.图中Y点所示条件下,增加O2的浓度不能提高NO转化率 |
| D.实线部分先增大后减小的主要原因是:随着温度升高,平衡先向右移动,然后再向左移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下面的实验装置及其实验目的或实验结论,表述正确的是
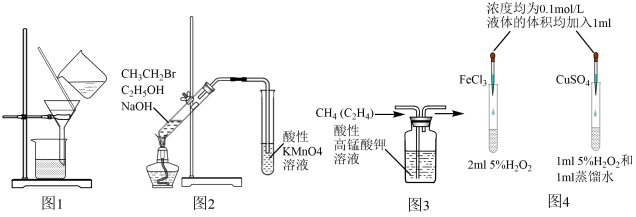

| A.图1用苯分离出碘水中的碘单质 |
B.图2酸性 溶液褪色,说明产生了乙烯 溶液褪色,说明产生了乙烯 |
| C.图3后加装有碱石灰的球形干燥管,才能获得纯净干燥的甲烷 |
| D.图4中产生气泡快,说明反应物浓度大,反应速率快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】为达成下列实验目的,所用方法错误的是
| 实验目的 | 实验方法 | |
| A | 检测淀粉是否完全水解 | 向水解液中滴加碘水 |
| B | 实验室制取溴苯 | 向苯和液溴的混合液中加入铁粉 |
| C | 检测蔗糖是否水解 | 向蔗糖溶液中滴加几滴稀硫酸,水浴加热几分钟,再加入银氨溶液,水浴加热 |
| D | 比较乙醇和水中氢的活泼性 | 将少量钠分别投入盛有无水乙醇和水的烧杯中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

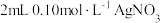 溶液中滴加2滴等浓度的
溶液中滴加2滴等浓度的 溶液,再加入2滴等浓度的
溶液,再加入2滴等浓度的 溶液,先产生白色
溶液,先产生白色 沉淀,后产生黄色
沉淀,后产生黄色 沉淀
沉淀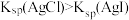
 溶液中加入少量
溶液中加入少量 固体,有白色沉淀生成,溶液红色变浅
固体,有白色沉淀生成,溶液红色变浅 水解引起的
水解引起的 试纸分别测定
试纸分别测定 溶液的酸碱性,
溶液的酸碱性,
 溶液与
溶液与