以粉煤灰(主要成分为Al2O3、SiO2,还含少量Fe2O3等)为原料制取氧化铝的部分工艺流程如下:
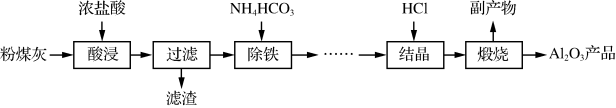
(1)“酸浸”过程发生的主要反应的离子方程式是_______________________________________________ 。
“酸浸”在恒容密闭反应釜中进行,温度不宜过高的原因是________________________________________________________________________ 。
(2)“除铁”生成Fe(OH)3的离子方程式为_________________ ,检验溶液中铁元素已经除尽的方法是________________________________________________________________________ 。
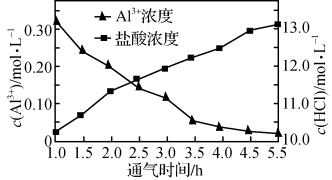
(3)“结晶”是向浓溶液中通入HCl气体,从而获得AlCl3·6H2O晶体的过程,溶液中Al3+和盐酸的浓度随通气时间的变化如下图所示。Al3+浓度减小的原因是_________________________ 。
(4)上述流程中,可以循环利用的物质是____ 。

(1)“酸浸”过程发生的主要反应的离子方程式是
“酸浸”在恒容密闭反应釜中进行,温度不宜过高的原因是
(2)“除铁”生成Fe(OH)3的离子方程式为
(3)“结晶”是向浓溶液中通入HCl气体,从而获得AlCl3·6H2O晶体的过程,溶液中Al3+和盐酸的浓度随通气时间的变化如下图所示。Al3+浓度减小的原因是

(4)上述流程中,可以循环利用的物质是
2019·江苏南通·一模 查看更多[5]
陕西省西安中学2023-2024学年高三上学期8月月考化学试题(已下线)小题34 工业流程中的分离与提纯——备战2021年高考化学经典小题考前必刷(全国通用)山西省太原市2021届高三上学期期中考试化学试题江苏省无锡江阴市2021届高三暑期作业开学检测化学试题【市级联考】江苏省南通市2019届高三上学期第一次模拟考试化学试题
更新时间:2019-03-04 11:17:51
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】叶蛇纹石是一种富镁硅酸盐矿物[主要成分为Mg6(Si4O10)(OH)8,还含有Al2O3、Fe2O3、FeO等杂质],利用该矿物生产铁红(Fe2O3)和碱式碳酸镁的工艺流程如图所示:
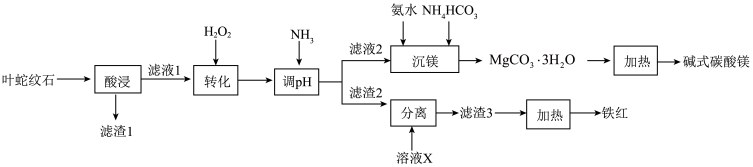
回答下列问题:
(1)“转化”步骤中,温度不能过高的原因是_______ 。“转化”时反应的离子方程式为_______ 。
(2)滤渣2的成分为_______ 。
(3)X通常选用_______ (填化学式)。
(4)“沉镁”步骤中氨水加入的量不能太多,否则MgCO3·H2O的产率会降低,其原因是_______ 。
(5)取9.1g碱式碳酸镁[xMgCO3·yMg(OH)2·zH2O],高温分解后,测得生成3.3gCO2、4.0gMgO,化学式中z=_______ 写出由MgCO3·3H2O生成产品的化学方程式:_______ 。
(6)碱式碳酸镁常用作新型阻燃剂,试分析碱式碳酸镁能够阻燃的原因:_______ 。(写出两点即可)。

回答下列问题:
(1)“转化”步骤中,温度不能过高的原因是
(2)滤渣2的成分为
(3)X通常选用
(4)“沉镁”步骤中氨水加入的量不能太多,否则MgCO3·H2O的产率会降低,其原因是
(5)取9.1g碱式碳酸镁[xMgCO3·yMg(OH)2·zH2O],高温分解后,测得生成3.3gCO2、4.0gMgO,化学式中z=
(6)碱式碳酸镁常用作新型阻燃剂,试分析碱式碳酸镁能够阻燃的原因:
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】以粉煤灰(主要含3Al2O3·2SiO2、SiO2,还含有少量CaO、Fe2O3等物质)为原料制取Al2O3的流程如图:
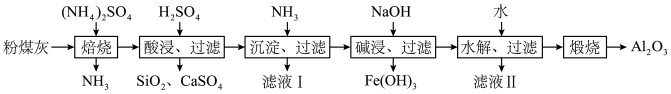
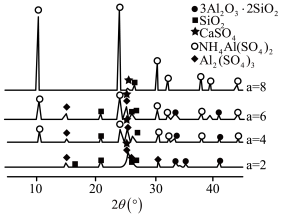
(1)当(NH4)2SO4和3Al2O3·2SiO2的配比a(a= )不同时,“焙烧”后所得产物的X射线衍射谱图如图所示(X射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。由图可知,当a=
)不同时,“焙烧”后所得产物的X射线衍射谱图如图所示(X射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。由图可知,当a=___ 时,3Al2O3·2SiO2的利用率最高。
(2)“沉淀、过滤”所得滤渣为Fe(OH)3和Al(OH)3,生成Fe(OH)3的离子反应方程式为___ 。
(3)“碱浸”加入NaOH发生反应的离子方程式为___ 。
(4)“水解、过滤”可得到Al(OH)3沉淀,升高温度有利于水解的原因是___ 。该步骤可将加水改成通入过量的___ 气体。
(5)流程中,可以回收并循环利用的物质除NH3外,还有___ 和___ 。

(1)当(NH4)2SO4和3Al2O3·2SiO2的配比a(a=
 )不同时,“焙烧”后所得产物的X射线衍射谱图如图所示(X射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。由图可知,当a=
)不同时,“焙烧”后所得产物的X射线衍射谱图如图所示(X射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。由图可知,当a=
(2)“沉淀、过滤”所得滤渣为Fe(OH)3和Al(OH)3,生成Fe(OH)3的离子反应方程式为
(3)“碱浸”加入NaOH发生反应的离子方程式为
(4)“水解、过滤”可得到Al(OH)3沉淀,升高温度有利于水解的原因是
(5)流程中,可以回收并循环利用的物质除NH3外,还有
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
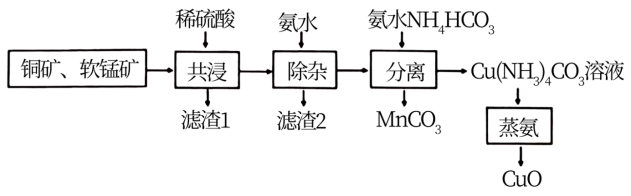
【推荐3】一种综合利用铜矿(主要为CuS,含少量FeS、SiO2)、软锰矿(主要为MnO2,含少量Fe2O3、Al2O3)制取MnCO3、CuO的工艺流程如图:
该工艺条件下,溶液中金属离子开始沉淀和沉淀完全的pH如表所示:
(1)“共浸”时,为提高浸取率,可采取的措施为___ 。(填一种方法即可)
(2)滤渣1含有S,为回收S,可先加入CS2,待固液分离后,再___ 得到S。
(3)“共浸”时,发生主要反应的离子方程式为___ 。
(4)该工艺“除杂”中,杂质离子沉淀的先后顺序为___ (填离子符号);“除杂”时控制pH为4.7~4.8,此时溶液中c(Fe3+):c(Al3+)=__ 。
(5)得到MnCO3的离子方程式为___ 。
(6)“蒸氨”是将氨从其盐及固液混合物中蒸出,相应的化学方程式为___ 。

该工艺条件下,溶液中金属离子开始沉淀和沉淀完全的pH如表所示:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ | Cu2+ |
| 开始沉淀pH | 1.9 | 7.0 | 3.0 | 8.1 | 4.8 |
| 沉淀完全(c=1.0×10-5mol·L-1)的pH | 3.2 | 9.0 | 4.7 | 10.1 | 6.7 |
(2)滤渣1含有S,为回收S,可先加入CS2,待固液分离后,再
(3)“共浸”时,发生主要反应的离子方程式为
(4)该工艺“除杂”中,杂质离子沉淀的先后顺序为
(5)得到MnCO3的离子方程式为
(6)“蒸氨”是将氨从其盐及固液混合物中蒸出,相应的化学方程式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
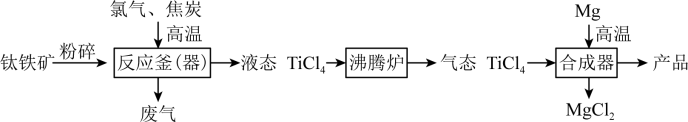
【推荐1】钛和钛合金被认为是21世纪的重要金属材料,广泛用于火箭、飞机制造业等。如图是工业上利用钛铁矿,其主要成分为钛酸亚铁(FeTiO3)制备金属钛的工艺流程。
资料:Ti为固体,化学性质稳定,不溶于稀硫酸、稀盐酸等。
(1)钛酸亚铁(FeTiO3)中钛元素的化合价是___________ 。
(2)反应釜中发生的反应是:2FeTiO3+7Cl2+6C 2X+2TiCl4+6CO,X的化学式是
2X+2TiCl4+6CO,X的化学式是___________ 。FeTiO3在该反应中发生了反应___________ (填“氧化”或“还原”)。
(3)利用上述方法制取的金属钛中可能会含有少量杂质,该杂质是金属___________ 。由金属钛的性质可知,除去这种杂质可以用___________ 。
资料:Ti为固体,化学性质稳定,不溶于稀硫酸、稀盐酸等。

(1)钛酸亚铁(FeTiO3)中钛元素的化合价是
(2)反应釜中发生的反应是:2FeTiO3+7Cl2+6C
 2X+2TiCl4+6CO,X的化学式是
2X+2TiCl4+6CO,X的化学式是(3)利用上述方法制取的金属钛中可能会含有少量杂质,该杂质是金属
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备金属铝的主要原料.工业上提取铝的工艺流程如下:
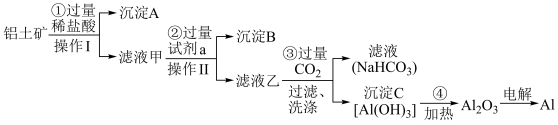
(1)沉淀A的化学式是____ ,沉淀B的化学式是____ ,滤液甲中所含金属离子是___ 、____ ,试剂a的化学式为__________ ;
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为___________________________________ ;
(3)Al2O3中所含的化学键的类型为________________ ;
(4)工业上用电解熔融Al2O3的方法制备金属铝,其反应方程式为_____________________________ ;
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂,下列氧化物中不能与铝粉组成铝热剂的是( )
a.MgO b.V2O5 c.Fe3O4 d.MnO2

(1)沉淀A的化学式是
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为
(3)Al2O3中所含的化学键的类型为
(4)工业上用电解熔融Al2O3的方法制备金属铝,其反应方程式为
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂,下列氧化物中不能与铝粉组成铝热剂的是
a.MgO b.V2O5 c.Fe3O4 d.MnO2
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】NiSO4•6H2O是一种绿色易溶于水的晶体,可由电镀废渣(除镍外,还含有铜、锌、铁等元素的化合物杂质)为原料获得。操作步骤如图:
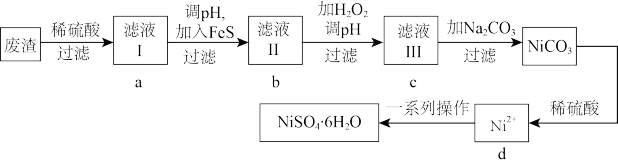
已知:各离子开始沉淀及完全沉淀时的pH如表所示:
(1)向滤液Ⅰ中加入FeS固体是为了生成更难溶于水的硫化物沉淀而除去Cu2+、Zn2+等杂质,则除去Cu2+的离子方程式为___ ,当c(Cu2+)≤1.0×10-5mol•L-1时,可认为Cu2+已沉淀完全,此时溶液中S2-的浓度不小于___ 。(已知:Ksp(CuS)=6.3×10-36。)
(2)根据对滤液Ⅱ的操作作答:
①向滤液Ⅱ中加H2O2的目的是___ 。
②调节滤液Ⅱ的pH,pH应控制在范围___ 。
③检验滤液Ⅱ中杂质金属离子是否除尽的试剂是___ 。
(3)滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后得到NiCO3固体,再加适量稀硫酸溶解又生成NiSO4,这两步操作的目的是___ 。
(4)得到的NiSO4溶液经蒸发浓缩、冷却结晶、过滤等一系列操作可得到NiSO4•6H2O晶体。为了提高产率,得到的母液要循环使用,则应该回流到流程中的___ 位置。(填a、b、c、d)

已知:各离子开始沉淀及完全沉淀时的pH如表所示:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.3 | 9.7 |
| Fe3+ | 2.2 | 3.2 |
| Ni2+ | 6.4 | 8.4 |
(1)向滤液Ⅰ中加入FeS固体是为了生成更难溶于水的硫化物沉淀而除去Cu2+、Zn2+等杂质,则除去Cu2+的离子方程式为
(2)根据对滤液Ⅱ的操作作答:
①向滤液Ⅱ中加H2O2的目的是
②调节滤液Ⅱ的pH,pH应控制在范围
③检验滤液Ⅱ中杂质金属离子是否除尽的试剂是
(3)滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后得到NiCO3固体,再加适量稀硫酸溶解又生成NiSO4,这两步操作的目的是
(4)得到的NiSO4溶液经蒸发浓缩、冷却结晶、过滤等一系列操作可得到NiSO4•6H2O晶体。为了提高产率,得到的母液要循环使用,则应该回流到流程中的
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】医用 用途广泛,可内用作催吐剂、外用作滴眼液。工业上用闪锌矿(主要成分为
用途广泛,可内用作催吐剂、外用作滴眼液。工业上用闪锌矿(主要成分为 、含少量
、含少量 、
、 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的流程如图:
的流程如图:
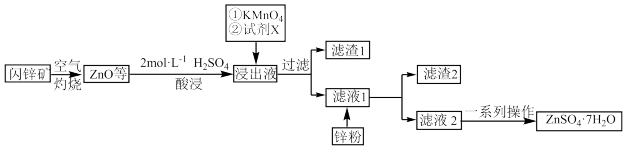
 金属阳离子沉淀的
金属阳离子沉淀的 如下表
如下表
回答下列问题:
(1)实验室进行“灼烧”操作时在___________ (填仪器名称)中进行,闪锌矿在灼烧时产生的有毒气体的分子式为___________ 。写出一种提高“酸浸”浸出率的方法:___________ 。
(2)向浸出液中加入 溶液的目的是除去浸出液中的
溶液的目的是除去浸出液中的 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。同时加入试剂 调节
调节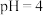 除去
除去 ,试剂X可以为
,试剂X可以为___________ (填化学式)。
(3)加入锌粉可以除去滤液中的 、
、 ,除去
,除去 的离子方程式为
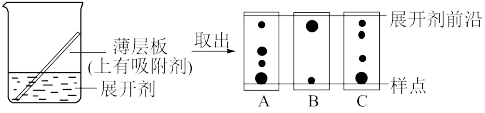
的离子方程式为___________ 。薄层色谱法是一种对混合样品进行快速分离和定性分析的一种实验技术,原理是利用样品中不同组分对同一吸附剂(固定相)的吸附能力不同,在展开剂溶液(移动相)流过吸附剂时,各组分就以不同速率随展开剂扩散,最后达到分析分离的目的。某实验小组利用薄层色谱法监控上述用 除去
除去 、
、 反应的进程,三组实验的结果如图所示,则还需要加入锌粉的是
反应的进程,三组实验的结果如图所示,则还需要加入锌粉的是___________ (填字母)。
(4)滤液2得到 的一系列操作为:加入
的一系列操作为:加入 调节溶液
调节溶液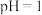 、
、___________ 、减压过滤、洗涤、干燥。
(5)某化工厂用mt闪锌矿(含 )制备
)制备 ,最后制得
,最后制得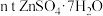 ,忽略工艺中后引入的锌元素,
,忽略工艺中后引入的锌元素, 的产率为
的产率为___________ (用含m、n、w的代数式表示)。
 用途广泛,可内用作催吐剂、外用作滴眼液。工业上用闪锌矿(主要成分为
用途广泛,可内用作催吐剂、外用作滴眼液。工业上用闪锌矿(主要成分为 、含少量
、含少量 、
、 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的流程如图:
的流程如图:
 金属阳离子沉淀的
金属阳离子沉淀的 如下表
如下表| 金属离子 |  |  |  |  |  |  |
开始沉淀 | 8.1 | 6.7 | 1.9 | 6.1 | 7.2 | 7.7 |
完全沉淀 | 10.1 | 9.0 | 3.2 | 8.2 | 9.2 | 9.7 |
回答下列问题:
(1)实验室进行“灼烧”操作时在
(2)向浸出液中加入
 溶液的目的是除去浸出液中的
溶液的目的是除去浸出液中的 ,该反应的离子方程式为
,该反应的离子方程式为 调节
调节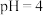 除去
除去 ,试剂X可以为
,试剂X可以为(3)加入锌粉可以除去滤液中的
 、
、 ,除去
,除去 的离子方程式为
的离子方程式为 除去
除去 、
、 反应的进程,三组实验的结果如图所示,则还需要加入锌粉的是
反应的进程,三组实验的结果如图所示,则还需要加入锌粉的是
(4)滤液2得到
 的一系列操作为:加入
的一系列操作为:加入 调节溶液
调节溶液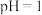 、
、(5)某化工厂用mt闪锌矿(含
 )制备
)制备 ,最后制得
,最后制得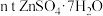 ,忽略工艺中后引入的锌元素,
,忽略工艺中后引入的锌元素, 的产率为
的产率为
您最近半年使用:0次
【推荐2】钯催化剂(主要成分为Pd、α−Al2O3,还含少量铁、铜等)在使用过程中,Pd易被氧化为难溶于酸的PdO而失活。一种从废钯催化剂中回收海绵钯的工艺流程如下图:

(1)“还原I”加入甲酸的目的是还原_______ (填化学式)。
(2)“酸浸”过程用盐酸和H2O2,Pd转化为 的离子方程式为
的离子方程式为_______ 。
(3)“还原II”中氧化剂和还原剂的物质的量之比为_______ 。
(4)酸浸在一定温度下充分浸取钯,得到氯亚钯酸(H2PdCl4)溶液,钯的浸出率与反应的温度、HCl浓度的关系如图所示。最佳的浸取温度是_______ ,最佳的HCl浓度为_______ 。

(5)“离子交换”和“洗脱”可简单表示为(RCl为阴离子交换树脂):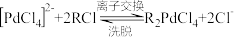 ,“离子交换”流出液中阳离子有H、
,“离子交换”流出液中阳离子有H、_______ (填离子符号)。
(6)“沉钯”过程中先加入氨水得到Pd(NH3)4Cl2溶液,再加入盐酸后得到Pd(NH3)2Cl2沉淀,用化学平衡知识解释加入盐酸的作用_______ 。
(7)已知:常温下,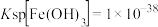 ,
,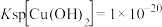 。假设在流出液中各离子的浓度均为0.1mol/L,加入氨水调节pH后过滤,滤液经一系列操作可以得到CuCl2·6H2O。需调节pH的范围是
。假设在流出液中各离子的浓度均为0.1mol/L,加入氨水调节pH后过滤,滤液经一系列操作可以得到CuCl2·6H2O。需调节pH的范围是_______ 。(当离子浓度小于 mol/L时认为已沉淀完全)。
mol/L时认为已沉淀完全)。

(1)“还原I”加入甲酸的目的是还原
(2)“酸浸”过程用盐酸和H2O2,Pd转化为
 的离子方程式为
的离子方程式为(3)“还原II”中氧化剂和还原剂的物质的量之比为
(4)酸浸在一定温度下充分浸取钯,得到氯亚钯酸(H2PdCl4)溶液,钯的浸出率与反应的温度、HCl浓度的关系如图所示。最佳的浸取温度是

(5)“离子交换”和“洗脱”可简单表示为(RCl为阴离子交换树脂):
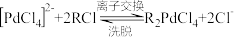 ,“离子交换”流出液中阳离子有H、
,“离子交换”流出液中阳离子有H、(6)“沉钯”过程中先加入氨水得到Pd(NH3)4Cl2溶液,再加入盐酸后得到Pd(NH3)2Cl2沉淀,用化学平衡知识解释加入盐酸的作用
(7)已知:常温下,
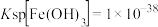 ,
,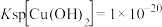 。假设在流出液中各离子的浓度均为0.1mol/L,加入氨水调节pH后过滤,滤液经一系列操作可以得到CuCl2·6H2O。需调节pH的范围是
。假设在流出液中各离子的浓度均为0.1mol/L,加入氨水调节pH后过滤,滤液经一系列操作可以得到CuCl2·6H2O。需调节pH的范围是 mol/L时认为已沉淀完全)。
mol/L时认为已沉淀完全)。
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】二氯异氰尿酸钠(NaC3N3O3Cl2)是一种高效广谱杀菌消毒剂,它常温下为白色固体,难溶于冷水。实验室利用下列装置先制备高浓度的NaClO溶液,再由三颈烧瓶上口加入氰尿酸(C3H3N2O3)固体,在10℃下反应制备二氯异氰尿酸钠。已知:2NaClO+C3H3N3O3→NaC3N3O3Cl2+NaOH+H2O
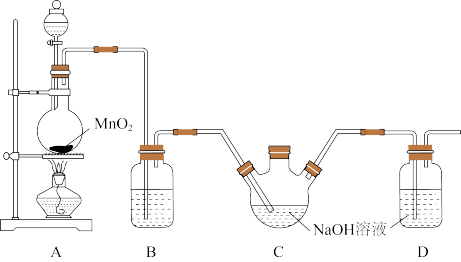
回答下列问题:
(1)装置A中的化学反应方程式为_________ 。
(2)装置B内盛装的试剂为__________ 。
(3)装置C内制备 NaClO溶液完成的现象是________ 。
(4)反应过程中仍需不断通入气体的原因是________ 。
(5)反应结束后,C中浊液经过滤、____________ 、干燥得粗产品二氯异氰尿酸钠。
(6)通过下列实验检测二氯异氰尿酸钠样品中有效氯的含量。实验检测原理为:
C3N3O3Cl +H++2H2O = C3H3N3O3+2HClO
+H++2H2O = C3H3N3O3+2HClO
HClO + 2I−+ H+ = I2+Cl−+ H2O
I2+2S2O = S4O
= S4O +2I−
+2I−
准确称取1.1000g样品,用容量瓶配成100mL溶液;取10.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用0.1000mol•L−1Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。该样品的有效氯为_______ (计算结果保留三位有效数字。该样品的有效氯=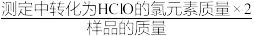 ×100%)。
×100%)。

回答下列问题:
(1)装置A中的化学反应方程式为
(2)装置B内盛装的试剂为
(3)装置C内制备 NaClO溶液完成的现象是
(4)反应过程中仍需不断通入气体的原因是
(5)反应结束后,C中浊液经过滤、
(6)通过下列实验检测二氯异氰尿酸钠样品中有效氯的含量。实验检测原理为:
C3N3O3Cl
 +H++2H2O = C3H3N3O3+2HClO
+H++2H2O = C3H3N3O3+2HClOHClO + 2I−+ H+ = I2+Cl−+ H2O
I2+2S2O
 = S4O
= S4O +2I−
+2I−准确称取1.1000g样品,用容量瓶配成100mL溶液;取10.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用0.1000mol•L−1Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。该样品的有效氯为
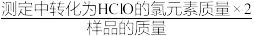 ×100%)。
×100%)。
您最近半年使用:0次
【推荐1】铬(Cr)广泛应用于冶金、化工、航天等领域。工业上以络铁矿(主要成分为 ,含有少量
,含有少量 )为原料制备金属铬的工艺流程如图所示:
)为原料制备金属铬的工艺流程如图所示:
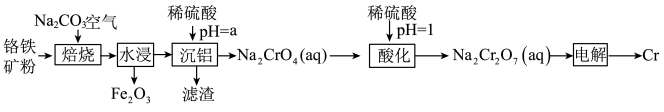
回答下列问题:
(1)基态 核外电子中未成对电子数为
核外电子中未成对电子数为___________ 。
(2)“焙烧”中生成的氧化产物有___________ (填化学式,下同), 转化为
转化为___________ 。
(3)常温下,“沉铝”时调节pH,当a=5时,溶液中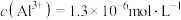 ,则
,则 的溶度积常数为
的溶度积常数为___________ 。
(4)“酸化”中反应的离子方程式为___________ ,若该反应的平衡常数 ,已知:“酸化”后溶液中
,已知:“酸化”后溶液中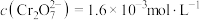 ,则溶液中
,则溶液中
___________  。
。
(5)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中 、
、 采用面心立方最密堆积方式(处于面对角线上的钙离子与氧离子紧密相邻)。
采用面心立方最密堆积方式(处于面对角线上的钙离子与氧离子紧密相邻)。
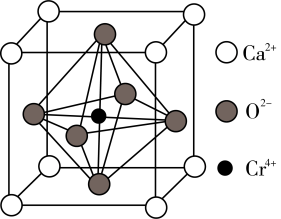
①已知钙离子、氧离子半径分别为xpm、ypm,晶胞中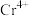 位于
位于 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为___________ pm。
②已知阿伏加德罗常数为 ,则该复合氧化物的摩尔体积
,则该复合氧化物的摩尔体积
___________  (列出计算式)。
(列出计算式)。
 ,含有少量
,含有少量 )为原料制备金属铬的工艺流程如图所示:
)为原料制备金属铬的工艺流程如图所示:
回答下列问题:
(1)基态
 核外电子中未成对电子数为
核外电子中未成对电子数为(2)“焙烧”中生成的氧化产物有
 转化为
转化为(3)常温下,“沉铝”时调节pH,当a=5时,溶液中
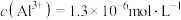 ,则
,则 的溶度积常数为
的溶度积常数为(4)“酸化”中反应的离子方程式为
 ,已知:“酸化”后溶液中
,已知:“酸化”后溶液中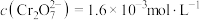 ,则溶液中
,则溶液中
 。
。(5)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中
 、
、 采用面心立方最密堆积方式(处于面对角线上的钙离子与氧离子紧密相邻)。
采用面心立方最密堆积方式(处于面对角线上的钙离子与氧离子紧密相邻)。
①已知钙离子、氧离子半径分别为xpm、ypm,晶胞中
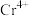 位于
位于 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为②已知阿伏加德罗常数为
 ,则该复合氧化物的摩尔体积
,则该复合氧化物的摩尔体积
 (列出计算式)。
(列出计算式)。
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】侯氏制碱法为我国纯碱工业做出了重要贡献。
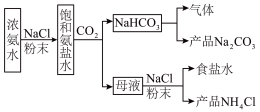
I.某化学兴趣小组模拟侯氏制碱法制备 ,进一步处理得到
,进一步处理得到 和
和 ,实验流程如图:
,实验流程如图:
回答下列问题:
(1)生成 的总反应的化学方程式为
的总反应的化学方程式为___________ 。
II.实验中制得的纯碱中含有少量NaCl,该小组设计如图所示装置,测定实验得到的纯碱中 的含量。
的含量。
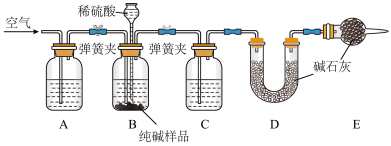
(2)装置A中的试剂为___________ ,装置C中的试剂为___________ 。
(3)实验结束后通入空气的目的:___________ 。
(4)实验前称取26.50g样品,实验后测得D装置增重8.80g,则样品中 的质量分数为
的质量分数为___________ (保留2位小数)。按照以上装置及操作,有同学提出测定结果可能会偏大,他的理由是___________ 。
I.某化学兴趣小组模拟侯氏制碱法制备
 ,进一步处理得到
,进一步处理得到 和
和 ,实验流程如图:
,实验流程如图:
回答下列问题:
(1)生成
 的总反应的化学方程式为
的总反应的化学方程式为II.实验中制得的纯碱中含有少量NaCl,该小组设计如图所示装置,测定实验得到的纯碱中
 的含量。
的含量。
(2)装置A中的试剂为
(3)实验结束后通入空气的目的:
(4)实验前称取26.50g样品,实验后测得D装置增重8.80g,则样品中
 的质量分数为
的质量分数为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
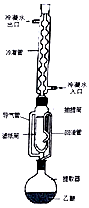
【推荐3】索氏提取法是测定动植物样品中粗脂肪含量的标准方法。其原理是利用如图装置,用无水乙醚等有机溶剂连续、反复、多次萃取动植物样品中的粗脂肪。具体步骤如下:
①包装: 取滤纸制成滤纸筒,放入烘箱中干燥后,移至仪器X中冷却至室温,然后放入称量瓶中称量,质量记作a; 在滤纸筒中包入一定质量研细的样品,放入烘箱中干燥后,移至仪器X 中冷却至室温,然后放入称量瓶中称量,质量记作b。
②萃取: 将装有样品的滤纸筒用长镊子放入抽提筒中,注入一定量的无水乙醚,使滤纸筒完全浸没入乙醚中,接通冷凝水,加热并调节温度,使冷凝下滴的无水乙醚呈连珠状,至抽提筒中的无水乙醚用滤纸点滴检查无油迹为止(大约6h~12h)。
③称量: 萃取完毕后,用长镊子取出滤纸筒,在通风处使无水乙醚挥发,待无水乙醚挥发后,将滤纸筒放入烘箱中干燥后,移至仪器X 中冷却至室温,然后放入称量瓶中称量,质量记作c。
回答下列问题:
(1)实验中三次使用的仪器X 的名称为__________________ 。为提高乙
醚蒸气的冷凝效果,索氏提取器可选用下列_______ (填字母) 代。



a空气冷凝管b直形冷凝管c蛇形冷凝管
(2) 实验中必须十分注意乙醚的安全使用,如不能用明火加热、室内保持通风
等。为防止乙醚挥发到空气中形成燃爆,常在冷凝管上口连接一个球形干燥管,其中装入
的药品为_______ (填字母)。
a活性炭b碱石灰c P2O5d浓硫酸
无水乙醚在空气中可能氧化生成少量过氧化物,加热时发生爆炸。检验无水乙醚中是否含有过氧化物的方法是_______________________ 。
(3) 实验中需控制温度在70℃~80℃之间,考虑到安全等因素,应采取的加热方式是_______ 。当无水乙醚加热沸腾后,蒸气通过导气管上升,被冷凝为液体滴入抽提筒中,当液面超过回流管最高处时,萃取液即回流入提取器(烧瓶)中……该过程连续、反复、多次进行,则萃取液回流入提取器(烧瓶) 的物理现象为_______ 。索氏提取法与一般萃取法相比较,其优点为___________________________ 。
(4) 数据处理: 样品中纯脂肪百分含量_________ (填“<”、“>”或“=”) (b-c)/(b-a)×100%;测定中的样品、装置、乙醚都需要进行脱水处理,否则导致测定结果__________ (填“偏高”、“偏低”或“无影响”)。
①包装: 取滤纸制成滤纸筒,放入烘箱中干燥后,移至仪器X中冷却至室温,然后放入称量瓶中称量,质量记作a; 在滤纸筒中包入一定质量研细的样品,放入烘箱中干燥后,移至仪器X 中冷却至室温,然后放入称量瓶中称量,质量记作b。
②萃取: 将装有样品的滤纸筒用长镊子放入抽提筒中,注入一定量的无水乙醚,使滤纸筒完全浸没入乙醚中,接通冷凝水,加热并调节温度,使冷凝下滴的无水乙醚呈连珠状,至抽提筒中的无水乙醚用滤纸点滴检查无油迹为止(大约6h~12h)。
③称量: 萃取完毕后,用长镊子取出滤纸筒,在通风处使无水乙醚挥发,待无水乙醚挥发后,将滤纸筒放入烘箱中干燥后,移至仪器X 中冷却至室温,然后放入称量瓶中称量,质量记作c。
回答下列问题:
(1)实验中三次使用的仪器X 的名称为
醚蒸气的冷凝效果,索氏提取器可选用下列



a空气冷凝管b直形冷凝管c蛇形冷凝管
(2) 实验中必须十分注意乙醚的安全使用,如不能用明火加热、室内保持通风
等。为防止乙醚挥发到空气中形成燃爆,常在冷凝管上口连接一个球形干燥管,其中装入
的药品为

a活性炭b碱石灰c P2O5d浓硫酸
无水乙醚在空气中可能氧化生成少量过氧化物,加热时发生爆炸。检验无水乙醚中是否含有过氧化物的方法是
(3) 实验中需控制温度在70℃~80℃之间,考虑到安全等因素,应采取的加热方式是
(4) 数据处理: 样品中纯脂肪百分含量
您最近半年使用:0次



