用活性炭还原法可以处理氮氧化物。某研究小组向2L密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g) 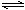 N2(g)+CO2(g) △H<0。在T1℃时,反应进行到不同时间测得各物质的浓度(mol/L)如表所示,则下列说法不正确的是
N2(g)+CO2(g) △H<0。在T1℃时,反应进行到不同时间测得各物质的浓度(mol/L)如表所示,则下列说法不正确的是
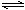 N2(g)+CO2(g) △H<0。在T1℃时,反应进行到不同时间测得各物质的浓度(mol/L)如表所示,则下列说法不正确的是
N2(g)+CO2(g) △H<0。在T1℃时,反应进行到不同时间测得各物质的浓度(mol/L)如表所示,则下列说法不正确的是| 时间/t(min) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| A.10~20 min内,NO的平均反应速率为0.018mol/(L∙min) |
| B.T1℃时,该反应的平衡常数K=0.25 |
| C.保持与前30min的反应条件相同,再向容器中加入2molN2和2molNO,则平衡向左移动 |
| D.30min后,只改变了一个条件,根据上述表格判断,该条件可能为缩小容器体积 |
2019·江西赣州·二模 查看更多[4]
【校级联考】江西省南康中学、于都中学2019届高三下学期第二次联考化学试题【全国百强校】福建省厦门双十中学2018-2019学年高二下学期第二次月考化学试题(已下线)课时35 化学反应速率及影响因素-2022年高考化学一轮复习小题多维练(全国通用)天津汇文中学2022-2023学年高二上学期第一次阶段性测试化学试题
更新时间:2019/03/07 08:48:43
|
相似题推荐
单选题-单题
|
较难
(0.4)
【推荐1】常温下,往烧杯中加入10mL 1mol/L  溶液和10mL 2mol/L KI溶液,
溶液和10mL 2mol/L KI溶液, 随时间变化如图所示,不考虑溶液混合时体积的改变。下列说法正确的是
随时间变化如图所示,不考虑溶液混合时体积的改变。下列说法正确的是
 溶液和10mL 2mol/L KI溶液,
溶液和10mL 2mol/L KI溶液, 随时间变化如图所示,不考虑溶液混合时体积的改变。下列说法正确的是
随时间变化如图所示,不考虑溶液混合时体积的改变。下列说法正确的是 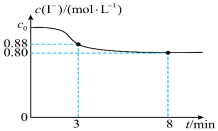
| A.反应一段时间后溶液颜色逐渐变浅 |
B. |
C.3~8min内, 的平均反应速率为0.016mol/(L·min) 的平均反应速率为0.016mol/(L·min) |
| D.8min时,往烧杯中滴加KSCN溶液,溶液不变红 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】将0.20mol NO和0.20mol CO混合气体充入容积为1.0L的恒容密闭容器中,分别在 和
和 温度下发生反应:
温度下发生反应: 。反应过程中容器内
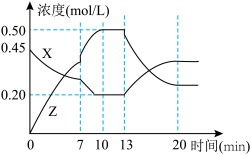
。反应过程中容器内 的物质的量随时间变化关系如图所示,下列说法正确的是
的物质的量随时间变化关系如图所示,下列说法正确的是

 和
和 温度下发生反应:
温度下发生反应: 。反应过程中容器内
。反应过程中容器内 的物质的量随时间变化关系如图所示,下列说法正确的是
的物质的量随时间变化关系如图所示,下列说法正确的是
A. 的 的 |
B.温度 时,前12分钟 时,前12分钟 的平均反应速率 的平均反应速率 |
C.温度 时,该反应的平衡常数 时,该反应的平衡常数 |
D.温度 时,若起始向容器中通入0.10mol NO、0.30mol CO、0.10mol 时,若起始向容器中通入0.10mol NO、0.30mol CO、0.10mol 和0.10mol 和0.10mol ,反应向正方向进行 ,反应向正方向进行 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】对于平衡体系mA(g)+nB(g)⇌pC(g)+qD(g) △H=b kJ·mol-1,下列结论中错误的是
| A.若温度不变,将容器的体积缩小到原来的一半,达到新平衡时A的浓度为原来的2.2倍,则m+n<p+q |
| B.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n |
| C.保持其它条件不变,升高温度,D的体积分数增大说明该反应的△H<0。 |
| D.若m+n=p+q,则向含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在特制的密闭真空容器中加入一定量纯净的氨基甲酸铵固体(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g) ΔH>0。下列说法中正确的是
2NH3(g)+CO2(g) ΔH>0。下列说法中正确的是
 2NH3(g)+CO2(g) ΔH>0。下列说法中正确的是
2NH3(g)+CO2(g) ΔH>0。下列说法中正确的是| A.密闭容器中气体的平均相对分子质量不变则该反应达到平衡状态 |
| B.该反应在任何条件下都能自发进行 |
| C.再加入一定量氨基甲酸铵,可加快反应速率 |
| D.保持温度不变,压缩体积,达到新的平衡时,NH3的浓度不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】在恒温恒压下,向密闭容器中充入4molSO2和2molO2,发生如下反应:2SO2(g)+O2(g)  2SO3(g) ΔH<0,2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量QkJ。则下列分析正确的是
2SO3(g) ΔH<0,2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量QkJ。则下列分析正确的是
 2SO3(g) ΔH<0,2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量QkJ。则下列分析正确的是
2SO3(g) ΔH<0,2min后,反应达到平衡,生成SO3为1.4mol,同时放出热量QkJ。则下列分析正确的是| A.若把条件“恒温恒压”改为“恒温恒容”,则平衡时放出热量小于QkJ |
| B.2min后,向容器中再通入一定量的SO3气体,重新达到平衡时,SO2的含量变小 |
| C.若把条件“恒温恒压”改为“恒压绝热”,则平衡后n(SO3)大于1.4mol |
| D.若反应开始时容器体积为2L,则v(SO3)=0.7mol·L-1·min-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】某温度下,在三个容积均为1L的恒容密闭容器中仅发生反应: 2NO(g)+Br2(g) 2NOBr(g)(正反应放热)。下列说法正确的是
2NOBr(g)(正反应放热)。下列说法正确的是
 2NOBr(g)(正反应放热)。下列说法正确的是
2NOBr(g)(正反应放热)。下列说法正确的是容器 编号 | 物质的起始浓度(mol/L) | 物质的平衡浓度(mol/L) | ||
c(NO) | c(Br2) | c(NOBr) | c(NOBr) | |
I | 0.3 | 0.15 | 0.1 | 0.2 |
II | 0.4 | 0.2 | 0 | |
III | 0 | 0 | 0.2 | |
| A.容器II达平衡所需的时间为4min,则v(Br2)=0.05mol/(L•min) |
| B.达平衡时,容器I与容器III中的总压强之比为2:1 |
| C.升高温度,逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
| D.达平衡时,容器II中c(Br2)/c(NOBr)比容器III中的小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
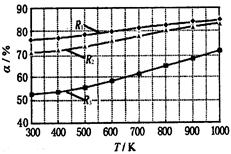
【推荐2】碳酸甲乙酯(CH3OCOOC2H5)是一种理想的锂电池有机电解液。生成碳酸甲乙酯的原理为:C2H5OCOOC2H5(g)+ CH3OCOOCH3(g) 2 CH3OCOOC2H5(g).其他条件相同,CH3OCOOCH3的平衡转化率(α)与温度(T),反应物配比(R=n(C2H5OCOOC2H5):n(CH3OCOOCH3))的关系如下图所示.三种反应物配比分别为1:1,2:1,3:1.下列说法不正确的是
2 CH3OCOOC2H5(g).其他条件相同,CH3OCOOCH3的平衡转化率(α)与温度(T),反应物配比(R=n(C2H5OCOOC2H5):n(CH3OCOOCH3))的关系如下图所示.三种反应物配比分别为1:1,2:1,3:1.下列说法不正确的是
 2 CH3OCOOC2H5(g).其他条件相同,CH3OCOOCH3的平衡转化率(α)与温度(T),反应物配比(R=n(C2H5OCOOC2H5):n(CH3OCOOCH3))的关系如下图所示.三种反应物配比分别为1:1,2:1,3:1.下列说法不正确的是
2 CH3OCOOC2H5(g).其他条件相同,CH3OCOOCH3的平衡转化率(α)与温度(T),反应物配比(R=n(C2H5OCOOC2H5):n(CH3OCOOCH3))的关系如下图所示.三种反应物配比分别为1:1,2:1,3:1.下列说法不正确的是
| A.该反应△H > 0 |
| B.R1对应的反应物配比为3:1 |
| C.650℃,反应物配比为1:1时,平衡常数K = 6 |
| D.该反应为取代反应 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
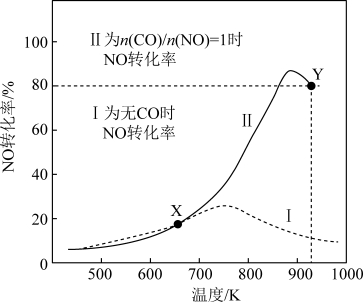
【推荐3】某研究小组以AgZSM为催化剂,在容积为1L的容器中,相同时间下测得0.1molNO转化为N2的转化率随温度变化如图所示[无CO时反应为2NO(g) ⇌N2(g)+O2(g);有CO时反应为2CO(g)+2NO(g) ⇌ 2CO2+N2(g)]。下列说法正确的是

| A.反应2NO(g)⇌N2(g)+O2(g)的△H>0 |
B.达平衡后,其他条件不变,使 >1,CO转化率下降 >1,CO转化率下降 |
| C.X点可以通过更换高效催化剂提高相同时间下NO的转化率 |
| D.Y点再通入CO、N2各0.01mol,此时v(CO,正)<v(CO,逆) |
您最近一年使用:0次

 bZ(g)
bZ(g)