有A、B、C、D、E、F、G七种元素,它们的原子序数依次增大。其中A、B、C、D、E 、F为短周期主族元素, G为第四周期元素。请回答问题。
(1)D是___________ ,E是___________ (填元素符号)。
(2)B基态原子中能量最高的电子,原子轨道呈__________ 形。
(3)比较键长:A — B__________ A — C (填“>”、“=”或“<”)
(4)G的原子结构示意图为:____________ ,G3+ 离子电子排布式为_________________ 。
(5)某同学根据上述信息,推断D基态原子的核外电子排布图为,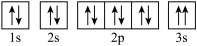 该同学所画的电子排布图违背了
该同学所画的电子排布图违背了____________________ 。
(6)金属铜和B的最高价氧化物的水化物的稀溶液可以反应,反应的离子方程式为:_________________ 。
| A是宇宙中最丰富的元素,其电子数和电子层数相等 |
| B原子的核外p电子数比s电子数少1 |
| C基态原子L层无空轨道,且成对电子与不成对电子占据的轨道数相等 |
| D原子的第一至第四电离能分别是: I1=730 kJ/mol I2 = 1455 kJ/mol I3 = 8633 kJ/mol I4= 11580 kJ/mol |
| E常温常压下,单质是淡黄色固体,常在火山口附近沉积 |
| F电负性比E大,其单质的水溶液具有漂白性 |
| G在周期表的第八列,是地壳中含量第二位的金属 |
(1)D是
(2)B基态原子中能量最高的电子,原子轨道呈
(3)比较键长:A — B
(4)G的原子结构示意图为:
(5)某同学根据上述信息,推断D基态原子的核外电子排布图为,
 该同学所画的电子排布图违背了
该同学所画的电子排布图违背了(6)金属铜和B的最高价氧化物的水化物的稀溶液可以反应,反应的离子方程式为:
更新时间:2019/04/01 09:27:52
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】氟代硼酸钾(KBe2BO3F2)是激光器的核心材料,我国化学家在此领域的研究走在了世界的最前列。回答下列问题:
(1)氟代硼酸钾中各元素原子的第一电离能大小顺序是F>O>______________ 。基态K+电子占据最高能级的电子云轮廓图为_____________ 形。
(2) NaBH4是有机合成中常用的还原剂,其中阴离子的键角为___________ 。
(3)下列硼原子电子排布图表示的状态中,能量最低和最高的分别为___________ 、___________ (填字母标号)。
A. B.
B.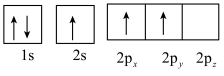
C. D.
D.
(4)硼元素的简单氢化物BH3不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。

①B2H6分子结构如图,则B原子的杂化方式为_________ 。
②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是_______________ ,写出一种与氨硼烷互为等电子体的分子________________ (填化学式)。
(5)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。P的配位数为_____________ ,磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是_______________ ,已知晶胞边长为apm,则磷化硼晶体的密度是___________ g·cm-3。

(1)氟代硼酸钾中各元素原子的第一电离能大小顺序是F>O>
(2) NaBH4是有机合成中常用的还原剂,其中阴离子的键角为
(3)下列硼原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B.
C.
 D.
D.
(4)硼元素的简单氢化物BH3不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。

①B2H6分子结构如图,则B原子的杂化方式为
②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是
(5)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。P的配位数为

您最近半年使用:0次
【推荐2】已知X、Y和Z三种元素的原子序数之和等于42,X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
(1)X元素原子基态时的电子排布式为___________ 。
(2)Y元素原子的价层电子的轨道表示式为___________ 。
(3)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是___________ 。
(4)比较X的氢化物与同族第二、第三周期元素所形成的氢化物稳定性、沸点高低并说明理由___________ 。
(1)X元素原子基态时的电子排布式为
(2)Y元素原子的价层电子的轨道表示式为
(3)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是
(4)比较X的氢化物与同族第二、第三周期元素所形成的氢化物稳定性、沸点高低并说明理由
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】硼及其化合物在结构上的复杂性和键型上的多样性,极大地丰富和扩展了现有的共价键理论,因此,IIIA族元素及其化合物在无机化学发展中占有独特的地位。回答以下问题:
(1)某同学写出了铝原子的4种不同状态的电子排布图,其中能量最低的是___ (填字母代号),电子由状态C到状态B所得原子光谱为_____ 光谱(填“发射”或“吸收”)。
A. B.
B.
C. D.
D.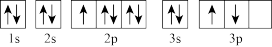
(2)BF3、NF3、CH4的键角由大到小的顺序为_____ 。
(3)BF3可与HF形成HBF4(四氟硼酸),在水中可以部分电离产生H+和BF ,BF
,BF 的构型为
的构型为____ ,与BF 互为等电子体的分子有
互为等电子体的分子有____ (写一个)。
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:

①在Xm-中,硼原子轨道的杂化类型有_____ ;配位键存在于_____ 原子之间(填原子的数字标号);m=_____ (填数字)。
②硼砂晶体由Na+、Xm-和H2O构成,它们之间存在的作用力有____ (填序号)。
A.离子键 B.共价键 C.金属键 D.范德华力 E.氢键
(1)某同学写出了铝原子的4种不同状态的电子排布图,其中能量最低的是
A.
 B.
B.
C.
 D.
D.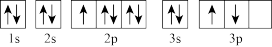
(2)BF3、NF3、CH4的键角由大到小的顺序为
(3)BF3可与HF形成HBF4(四氟硼酸),在水中可以部分电离产生H+和BF
 ,BF
,BF 的构型为
的构型为 互为等电子体的分子有
互为等电子体的分子有(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:

①在Xm-中,硼原子轨道的杂化类型有
②硼砂晶体由Na+、Xm-和H2O构成,它们之间存在的作用力有
A.离子键 B.共价键 C.金属键 D.范德华力 E.氢键
您最近半年使用:0次
【推荐1】A.原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种数最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29。
回答下列问题:
(1)Y2X2分子中Y原子轨道的杂化类型为_______ ,1mol Y2X2含有σ键的数目为_______ 。
(2)化合物ZX3的沸点比化合物YX4的高,其主要原因是_______ 。
(3)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是_______ 。
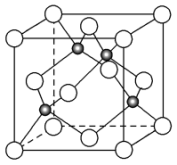
(4)元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是_______ ,它可与浓盐酸发生非氧化还原反应,生成配合物HnWCl3,反应的化学方程式为_______ 。
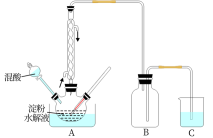
B.草酸是一种重要的化工产品。实验室用硝酸氧化淀粉水解液制备草酸的装置如图所示(加热、搅拌和仪器固定装置均已略去)
实验过程如下:
①将一定量的淀粉水解液加入三颈瓶中
②控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液
③反应3h左右,冷却,抽滤后再重结晶得草酸晶体。
硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3 →3H2C2O4+9NO2↑ +3NO↑ +9H2O
C6H12O6+8HNO3 →6CO2+8NO↑ +10H2O
3H2C2O4+2HNO3 →6CO2+2NO↑ +4H2O
(1)检验淀粉是否水解完全所需用的试剂为_______
(2)实验中若混酸滴加过快,将导致草酸产率下降,其原因是_______
(3)装置C用于尾气吸收,当尾气中n(NO2):n(NO)=1:1时,过量的NaOH溶液能将NO,全部吸收,原因是_______ (用化学方程式表示)
(4)与用NaOH溶液吸收尾气相比较,若用淀粉水解液吸收尾气,其优、缺点是_______ 。
(5)草酸重结晶的减压过滤操作中,除烧杯、玻璃棒外,还必须使用属于硅酸盐材料的仪器有_______ 。
回答下列问题:
(1)Y2X2分子中Y原子轨道的杂化类型为
(2)化合物ZX3的沸点比化合物YX4的高,其主要原因是
(3)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是
(4)元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是

B.草酸是一种重要的化工产品。实验室用硝酸氧化淀粉水解液制备草酸的装置如图所示(加热、搅拌和仪器固定装置均已略去)

实验过程如下:
①将一定量的淀粉水解液加入三颈瓶中
②控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液
③反应3h左右,冷却,抽滤后再重结晶得草酸晶体。
硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3 →3H2C2O4+9NO2↑ +3NO↑ +9H2O
C6H12O6+8HNO3 →6CO2+8NO↑ +10H2O
3H2C2O4+2HNO3 →6CO2+2NO↑ +4H2O
(1)检验淀粉是否水解完全所需用的试剂为
(2)实验中若混酸滴加过快,将导致草酸产率下降,其原因是
(3)装置C用于尾气吸收,当尾气中n(NO2):n(NO)=1:1时,过量的NaOH溶液能将NO,全部吸收,原因是
(4)与用NaOH溶液吸收尾气相比较,若用淀粉水解液吸收尾气,其优、缺点是
(5)草酸重结晶的减压过滤操作中,除烧杯、玻璃棒外,还必须使用属于硅酸盐材料的仪器有
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】现有下列短周期元素的数据(已知Be的原子半径为0.089 nm):
(1)②号元素在元素周期表中的位置是_______ ;①至⑧号元素中,处于同一主族的有_______ (用元素符号表示)。
(2)元素①和⑥能形成两种化合物,其中较稳定的化合物的电子式是_______ 。
(3)由③的单质制成的电池需要注意防水,其原因是_______ (用化学方程式表示)。
(4)利用如下图装置来验证溴与碘的氧化性强弱,具体操作是先通入过量⑤的单质,充分反应后,观察到溶液变为橙黄色:将分液漏斗中液体滴入试管内,KI溶液变为棕黄色。判断该实验能否验证溴、碘的氧化性强弱并说明理由:_______ 。

| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径/nm | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 |
| 最高正化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低负化合价 | -2 | -3 | -1 | -3 |
(2)元素①和⑥能形成两种化合物,其中较稳定的化合物的电子式是
(3)由③的单质制成的电池需要注意防水,其原因是
(4)利用如下图装置来验证溴与碘的氧化性强弱,具体操作是先通入过量⑤的单质,充分反应后,观察到溶液变为橙黄色:将分液漏斗中液体滴入试管内,KI溶液变为棕黄色。判断该实验能否验证溴、碘的氧化性强弱并说明理由:

您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】短周期主族元素X、Y、Z、W、M、T的原子序数依次增大,X的周期序数等于核外电子总数,Y与Z相邻且Z的最外层电子数是次外层的3倍,Z、W的最外层电子数之和与T的最外层电子数相等,M是地壳中含量最多的金属元素。回答下列问题:
(1)Y的元素符号是___________ ,W在元素周期表中的位置___________ 。
(2)Z、W、M、T的简单离子半径从大到小的顺序为___________ (用离子符号表示)。
(3)X、Z、W可形成多种二元化合物,下列说法不正确的是___________(填字母)。
(4)M的氧化物与W的最高价氧化物对应水化物的溶液反应的离子方程式是___________ 。
(5)由X和Y组成的18电子分子Y2X4,该分子的结构式为___________ 。
(6)不能证明T元素的非金属性比碘元素的非金属性强的事实是___________(填序号)。
(1)Y的元素符号是
(2)Z、W、M、T的简单离子半径从大到小的顺序为
(3)X、Z、W可形成多种二元化合物,下列说法不正确的是___________(填字母)。
| A.X2Z2和W2Z2中都含有非极性共价键 |
| B.X、W可形成离子化合物WX,其电子式为:Na+[:H]- |
| C.W2Z、W2Z2溶于X2Z中时,都发生化合反应 |
| D.W2Z2常用于呼吸面具中作为氧气的来源 |
(5)由X和Y组成的18电子分子Y2X4,该分子的结构式为
(6)不能证明T元素的非金属性比碘元素的非金属性强的事实是___________(填序号)。
| A.T的气态氢化物比碘的气态氢化物稳定 |
| B.T的氧化物对应水化物的酸性强于碘的氧化物对应水化物的酸性 |
| C.T的单质能将碘从其钠盐溶液中置换出来 |
| D.T的单质比碘单质更容易与H2反应 |
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】如表为元素周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)元素②形成的含氧酸中,酸根离子呈正三角形的酸是_______ (填化学式)。
(2)元素②③⑧的第一电离能由大到小的顺序是_______ (填元素符号)。
(3)元素④⑥⑦的简单气态氢化物中最稳定的是_______ (填化学式),元素⑤⑧的最高价氧化物对应水化物反应的离子方程式为_______ 。
(4)写出元素⑨的基态原子的价电子排布式:_______ 。
(5)将元素⑩的无水硫酸盐溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子,写出该配合离子的结构简式_______ (必须将配位键表示出来)。
(6)元素①和②③形成的:二元共价化合物中,分子呈三角锥形的化合物为_______ (填化学式);分子中既含有极性共价键,又含有非极性共价键的化合物有_______ (填化学式,写一种)。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | |||||||||||||||
| ⑧ | ⑨ | ⑩ |
(1)元素②形成的含氧酸中,酸根离子呈正三角形的酸是
(2)元素②③⑧的第一电离能由大到小的顺序是
(3)元素④⑥⑦的简单气态氢化物中最稳定的是
(4)写出元素⑨的基态原子的价电子排布式:
(5)将元素⑩的无水硫酸盐溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子,写出该配合离子的结构简式
(6)元素①和②③形成的:二元共价化合物中,分子呈三角锥形的化合物为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】X、Y、Z、W是元素周期表前四周期中的常见元素,其原子序数依次增大。X元素的一种核素的质量数为12,中子数为6;Y元素是动植物生长不可缺少的、构成蛋白质的重要组成元素;Z的基态原子核外9个原子轨道上填充了电子且有2个未成对电子,与X不同族;W核电荷数为26,可以形成3种氧化物,其中一种氧化物是具有磁性的黑色晶体。
(1)写出下列元素的名称X_______ ,Y_______ ,Z_______ ,W_______ 。
(2)X-H和Y-H属于极性共价键,其中极性较强的是_______ (X、Y用元素符号表示)。X的第一电离能比Y的_______ (填“大”或“小”)。
(3)写出X的单质与Z的最高价氧化物对应水化物的浓溶液反应的化学方程式:_______ 。
(4)W的基态原子的电子排布式为_______ 。
(5)Y元素的核外电子轨道表示式为_______ 。
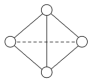
(6)已知一种Y4分子结构如图所示:_______ (填“吸收”或“放出”)_______ kJ。
(1)写出下列元素的名称X
(2)X-H和Y-H属于极性共价键,其中极性较强的是
(3)写出X的单质与Z的最高价氧化物对应水化物的浓溶液反应的化学方程式:
(4)W的基态原子的电子排布式为
(5)Y元素的核外电子轨道表示式为
(6)已知一种Y4分子结构如图所示:
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】钼酸锂(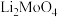 )主要用于电极材料、金属陶瓷、电阻器材料等领域,通过如图流程,以钼矿(主要成分是
)主要用于电极材料、金属陶瓷、电阻器材料等领域,通过如图流程,以钼矿(主要成分是 ,还有杂质CuO、FeO)为原料可制备钼酸锂。
,还有杂质CuO、FeO)为原料可制备钼酸锂。

回答下列问题:
(1)已知基态Mo的价层电子排布式为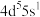 ,则Mo位于元素周期表第
,则Mo位于元素周期表第_______ 周期第_______ 族。
(2)写出焙烧过程中发生的主要反应的化学方程式_______ 。
(3)“碱浸”前需对粗 进行粉碎,这一操作的目的是
进行粉碎,这一操作的目的是_______ ,该操作过程中测定浸取率与温度的关系数据如表:
从浸取率和经济角度考虑,选取的合适温度是_______ ℃。
(4)“转化”操作中加入双氧水的目的是将其中少量的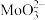 氧化为
氧化为 ,该反应的离子方程式是
,该反应的离子方程式是_______ 。
(5)“合成”的温度是1000~1200℃,则气体Y中含有 、
、_______ (填化学式)。
(6)电解硝酸工业的尾气NO可制备 ,其工作原理如图所示:
,其工作原理如图所示:

①阴极的电极反应式为_______ 。
②将电解生成的 全部转化为
全部转化为 ,则通入的
,则通入的 与实际参加反应的NO的物质的量之比至少为
与实际参加反应的NO的物质的量之比至少为_______ 。
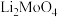 )主要用于电极材料、金属陶瓷、电阻器材料等领域,通过如图流程,以钼矿(主要成分是
)主要用于电极材料、金属陶瓷、电阻器材料等领域,通过如图流程,以钼矿(主要成分是 ,还有杂质CuO、FeO)为原料可制备钼酸锂。
,还有杂质CuO、FeO)为原料可制备钼酸锂。
回答下列问题:
(1)已知基态Mo的价层电子排布式为
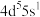 ,则Mo位于元素周期表第
,则Mo位于元素周期表第(2)写出焙烧过程中发生的主要反应的化学方程式
(3)“碱浸”前需对粗
 进行粉碎,这一操作的目的是
进行粉碎,这一操作的目的是| 温度/℃ | 40 | 50 | 60 | 70 | 80 | 90 |
| 浸取率/% | 85.5 | 88.5 | 95.3 | 95.7 | 96.0 | 89.5 |
从浸取率和经济角度考虑,选取的合适温度是
(4)“转化”操作中加入双氧水的目的是将其中少量的
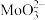 氧化为
氧化为 ,该反应的离子方程式是
,该反应的离子方程式是(5)“合成”的温度是1000~1200℃,则气体Y中含有
 、
、(6)电解硝酸工业的尾气NO可制备
 ,其工作原理如图所示:
,其工作原理如图所示:
①阴极的电极反应式为
②将电解生成的
 全部转化为
全部转化为 ,则通入的
,则通入的 与实际参加反应的NO的物质的量之比至少为
与实际参加反应的NO的物质的量之比至少为
您最近半年使用:0次
【推荐1】以粉煤灰(主要成分:Al2O3、SiO2、少量Fe2O3)为原料,制取Al2O3的部分工艺流程如下:

完成下列填空:
(1)铝原子核外有_______ 种不同能量的电子,最外层电子的轨道式是_______ ,上述流程涉及第二周期元素的原子半径由小到大的顺序是_______ 。
(2)“除铁”是将Fe3+转化为Fe(OH)3沉淀,反应的离子方程式为_______ ,检验溶液中Fe3+是否除尽的方法是_______ 。
(3)解释“结晶”过程中向AlCl3浓溶液中通入HCl气体的原因。_______
(4)上述流程可循环的物质是_______ 。
(5)工业上是通过电解熔化状态下Al2O3,而不是电解熔化状态下AlCl3来获得铝,其原因是_______ 。

完成下列填空:
(1)铝原子核外有
(2)“除铁”是将Fe3+转化为Fe(OH)3沉淀,反应的离子方程式为
(3)解释“结晶”过程中向AlCl3浓溶液中通入HCl气体的原因。
(4)上述流程可循环的物质是
(5)工业上是通过电解熔化状态下Al2O3,而不是电解熔化状态下AlCl3来获得铝,其原因是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】 、
、 、
、 都是重要的材料元素,其单质及化合物在诸多领域中都有广泛的应用。
都是重要的材料元素,其单质及化合物在诸多领域中都有广泛的应用。
(1) 位于元素周期表的
位于元素周期表的___________ 区, 的价层电子排布图为
的价层电子排布图为___________ 。
(2)向黄色的三氯化铁溶液中加入无色的 溶液,溶液变成红色。该反应在有的教材中用方程式
溶液,溶液变成红色。该反应在有的教材中用方程式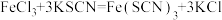 表示。经研究表明,
表示。经研究表明,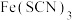 是配合物,
是配合物, 与
与 不仅能以1∶3的个数比配合,还可以其他个数比配合。请按要求填空:
不仅能以1∶3的个数比配合,还可以其他个数比配合。请按要求填空:
①所得 与
与 的配合物中,主要是
的配合物中,主要是 与
与 以个数比1∶1配合所得离子显红色。含该离子的化学式是
以个数比1∶1配合所得离子显红色。含该离子的化学式是___________ 。
②铁的另一种配合物铁氰化钾 俗称赤血盐,可用于检验
俗称赤血盐,可用于检验 ,两者反应生成带有特征蓝色的沉淀,请用离子方程式说明原理
,两者反应生成带有特征蓝色的沉淀,请用离子方程式说明原理___________ ,该赤血盐其配体的电子式为:___________ 。
(3) 的某种化合物的结构如图所示,该化合物中既含有配位键,又含有氢键,其中配位键和氢键均采用虚线表示。
的某种化合物的结构如图所示,该化合物中既含有配位键,又含有氢键,其中配位键和氢键均采用虚线表示。
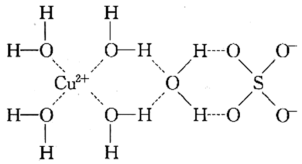
 该化合物中含有
该化合物中含有 键的个数为
键的个数为___________ 。
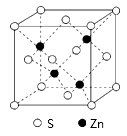
(4)S与 形成的某种晶体的晶胞如图所示,该晶胞中
形成的某种晶体的晶胞如图所示,该晶胞中 微粒的配位数为
微粒的配位数为___________ ,该化合物的化学式为___________ 。
(5)已知 晶体的熔点约为
晶体的熔点约为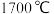 ,构成
,构成 晶体的作用力是
晶体的作用力是___________ 。
 、
、 、
、 都是重要的材料元素,其单质及化合物在诸多领域中都有广泛的应用。
都是重要的材料元素,其单质及化合物在诸多领域中都有广泛的应用。(1)
 位于元素周期表的
位于元素周期表的 的价层电子排布图为
的价层电子排布图为(2)向黄色的三氯化铁溶液中加入无色的
 溶液,溶液变成红色。该反应在有的教材中用方程式
溶液,溶液变成红色。该反应在有的教材中用方程式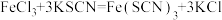 表示。经研究表明,
表示。经研究表明,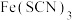 是配合物,
是配合物, 与
与 不仅能以1∶3的个数比配合,还可以其他个数比配合。请按要求填空:
不仅能以1∶3的个数比配合,还可以其他个数比配合。请按要求填空:①所得
 与
与 的配合物中,主要是
的配合物中,主要是 与
与 以个数比1∶1配合所得离子显红色。含该离子的化学式是
以个数比1∶1配合所得离子显红色。含该离子的化学式是②铁的另一种配合物铁氰化钾
 俗称赤血盐,可用于检验
俗称赤血盐,可用于检验 ,两者反应生成带有特征蓝色的沉淀,请用离子方程式说明原理
,两者反应生成带有特征蓝色的沉淀,请用离子方程式说明原理(3)
 的某种化合物的结构如图所示,该化合物中既含有配位键,又含有氢键,其中配位键和氢键均采用虚线表示。
的某种化合物的结构如图所示,该化合物中既含有配位键,又含有氢键,其中配位键和氢键均采用虚线表示。
 该化合物中含有
该化合物中含有 键的个数为
键的个数为(4)S与
 形成的某种晶体的晶胞如图所示,该晶胞中
形成的某种晶体的晶胞如图所示,该晶胞中 微粒的配位数为
微粒的配位数为
(5)已知
 晶体的熔点约为
晶体的熔点约为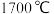 ,构成
,构成 晶体的作用力是
晶体的作用力是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】铁及其化合物有重要且广泛的应用
(1)基态Fe2+的价层电子的轨道表示式为_____________
(2)检验Fe3+可以用KSCN溶液,写出SCN-的一种等电子体分子_______ 。
(3)部分电离能数据如下表:
根据表中数据可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是_______________________________________________________
(4)过渡金属原子可以与CO分子形成配合物,配合物价电子总数符合“18电子规则”。如Cr可以与CO形成Cr(CO)6 分子:价电子总数(18)= Cr的价电子数(6)+CO提供电子数(2×6).Fe原子也能与CO形成配合物,其化学式为________ .
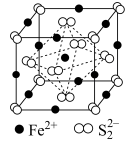
(5)FeS2晶体的晶胞如图所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加 德罗常数的值为NA,其晶体密度的计算表达式为___________ g·cm−3。
(1)基态Fe2+的价层电子的轨道表示式为
(2)检验Fe3+可以用KSCN溶液,写出SCN-的一种等电子体分子
(3)部分电离能数据如下表:
| 元素 | Mn | Fe | |
| 电离能(kJ/mol) |  | 717 | 759 |
 | 1 509 | 1 561 | |
 | 3 248 | 2 957 | |
根据表中数据可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是
(4)过渡金属原子可以与CO分子形成配合物,配合物价电子总数符合“18电子规则”。如Cr可以与CO形成Cr(CO)6 分子:价电子总数(18)= Cr的价电子数(6)+CO提供电子数(2×6).Fe原子也能与CO形成配合物,其化学式为
(5)FeS2晶体的晶胞如图所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加 德罗常数的值为NA,其晶体密度的计算表达式为

您最近半年使用:0次



