钼酸锂(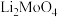 )主要用于电极材料、金属陶瓷、电阻器材料等领域,通过如图流程,以钼矿(主要成分是
)主要用于电极材料、金属陶瓷、电阻器材料等领域,通过如图流程,以钼矿(主要成分是 ,还有杂质CuO、FeO)为原料可制备钼酸锂。
,还有杂质CuO、FeO)为原料可制备钼酸锂。

回答下列问题:
(1)已知基态Mo的价层电子排布式为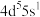 ,则Mo位于元素周期表第
,则Mo位于元素周期表第_______ 周期第_______ 族。
(2)写出焙烧过程中发生的主要反应的化学方程式_______ 。
(3)“碱浸”前需对粗 进行粉碎,这一操作的目的是
进行粉碎,这一操作的目的是_______ ,该操作过程中测定浸取率与温度的关系数据如表:
从浸取率和经济角度考虑,选取的合适温度是_______ ℃。
(4)“转化”操作中加入双氧水的目的是将其中少量的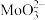 氧化为
氧化为 ,该反应的离子方程式是
,该反应的离子方程式是_______ 。
(5)“合成”的温度是1000~1200℃,则气体Y中含有 、
、_______ (填化学式)。
(6)电解硝酸工业的尾气NO可制备 ,其工作原理如图所示:
,其工作原理如图所示:

①阴极的电极反应式为_______ 。
②将电解生成的 全部转化为
全部转化为 ,则通入的
,则通入的 与实际参加反应的NO的物质的量之比至少为
与实际参加反应的NO的物质的量之比至少为_______ 。
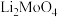 )主要用于电极材料、金属陶瓷、电阻器材料等领域,通过如图流程,以钼矿(主要成分是
)主要用于电极材料、金属陶瓷、电阻器材料等领域,通过如图流程,以钼矿(主要成分是 ,还有杂质CuO、FeO)为原料可制备钼酸锂。
,还有杂质CuO、FeO)为原料可制备钼酸锂。
回答下列问题:
(1)已知基态Mo的价层电子排布式为
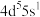 ,则Mo位于元素周期表第
,则Mo位于元素周期表第(2)写出焙烧过程中发生的主要反应的化学方程式
(3)“碱浸”前需对粗
 进行粉碎,这一操作的目的是
进行粉碎,这一操作的目的是| 温度/℃ | 40 | 50 | 60 | 70 | 80 | 90 |
| 浸取率/% | 85.5 | 88.5 | 95.3 | 95.7 | 96.0 | 89.5 |
从浸取率和经济角度考虑,选取的合适温度是
(4)“转化”操作中加入双氧水的目的是将其中少量的
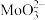 氧化为
氧化为 ,该反应的离子方程式是
,该反应的离子方程式是(5)“合成”的温度是1000~1200℃,则气体Y中含有
 、
、(6)电解硝酸工业的尾气NO可制备
 ,其工作原理如图所示:
,其工作原理如图所示:
①阴极的电极反应式为
②将电解生成的
 全部转化为
全部转化为 ,则通入的
,则通入的 与实际参加反应的NO的物质的量之比至少为
与实际参加反应的NO的物质的量之比至少为
更新时间:2022-11-07 17:57:55
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】电化学方法是化工生产及生活中常用的一种方法。回答下列问题:
(1)二氧化氯 为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出用电解法制取
为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出用电解法制取 的新工艺如图所示:
的新工艺如图所示: 。产生
。产生  的电极应连接电源的
的电极应连接电源的___________ (填“正极”或“负极”),对应的电极反应式为___________ 。
② 极区
极区 
___________ (填“增大”“减小”或“不变”)。
③图中应使用___________ (填“阴”或“阳”)离子交换膜。
(2)电解 溶液可制备
溶液可制备  工业上,通常以软锰矿(主要成分是
工业上,通常以软锰矿(主要成分是  )与
)与  的混合物在铁埚(熔融池)中混合均匀,小火加热至熔融,即可得到绿色的
的混合物在铁埚(熔融池)中混合均匀,小火加热至熔融,即可得到绿色的  ,化学方程式为
,化学方程式为 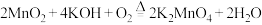 。用镍片作阳极(镍不参与反应),铁板为阴极,电解
。用镍片作阳极(镍不参与反应),铁板为阴极,电解  溶液可制备
溶液可制备  。
。
上述过程用流程图表示如下: 的化学式为
的化学式为___________ ;阳极的电极反应式为___________ ;阳离子迁移方向是___________ (填“由阳极室移向阴极室”或“由阴极室移向阳极室”)。
(3)电解硝酸工业的尾气 可制备
可制备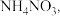 其工作原理如图所示:
其工作原理如图所示:___________ 。
②将电解生成的 全部转化为
全部转化为 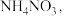 则通入的
则通入的  与实际参加反应的
与实际参加反应的 的物质的量之比至少为
的物质的量之比至少为___________ 。
(1)二氧化氯
 为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出用电解法制取
为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出用电解法制取 的新工艺如图所示:
的新工艺如图所示: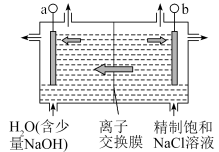
 。产生
。产生  的电极应连接电源的
的电极应连接电源的②
 极区
极区 
③图中应使用
(2)电解
 溶液可制备
溶液可制备  工业上,通常以软锰矿(主要成分是
工业上,通常以软锰矿(主要成分是  )与
)与  的混合物在铁埚(熔融池)中混合均匀,小火加热至熔融,即可得到绿色的
的混合物在铁埚(熔融池)中混合均匀,小火加热至熔融,即可得到绿色的  ,化学方程式为
,化学方程式为 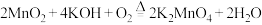 。用镍片作阳极(镍不参与反应),铁板为阴极,电解
。用镍片作阳极(镍不参与反应),铁板为阴极,电解  溶液可制备
溶液可制备  。
。上述过程用流程图表示如下:

 的化学式为
的化学式为(3)电解硝酸工业的尾气
 可制备
可制备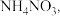 其工作原理如图所示:
其工作原理如图所示: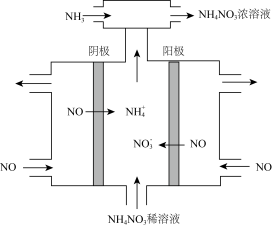
②将电解生成的
 全部转化为
全部转化为 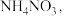 则通入的
则通入的  与实际参加反应的
与实际参加反应的 的物质的量之比至少为
的物质的量之比至少为
您最近一年使用:0次
【推荐2】环氧乙烷( )、环氧丙烷(
)、环氧丙烷(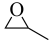 )都是重要的化工原料且用途广泛。回答下列问题:
)都是重要的化工原料且用途广泛。回答下列问题:
(1)已知:
①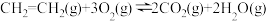

②2
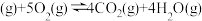
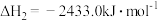
③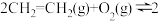


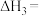
_____ 
(2)某温度下,物质的量均为1mol的CH2=CH2和O2在0.5L的刚性容器内发生反应③,5min后反应达到平衡,气体总压减少了20%。
①平衡时CH2=CH2(g)的转化率为____ ,达到平衡后,欲增加CH2=CH2(g)的平衡转化率,可采取的措施是____ (填一条措施即可)。
②0~5min内,环氧乙烷的生成速率为____ 。
③该反应的平衡常数K_____ (精确到0.01)。
④当进料气CH2=CH2和O2的物质的量不变时,T1℃时达到反应平衡,请在图1中画出温度由T1℃变化到T2℃的过程中乙烯的转化率与温度的关系____ 。
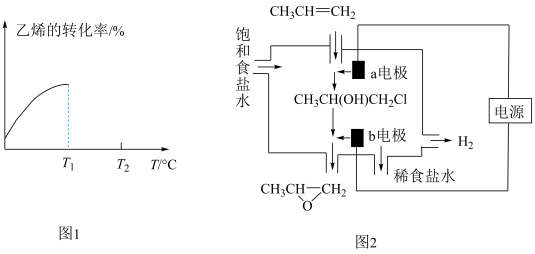
(3)将丙烯与饱和食盐水的电解产物反应,转化为氯丙醇[CH3CH(OH)CH2Cl][已知:CH3CH=CH2+H2O+Cl2→CH3CH(OH)CH2Cl+HCl],氯丙醇进一步反应生成环氧丙烷,其电解简易装置如图2所示。
①a电极上的电极反应式为______ 。
②b电极区域生成环氧丙烷的化学方程式为______ 。
 )、环氧丙烷(
)、环氧丙烷( )都是重要的化工原料且用途广泛。回答下列问题:
)都是重要的化工原料且用途广泛。回答下列问题:(1)已知:
①
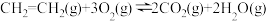

②2

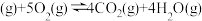
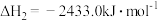
③
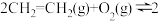


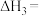

(2)某温度下,物质的量均为1mol的CH2=CH2和O2在0.5L的刚性容器内发生反应③,5min后反应达到平衡,气体总压减少了20%。
①平衡时CH2=CH2(g)的转化率为
②0~5min内,环氧乙烷的生成速率为
③该反应的平衡常数K
④当进料气CH2=CH2和O2的物质的量不变时,T1℃时达到反应平衡,请在图1中画出温度由T1℃变化到T2℃的过程中乙烯的转化率与温度的关系

(3)将丙烯与饱和食盐水的电解产物反应,转化为氯丙醇[CH3CH(OH)CH2Cl][已知:CH3CH=CH2+H2O+Cl2→CH3CH(OH)CH2Cl+HCl],氯丙醇进一步反应生成环氧丙烷,其电解简易装置如图2所示。
①a电极上的电极反应式为
②b电极区域生成环氧丙烷的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铜的电解实现了铜与杂质的分离,也造成了一部分资重金属进入阳极泥中,通过对阳极泥的综合处理可以回收可观的宝贵金属。稀散元素硒和碲广泛用于冶金工业、 电子工业、国防工业、 医学和农业等领域,需求量越来越大。电解精炼铜的阳极泥主要成分为Cu2Se、Cu2Te和少量金属单质Au等, 工业上从其中同收碲、硒的一种工艺流程如图:

已知: TeO2是两性氧化物,Se和TeO2的物理性质如下表:
(1)“焙烧”时所加的硫酸浓度最好为_____ (填序号)。
a.10% b.50% c.70% d.98%
(2)加硫酸焙烧过程中Cu2Se参与反应的化学方程式为_________ ,氧化产物和还原产物的物质的量之比是_______ 。
(3)滤渣的主要成分是_______ (填化学式)。
(4)“酸溶”后,将TeO2先溶于盐酸得到四氯化碲,然后再通入二氧化硫得到碲单质,后者发生反应的化学方程式为______________ 。
(5)“沉碲”时控制溶液的pH为4.5-5.0,生成TeO2沉淀。如果H2SO4过量,溶液酸度过大,将导致“沉碲”不完全,原因是______________ 。
(6)过滤所得粗硒中含有Ni、Fe、Cu等杂质,可采用真空蒸馏的方法进行提纯,获得纯硒。真空蒸馏的挥发物中硒含量与温度的关系如图所示。蒸馏操作中控制的最佳温度是_____ (填序号)

a. 455℃ b. 462℃ c.475℃ d. 515℃
(7)工业上还可以通过电解铜阳极泥碱浸,过滤后的滤液得到单质碲。已知电解时的电极均为石墨,则阴极的电极反应式为___________ 。

已知: TeO2是两性氧化物,Se和TeO2的物理性质如下表:
| 物理性质 | 熔点 | 沸点 | 水溶性 |
| Se | 221℃ | 685℃ | 难溶于水 |
| TeO2 | 733℃ | 1260℃ | 微溶于水 |
(1)“焙烧”时所加的硫酸浓度最好为
a.10% b.50% c.70% d.98%
(2)加硫酸焙烧过程中Cu2Se参与反应的化学方程式为
(3)滤渣的主要成分是
(4)“酸溶”后,将TeO2先溶于盐酸得到四氯化碲,然后再通入二氧化硫得到碲单质,后者发生反应的化学方程式为
(5)“沉碲”时控制溶液的pH为4.5-5.0,生成TeO2沉淀。如果H2SO4过量,溶液酸度过大,将导致“沉碲”不完全,原因是
(6)过滤所得粗硒中含有Ni、Fe、Cu等杂质,可采用真空蒸馏的方法进行提纯,获得纯硒。真空蒸馏的挥发物中硒含量与温度的关系如图所示。蒸馏操作中控制的最佳温度是

a. 455℃ b. 462℃ c.475℃ d. 515℃
(7)工业上还可以通过电解铜阳极泥碱浸,过滤后的滤液得到单质碲。已知电解时的电极均为石墨,则阴极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】S元素是动植物生长所必需的元素,在生活中应用广泛。
(1)基态S原子的价电子排布式为___________ 。
(2) 的空间构型为
的空间构型为___________ , 的键角由大到小的顺序为
的键角由大到小的顺序为___________ (填化学式)。
(3)用杂化轨道理论解释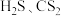 的键角差别很大的原因是
的键角差别很大的原因是___________ 。从结构的角度解释 的酸性比
的酸性比 强的原因是
强的原因是___________ 。
(4) 结构有两种,硫氰酸
结构有两种,硫氰酸 的沸点
的沸点___________ (填“高于”或“低于”)异硫氰酸。
(5) 晶胞如图所示,
晶胞如图所示, 填在由
填在由 形成的
形成的___________ 空隙中。已知晶胞中 与
与 最近的距离为
最近的距离为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则晶体密度为
,则晶体密度为___________  。
。
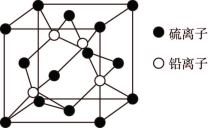
(6)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图所示。
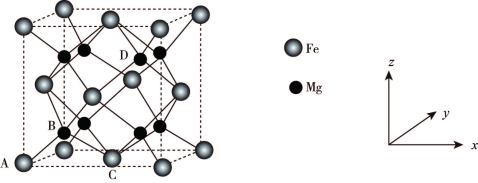
晶体中每个铁原子周围距离最近的镁原子有___________ 个,原子坐标参数可以表示晶胞内部原子的相对位置,其中原子坐标参数A为 ,B为
,B为 ,C为
,C为 ,则D点坐标参数为
,则D点坐标参数为___________ 。
(1)基态S原子的价电子排布式为
(2)
 的空间构型为
的空间构型为 的键角由大到小的顺序为
的键角由大到小的顺序为(3)用杂化轨道理论解释
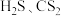 的键角差别很大的原因是
的键角差别很大的原因是 的酸性比
的酸性比 强的原因是
强的原因是(4)
 结构有两种,硫氰酸
结构有两种,硫氰酸 的沸点
的沸点(5)
 晶胞如图所示,
晶胞如图所示, 填在由
填在由 形成的
形成的 与
与 最近的距离为
最近的距离为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则晶体密度为
,则晶体密度为 。
。
(6)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图所示。

晶体中每个铁原子周围距离最近的镁原子有
 ,B为
,B为 ,C为
,C为 ,则D点坐标参数为
,则D点坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】《自然·通讯》近日发表了我国复旦大学魏大程团队开发的一种共形六方氮化硼修饰技术,可直接在二氧化硅表面生长高质量六方氮化硼薄膜。
(1)基态B原子的电子排布式为________ ,第二周期主族元素中,第一电离能在B和N之间的元素有________ 种。
(2)Na与N形成的NaN3可用于制造汽车的安全气囊,其中阴离子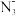 的空间构型为
的空间构型为________ ,Na在空气中燃烧发出黄色火焰,这种焰色用光谱仪摄取的光谱为________ 光谱(填“发射”或“吸收”)。
(3)BH3.NH3是一种有效、安全的固体储氢材料,可由BH3与NH3反应生成,BH3.NH3分子中B与N之间形成配位键,提供空轨道的原子为________ (填元素符号),分子中B原子的杂化类型为________ 。
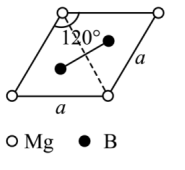
(4)一种硼镁化合物具有超导性能,晶体结构属于立方晶系,其晶体结构、晶胞沿c轴的投影图如图所示,该物质化学式为________ ,B—B键最近距离为________ 。

(1)基态B原子的电子排布式为
(2)Na与N形成的NaN3可用于制造汽车的安全气囊,其中阴离子
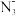 的空间构型为
的空间构型为(3)BH3.NH3是一种有效、安全的固体储氢材料,可由BH3与NH3反应生成,BH3.NH3分子中B与N之间形成配位键,提供空轨道的原子为
(4)一种硼镁化合物具有超导性能,晶体结构属于立方晶系,其晶体结构、晶胞沿c轴的投影图如图所示,该物质化学式为


您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】有四种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)A原子的外围电子排布式__________________________________ 。
(2)B元素在周期表中的位置________ ;离子半径:B________ A(填“大于”或“小于”)。
(3)C元素原子核外有________ 个未成对电子,能量最高的电子为________ 轨道上的电子,其轨道呈________ 形。
(4)D元素原子的价电子排布式为________ ,D-的结构示意图是________ 。
(5)B的最高价氧化物对应的水化物的化学式___________________ ,与A的最高价氧化物对应的水化物相比,碱性较强的是:_______________ (填化学式)。
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(1)A原子的外围电子排布式
(2)B元素在周期表中的位置
(3)C元素原子核外有
(4)D元素原子的价电子排布式为
(5)B的最高价氧化物对应的水化物的化学式
您最近一年使用:0次
【推荐1】聚合氯化铝化学式为[Al2(OH)aCl6-a]n,是一种无机高分子铝的聚合物,已广泛用于生活废水处理。由偏铝酸钙[Ca(AlO2)2]制备聚合氯化铝的一种工艺流程如下:
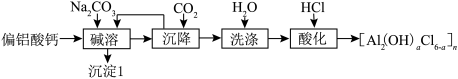
(1)经测定“碱溶”后溶液的pH=12,要使“沉淀Ⅰ”中不含有Ca(OH)2,则溶液中的c( )>
)>_________ mol·L-1。{Ksp[Ca(OH)2]=6×10-6,Ksp(CaCO3)=3×10-9}
(2)“沉降”的温度控制在40℃左右,主要原因是_________ ,“沉降”时的离子方程式为_________ 。
(3)“酸化”时的装置如图所示,先将氢氧化铝滤饼分散在水中,然后向其中滴加定量的盐酸,相比与直接向滤饼加盐酸的优点是_________ ,若要使聚合氯化铝[Al2(OH)aCl6-a]n中a=2,则实验过程中需要控制条件除温度外,还要控制条件是_________ 。
(4)已知溶液pH不同时,钒元素与铝元素存在形式如下表所示,请完成利用(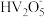 、
、 )碱性废水制备聚合氯化铝的实验步骤:
)碱性废水制备聚合氯化铝的实验步骤:
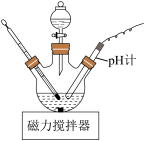
取适量废水_________ ,将纯净的氢氧化铝滤饼分散到水中,向其中滴加盐酸,得到聚合氯化铝。(实验中须使用的试剂有:0.1 mol·L-1HCl、5%的双氧水、蒸馏水)

(1)经测定“碱溶”后溶液的pH=12,要使“沉淀Ⅰ”中不含有Ca(OH)2,则溶液中的c(
 )>
)>(2)“沉降”的温度控制在40℃左右,主要原因是
(3)“酸化”时的装置如图所示,先将氢氧化铝滤饼分散在水中,然后向其中滴加定量的盐酸,相比与直接向滤饼加盐酸的优点是
(4)已知溶液pH不同时,钒元素与铝元素存在形式如下表所示,请完成利用(
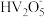 、
、 )碱性废水制备聚合氯化铝的实验步骤:
)碱性废水制备聚合氯化铝的实验步骤:
| 钒的化合价 | pH=5 | pH=13 |
| +4价V | VO(OH)2沉淀 | HV2O5- |
| +5价V | 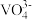 | 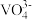 |
| +3价Al | Al(OH)3沉淀 |  |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】钛和钛合金被认为是21世纪的重要金属材料,广泛用于火箭、飞机制造业等。如图是工业上利用钛铁矿,其主要成分为钛酸亚铁(FeTiO3)制备金属钛的工艺流程。
资料:Ti为固体,化学性质稳定,不溶于稀硫酸、稀盐酸等。
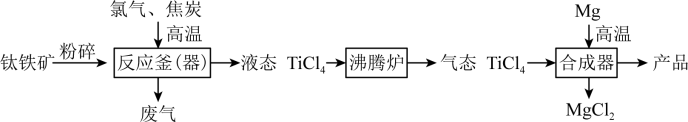
(1)钛酸亚铁(FeTiO3)中钛元素的化合价是___________ 。
(2)反应釜中发生的反应是:2FeTiO3+7Cl2+6C 2X+2TiCl4+6CO,X的化学式是
2X+2TiCl4+6CO,X的化学式是___________ 。FeTiO3在该反应中发生了反应___________ (填“氧化”或“还原”)。
(3)利用上述方法制取的金属钛中可能会含有少量杂质,该杂质是金属___________ 。由金属钛的性质可知,除去这种杂质可以用___________ 。
资料:Ti为固体,化学性质稳定,不溶于稀硫酸、稀盐酸等。

(1)钛酸亚铁(FeTiO3)中钛元素的化合价是
(2)反应釜中发生的反应是:2FeTiO3+7Cl2+6C
 2X+2TiCl4+6CO,X的化学式是
2X+2TiCl4+6CO,X的化学式是(3)利用上述方法制取的金属钛中可能会含有少量杂质,该杂质是金属
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铁黄是一种重要的颜料,化学式为Fe2O3·xH2O,广泛用于涂料、橡胶、塑料、文教用品等工业。实验室模拟工业利用硫酸渣(含Fe2O3及少量的CaO、MgO等)和黄铁矿粉(主要成分为FeS2)制备铁黄的流程如下:
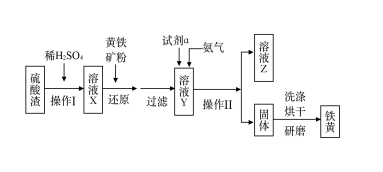
(1)操作Ⅰ与操作Ⅱ中都用到玻璃棒,玻璃棒在两种操作中的作用分别是______________ 、________________ 。
(2)试剂a最好选用__________________ (供选择使用的有:铝粉、空气、浓HNO3);
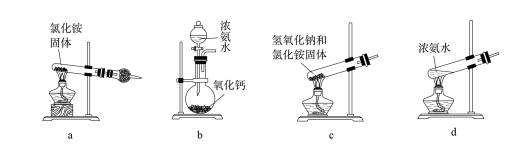
(3)上述步骤中需用到氨气。下列装置可用于实验室制氨气的是_____ (填序号)。
(4)查阅资料知,在不同温度下Fe2O3被CO还原,产物可能为Fe3O4、FeO或Fe,固体质量与反应温度的关系如下图所示。
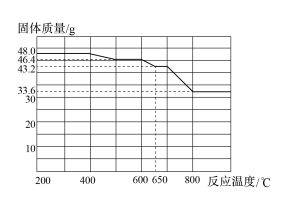
根据图像推断670℃时Fe2O3还原产物的化学式为_________ ,并设计一个简单的实验,证明该还原产物的成分(简述实验操作、现象和结论)_____________________________
仪器自选。可供选择的试剂:稀硫酸、稀盐酸、H2O2溶液、NaOH溶液、KSCN溶液。

(1)操作Ⅰ与操作Ⅱ中都用到玻璃棒,玻璃棒在两种操作中的作用分别是
(2)试剂a最好选用
(3)上述步骤中需用到氨气。下列装置可用于实验室制氨气的是

(4)查阅资料知,在不同温度下Fe2O3被CO还原,产物可能为Fe3O4、FeO或Fe,固体质量与反应温度的关系如下图所示。

根据图像推断670℃时Fe2O3还原产物的化学式为
仪器自选。可供选择的试剂:稀硫酸、稀盐酸、H2O2溶液、NaOH溶液、KSCN溶液。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】碱性锌锰电池的工作原理: Zn + 2MnO2 + 2H2O=2MnO(OH) +Zn(OH)2,其中的电解质溶液是KOH溶液。某课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新型材料——MnXZn(1-x)Fe2O4,其工艺流程如图所示:

(1)已知MnXZn(1-x)Fe2O4中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中的锰相同,则铁元素的化合价为___________________ 。
(2)“浸取”工序得到的滤液A经蒸发结晶,可以获得化工产品M,M的电子式为_______ 。
(3)“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将+3价锰的化合物全部还原成Mn2+,写出该反应的离子方程式:____________ 。
(4)“调铁”工序的目的是调整滤液中铁离子的总浓度,使其中金属元素的物质的量之比与产品的化学式MnXZn(1-x)Fe2O4相符合。写出“调铁”工序中发生反应的离子方程式:________ 、____________ 。
(5)在“氧化”工序中,加入双氧水的目的是_____________ ;生产过程中发现实际消耗双氧水的量大于理论值,其可能原因除温度外,主要是_________ 。
(6)用氨水“调pH”后,经“结晶”“过滤”可得到产品和滤液C,从滤液C中还可分离出一种氨肥。该氮肥的溶液中离子浓度由大到小的排序为_______________ 。

(1)已知MnXZn(1-x)Fe2O4中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中的锰相同,则铁元素的化合价为
(2)“浸取”工序得到的滤液A经蒸发结晶,可以获得化工产品M,M的电子式为
(3)“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将+3价锰的化合物全部还原成Mn2+,写出该反应的离子方程式:
(4)“调铁”工序的目的是调整滤液中铁离子的总浓度,使其中金属元素的物质的量之比与产品的化学式MnXZn(1-x)Fe2O4相符合。写出“调铁”工序中发生反应的离子方程式:
(5)在“氧化”工序中,加入双氧水的目的是
(6)用氨水“调pH”后,经“结晶”“过滤”可得到产品和滤液C,从滤液C中还可分离出一种氨肥。该氮肥的溶液中离子浓度由大到小的排序为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】硫代硫酸钠是一种重要的化工产品。某兴趣小组制备硫代硫酸钠晶体(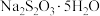 )的实验装置如下图所示(省略夹持装置):
)的实验装置如下图所示(省略夹持装置):

主要实验步骤为:
①检查装置气密性,按图示加入试剂;
②先向A中烧瓶滴加浓 ,再向C中烧瓶加入
,再向C中烧瓶加入 和
和 混合溶液;
混合溶液;
③待 和
和 完全消耗后,结束反应。过滤C中混合物,滤液经
完全消耗后,结束反应。过滤C中混合物,滤液经一系列实验操作 后得到产品。
已知:
i.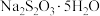 是无色透明晶体,易溶于水,其稀溶液与
是无色透明晶体,易溶于水,其稀溶液与 溶液混合无沉淀生成;
溶液混合无沉淀生成;
ii.向 和
和 混合溶液中通入
混合溶液中通入 可制得
可制得 ,所得产品常含有少量
,所得产品常含有少量 和
和 。
。
回答下列问题:
(1)仪器a的名称是_______ ;B、D装置的作用是_______ 。
(2)上述实验步骤③中的一系列实验操作 主要有_______ 、冷却结晶、过滤、洗涤、干燥;E中的试剂是_______ 。
(3)为检验产品中是否含有 和
和 ,该小组设计了以下实验方案(所需试剂从稀
,该小组设计了以下实验方案(所需试剂从稀 、稀
、稀 、稀HCl、蒸馏水中选择),请将方案补充完整:取适量产品配成稀溶液,滴加足量
、稀HCl、蒸馏水中选择),请将方案补充完整:取适量产品配成稀溶液,滴加足量 溶液,有白色沉淀生成,向沉淀中滴加足量的
溶液,有白色沉淀生成,向沉淀中滴加足量的_______ ,若_______ (填实验现象),则可以确定产品中含有 和
和 。
。
(4)写出制备 的总反应的化学方程式
的总反应的化学方程式_______ 。
(5)称取样品29.10g,配成500mL溶液,取出250mL向其中加入足量稀硫酸,充分反应,静置、过滤、洗涤、干燥、称量得沉淀1.60g,则样品中硫代硫酸钠晶体的百分含量为_______ 。(保留到0.1%)
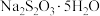 )的实验装置如下图所示(省略夹持装置):
)的实验装置如下图所示(省略夹持装置):
主要实验步骤为:
①检查装置气密性,按图示加入试剂;
②先向A中烧瓶滴加浓
 ,再向C中烧瓶加入
,再向C中烧瓶加入 和
和 混合溶液;
混合溶液;③待
 和
和 完全消耗后,结束反应。过滤C中混合物,滤液经
完全消耗后,结束反应。过滤C中混合物,滤液经已知:
i.
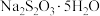 是无色透明晶体,易溶于水,其稀溶液与
是无色透明晶体,易溶于水,其稀溶液与 溶液混合无沉淀生成;
溶液混合无沉淀生成;ii.向
 和
和 混合溶液中通入
混合溶液中通入 可制得
可制得 ,所得产品常含有少量
,所得产品常含有少量 和
和 。
。回答下列问题:
(1)仪器a的名称是
(2)上述实验步骤③中的
(3)为检验产品中是否含有
 和
和 ,该小组设计了以下实验方案(所需试剂从稀
,该小组设计了以下实验方案(所需试剂从稀 、稀
、稀 、稀HCl、蒸馏水中选择),请将方案补充完整:取适量产品配成稀溶液,滴加足量
、稀HCl、蒸馏水中选择),请将方案补充完整:取适量产品配成稀溶液,滴加足量 溶液,有白色沉淀生成,向沉淀中滴加足量的
溶液,有白色沉淀生成,向沉淀中滴加足量的 和
和 。
。(4)写出制备
 的总反应的化学方程式
的总反应的化学方程式(5)称取样品29.10g,配成500mL溶液,取出250mL向其中加入足量稀硫酸,充分反应,静置、过滤、洗涤、干燥、称量得沉淀1.60g,则样品中硫代硫酸钠晶体的百分含量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】金属镓( )是合成半导体材料砷化镓(
)是合成半导体材料砷化镓( )的重要基础材料,一种由砷化镓废料(主要成分
)的重要基础材料,一种由砷化镓废料(主要成分 ,含
,含 、
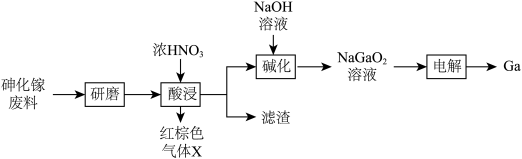
、 等杂质)制备镓的实验流程如下。
等杂质)制备镓的实验流程如下。
已知:
i. 和
和 位于同一主族,性质相似。
位于同一主族,性质相似。
ii. 难溶于水。
难溶于水。
(1)“研磨”的目的是_______ 。
(2)“滤渣”的主要成分是_______ (填化学式)。
(3)写出“酸浸”过程发生反应的化学方程式_______ 。若取A、B两组样品分别进行实验,“酸浸”时向A中不断通入 ,其他条件、操作完全一样,得到镓元素的浸出率随时间变化情况如图所示:
,其他条件、操作完全一样,得到镓元素的浸出率随时间变化情况如图所示:
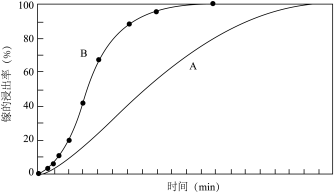
浸出速率A____ B(填>、=或<),推测A、B曲线变化的原因是______ 。
(4)“碱化”时发生反应的离子方程式为_______ 。
 )是合成半导体材料砷化镓(
)是合成半导体材料砷化镓( )的重要基础材料,一种由砷化镓废料(主要成分
)的重要基础材料,一种由砷化镓废料(主要成分 ,含
,含 、
、 等杂质)制备镓的实验流程如下。
等杂质)制备镓的实验流程如下。
已知:
i.
 和
和 位于同一主族,性质相似。
位于同一主族,性质相似。ii.
 难溶于水。
难溶于水。(1)“研磨”的目的是
(2)“滤渣”的主要成分是
(3)写出“酸浸”过程发生反应的化学方程式
 ,其他条件、操作完全一样,得到镓元素的浸出率随时间变化情况如图所示:
,其他条件、操作完全一样,得到镓元素的浸出率随时间变化情况如图所示:
浸出速率A
(4)“碱化”时发生反应的离子方程式为
您最近一年使用:0次



