S元素是动植物生长所必需的元素,在生活中应用广泛。
(1)基态S原子的价电子排布式为___________ 。
(2) 的空间构型为
的空间构型为___________ , 的键角由大到小的顺序为
的键角由大到小的顺序为___________ (填化学式)。
(3)用杂化轨道理论解释 的键角差别很大的原因是
的键角差别很大的原因是___________ 。从结构的角度解释 的酸性比
的酸性比 强的原因是
强的原因是___________ 。
(4) 结构有两种,硫氰酸
结构有两种,硫氰酸 的沸点
的沸点___________ (填“高于”或“低于”)异硫氰酸。
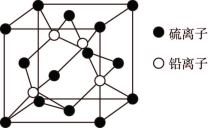
(5) 晶胞如图所示,
晶胞如图所示, 填在由
填在由 形成的
形成的___________ 空隙中。已知晶胞中 与
与 最近的距离为
最近的距离为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则晶体密度为
,则晶体密度为___________  。
。
(6)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图所示。
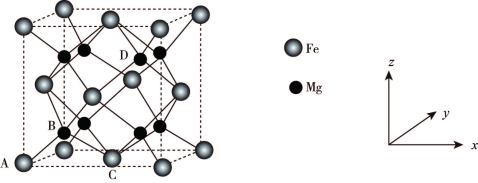
晶体中每个铁原子周围距离最近的镁原子有___________ 个,原子坐标参数可以表示晶胞内部原子的相对位置,其中原子坐标参数A为 ,B为
,B为 ,C为
,C为 ,则D点坐标参数为
,则D点坐标参数为___________ 。
(1)基态S原子的价电子排布式为
(2)
 的空间构型为
的空间构型为 的键角由大到小的顺序为
的键角由大到小的顺序为(3)用杂化轨道理论解释
 的键角差别很大的原因是
的键角差别很大的原因是 的酸性比
的酸性比 强的原因是
强的原因是(4)
 结构有两种,硫氰酸
结构有两种,硫氰酸 的沸点
的沸点(5)
 晶胞如图所示,
晶胞如图所示, 填在由
填在由 形成的
形成的 与
与 最近的距离为
最近的距离为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则晶体密度为
,则晶体密度为 。
。
(6)铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图所示。

晶体中每个铁原子周围距离最近的镁原子有
 ,B为
,B为 ,C为
,C为 ,则D点坐标参数为
,则D点坐标参数为
更新时间:2022-02-28 19:43:40
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】铁、铜及其化合物应用广泛。回答下列问题:
(1)基态铁原子核外最后一个电子填充在_______ (填能级符号)上,含有_______ 个未成对电子。
(2)铁氰化钾 是检验
是检验 的重要试剂。
的重要试剂。
①铁氰化钾中,所涉及的元素的第一电离能由大到小的顺序为_______ 。
②铁氰化钾中,不存在_______ (填字母)。
A.离子键 B. 键 C.
键 C. 键 D.氢键 E.金属键
键 D.氢键 E.金属键
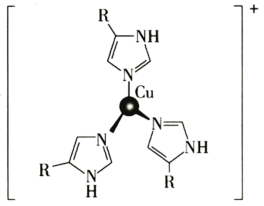
(3)血蓝蛋白是某些节肢动物体内能与氧气可逆结合的一种铜蛋白,其部分结构示意图如图所示。其中Cu的化合价为_______ 价,N的杂化轨道类型是_______ 。
(4)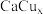 合金可看作由如图所示的(a)、(b)两种原子层交替堆积排列而成。图中虚线构建的六边形,表示由这两种层平行堆积时垂直于层的相对位置;(c)是由(a)和(b)两种原子层交替堆积成的
合金可看作由如图所示的(a)、(b)两种原子层交替堆积排列而成。图中虚线构建的六边形,表示由这两种层平行堆积时垂直于层的相对位置;(c)是由(a)和(b)两种原子层交替堆积成的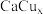 合金的晶胞结构图。在这种结构中,同一层的Ca与Cu距离为
合金的晶胞结构图。在这种结构中,同一层的Ca与Cu距离为 。
。
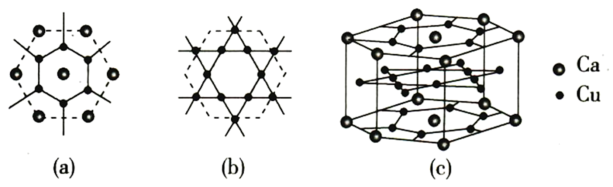
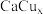 合金中
合金中
_______ 。
(1)基态铁原子核外最后一个电子填充在
(2)铁氰化钾
 是检验
是检验 的重要试剂。
的重要试剂。①铁氰化钾中,所涉及的元素的第一电离能由大到小的顺序为
②铁氰化钾中,不存在
A.离子键 B.
 键 C.
键 C. 键 D.氢键 E.金属键
键 D.氢键 E.金属键(3)血蓝蛋白是某些节肢动物体内能与氧气可逆结合的一种铜蛋白,其部分结构示意图如图所示。其中Cu的化合价为

(4)
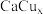 合金可看作由如图所示的(a)、(b)两种原子层交替堆积排列而成。图中虚线构建的六边形,表示由这两种层平行堆积时垂直于层的相对位置;(c)是由(a)和(b)两种原子层交替堆积成的
合金可看作由如图所示的(a)、(b)两种原子层交替堆积排列而成。图中虚线构建的六边形,表示由这两种层平行堆积时垂直于层的相对位置;(c)是由(a)和(b)两种原子层交替堆积成的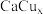 合金的晶胞结构图。在这种结构中,同一层的Ca与Cu距离为
合金的晶胞结构图。在这种结构中,同一层的Ca与Cu距离为 。
。
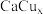 合金中
合金中
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】按要求完成下列问题:
(1)写出CCl4中心原子成键时采取的杂化轨道类型及分子中共价键的键角:___________ 、___________ 。
(2)气态 分子的空间构型为
分子的空间构型为___________ , 离子的空间构型为
离子的空间构型为___________ ;
(3)写出基态铁原子的简化电子排布式和Mg2+的核外电子排布式:___________ 、___________ 。
(4) 的沸点比
的沸点比 高的原因是
高的原因是___________ 。
(1)写出CCl4中心原子成键时采取的杂化轨道类型及分子中共价键的键角:
(2)气态
 分子的空间构型为
分子的空间构型为 离子的空间构型为
离子的空间构型为(3)写出基态铁原子的简化电子排布式和Mg2+的核外电子排布式:
(4)
 的沸点比
的沸点比 高的原因是
高的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】O、S、Se、Te是元素周期表中第ⅥA族元素。
(1)第ⅥA族元素原子的价层电子排布式为_______ 。
(2)常压下, 、
、 、
、 的沸点分别为100℃、-61℃和-41℃,三者沸点差异的原因为
的沸点分别为100℃、-61℃和-41℃,三者沸点差异的原因为_______ 。
(3)半胱氨酸亚金钠可用于配制无氰镀金溶液,其结构简式如图所示。
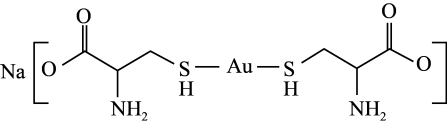
①半胱氨酸亚金钠中,碳原子的杂化轨道类型为_______ 。
②半胱氨酸亚金钠晶体中,不存在的化学键是_______ (填标号)。
A.共价键 B.离子键 C.金属键 D.配位键
(4)FexSeyTez是一种准二维结构的铁系超导材料,其晶胞示意图如图所示。
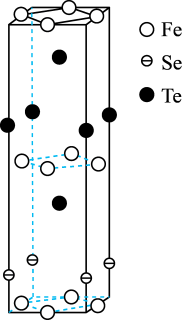
①
_______ 。
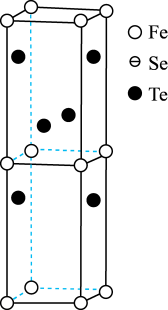
②若以铁原子为晶胞顶点,请在图中补画出铁、硒原子_______ 。
(1)第ⅥA族元素原子的价层电子排布式为
(2)常压下,
 、
、 、
、 的沸点分别为100℃、-61℃和-41℃,三者沸点差异的原因为
的沸点分别为100℃、-61℃和-41℃,三者沸点差异的原因为(3)半胱氨酸亚金钠可用于配制无氰镀金溶液,其结构简式如图所示。
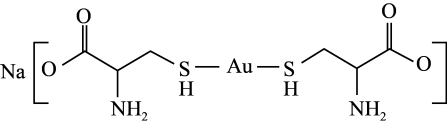
①半胱氨酸亚金钠中,碳原子的杂化轨道类型为
②半胱氨酸亚金钠晶体中,不存在的化学键是
A.共价键 B.离子键 C.金属键 D.配位键
(4)FexSeyTez是一种准二维结构的铁系超导材料,其晶胞示意图如图所示。

①

②若以铁原子为晶胞顶点,请在图中补画出铁、硒原子

您最近一年使用:0次
【推荐1】按要求回答下列问题:
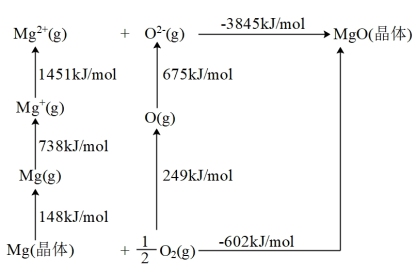
(1)MgO的Born-Haber循环如图所示。O=O键键能为_______ kJ·mol-1,Mg原子的第一电离能为_______ kJ·mol-1。
(2)已知共价键的键能:Cl-Cl:243 kJ·mol-1,Si-Si:176 kJ·mol-1,Si-Cl:360 kJ·mol-1,则反应Si(s)+2Cl2(g)=SiCl4(g) △H=_______ kJ·mol-1
(3)元素的化合价与元素的电负性、原子所处的具体的化学环境紧密相关。如:有机化合物CH3I发生水解时的反应为:CHЗI+H2O→CHЗOH+HI,已知有机化合物CFЗI中I为+1价,请写出CF3I发生水解反应的化学方程式:_______ 。
(1)MgO的Born-Haber循环如图所示。O=O键键能为

(2)已知共价键的键能:Cl-Cl:243 kJ·mol-1,Si-Si:176 kJ·mol-1,Si-Cl:360 kJ·mol-1,则反应Si(s)+2Cl2(g)=SiCl4(g) △H=
(3)元素的化合价与元素的电负性、原子所处的具体的化学环境紧密相关。如:有机化合物CH3I发生水解时的反应为:CHЗI+H2O→CHЗOH+HI,已知有机化合物CFЗI中I为+1价,请写出CF3I发生水解反应的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铜是人类最早使用的金属之一,铜的化合物丰富多彩。
(1)Cu在周期表中位于___________ 区,Cu2+价电子排布式为___________ 。
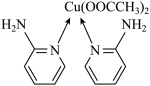
(2)邻氨基吡啶( )的铜配合物在有机合成中有重要作用。C、N、O的第一电离能由大到小的顺序为
)的铜配合物在有机合成中有重要作用。C、N、O的第一电离能由大到小的顺序为___________ ;1mol 中σ键的数目为
中σ键的数目为___________ 。邻氨基吡啶的铜配合物结构简式如下图所示,C原子轨道杂化类型为___________ 。
(3)向CuSO4溶液中加入过量氨水再加少许乙醇可以析出蓝色晶体[Cu(NH3)4]SO4∙H2O。
①NH3分子中H-N-H键角为107°,在[Cu(NH3)4]2+中H-N-H键角近似109.5°,键角变大的原因是___________ 。
②NF3与NH3均为三角锥形分子,NF3分子中的氮原子不易与Cu2+形成配离子,请从电负性角度分析其原因是___________ 。
(1)Cu在周期表中位于
(2)邻氨基吡啶(
 )的铜配合物在有机合成中有重要作用。C、N、O的第一电离能由大到小的顺序为
)的铜配合物在有机合成中有重要作用。C、N、O的第一电离能由大到小的顺序为 中σ键的数目为
中σ键的数目为
(3)向CuSO4溶液中加入过量氨水再加少许乙醇可以析出蓝色晶体[Cu(NH3)4]SO4∙H2O。
①NH3分子中H-N-H键角为107°,在[Cu(NH3)4]2+中H-N-H键角近似109.5°,键角变大的原因是
②NF3与NH3均为三角锥形分子,NF3分子中的氮原子不易与Cu2+形成配离子,请从电负性角度分析其原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】填空题。
(1)某元素原子的价电子构型为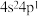 ,该元素的符号为
,该元素的符号为_______ 。
(2)某元素 价离子的
价离子的 轨道半充满,该元素的符号为
轨道半充满,该元素的符号为_______ 。
(3)A元素的负二价离子和B元素的正二价离子的电子层结构都与氩相同,A和B形成的化合物的化学式为_______ 。
(4)下列关于物质熔点的排列顺序不正确的是_______。
三种常见元素原子的结构信息如表所示,试回答下列问题。
(5)C元素位于元素周期表中_______ 区,C元素原子的价电子排布式为_______ 。
(6)A的简单氢化物分子结合一个 形成阳离子后,其键角
形成阳离子后,其键角_______ (填“变大”“变小”或“不变”)。
(7)下列分子结构图中“●”表示某种元素的原子,①中“●”表示A元素的原子,②③中“●”表示的原子其元素与A元素同周期,④中“●”表示的原子其元素与B元素同主族且与A元素同周期,“○”均表示氢原子,小黑点“·”均表示没有参与形成共价键的电子,短线均表示共价键。

上述四种物质中②的分子式为_______ ,四种物质中中心原子采取 杂化的是
杂化的是_______ (填序号)。
(1)某元素原子的价电子构型为
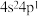 ,该元素的符号为
,该元素的符号为(2)某元素
 价离子的
价离子的 轨道半充满,该元素的符号为
轨道半充满,该元素的符号为(3)A元素的负二价离子和B元素的正二价离子的电子层结构都与氩相同,A和B形成的化合物的化学式为
(4)下列关于物质熔点的排列顺序不正确的是_______。
| A.生铁>纯铁>钠 | B. |
C. | D.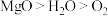 |
三种常见元素原子的结构信息如表所示,试回答下列问题。
| 元素 | A | B | C |
| 结构信息 | 原子核外有2个电子层,最外层有3个未成对电子 | 原子核外M层有1个成对的p电子 | 原子核外M层充满电子,N层有1个未成对的s电子 |
(6)A的简单氢化物分子结合一个
 形成阳离子后,其键角
形成阳离子后,其键角(7)下列分子结构图中“●”表示某种元素的原子,①中“●”表示A元素的原子,②③中“●”表示的原子其元素与A元素同周期,④中“●”表示的原子其元素与B元素同主族且与A元素同周期,“○”均表示氢原子,小黑点“·”均表示没有参与形成共价键的电子,短线均表示共价键。

上述四种物质中②的分子式为
 杂化的是
杂化的是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】以Cu2O、ZnO等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:
(1)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是_______ 。
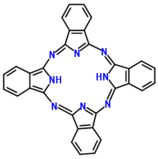
(2)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价值。酞菁分子结构如下图,分子中所有原子共平面,所有N原子的杂化轨道类型相同,均采取_______ 杂化。邻苯二甲酸酐( )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺(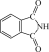 )都是合成酞菁的原料,后者熔点高于前者,主要原因是
)都是合成酞菁的原料,后者熔点高于前者,主要原因是_______ 。
(3)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为_______ 。
(4)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小于Zn-O键,原因是_______ 。
(5)下图为某ZnO晶胞示意图,下图是若干晶胞无隙并置而成的底面O原子排列局部平面图。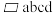 为所取晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母表示出与所取晶胞相邻的两个晶胞的底面
为所取晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母表示出与所取晶胞相邻的两个晶胞的底面_______ 、_______ 。

(1)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是
(2)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价值。酞菁分子结构如下图,分子中所有原子共平面,所有N原子的杂化轨道类型相同,均采取
 )和邻苯二甲酰亚胺(
)和邻苯二甲酰亚胺( )都是合成酞菁的原料,后者熔点高于前者,主要原因是
)都是合成酞菁的原料,后者熔点高于前者,主要原因是
(3)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为
(4)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小于Zn-O键,原因是
(5)下图为某ZnO晶胞示意图,下图是若干晶胞无隙并置而成的底面O原子排列局部平面图。
 为所取晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母表示出与所取晶胞相邻的两个晶胞的底面
为所取晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母表示出与所取晶胞相邻的两个晶胞的底面
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】Q、R、X、M、Y、Z是元素周期表前四周期的六种元素,原子序数依次递增。已知:
①Z位于ds区,最外能层没有单电子,其余的均为短周期主族元素;
②Y原子价电子排布为msnmpn(m≠n);
③M的基态原子2p能级有1个单电子;
④Q、X原子p轨道的未成对电子数都是2。
用化学术语回答下列问题:
(1)Z在周期表中的位置______________ 。
(2)Q、R、X、M四种元素第一电离能由大到小的顺序为__________ (用对应元素的符号填写)。
(3)X、M两元素形成的化合物XM2的VSEPR模型名称为_________ ,已知XM2分子的极性比水分子的极性弱,其原因是__________________ 。
(4)分析下表中两种物质的键能数据(单位:kJ/mol)。
①结合数据说明QX比R2活泼的原因:________________________ 。
②QX与R2互为等电子体,QX的结构式为(若有配位键请用→表示)______ 。Fe易与QX形成配合物,化学式遵循18电子规则:中心原子的价电子数加上配体提供的电子数之和等于18,则此配合物化学式为_______ 。
①Z位于ds区,最外能层没有单电子,其余的均为短周期主族元素;
②Y原子价电子排布为msnmpn(m≠n);
③M的基态原子2p能级有1个单电子;
④Q、X原子p轨道的未成对电子数都是2。
用化学术语回答下列问题:
(1)Z在周期表中的位置
(2)Q、R、X、M四种元素第一电离能由大到小的顺序为
(3)X、M两元素形成的化合物XM2的VSEPR模型名称为
(4)分析下表中两种物质的键能数据(单位:kJ/mol)。
A—B | A=B | A≡B | |
QX | 357.7 | 798.9 | 1 071.9 |
R2 | 154.8 | 418.4 | 941.7 |
②QX与R2互为等电子体,QX的结构式为(若有配位键请用→表示)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】点击化学的代表反应为铜催化的叠氮-炔基Huisgen环加成反应, 、
、 、
、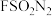 等均是点击化学中常用的无机试剂。回答下列问题:
等均是点击化学中常用的无机试剂。回答下列问题:
(1)基态 核外价电子排布式为
核外价电子排布式为_______ ;基态C原子中未成对电子有_______ 个。
(2)F、O、N、C的第一电离能从小到大的顺序是_______ 。
(3) 的VSEPR模型为
的VSEPR模型为_______ ,写出 的一种等电子体:
的一种等电子体:_______ 。从分子结构角度分析, 的酸性强于
的酸性强于 的原因是
的原因是_______ 。
(4)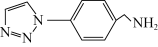 是一种叠氮-炔基Huisgen环加成反应产物,该分子中N原子的杂化方式为
是一种叠氮-炔基Huisgen环加成反应产物,该分子中N原子的杂化方式为_______ 。
(5) (叠氮酸)可表示为:
(叠氮酸)可表示为: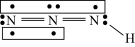 ,下列说法正确的是_______(填标号)。
,下列说法正确的是_______(填标号)。
 、
、 、
、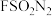 等均是点击化学中常用的无机试剂。回答下列问题:
等均是点击化学中常用的无机试剂。回答下列问题:(1)基态
 核外价电子排布式为
核外价电子排布式为(2)F、O、N、C的第一电离能从小到大的顺序是
(3)
 的VSEPR模型为
的VSEPR模型为 的一种等电子体:
的一种等电子体: 的酸性强于
的酸性强于 的原因是
的原因是(4)
 是一种叠氮-炔基Huisgen环加成反应产物,该分子中N原子的杂化方式为
是一种叠氮-炔基Huisgen环加成反应产物,该分子中N原子的杂化方式为(5)
 (叠氮酸)可表示为:
(叠氮酸)可表示为: ,下列说法正确的是_______(填标号)。
,下列说法正确的是_______(填标号)。A. 中含有5个 中含有5个 键 键 | B. 中3个氮原子采用的都是 中3个氮原子采用的都是 杂化 杂化 |
C. 分子间存在氢键 分子间存在氢键 | D. 、 、 、 、 、 、 都是极性分子 都是极性分子 |
您最近一年使用:0次
【推荐1】铁及其化合物在生产生活中有着广泛的应用。回答下列问题:
(1)基态Fe原子的外围电子排布图为____ ,基态Fe2+中,核外电子占据最高能层的符号是____ ,Fe2+和Fe3+是铁的两种常见离子,Fe3+的稳定性强于Fe2+,原因是____ 。
(2)Fe3+可以与SCN—形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验Fe3+的存在,KSCN中四种元素的电负性由小到大的顺序为_______ ,SCN—的几何构型为______ ,中心原子的杂化类型为_______ 。
(3)实验中常用K3[Fe(CN)6]检验Fe2+, K3[Fe(CN)6]晶体中的化学键有_________ (填写选项字母)
a.离子键. b.共价键 c,氢键 d .配位键 e.金属键
1mol K3[Fe(CN)6]中含有σ键与π键的数目比为_____________ 。
(4)FexO为氯化钠型结构,在实际晶体中,由于存在缺陷,x<1。 测得Fe0.92O晶体的晶胞参数a=428.0pm,则该晶体的密度ρ=__________ g/cm3 (列出计算式),晶体中最近的两个铁离子间的距离为_______ pm。
(1)基态Fe原子的外围电子排布图为
(2)Fe3+可以与SCN—形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验Fe3+的存在,KSCN中四种元素的电负性由小到大的顺序为
(3)实验中常用K3[Fe(CN)6]检验Fe2+, K3[Fe(CN)6]晶体中的化学键有
a.离子键. b.共价键 c,氢键 d .配位键 e.金属键
1mol K3[Fe(CN)6]中含有σ键与π键的数目比为
(4)FexO为氯化钠型结构,在实际晶体中,由于存在缺陷,x<1。 测得Fe0.92O晶体的晶胞参数a=428.0pm,则该晶体的密度ρ=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】钾长石(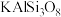 )是一种火成岩矿物,常见于火山岩和花岗岩中。可用于制作瓷砖、墙壁等,钾长石还可以用于制造化肥。以钾长石为原料制取钾肥(
)是一种火成岩矿物,常见于火山岩和花岗岩中。可用于制作瓷砖、墙壁等,钾长石还可以用于制造化肥。以钾长石为原料制取钾肥( )的一种工艺流程如图所示。
)的一种工艺流程如图所示。 作用下转化为
作用下转化为 和
和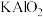
回答下列问题:
(1)钾长石用氧化物表示的化学式为___________ ;浸渣1的主要成分为___________ 。
(2)钾离子的基态电子排布式为___________ ,流程中可循环利用的物质有 、
、___________ 。(填俗名)
(3)写出调pH生成浸渣2的离子方程式为___________ 。
(4)碱化步骤中加入NaOH的目的是___________ 。
(5) 的晶胞结构如图所示,晶胞参数a=x nm,晶胞中氧原子的配位数为
的晶胞结构如图所示,晶胞参数a=x nm,晶胞中氧原子的配位数为___________ ,列式计算晶体 的密度为
的密度为___________  。
。
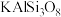 )是一种火成岩矿物,常见于火山岩和花岗岩中。可用于制作瓷砖、墙壁等,钾长石还可以用于制造化肥。以钾长石为原料制取钾肥(
)是一种火成岩矿物,常见于火山岩和花岗岩中。可用于制作瓷砖、墙壁等,钾长石还可以用于制造化肥。以钾长石为原料制取钾肥( )的一种工艺流程如图所示。
)的一种工艺流程如图所示。
 作用下转化为
作用下转化为 和
和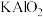
回答下列问题:
(1)钾长石用氧化物表示的化学式为
(2)钾离子的基态电子排布式为
 、
、(3)写出调pH生成浸渣2的离子方程式为
(4)碱化步骤中加入NaOH的目的是
(5)
 的晶胞结构如图所示,晶胞参数a=x nm,晶胞中氧原子的配位数为
的晶胞结构如图所示,晶胞参数a=x nm,晶胞中氧原子的配位数为 的密度为
的密度为 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
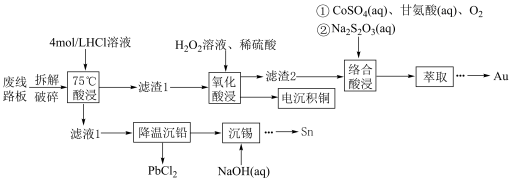
【推荐3】废旧手机的废线路板中富含Cu、Sn、Ni、Pb等金属和少量Ag、Au,具有较高的回收价值,其中部分金属的回收工艺流程如下: 微溶于水,可与
微溶于水,可与 结合生成
结合生成 配离子:
配离子: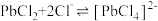 。
。
②25℃时,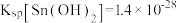 ,
,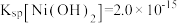 。
。
回答下列问题:
(1)“拆解破碎”的目的是_______ 。
(2)“75℃酸浸”中,金属Sn与盐酸反应的离子方程式为_______ ,选用浓度较大的4 mol·L 盐酸可提高铅元素的浸出率,理由是
盐酸可提高铅元素的浸出率,理由是_______ (从平衡移动角度分析)。
(3)“滤渣1”的主要成分是_______ (填化学式),“氧化酸浸”中,生成Cu²⁺反应的离子方程式为_______ 。
(4) 的排放标准为
的排放标准为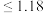 mg·L
mg·L 。“沉锡”残余液排放前应调节溶液的pH范围为
。“沉锡”残余液排放前应调节溶液的pH范围为_____ 。
(5)“络合酸浸”中,Co2+作催化剂,催化Au浸出,化学方程式为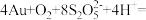
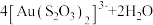 ,其反应过程按如下步骤进行:
,其反应过程按如下步骤进行:
① 先与甘氨酸根(简写为
先与甘氨酸根(简写为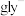 )形成配合物
)形成配合物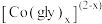 (
(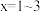 )。
)。
②在氧气作用下,Co(Ⅱ)被氧化成Co(Ⅲ):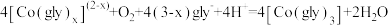 。
。
③Au溶解。
④加入硫代硫酸钠溶液,发生反应: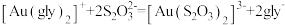 。
。
步骤③Au溶解的离子方程式为_______ 。
(6)锡有白锡和灰锡两种单质。白锡晶体中锡原子的堆积方式如图所示,该六棱柱底边边长为a pm,高为c pm,阿伏加德罗常数的值为 ,白锡晶体的密度为
,白锡晶体的密度为_______  (列出计算式)。
(列出计算式)。
 微溶于水,可与
微溶于水,可与 结合生成
结合生成 配离子:
配离子: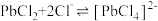 。
。②25℃时,
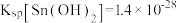 ,
,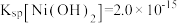 。
。回答下列问题:
(1)“拆解破碎”的目的是
(2)“75℃酸浸”中,金属Sn与盐酸反应的离子方程式为
 盐酸可提高铅元素的浸出率,理由是
盐酸可提高铅元素的浸出率,理由是(3)“滤渣1”的主要成分是
(4)
 的排放标准为
的排放标准为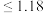 mg·L
mg·L 。“沉锡”残余液排放前应调节溶液的pH范围为
。“沉锡”残余液排放前应调节溶液的pH范围为(5)“络合酸浸”中,Co2+作催化剂,催化Au浸出,化学方程式为
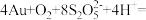
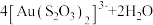 ,其反应过程按如下步骤进行:
,其反应过程按如下步骤进行:①
 先与甘氨酸根(简写为
先与甘氨酸根(简写为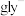 )形成配合物
)形成配合物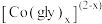 (
(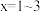 )。
)。②在氧气作用下,Co(Ⅱ)被氧化成Co(Ⅲ):
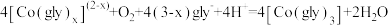 。
。③Au溶解。
④加入硫代硫酸钠溶液,发生反应:
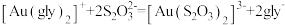 。
。步骤③Au溶解的离子方程式为
(6)锡有白锡和灰锡两种单质。白锡晶体中锡原子的堆积方式如图所示,该六棱柱底边边长为a pm,高为c pm,阿伏加德罗常数的值为
 ,白锡晶体的密度为
,白锡晶体的密度为 (列出计算式)。
(列出计算式)。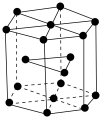
您最近一年使用:0次



