铁及其化合物在生产生活中有着广泛的应用。回答下列问题:
(1)基态Fe原子的外围电子排布图为____ ,基态Fe2+中,核外电子占据最高能层的符号是____ ,Fe2+和Fe3+是铁的两种常见离子,Fe3+的稳定性强于Fe2+,原因是____ 。
(2)Fe3+可以与SCN—形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验Fe3+的存在,KSCN中四种元素的电负性由小到大的顺序为_______ ,SCN—的几何构型为______ ,中心原子的杂化类型为_______ 。
(3)实验中常用K3[Fe(CN)6]检验Fe2+, K3[Fe(CN)6]晶体中的化学键有_________ (填写选项字母)
a.离子键. b.共价键 c,氢键 d .配位键 e.金属键
1mol K3[Fe(CN)6]中含有σ键与π键的数目比为_____________ 。
(4)FexO为氯化钠型结构,在实际晶体中,由于存在缺陷,x<1。 测得Fe0.92O晶体的晶胞参数a=428.0pm,则该晶体的密度ρ=__________ g/cm3 (列出计算式),晶体中最近的两个铁离子间的距离为_______ pm。
(1)基态Fe原子的外围电子排布图为
(2)Fe3+可以与SCN—形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验Fe3+的存在,KSCN中四种元素的电负性由小到大的顺序为
(3)实验中常用K3[Fe(CN)6]检验Fe2+, K3[Fe(CN)6]晶体中的化学键有
a.离子键. b.共价键 c,氢键 d .配位键 e.金属键
1mol K3[Fe(CN)6]中含有σ键与π键的数目比为
(4)FexO为氯化钠型结构,在实际晶体中,由于存在缺陷,x<1。 测得Fe0.92O晶体的晶胞参数a=428.0pm,则该晶体的密度ρ=
更新时间:2020-05-20 08:28:54
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】由P、S、Cl、Ni等元素组成的新型材料有着广泛的用途,回答下列问题。
(1)基态Cl原子核外电子占有的原子轨道数为_ 个,P、S、Cl的氢化物稳定性由强到弱顺序为___ 。
(2)已知MO与NiO的晶体结构(如图1)相同,其中Mg2+和Ni2+的离子半径分别为66pm和69pm。则熔点:MgO__ NiO(填“>”、“<”或“=”),理由是:___ 。
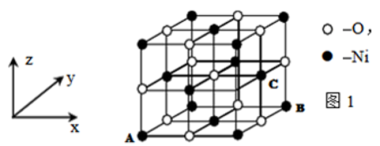
(3)若NiO晶胞中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为_____ 。
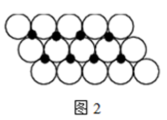
(4)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图2),已知O2-的半径为am,每平方米面积上分散的该晶体的质量为____ g。(用a、NA表示,相对原子质量:O-16,Ni-59)
(1)基态Cl原子核外电子占有的原子轨道数为
(2)已知MO与NiO的晶体结构(如图1)相同,其中Mg2+和Ni2+的离子半径分别为66pm和69pm。则熔点:MgO

(3)若NiO晶胞中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为
(4)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图2),已知O2-的半径为am,每平方米面积上分散的该晶体的质量为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】Fe、Cu为过渡金属元素,它们在工业生产中都有重要的应用。回答下列问题:
(1)将乙醇蒸气通过赤热的氧化铜粉末,会发生反应: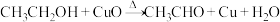
①有同学书写基态碳原子的核外电子排布图为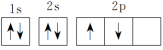 ,这样的书写不正确,违背了
,这样的书写不正确,违背了___________ 。
②乙醛和乙醇的相对分子质量相差2,但是,乙醇的沸点高于乙醛,其主要原因是___________ 。
(2)Fe、 都能被硝酸氧化。
都能被硝酸氧化。 中氮原子轨道的杂化类型为
中氮原子轨道的杂化类型为___________ 。
(3)研究发现,阳离子的颜色与未成对电子数有关。例如: 、
、 、
、 等。
等。 呈无色,其原因是
呈无色,其原因是___________ 。
(1)将乙醇蒸气通过赤热的氧化铜粉末,会发生反应:
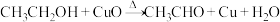
①有同学书写基态碳原子的核外电子排布图为
 ,这样的书写不正确,违背了
,这样的书写不正确,违背了②乙醛和乙醇的相对分子质量相差2,但是,乙醇的沸点高于乙醛,其主要原因是
(2)Fe、
 都能被硝酸氧化。
都能被硝酸氧化。 中氮原子轨道的杂化类型为
中氮原子轨道的杂化类型为(3)研究发现,阳离子的颜色与未成对电子数有关。例如:
 、
、 、
、 等。
等。 呈无色,其原因是
呈无色,其原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】I. Goodenough 等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)基态Fe3+离子中未成对的电子数为___________ 。
(2)Li及其周期表中相邻元素的第一电离能I1大小比较关系如下:I2(Li>I1(Na),原因是___________ ,Li、Be、B三元素的第一电离能I1(Be)、I1(B)、I1(Li)之间的大小关系是___________ 。
(3)磷酸根离子的空间构型为___________ ,其中P的价层电子对数为___________ 、杂化轨道类型为___________ 。
II.铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂等。
(4)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-(不考虑空间构型),[Cu(OH)4]2-结构可用示意图表示为___________ 。
(5)胆矾CuSO4·5H2O可写为[Cu(H2O)4]SO4·H2O,其结构示意如下图:则关于[Cu(H2O)4]SO4的下列说法中错误的是___________

III.经研究表明,Fe(SCN)3是配合物,Fe3+与SCN-不仅能以1:3 的个数比配合,还可以以其他个数比配合。
(6)若所得的Fe3+和SCN-的配合物中,主要是Fe3+与SCN-以个数比1:1配合,所得离子显红色。该离子的离子符号是___________ 。
(7)若所得的Fe3+和SCN-以个数比1:5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示___________ 。
(1)基态Fe3+离子中未成对的电子数为
(2)Li及其周期表中相邻元素的第一电离能I1大小比较关系如下:I2(Li>I1(Na),原因是
(3)磷酸根离子的空间构型为
II.铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂等。
(4)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-(不考虑空间构型),[Cu(OH)4]2-结构可用示意图表示为
(5)胆矾CuSO4·5H2O可写为[Cu(H2O)4]SO4·H2O,其结构示意如下图:则关于[Cu(H2O)4]SO4的下列说法中错误的是___________

| A.此配合物中心离子的配位数为4 |
| B.配体为H2O,配位原子是氧原子 |
| C.此配合物中Cu2+提供孤对电子 |
| D.向此配合物溶液中加入BaCl2溶液,将出现白色沉淀 |
III.经研究表明,Fe(SCN)3是配合物,Fe3+与SCN-不仅能以1:3 的个数比配合,还可以以其他个数比配合。
(6)若所得的Fe3+和SCN-的配合物中,主要是Fe3+与SCN-以个数比1:1配合,所得离子显红色。该离子的离子符号是
(7)若所得的Fe3+和SCN-以个数比1:5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示
您最近一年使用:0次
【推荐1】钛(Ti)被称为“未来金属”,广泛应用于国防、航空航天、生物材料等领域。钛的氯化物有如下转变关系:2TiCl3 TiCl4↑+TiCl2,回答下列问题:
TiCl4↑+TiCl2,回答下列问题:
(1)基态钛原子的价电子排布式为___________ 。与钛同周期的第ⅡB族和ⅢA族两种元素中第一电离能较大的是___________ (写元素符号),原因是___________ 。
(2)钛的氯化物的部分物理性质如下表:
①TiCl4与TiCl2的晶体类型分别是___________ 、___________ 。
②TiCl4与 互为等电子体,因为它们
互为等电子体,因为它们___________ 相同; 中心原子的杂化方式是
中心原子的杂化方式是___________ 。
(3)Ti的配合物有多种。 的配体所含原子中电负性最小的是
的配体所含原子中电负性最小的是___________ ; 的球棍结构如图Ⅰ,Ti的配位数是
的球棍结构如图Ⅰ,Ti的配位数是___________ 。

(4)钙钛矿(CaTiO3)是自然界中的一种常见矿物,其晶胞结构如图Ⅱ。
①设NA为阿伏加德罗常数的值,计算一个晶胞的质量为___________ g。
②假设O2-采用面心立方最密堆积,Ti4+与O2-相切,则
___________ 。
 TiCl4↑+TiCl2,回答下列问题:
TiCl4↑+TiCl2,回答下列问题:(1)基态钛原子的价电子排布式为
(2)钛的氯化物的部分物理性质如下表:
| 氯化物 | 熔点/℃ | 沸点/℃ | 溶解性 |
| TiCl4 | -24 | 136 | 可溶于非极性的甲苯和氯代烃 |
| TiCl2 | 1035 | 1500 | 不溶于氯仿、乙醚 |
②TiCl4与
 互为等电子体,因为它们
互为等电子体,因为它们 中心原子的杂化方式是
中心原子的杂化方式是(3)Ti的配合物有多种。
 的配体所含原子中电负性最小的是
的配体所含原子中电负性最小的是 的球棍结构如图Ⅰ,Ti的配位数是
的球棍结构如图Ⅰ,Ti的配位数是
(4)钙钛矿(CaTiO3)是自然界中的一种常见矿物,其晶胞结构如图Ⅱ。
①设NA为阿伏加德罗常数的值,计算一个晶胞的质量为
②假设O2-采用面心立方最密堆积,Ti4+与O2-相切,则

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】氨硼烷(NH3BH3)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答问题:
(1)H、B、N中,原子半径最大的是__ 。根据对角线规则,B的一些化学性质与元素__ 的相似。
(2)NH3BH3分子中,N—B化学键称为__ 键,其电子对由____ 提供。氨硼烷在催化剂作用下水解释放氢气:3NH3BH3+6H2O=3NH3+B3O +9H2,B3O
+9H2,B3O 的结构如图所示:
的结构如图所示:

在该反应中,B原子的杂化轨道类型由__ 变为__ 。
(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序是__ 。与NH3BH3原子总数相等的等电子体是__ (写结构简式),其熔点比NH3BH3__ (填“高”或“低”),原因是在NH3BH3分子之间,存在__ ,也称“双氢键”。
(1)H、B、N中,原子半径最大的是
(2)NH3BH3分子中,N—B化学键称为
 +9H2,B3O
+9H2,B3O 的结构如图所示:
的结构如图所示:
在该反应中,B原子的杂化轨道类型由
(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】氨硼烷( )含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
(1)基态 原子电子占据
原子电子占据_____ 个能层,电子占据的最高能级的符号是______ 。基态 原子共有
原子共有_____ 种不同运动状态的电子。
(2) 的第一电离能
的第一电离能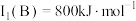 ,判断
,判断
_____  (填“>”或“<”),从
(填“>”或“<”),从电子排布的角度 说明判断理由_______ 。
(3) 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 。在H、B、N三种元素中,电负性由大到小的顺序是
。在H、B、N三种元素中,电负性由大到小的顺序是________ 。
(4) 是目前氨硼烷水解产氢催化剂研究的热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。这四种催化剂中:
是目前氨硼烷水解产氢催化剂研究的热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。这四种催化剂中:

①位于ds区的元素符号是______ 。
②催化效果最好的金属基态原子中未成对的电子数为______ 。
 )含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:(1)基态
 原子电子占据
原子电子占据 原子共有
原子共有(2)
 的第一电离能
的第一电离能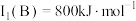 ,判断
,判断
 (填“>”或“<”),从
(填“>”或“<”),从(3)
 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 。在H、B、N三种元素中,电负性由大到小的顺序是
。在H、B、N三种元素中,电负性由大到小的顺序是(4)
 是目前氨硼烷水解产氢催化剂研究的热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。这四种催化剂中:
是目前氨硼烷水解产氢催化剂研究的热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。这四种催化剂中:
①位于ds区的元素符号是
②催化效果最好的金属基态原子中未成对的电子数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铬、铁、钴、铜等金属及其化合物在工业上有重要用途。请回答:
(1)基态铬原子的价电子排布图为___________ 。
(2)CrO2Cl2和NaClO均可作化工生产的氧化剂或氯化剂。制备CrO2Cl2的反应为K2Cr2O2+3CCl4=2KCl +2CrO2Cl2+3COCl2↑。
①上述反应式中非金属元素电负性由大到小的顺序是__________ (用元素符号表示)。
②常温时CrO2Cl2是一种易溶于CCl4的液体,则固态CrO2Cl2属于__________ 晶体。
③配合物CrCl3·6H2O中心离子Cr3+的配位数为6,向含0.1molCrCl3·6H2O 的溶液中滴加2mol·L-1 AgNO3溶液,反应完全后共消耗AgNO3溶液50mL,则配离子的化学式为___________ 。
(3)Co3+与NO2―形成的配合物与K+生成黄色沉淀检验溶液中的K+。配体NO2―的立体构型为__________ ,某常见气体化合物为NO2―的等电子体,该化合物的分子式为__________ 。
(4)氯和钾与+2价的铜可生成一种催化乙炔聚合反应的化合物,其阴离子为无限长链结构(如下图),a位置上Cl原子的杂化轨道类型为________ 杂化,这种化合物的化学式为_________

(5)铁和氨气在640 ℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:_____ 。若两个最近的Fe原子间的距离为a cm,则该晶体的密度是_____ g/cm3(设阿伏加 德罗常数的值为NA)。

(1)基态铬原子的价电子排布图为
(2)CrO2Cl2和NaClO均可作化工生产的氧化剂或氯化剂。制备CrO2Cl2的反应为K2Cr2O2+3CCl4=2KCl +2CrO2Cl2+3COCl2↑。
①上述反应式中非金属元素电负性由大到小的顺序是
②常温时CrO2Cl2是一种易溶于CCl4的液体,则固态CrO2Cl2属于
③配合物CrCl3·6H2O中心离子Cr3+的配位数为6,向含0.1molCrCl3·6H2O 的溶液中滴加2mol·L-1 AgNO3溶液,反应完全后共消耗AgNO3溶液50mL,则配离子的化学式为
(3)Co3+与NO2―形成的配合物与K+生成黄色沉淀检验溶液中的K+。配体NO2―的立体构型为
(4)氯和钾与+2价的铜可生成一种催化乙炔聚合反应的化合物,其阴离子为无限长链结构(如下图),a位置上Cl原子的杂化轨道类型为

(5)铁和氨气在640 ℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】钪及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广泛的应用。从钛白工业废酸(含钪、钛、铁、锰等离子)中提取氧化钪( )的一种流程如下:
)的一种流程如下:
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合的实验操作是_______________________________________________________________________ 。
(2)常温下,先加入氨水调节pH=3,过滤,滤渣主要成分是___________ ;再向滤液加入氨水调节pH=6,滤液中 的浓度为
的浓度为___________ 。
{已知: 、
、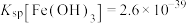 、
、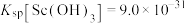 }
}
(3)用草酸“沉钪”,写出“沉钪”得到草酸钪的离子方程式:___________________ 。
(4)草酸钪“灼烧”氧化的化学方程式为____________________ 。
(5)镧与Sc同族位于第六周期,一种镧、锑形成的配合物结构如图所示: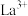 配位数为
配位数为___________ 。
(6)某铁、镧、锑的合金晶胞如图1,铁原子位于锑原子构成的正八面体的体心,晶胞的六个表面结构都如图2: ,则B点铁原子的分数坐标为
,则B点铁原子的分数坐标为__________ 。
②若该晶体的密度为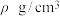 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,La、Fe、Sb的摩尔质量分别表示为
,La、Fe、Sb的摩尔质量分别表示为 、
、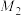 、
、 ,则Sb原子与Sb原子的最近距离为
,则Sb原子与Sb原子的最近距离为__________ cm。
 )的一种流程如下:
)的一种流程如下: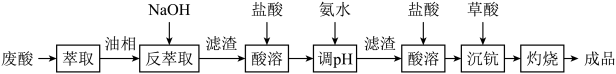
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合的实验操作是
(2)常温下,先加入氨水调节pH=3,过滤,滤渣主要成分是
 的浓度为
的浓度为{已知:
 、
、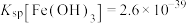 、
、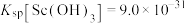 }
}(3)用草酸“沉钪”,写出“沉钪”得到草酸钪的离子方程式:
(4)草酸钪“灼烧”氧化的化学方程式为
(5)镧与Sc同族位于第六周期,一种镧、锑形成的配合物结构如图所示:

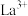 配位数为
配位数为(6)某铁、镧、锑的合金晶胞如图1,铁原子位于锑原子构成的正八面体的体心,晶胞的六个表面结构都如图2:

 ,则B点铁原子的分数坐标为
,则B点铁原子的分数坐标为②若该晶体的密度为
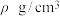 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,La、Fe、Sb的摩尔质量分别表示为
,La、Fe、Sb的摩尔质量分别表示为 、
、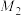 、
、 ,则Sb原子与Sb原子的最近距离为
,则Sb原子与Sb原子的最近距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】利用绿矾 和硫铁矿
和硫铁矿 可联合制备铁精粉
可联合制备铁精粉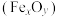 和硫酸。
和硫酸。
(1) 的结构示意图如图所示。
的结构示意图如图所示。___________ 。
② 中O原子和
中O原子和 中S原子均为
中S原子均为 杂化。
杂化。 分子中的
分子中的 键角
键角___________ (填“大于”、“等于”或“小于”)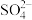 离子中
离子中 键角,其原因是
键角,其原因是___________ 。
③ 属于配位化合物。由结构示意图可知,
属于配位化合物。由结构示意图可知, 中
中 的配位数为
的配位数为___________ 。
(2) 晶体的晶胞形状为立方体,边长为
晶体的晶胞形状为立方体,边长为 ,结构如图所示。
,结构如图所示。 的电子式为
的电子式为___________ 。
② 晶体中
晶体中 位于
位于 形成的
形成的___________ (填“正四面体”或“正八面体”)空隙中。
③ 的摩尔质量为
的摩尔质量为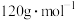 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。该晶体的密度为
。该晶体的密度为___________  。(列出算式即可,无需化简。
。(列出算式即可,无需化简。 )
)
 和硫铁矿
和硫铁矿 可联合制备铁精粉
可联合制备铁精粉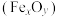 和硫酸。
和硫酸。(1)
 的结构示意图如图所示。
的结构示意图如图所示。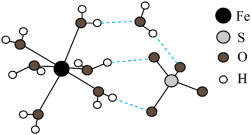
②
 中O原子和
中O原子和 中S原子均为
中S原子均为 杂化。
杂化。 分子中的
分子中的 键角
键角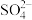 离子中
离子中 键角,其原因是
键角,其原因是③
 属于配位化合物。由结构示意图可知,
属于配位化合物。由结构示意图可知, 中
中 的配位数为
的配位数为(2)
 晶体的晶胞形状为立方体,边长为
晶体的晶胞形状为立方体,边长为 ,结构如图所示。
,结构如图所示。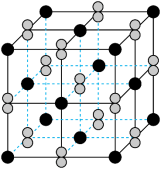
 的电子式为
的电子式为②
 晶体中
晶体中 位于
位于 形成的
形成的③
 的摩尔质量为
的摩尔质量为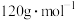 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。该晶体的密度为
。该晶体的密度为 。(列出算式即可,无需化简。
。(列出算式即可,无需化简。 )
)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】Mg、Al、Si、Cu是常用的生活材料。请回答下列问题:
(1)基态Cu2+中电子占有的能级数目是_______________ 。
(2)Mg、A1元素及其化合物有以下性质:
①Mg原子的配位数是12,属于__ 堆积方式解释第一电离能Mg比Al大的原因:_______________ 。
②解释熔点MgCl2比AlCl3高的原因:_______________ 。
③资料表明铝的氧化物分子式是Al2Cl6,其中Al的杂化方式是_____ ,从共用电子对提供的角度可知该分于中存在的化学键类型是_________ .
(3)金刚砂(SiC)的晶胞结构如图,若NA表示阿伏伽德罗常数的值,晶体的密度是ρg/cm3,则Si原子的半径R为__ cm(不必化简)。

(1)基态Cu2+中电子占有的能级数目是
(2)Mg、A1元素及其化合物有以下性质:
| Mg元素及其化合物 | Al元素及其化合物 | |
| 电离能/(KJ/mol) | Mg:I1=738.14,I2=1451,I3=7733 | Al:I1=578,I2=1817,I3=2745 |
| 熔点/℃ | MgCl2:714 | AlCl3:190(2.5×105Pa) |
①Mg原子的配位数是12,属于
②解释熔点MgCl2比AlCl3高的原因:
③资料表明铝的氧化物分子式是Al2Cl6,其中Al的杂化方式是
(3)金刚砂(SiC)的晶胞结构如图,若NA表示阿伏伽德罗常数的值,晶体的密度是ρg/cm3,则Si原子的半径R为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】LiMn2O4是一种锂离子电池的正极材料。用高锰酸钾废渣(主要成分为MnO2、Fe2O3、Al2O3、SiO2)和硫铁矿(主要成分为FeS2)制备LiMn2O4的工艺流程如图:
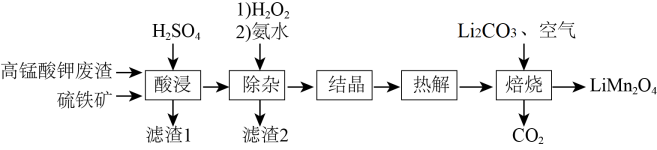
已知:①酸浸液主要含有Mn2+、Fe2+、Fe3+、Al3+等金属间离子;
②25℃时,相关物质的Ksp见表。
(1)酸浸。MnO2与FeS2反应生成Fe3+和SO 的离子方程式为
的离子方程式为____ 。保持温度、浸取时间不变,能提高锰元素浸出率的措施有____ 。
(2)除杂。欲使溶液中的Al3+、Fe3+沉淀完全,调节溶液的pH最小值为____ (当溶液中某离子浓度c≤1×10-5mol·L-1时,可认为该离子沉淀完全)。
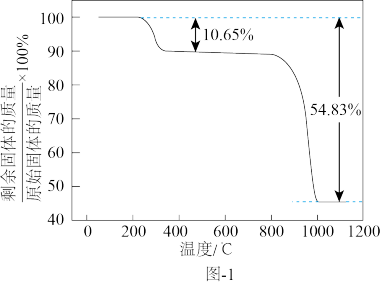
(3)热解。在真空中加热分解MnSO4•H2O,测得固体的质量随温度变化如图1所示。真空热解MnSO4•H2O制备Mn3O4,需控制的温度为_____ 。(写出计算推理过程)。
(4)焙烧。生成LiMn2O4的反应中,还原剂是____ (填化学式)。
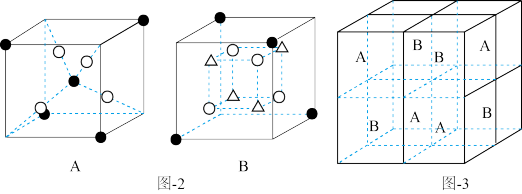
(5)一种LiMn2O4晶胞可看成由图2中A、B单元按图3方式构成。图2中“○”表示O2-,则“●”表示的微粒是____ (填离子符号)。

已知:①酸浸液主要含有Mn2+、Fe2+、Fe3+、Al3+等金属间离子;
②25℃时,相关物质的Ksp见表。
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-32.3 | 1×10-12.7 |
 的离子方程式为
的离子方程式为(2)除杂。欲使溶液中的Al3+、Fe3+沉淀完全,调节溶液的pH最小值为
(3)热解。在真空中加热分解MnSO4•H2O,测得固体的质量随温度变化如图1所示。真空热解MnSO4•H2O制备Mn3O4,需控制的温度为

(4)焙烧。生成LiMn2O4的反应中,还原剂是
(5)一种LiMn2O4晶胞可看成由图2中A、B单元按图3方式构成。图2中“○”表示O2-,则“●”表示的微粒是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】回答下列问题
(1)钦铝合金是制造航空航天及武器装备热端部件的理想材料。
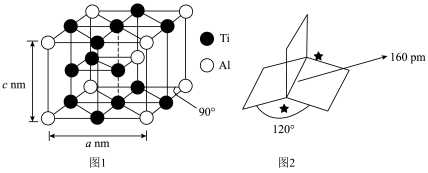
①基态 原子的价电子的轨道表示式
原子的价电子的轨道表示式__________ 。
②下列说法正确的是__________ 。
A.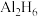 分子中既存在共价键又存在离子键
分子中既存在共价键又存在离子键
B.化学键中离子键成分的百分数: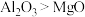
C.第一电离能:
D.测定接近沸点的水蒸气的相对分子质量,测量值偏大的理由是存在相当量的水分子因氢键而相互缔合
③该合金的化学式是__________ ,密度为__________  。
。
(2)碳和氧是构建化合物的常见元素。
某烃结构如图,结合图2所示信息,分析带星号碳的杂化方式为__________ ;带星号碳碳之间的键长比一般碳碳单键的键长要长,请从碳成键轨道的成分角度分析其原因__________ 。
(1)钦铝合金是制造航空航天及武器装备热端部件的理想材料。

①基态
 原子的价电子的轨道表示式
原子的价电子的轨道表示式②下列说法正确的是
A.
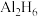 分子中既存在共价键又存在离子键
分子中既存在共价键又存在离子键B.化学键中离子键成分的百分数:
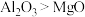
C.第一电离能:

D.测定接近沸点的水蒸气的相对分子质量,测量值偏大的理由是存在相当量的水分子因氢键而相互缔合
③该合金的化学式是
 。
。(2)碳和氧是构建化合物的常见元素。
某烃结构如图,结合图2所示信息,分析带星号碳的杂化方式为
您最近一年使用:0次



