O、S、Se、Te是元素周期表中第ⅥA族元素。
(1)第ⅥA族元素原子的价层电子排布式为_______ 。
(2)常压下, 、
、 、
、 的沸点分别为100℃、-61℃和-41℃,三者沸点差异的原因为
的沸点分别为100℃、-61℃和-41℃,三者沸点差异的原因为_______ 。
(3)半胱氨酸亚金钠可用于配制无氰镀金溶液,其结构简式如图所示。
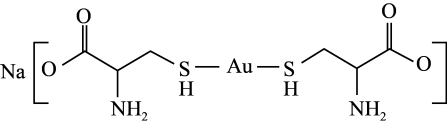
①半胱氨酸亚金钠中,碳原子的杂化轨道类型为_______ 。
②半胱氨酸亚金钠晶体中,不存在的化学键是_______ (填标号)。
A.共价键 B.离子键 C.金属键 D.配位键
(4)FexSeyTez是一种准二维结构的铁系超导材料,其晶胞示意图如图所示。
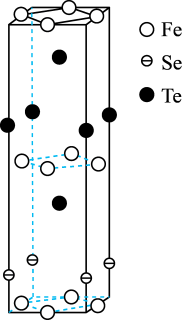
①
_______ 。
②若以铁原子为晶胞顶点,请在图中补画出铁、硒原子_______ 。
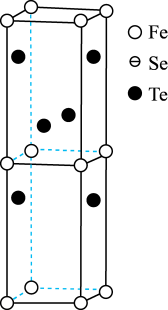
(1)第ⅥA族元素原子的价层电子排布式为
(2)常压下,
 、
、 、
、 的沸点分别为100℃、-61℃和-41℃,三者沸点差异的原因为
的沸点分别为100℃、-61℃和-41℃,三者沸点差异的原因为(3)半胱氨酸亚金钠可用于配制无氰镀金溶液,其结构简式如图所示。
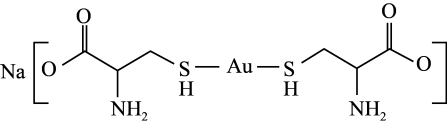
①半胱氨酸亚金钠中,碳原子的杂化轨道类型为
②半胱氨酸亚金钠晶体中,不存在的化学键是
A.共价键 B.离子键 C.金属键 D.配位键
(4)FexSeyTez是一种准二维结构的铁系超导材料,其晶胞示意图如图所示。

①

②若以铁原子为晶胞顶点,请在图中补画出铁、硒原子

更新时间:2022-03-04 17:20:41
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】按要求填空。
(1)已知钴元素在周期表中的信息如下,回答下列问题:___________ ,基态原子核外有___________ 种不同运动状态的电子,画出该原子的原子结构示意图___________ 。
(2)已知高温下 比CuO更稳定,试从核外电子排布角度解释原因
比CuO更稳定,试从核外电子排布角度解释原因___________ 。
(3)氰化钾是一种剧毒物质,贮存和使用时必须注意安全。已知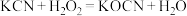 ,则
,则 中所含三种元素的电负性由大到小的顺序为
中所含三种元素的电负性由大到小的顺序为___________ (用元素符号表示,下同),第一电离能从大到小顺序为___________ ,基态氮原子的电子排布式为___________ ,其能量最高的电子所在原子轨道的电子云轮廓图为___________ 形。
(1)已知钴元素在周期表中的信息如下,回答下列问题:

(2)已知高温下
 比CuO更稳定,试从核外电子排布角度解释原因
比CuO更稳定,试从核外电子排布角度解释原因(3)氰化钾是一种剧毒物质,贮存和使用时必须注意安全。已知
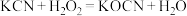 ,则
,则 中所含三种元素的电负性由大到小的顺序为
中所含三种元素的电负性由大到小的顺序为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】【化学—选修3物质结构与性质】
(1)元素的第一电离能:N_______ O(填“>”或:“<”)
(2)基态Fe2+的电子排布式为____________ 。
(3)在N、Mg、Al、Si四种元素中,有一种元素的电离能数据如下:
则该元素的元素符号是_______ 。
(4)NO 的空间构型
的空间构型______ (用文字描述),SO 中S原子的杂化方式为
中S原子的杂化方式为______ 。
(5)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如下图所示,呈现这种变化关系的原因是______________________________ 。

(6)金属铜原子的堆积方式为面心立方最密堆积,铜的原子半径为r nm,则铜晶胞的体积表达式为____ cm3。
(1)元素的第一电离能:N
(2)基态Fe2+的电子排布式为
(3)在N、Mg、Al、Si四种元素中,有一种元素的电离能数据如下:
电离能 | I1 | I2 | I3 | I4 | …… |
In/kJ·mol-1 | 578 | 1817 | 2745 | 11575 | …… |
则该元素的元素符号是
(4)NO
 的空间构型
的空间构型 中S原子的杂化方式为
中S原子的杂化方式为(5)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如下图所示,呈现这种变化关系的原因是

(6)金属铜原子的堆积方式为面心立方最密堆积,铜的原子半径为r nm,则铜晶胞的体积表达式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】物质的结构决定物质的性质。请回答下列涉及物质结构和性质的问题:
(1)第二周期中,元素的第一电离能处于B与N之间的元素有_________ 种。
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为_________________
(3)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P=O存在下加热脱H2O得到。乙烯酮分子中碳原子杂化轨道类型是_____________ ,1mol (C2H5O)3P=O分子中含有的σ键与π键的数目比为__________________ 。
(4)已知固态NH3、H2O、HF的氢键键能和结构如下:
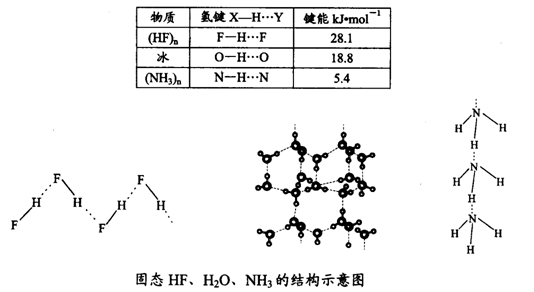
解释H2O、HF、NH3沸点依次降低的原因___________________ 。
(5)碳化硅的结构与金刚石类似(如图所示),其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有___________ 个,与碳原子等距离最近的碳原子有__________ 个。已知碳化硅晶胞边长为a pm,则碳化硅的密度为__________ g·cm3。

(1)第二周期中,元素的第一电离能处于B与N之间的元素有
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为
(3)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P=O存在下加热脱H2O得到。乙烯酮分子中碳原子杂化轨道类型是
(4)已知固态NH3、H2O、HF的氢键键能和结构如下:

解释H2O、HF、NH3沸点依次降低的原因
(5)碳化硅的结构与金刚石类似(如图所示),其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有

您最近一年使用:0次
【推荐1】能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.
(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,写出基态镍原子的外围电子排布式_____ ,它位于周期表____ 区.
(2)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途.富勒烯(C60)的结构如图,分子中碳原子轨道的杂化类型为________________ ;1mol C60分子中σ键的数目为____________ 个.

(3)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓(GaAs)、硫化镉(CdS)薄膜电池等.
①第一电离能:As____ Ga(填“>”、“<”或“=”).
②SeO2分子的空间构型为_____ .
(4)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在太阳能电池制造中得到广泛应用.它可在铜的催化作用下由F2和过量的NH3反应得到,该反应中NH3的沸点____ (填“>”、“<”或“=”)HF的沸点,NH4F固体属于____ 晶体.往硫酸铜溶液中加入过量氨水,可生成配离子.已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是______ .
(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,写出基态镍原子的外围电子排布式
(2)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途.富勒烯(C60)的结构如图,分子中碳原子轨道的杂化类型为

(3)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓(GaAs)、硫化镉(CdS)薄膜电池等.
①第一电离能:As
②SeO2分子的空间构型为
(4)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在太阳能电池制造中得到广泛应用.它可在铜的催化作用下由F2和过量的NH3反应得到,该反应中NH3的沸点
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】KZnF3被认为是良好的光学基质材料,可由K2CO3、ZnF2、NH4HF2制备。回答下列问题:
(1)基态F原子的外围电子轨道表示式_______ 。
(2)K2CO3中阴离子的空间结构为_______ 。
(3)NH4HF2的组成元素的电负性由大到小的顺序为_______ (用元素符号表示);其中N原子的杂化方式为_______ ;HF能形成分子缔合体(HF)n的原因为_______ 。
(4)ZnF2具有金红石型四方结构,KZnF3具有钙钛矿型立方结构,两种晶体的晶胞结构如图所示:

①ZnF2和KZnF3晶体(晶胞顶点为K+ )中,Zn的配位数之比为_______ 。
②若NA表示阿伏加德罗常数的值,则ZnF2晶体的密度为_______ g·cm-3(用含a、c、NA的代数式表示)。
(1)基态F原子的外围电子轨道表示式
(2)K2CO3中阴离子的空间结构为
(3)NH4HF2的组成元素的电负性由大到小的顺序为
(4)ZnF2具有金红石型四方结构,KZnF3具有钙钛矿型立方结构,两种晶体的晶胞结构如图所示:

①ZnF2和KZnF3晶体(晶胞顶点为K+ )中,Zn的配位数之比为
②若NA表示阿伏加德罗常数的值,则ZnF2晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铁在自然界中的含量丰富,而且在生活生产中应用广泛。
(1)铁在周期表中的位置为______ 。
(2)硝普试剂[Fe(NO)CN)5]2-可用于检验S2-,两者反应得紫色溶液,其中两个配体互为等电子体,已知硝普试剂[Fe(NO)(CN)5]2-中Fe为+2价,其基态离子的外围电子排布式为_______ 。
(3)K4[Fe(CN)6]溶液可用于检验Fe3+,K、C、N的第一电离能由大到小的顺序为______ ,K4[Fe(CN)6]内界中σ键与π键的个数比为______ 。
(4)二茂铁是由两个环戊二烯阴离子与Fe2+离子组成的三明治型化合物,即 。环戊二烯分子(
。环戊二烯分子(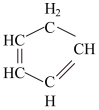 )中碳原子的杂化方式为
)中碳原子的杂化方式为_______ 。
(5)工业电解熔融的FeO、Fe2O3冶炼高纯铁。FeO与Fe2O3相比,_____ 熔点高,其主要原因是_______ 。
(6)铁单质晶体在不同温度下有两种主要的堆积方式——体心立方(A)与面心立方(B),假定Fe原子半径不变,在两种堆积中,配位数之比NA︰NB为_______ 晶体密度之比ρA︰ρB为_______ 。
(1)铁在周期表中的位置为
(2)硝普试剂[Fe(NO)CN)5]2-可用于检验S2-,两者反应得紫色溶液,其中两个配体互为等电子体,已知硝普试剂[Fe(NO)(CN)5]2-中Fe为+2价,其基态离子的外围电子排布式为
(3)K4[Fe(CN)6]溶液可用于检验Fe3+,K、C、N的第一电离能由大到小的顺序为
(4)二茂铁是由两个环戊二烯阴离子与Fe2+离子组成的三明治型化合物,即
 。环戊二烯分子(
。环戊二烯分子( )中碳原子的杂化方式为
)中碳原子的杂化方式为(5)工业电解熔融的FeO、Fe2O3冶炼高纯铁。FeO与Fe2O3相比,
(6)铁单质晶体在不同温度下有两种主要的堆积方式——体心立方(A)与面心立方(B),假定Fe原子半径不变,在两种堆积中,配位数之比NA︰NB为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】有研究团队通过光催化还原 ,将其合成一碳化合物(CO、HCOOH、
,将其合成一碳化合物(CO、HCOOH、 、
、 等)。常见的无机非贵金属光催化还原
等)。常见的无机非贵金属光催化还原 的催化剂有NiO、CuO、
的催化剂有NiO、CuO、 、
、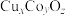 等。回答下列问题:
等。回答下列问题:
(1)CO可与金属镍形成四面体构型分子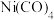 ,其中
,其中 的价电子排布式为
的价电子排布式为___________ 。该催化 还原的过程中可能产生
还原的过程中可能产生 ,该离子的VSEPR模型为
,该离子的VSEPR模型为___________ 。铁也可以与CO形成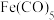 金属羰基化合物,
金属羰基化合物, 分子中含有
分子中含有___________  键。
键。
(2)镍能形成多种配合物,如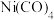 、
、 、
、 等,下列有关说法正确的是___________(填选项字母)。
等,下列有关说法正确的是___________(填选项字母)。
(3)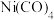 是无色液体,沸点42.1℃,熔点
是无色液体,沸点42.1℃,熔点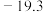 ℃,难溶于水,易溶于有机溶剂,那么固体
℃,难溶于水,易溶于有机溶剂,那么固体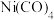 属于
属于___________ 晶体。金属Ni可以与Mg、C形成一种化合物M,M是一种新型超导体,它的临界温度为8K。已知M的晶胞结构如下图所示,则M的化学式为___________ 。

 ,将其合成一碳化合物(CO、HCOOH、
,将其合成一碳化合物(CO、HCOOH、 、
、 等)。常见的无机非贵金属光催化还原
等)。常见的无机非贵金属光催化还原 的催化剂有NiO、CuO、
的催化剂有NiO、CuO、 、
、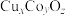 等。回答下列问题:
等。回答下列问题:(1)CO可与金属镍形成四面体构型分子
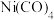 ,其中
,其中 的价电子排布式为
的价电子排布式为 还原的过程中可能产生
还原的过程中可能产生 ,该离子的VSEPR模型为
,该离子的VSEPR模型为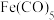 金属羰基化合物,
金属羰基化合物, 分子中含有
分子中含有 键。
键。(2)镍能形成多种配合物,如
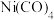 、
、 、
、 等,下列有关说法正确的是___________(填选项字母)。
等,下列有关说法正确的是___________(填选项字母)。A. 中含有共价键和离子键 中含有共价键和离子键 |
B.CO与 互为等电子体,其中CO分子内 互为等电子体,其中CO分子内 键和 键和 键的个数比为 键的个数比为 |
C. 中N原子为 中N原子为 杂化,其空间构型为正四面体形 杂化,其空间构型为正四面体形 |
D. 在形成配合物时其配位数只能为4,Fe在形成配合物时其配位数只能为6 在形成配合物时其配位数只能为4,Fe在形成配合物时其配位数只能为6 |
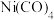 是无色液体,沸点42.1℃,熔点
是无色液体,沸点42.1℃,熔点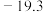 ℃,难溶于水,易溶于有机溶剂,那么固体
℃,难溶于水,易溶于有机溶剂,那么固体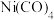 属于
属于
您最近一年使用:0次
【推荐2】东晋《华阳国志•南中志》记载云南镍白铜(铜镍合金),曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子3d能级上的未成对电子数为_____ 。单质铜及镍都是由_____ 键形成的晶体。
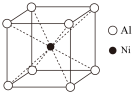
(2)一种铝镍合金的结构如图,与其结构相似的化合物是_____ (填字母)。
(3)雷尼镍(Raney-Ni)是一种历史悠久、应用广泛的催化剂,它催化的一实例为
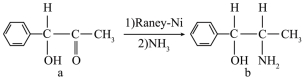
化合物a中所含元素电负性由大到小排序为_____ (填元素符号,下同),化合物b中进行sp3杂化的原子有_____ 。
(4)实验室检验Ni2+可用丁二酮肟(甲)与之作用生成红色配合物沉淀(乙)。反应原理如图:
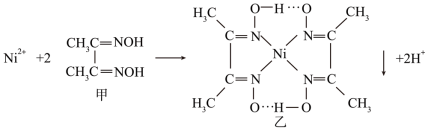
①甲中σ键与π键的个数之比是_____ ,乙中提供空轨道的是_____ (填微粒符号)。
②乙中的化学键类型有_____ (填字母)。
A.极性键 B.π键 C.氢键 D.配位键
(1)镍元素基态原子3d能级上的未成对电子数为
(2)一种铝镍合金的结构如图,与其结构相似的化合物是

| A.氯化钠 | B.氯化铯 | C.石英 | D.金刚石 |

化合物a中所含元素电负性由大到小排序为
(4)实验室检验Ni2+可用丁二酮肟(甲)与之作用生成红色配合物沉淀(乙)。反应原理如图:

①甲中σ键与π键的个数之比是
②乙中的化学键类型有
A.极性键 B.π键 C.氢键 D.配位键
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】乙酸俗称醋酸,是一种重要的化工原料。
(1)1968年,Monsanto以[Rh(CO)2I2]-为催化剂、以碘甲烷为助催化剂合成乙酸,反应历程如下图所示:_____ 。
②已知B为六配位离子,画出B的结构示意图_____ 。
③根据反应④,写出E生成CH3COOH的化学方程式_____ 。
(2)乙酸在催化剂的作用下和氢气反应可生成乙醇,反应体系主要发生如下反应:
Ⅰ.CH3COOH(g)+2H2(g) C2H5OH(g)+H2O(g) ΔH1=-44.2kJ·mol-1
C2H5OH(g)+H2O(g) ΔH1=-44.2kJ·mol-1
Ⅱ.CH3COOH(g)+C2H5OH(g) CH3COOC2H5(g)+H2O(g) ΔH2=-18.4kJ·mol-1
CH3COOC2H5(g)+H2O(g) ΔH2=-18.4kJ·mol-1
Ⅲ.CH3COOH(g)+H2(g) CH3CHO(g)+H2O(g) ΔH3=+24.5kJ·mol-1
CH3CHO(g)+H2O(g) ΔH3=+24.5kJ·mol-1
在200kPa反应条件下,将n(H2)∶n(CH3COOH)=10∶1的混合气进行上述反应。平衡时乙酸的转化率、产物的选择性S随温度变化如下图所示。
已知: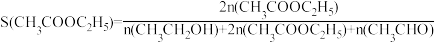
①CH3CHO(g)+H2(g) C2H5OH(g)的ΔH=
C2H5OH(g)的ΔH=_____ kJ·mol-1。
②图中表示乙酸的转化率随温度变化的曲线是_____ 。当温度低于340℃时,随着温度的升高,CH3COOC2H5选择性变大的原因是_____ 。_____ (任写一条)。
④恒温恒压条件下,向初始体积为1L的体积可变密闭容器中通入2molH2和1molCH3COOH,发生上述反应,达到平衡时容器的体积变为0.8L,S(CH3COOC2H5)=S(CH3CHO),n(H2)=0.7mol。反应Ⅱ的平衡常数K=_____ (保留2位小数)。
(1)1968年,Monsanto以[Rh(CO)2I2]-为催化剂、以碘甲烷为助催化剂合成乙酸,反应历程如下图所示:

②已知B为六配位离子,画出B的结构示意图
③根据反应④,写出E生成CH3COOH的化学方程式
(2)乙酸在催化剂的作用下和氢气反应可生成乙醇,反应体系主要发生如下反应:
Ⅰ.CH3COOH(g)+2H2(g)
 C2H5OH(g)+H2O(g) ΔH1=-44.2kJ·mol-1
C2H5OH(g)+H2O(g) ΔH1=-44.2kJ·mol-1Ⅱ.CH3COOH(g)+C2H5OH(g)
 CH3COOC2H5(g)+H2O(g) ΔH2=-18.4kJ·mol-1
CH3COOC2H5(g)+H2O(g) ΔH2=-18.4kJ·mol-1Ⅲ.CH3COOH(g)+H2(g)
 CH3CHO(g)+H2O(g) ΔH3=+24.5kJ·mol-1
CH3CHO(g)+H2O(g) ΔH3=+24.5kJ·mol-1在200kPa反应条件下,将n(H2)∶n(CH3COOH)=10∶1的混合气进行上述反应。平衡时乙酸的转化率、产物的选择性S随温度变化如下图所示。
已知:
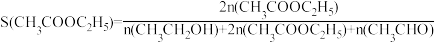
①CH3CHO(g)+H2(g)
 C2H5OH(g)的ΔH=
C2H5OH(g)的ΔH=②图中表示乙酸的转化率随温度变化的曲线是

④恒温恒压条件下,向初始体积为1L的体积可变密闭容器中通入2molH2和1molCH3COOH,发生上述反应,达到平衡时容器的体积变为0.8L,S(CH3COOC2H5)=S(CH3CHO),n(H2)=0.7mol。反应Ⅱ的平衡常数K=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】CuO在化学链(如气相烃类)燃烧和催化CO氧化过程中均展现出良好的性能,同时具有成本低廉的优势,有望成为贵金属催化剂的替代品。中国科学院工程热物理研究所的科研人员初步揭示了CO在CuO表面的催化机理,并深入研究了CO在铜基氧化物表面的反应机制,并提出了对应的反应动力学模型。
(1)基态铜原子的价电子排布式为_______ ,其核外电子的空间运动状态有_______ 种。
(2)N与C、O同周期,H、C、N三种元素的电负性从小到大的顺序为_______ ;C、N、O 的第一电离能从大到小的顺序为_______ 。
(3)NH3具有还原性,能被CuO氧化,NH3分子中N原子的杂化方式为_______ ,NH3的沸点高于PH3的原因是_______ 。
(4)已知Cu2O的熔点高于Cu2S的熔点,其原因是_______ 。
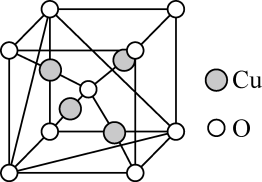
(5)铜的某种氧化物的晶胞结构如图所示,若该晶胞中Cu原子与O原子之间的最近距离为apm,设阿伏加德罗常数的值为NA,则该晶胞的密度为_______ g· cm-3(填含a、NA的代数式)。
(1)基态铜原子的价电子排布式为
(2)N与C、O同周期,H、C、N三种元素的电负性从小到大的顺序为
(3)NH3具有还原性,能被CuO氧化,NH3分子中N原子的杂化方式为
(4)已知Cu2O的熔点高于Cu2S的熔点,其原因是
(5)铜的某种氧化物的晶胞结构如图所示,若该晶胞中Cu原子与O原子之间的最近距离为apm,设阿伏加德罗常数的值为NA,则该晶胞的密度为

您最近一年使用:0次
【推荐2】W、X、Y、Z为短周期主族元素,原子序数依次增大。W、X、Y、Z的价电子数之和为10,Z的最外层电子数为其K层的一半,W与Y可形成个数比为2:1的18e-分子。
(1)下列有关叙述正确的是_______ 。
a.ZXW4中含有离子键、配位键和共价键
b.Y的最高化合价氧化物的水化物为弱酸
c.X的氟化物XF3中原子均为8电子稳定结构
(2)①基态Z原子的电子排布式为_______ 。
②基态Z原子电子占据最高能级的电子云为_______ 形。
(3)①W、X、Y中,原子半径最大的是_______ 。(填元素符号,下同)。
②根据对角线规则,X的一些化学性质与元素_______ 的相似。
③在XF3分子中F-X-F的键角是_______ 。
④XF3和过量NaF作用可生成NaXF4, 的立体构型为
的立体构型为_______ 。
⑤路易斯酸碱理论认为,任何可接受电子对的分子或离子叫做路易斯酸,任何可给出电子对的分子或离子叫做路易斯碱。从结构角度分析XF3是路易斯酸的原因:_______ 。
(4)YH3XH3分子中,①Y-X化学键称为_______ 键。
②YH3XH3中X原子的杂化轨道类型为_______ 。
③从原子结构角度解释Y的非金属性强于X的原因:_______ 。
(5)YH3XH3分子中,与Y原子相连的H呈正电性(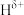 ),与X原子相连的H呈负电性(
),与X原子相连的H呈负电性(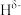 )。
)。
①与YH3XH3原子总数相等的等电子体是_______ (写分子式)。
②该等电子的熔点比YH3XH3的低,其原因是_______ ,也称为二氢键。
(6)研究发现,YH3XH3在低温高条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm, ,YH3XH3的2×2×2超晶胞结构如图所示。
,YH3XH3的2×2×2超晶胞结构如图所示。

YH3XH3晶体的密度ρ=_______ g/cm3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)下列有关叙述正确的是
a.ZXW4中含有离子键、配位键和共价键
b.Y的最高化合价氧化物的水化物为弱酸
c.X的氟化物XF3中原子均为8电子稳定结构
(2)①基态Z原子的电子排布式为
②基态Z原子电子占据最高能级的电子云为
(3)①W、X、Y中,原子半径最大的是
②根据对角线规则,X的一些化学性质与元素
③在XF3分子中F-X-F的键角是
④XF3和过量NaF作用可生成NaXF4,
 的立体构型为
的立体构型为⑤路易斯酸碱理论认为,任何可接受电子对的分子或离子叫做路易斯酸,任何可给出电子对的分子或离子叫做路易斯碱。从结构角度分析XF3是路易斯酸的原因:
(4)YH3XH3分子中,①Y-X化学键称为
②YH3XH3中X原子的杂化轨道类型为
③从原子结构角度解释Y的非金属性强于X的原因:
(5)YH3XH3分子中,与Y原子相连的H呈正电性(
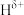 ),与X原子相连的H呈负电性(
),与X原子相连的H呈负电性(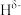 )。
)。①与YH3XH3原子总数相等的等电子体是
②该等电子的熔点比YH3XH3的低,其原因是
(6)研究发现,YH3XH3在低温高条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm,
 ,YH3XH3的2×2×2超晶胞结构如图所示。
,YH3XH3的2×2×2超晶胞结构如图所示。
YH3XH3晶体的密度ρ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铬(Cr)是人体必须的微量元素。
(1)Cr的基态原子价电子排布式为___________
(2)已知:K2Cr2O7+4H2O2+H2SO4=2CrO5(蓝色)+5H2O+K2SO4,该反应可用于检验H2O2,且该反应也是典型的过氧键转移的反应,化合价未发生变化。则1molCrO5中存在___________ mol过氧键。H2O2中的氧采用___________ 杂化,H2O2属于___________ 分子(填“极性”或“非极性”)
(3)一定条件下,CrCl3溶于水可得到紫色溶液,经检测溶液中存在配离子[Cr(H2O)6]3+(结构如图甲)。向溶液中加入NH3●H2O和NH4Cl混合物,[Cr(H2O)6]3+中的H2O逐渐被NH3取代,分别形成[Cr(NH3)2(H2O)4]3+、[Cr(NH3)3(H2O)3]3+等,NH3可代替H2O的原因是___________ ,其中[Cr(NH3)4(H2O)2]3+有___________ 种空间结构。NH3参与形成[Cr(NH3)6]3+后,如图乙,键角大小关系为
___________ β(填“>”、“=”或“<”)

(4)某种Cr、Fe合金如图丙形式堆积,其中,A层为Cr层,B、C层均为Fe层,这种堆积形式称为___________ ;金属Fe存在体心立方堆积的晶型(如图丁),其空间利用率为___________ (用含π的代数式表示)。

(1)Cr的基态原子价电子排布式为
(2)已知:K2Cr2O7+4H2O2+H2SO4=2CrO5(蓝色)+5H2O+K2SO4,该反应可用于检验H2O2,且该反应也是典型的过氧键转移的反应,化合价未发生变化。则1molCrO5中存在
(3)一定条件下,CrCl3溶于水可得到紫色溶液,经检测溶液中存在配离子[Cr(H2O)6]3+(结构如图甲)。向溶液中加入NH3●H2O和NH4Cl混合物,[Cr(H2O)6]3+中的H2O逐渐被NH3取代,分别形成[Cr(NH3)2(H2O)4]3+、[Cr(NH3)3(H2O)3]3+等,NH3可代替H2O的原因是


(4)某种Cr、Fe合金如图丙形式堆积,其中,A层为Cr层,B、C层均为Fe层,这种堆积形式称为

您最近一年使用:0次



