氮(N)、磷(P)、砷(As)等ⅤA元素化合物在研究和生产中有重要用途。如我国科研人员研究发现As2O3或写成As4O6,俗称砒霜)对白血病有明显的治疗作用。回答下列问题:
(1)As原子的简化的核外电子排布式为_____ ;P的第一电离能比S大的原因为________ 。
(2)写出一种与CN-互为等电子体的分子___ (用化学式表示);(SCN)2分子中σ键和π键个数比为__ 。
(3)砒霜剧毒,可用石灰消毒生成AsO33-少量AsO43-,其中AsO33-中As的杂化方式为___ ,AsO43-的空间构型为___ 。
(4)NH4+中H-N-H键角比NH3中H-N-H的键角大的原因是____ ;NH3和水分子与铜离子形成的化合物中阳离子呈轴向狭长的八面体结构(如图Ⅰ),该化合物加热时首先失去水,请从原子结构角度加以分析:____ 。
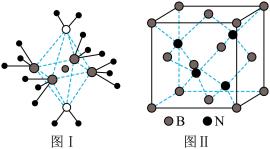
(5)BN的熔点为3000℃,密度为2.25g/cm3,其晶胞结构如上图Ⅱ所示,晶体中一个B原子周围距离最近的N原子有____ 个;若原子半径分别为rN和rB,阿伏伽德罗常数值为NA,则BN晶胞中原子的体积占晶胞体积的百分率为_____ 。
(1)As原子的简化的核外电子排布式为
(2)写出一种与CN-互为等电子体的分子
(3)砒霜剧毒,可用石灰消毒生成AsO33-少量AsO43-,其中AsO33-中As的杂化方式为
(4)NH4+中H-N-H键角比NH3中H-N-H的键角大的原因是

(5)BN的熔点为3000℃,密度为2.25g/cm3,其晶胞结构如上图Ⅱ所示,晶体中一个B原子周围距离最近的N原子有
更新时间:2019-04-21 12:23:20
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】现有七种元素,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息回答问题:
(1)B的元素符号为___________ ,基态原子价电子轨道表示式为___________ 。
(2)基态D原子中能量最高的电子所在的原子轨道的电子云在空间有___________ 个伸展方向,原子轨道呈___________ 形。
(3)某同学根据上述信息,推断C基态原子的核外电子轨道表示式为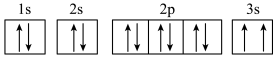 ,该同学所写的轨道表示式违反了
,该同学所写的轨道表示式违反了___________ 。
(4)E元素原子核外有___________ 种运动状态不同的电子。
(5)检验F元素的方法是___________ 。
| A | 元素原子半径在周期表中最小,也是宇宙中最丰富的元素 |
| B | 元素原子的核外p轨道总电子数比s轨道总电子数少1 |
| C | 元素的第一至第四电离能分别是I1=738 kJ·mol-1、I2=1 451 kJ·mol-1、I3=7 733 kJ·mol-1、I4=10 540 kJ·mol-1 |
| D | 原子核外所有p轨道全满或半满 |
| E | 元素的主族序数与周期序数的差为4,原子半径在同周期中最小 |
| F | 是前四周期中电负性最小的元素 |
(1)B的元素符号为
(2)基态D原子中能量最高的电子所在的原子轨道的电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子轨道表示式为
 ,该同学所写的轨道表示式违反了
,该同学所写的轨道表示式违反了(4)E元素原子核外有
(5)检验F元素的方法是
您最近一年使用:0次
【推荐2】根据有关知识,回答下列问题。
(1)符号 所代表的含义是_______(填字母)。
所代表的含义是_______(填字母)。
(2)铝原子核外电子云有_______ 种不同的伸展方向,有_______ 种不同运动状态的电子。
(3)短周期的化学元素(0族和放射性元素除外)中,第一电离能最小的元素是_______ (填元素符号,下同),电负性最大的元素是_______ 。
(4)Be的第一电离能大于B的第一电离能,这是因为_______ 。
(5)短周期元素中符合“对角线规则”的元素有Be和Al、B和Si,它们的性质分别有一定的相似性,写出 与NaOH溶液反应的离子方程式:
与NaOH溶液反应的离子方程式:_______ 。
(6)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
锰元素位于第四周期第ⅦB族。请写出基态 的价层电子排布式:
的价层电子排布式:_______ ,比较两元素的 、
、 ,可知,气态
,可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是_______ 。
(1)符号
 所代表的含义是_______(填字母)。
所代表的含义是_______(填字母)。A. 轨道上有3个电子 轨道上有3个电子 |
B.第3个电子层 轨道有三个伸展方向 轨道有三个伸展方向 |
C.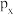 电子云有3个伸展方向 电子云有3个伸展方向 |
| D.第3个电子层沿x轴方向伸展的p轨道 |
(3)短周期的化学元素(0族和放射性元素除外)中,第一电离能最小的元素是
(4)Be的第一电离能大于B的第一电离能,这是因为
(5)短周期元素中符合“对角线规则”的元素有Be和Al、B和Si,它们的性质分别有一定的相似性,写出
 与NaOH溶液反应的离子方程式:
与NaOH溶液反应的离子方程式:(6)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
| 元素 | Mn | Fe | |
电离能/ |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
锰元素位于第四周期第ⅦB族。请写出基态
 的价层电子排布式:
的价层电子排布式: 、
、 ,可知,气态
,可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】自然界中存在大量的元素,如钠、镁、铝、铁、铜、砷、锌、镍等在生活中有着广泛的应用。
(1)请写出Fe的基态原子核外电子排布式_________ ,砷属于________ 区元素。
(2)金属A的原子只有3个电子层,其第一至第四电离能如下:
则A原子的价电子排布式为______ 。
(3)锌化铜是一种金属互化物,其化学式有多种形式,如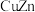 ,
,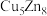 ,
,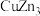 等。其中所含元素铜的第二电离能
等。其中所含元素铜的第二电离能________ (填“大于”“小于”或“等于”)锌的第二电离能。
(4)用锌还原 的盐酸溶液,经后续处理可制得绿色的晶体
的盐酸溶液,经后续处理可制得绿色的晶体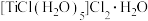 。该晶体所含元素中,电负性最大的元素是
。该晶体所含元素中,电负性最大的元素是________ ,与Ti形成配位键的配体是_____ 和________ , 该配合物中含有σ键的数目为
该配合物中含有σ键的数目为________ 。
(5) 能形成多种配离子,如
能形成多种配离子,如 ,
, 等。
等。 的空间构型为:
的空间构型为:________ ;与 互为等电子体的分子有:
互为等电子体的分子有:_______ (填分子式)。
(1)请写出Fe的基态原子核外电子排布式
(2)金属A的原子只有3个电子层,其第一至第四电离能如下:
电离能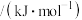 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
(3)锌化铜是一种金属互化物,其化学式有多种形式,如
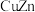 ,
,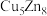 ,
,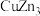 等。其中所含元素铜的第二电离能
等。其中所含元素铜的第二电离能(4)用锌还原
 的盐酸溶液,经后续处理可制得绿色的晶体
的盐酸溶液,经后续处理可制得绿色的晶体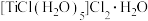 。该晶体所含元素中,电负性最大的元素是
。该晶体所含元素中,电负性最大的元素是 该配合物中含有σ键的数目为
该配合物中含有σ键的数目为(5)
 能形成多种配离子,如
能形成多种配离子,如 ,
, 等。
等。 的空间构型为:
的空间构型为: 互为等电子体的分子有:
互为等电子体的分子有:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】Ⅰ.碳族元素的单质和化合物在化工、医药、材料等领域有着广泛的应用。
(1)锗是优良的半导体材料,基态Ge原子中,最高能级电子云轮廓图的名称为____ 。Ge与C同族,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键,从原子结构角度分析,原因是____ 。
(2)碳可形成CO、CO2、H2CO3等多种无机化合物。
①在反应CO转化成CO2的过程中,下列说法正确的是____ 。
A.每个分子中孤对电子数增多 B.分子的极性不变
C.原子间成键方式未改变 D.分子的熔沸点变小
②干冰和冰是两种常见的分子晶体,晶体中的空间利用率:干冰____ 冰(填“>”、“<”或“=”);CO2与SiO2是否互为等电子体____ (填“是”或“否”)。
③X是碳的一种氧化物,X的五聚合体结构如图1所示。X分子中每个原子都满足最外层8电子结构,X分子的电子式为____ 。
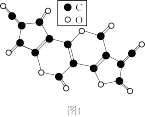
(3)C60分子是由许多正五边形构成的空心笼状结构如图2所示,分子中每个碳原子只跟相邻的3个碳原子形成化学键。则C60分子中含___ 个σ键。

(4)Ⅱ.某种Ga2O3的晶体结构如图3所示,O2-以六方最密方式堆积,Ga3+在其八面体空隙中(注:未全部标出,如:Ga3+在1、2、3、4、5、6构成的八面体体心)。

①该晶胞中O2-的配位数为____ 。
②该晶胞有_____ %(保留一位小数)八面体空隙填充阳离子。
③已知氧离子半径为rcm,晶胞的高为hcm,NA代表阿伏加德罗常数的值,该晶体的密度为____ g·cm-3(用含a、b和NA的代数式表示)。
(1)锗是优良的半导体材料,基态Ge原子中,最高能级电子云轮廓图的名称为
(2)碳可形成CO、CO2、H2CO3等多种无机化合物。
①在反应CO转化成CO2的过程中,下列说法正确的是
A.每个分子中孤对电子数增多 B.分子的极性不变
C.原子间成键方式未改变 D.分子的熔沸点变小
②干冰和冰是两种常见的分子晶体,晶体中的空间利用率:干冰
③X是碳的一种氧化物,X的五聚合体结构如图1所示。X分子中每个原子都满足最外层8电子结构,X分子的电子式为

(3)C60分子是由许多正五边形构成的空心笼状结构如图2所示,分子中每个碳原子只跟相邻的3个碳原子形成化学键。则C60分子中含

(4)Ⅱ.某种Ga2O3的晶体结构如图3所示,O2-以六方最密方式堆积,Ga3+在其八面体空隙中(注:未全部标出,如:Ga3+在1、2、3、4、5、6构成的八面体体心)。

①该晶胞中O2-的配位数为
②该晶胞有
③已知氧离子半径为rcm,晶胞的高为hcm,NA代表阿伏加德罗常数的值,该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】中国海军航母建设正在有计划、有步骤地向前推进,建造航母需要大量的新型材料。航母的龙骨要耐冲击,航母的甲板要耐高温,航母的外壳要耐腐蚀。
(1)镍铬钢抗腐蚀性能强,Ni2+的核外电子排布式为_______ ,铬元素位于周期表中_______ 区。
(2)航母甲板涂有一层耐高温的材料——聚硅氧烷(结构如图所示),其中C原子的杂化方式为_______ 杂化。

(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①根据下表数据判断,最有可能生成较稳定的单核阳离子的卤素原子是_______ (填元素符号)。
②根据价层电子对互斥理论,预测ClO 的空间构型为
的空间构型为_______ 形;写出一个ClO 的等电子体的化学符号:
的等电子体的化学符号:_______ 。
(4)乙二胺(H2NCH2CH2NH2)是一种有机化合物,分子中氮、碳的杂化类型分别是_______ 、_______ 。乙二胺能与Mg2+、Cu2+等金属离子形成稳定环状离子,其原因是_______ ,其中与乙二胺形成的化合物稳定性相对较高的是_______ (填“Mg2+”或“Cu2+”)。
(1)镍铬钢抗腐蚀性能强,Ni2+的核外电子排布式为
(2)航母甲板涂有一层耐高温的材料——聚硅氧烷(结构如图所示),其中C原子的杂化方式为

(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①根据下表数据判断,最有可能生成较稳定的单核阳离子的卤素原子是
| 卤素原子 | 氟 | 氯 | 溴 | 碘 |
| 第一电离能/(kJ/mol) | 1 681 | 1 251 | 1 140 | 1 008 |
 的空间构型为
的空间构型为 的等电子体的化学符号:
的等电子体的化学符号:(4)乙二胺(H2NCH2CH2NH2)是一种有机化合物,分子中氮、碳的杂化类型分别是
您最近一年使用:0次
【推荐3】原子序数依次递增且都小于36的A、B、C、D、E五种元素,其中A的一种核素中没有中子,B原子基态时最外层电子数是其内层电子数的2倍,D原子基态时2p原子轨道上有2个未成对的电子,E元素的原子结构中3d能级上未成对电子数是成对电子数的2倍.回答下列问题:

(1)B2A4分子中B原子轨道的杂化类型为________ ,B2A4分子中σ键和π键个数比为________
(2)A、B、C、D四种元素的电负性从大到小的顺序为________ (用元素符号表示);化合物CA3的沸点比化合物BA4的高,其主要原因是________
(3)元素B的一种氧化物与元素C的一种氧化物互为等电子体,元素C的这种氧化物的分子式是________
(4)元素E能形成多种配合物,如:E(CO)5等.
①基态E原子的价电子排布式为________ .
②E(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断E(CO)5晶体属于________ (填晶体类型),该晶体中E的化合价为________

(1)B2A4分子中B原子轨道的杂化类型为
(2)A、B、C、D四种元素的电负性从大到小的顺序为
(3)元素B的一种氧化物与元素C的一种氧化物互为等电子体,元素C的这种氧化物的分子式是
(4)元素E能形成多种配合物,如:E(CO)5等.
①基态E原子的价电子排布式为
②E(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断E(CO)5晶体属于
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】我国正在建造第四艘航空母舰,镍铬钢抗腐蚀性能强,可用于建造航母。
(1)航母甲板镍铬钢表面涂有一层耐高温的材料聚硅氧烷,基态 原子的价电子排布式为
原子的价电子排布式为____________ ,基态 原子电子占据最高能级的电子云轮廓图为
原子电子占据最高能级的电子云轮廓图为____________ 形,元素C、O、F的电负性由大到小的顺序为____________ 。
(2)海洋是航母的摇篮,也是元素的摇篮,海水中含有大量F、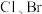 、I元素。
、I元素。
① 的空间构型为
的空间构型为____________ ,其中O原子杂化方式为____________ 杂化。
②海水综合利用中用 水溶液吸收
水溶液吸收 ,吸收率可达95%,有关反应的离子方程式为
,吸收率可达95%,有关反应的离子方程式为____________ ,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是____________ 。
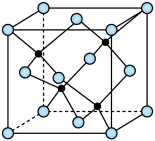
(3)海底金属软泥是在海洋底覆盖着的一层红棕色沉积物,蕴藏着大量的资源,含有硅、氧化铁、锰、锌等。 与
与 形成的一种晶胞结构如下图所示(黑球表示
形成的一种晶胞结构如下图所示(黑球表示 ,白球表示
,白球表示 ),
), 的配位数为
的配位数为____________ 。晶胞边长为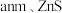 相对分子质量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为
相对分子质量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为____________  。
。
(1)航母甲板镍铬钢表面涂有一层耐高温的材料聚硅氧烷,基态
 原子的价电子排布式为
原子的价电子排布式为 原子电子占据最高能级的电子云轮廓图为
原子电子占据最高能级的电子云轮廓图为(2)海洋是航母的摇篮,也是元素的摇篮,海水中含有大量F、
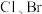 、I元素。
、I元素。①
 的空间构型为
的空间构型为②海水综合利用中用
 水溶液吸收
水溶液吸收 ,吸收率可达95%,有关反应的离子方程式为
,吸收率可达95%,有关反应的离子方程式为(3)海底金属软泥是在海洋底覆盖着的一层红棕色沉积物,蕴藏着大量的资源,含有硅、氧化铁、锰、锌等。
 与
与 形成的一种晶胞结构如下图所示(黑球表示
形成的一种晶胞结构如下图所示(黑球表示 ,白球表示
,白球表示 ),
), 的配位数为
的配位数为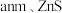 相对分子质量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为
相对分子质量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。
(1)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。
①Mn2+基态的电子排布式可表示为_______ 。
②NO 的空间构型是
的空间构型是_______ (用文字描述)。
(2)Cu+在酸性溶液中不稳定,可发生歧化反应生成Cu2+和Cu。但CuO在高温下会分解成Cu2O,试从结构角度解释高温下CuO为何会生成 Cu2O:_______ 。
(3)在铜锰氧化物的催化下,CO被氧化为CO2,HCHO被氧化为CO2和H2O。
①HCHO的中心原子的杂化方式为_______ 。
②1 mol CO2中含有的σ键数目为_______ 。
(4)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为_______ 。
(1)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。
①Mn2+基态的电子排布式可表示为
②NO
 的空间构型是
的空间构型是(2)Cu+在酸性溶液中不稳定,可发生歧化反应生成Cu2+和Cu。但CuO在高温下会分解成Cu2O,试从结构角度解释高温下CuO为何会生成 Cu2O:
(3)在铜锰氧化物的催化下,CO被氧化为CO2,HCHO被氧化为CO2和H2O。
①HCHO的中心原子的杂化方式为
②1 mol CO2中含有的σ键数目为
(4)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为
您最近一年使用:0次
【推荐3】现有a,b、c、d、e五种前四周期的元素,它们的原子序数依次增大,请根据下列相关信息,回答问题:
(1)元素a的名称是_______ ,c在元素周期表中的位置是_______ ,a2c的空间构型为_______ 。
(2)d元素基态原子中最高能层符号是_______ ,核外电子的空间运动状态有_______ 种。
(3)e元素处于周期表的_______ 区,价层电子的轨道表达式为_______ 。
(4)元素a,b、d的电负性由大到小的顺序是_______ (用元素符号表示,下同);元素c,d、e的第一电离能由大到小的顺序是_______ 。
(5)元素b、c、d的最高价氧化物的水化物酸性由强到弱的顺序是_______ (用化学式表示)。
| a | 基态原子的核外电子数等于电子层数 |
| b | 基态原子的核外s电子是p电子的2倍 |
| c | 最高正价与最低负价的代数和为4 |
| d | 基态原子的价层电子排布式为:(n+1)sn(n+1)pn+3 |
| e | 基态原子中未成对电子数是本周期中最多的元素 |
(2)d元素基态原子中最高能层符号是
(3)e元素处于周期表的
(4)元素a,b、d的电负性由大到小的顺序是
(5)元素b、c、d的最高价氧化物的水化物酸性由强到弱的顺序是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】金属、非金属及其化合物在科学研究和工业生产中具有重要的用途。
(1)FeCl3溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示:

①此配合物中,Fe3+ 的M层电子排布式为_________ ;
②此配离子中配体为C6H10O3,则该配离子的化学式为_________ ,配位数为_______ 。
(2)杂化轨道理论认为六配位的正八面体构型是由中心原子提供2个d轨道、1个s轨道和3个p轨道形成的杂化轨道,根据中心原子提供的d轨道是内层的还是外层的分为内轨型和外轨型。Fe(CN) 属于内轨型配离子,中心离子采取d2sp3杂化;SF6属于外轨型化合物,推测S原子采取
属于内轨型配离子,中心离子采取d2sp3杂化;SF6属于外轨型化合物,推测S原子采取_________ 杂化。
(3)科学家合成了一种阳离子为“N ”,其结构是对称的。5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N
”,其结构是对称的。5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N ”化学式为“N8”的离子晶体,写出“N
”化学式为“N8”的离子晶体,写出“N ”结构式
”结构式__________ ,写出一种与阴离子互为等电子体的分子的化学式:_________ 。
(4)N4H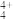 易被植物吸收,但它遇到碱时会生成类似白磷的N4分子,不能被吸收。1个N4H
易被植物吸收,但它遇到碱时会生成类似白磷的N4分子,不能被吸收。1个N4H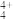 中含有
中含有______ 个σ键。
(5)某种磁性氮化铁的晶胞结构如图所示,该化合物的化学式为______ 。若晶胞底边长为a nm,高为c nm,则这种磁性氮化铁的晶体密度为 ___________ g/㎝3(用含a、c和NA的式子表示)。

(1)FeCl3溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示:

①此配合物中,Fe3+ 的M层电子排布式为
②此配离子中配体为C6H10O3,则该配离子的化学式为
(2)杂化轨道理论认为六配位的正八面体构型是由中心原子提供2个d轨道、1个s轨道和3个p轨道形成的杂化轨道,根据中心原子提供的d轨道是内层的还是外层的分为内轨型和外轨型。Fe(CN)
 属于内轨型配离子,中心离子采取d2sp3杂化;SF6属于外轨型化合物,推测S原子采取
属于内轨型配离子,中心离子采取d2sp3杂化;SF6属于外轨型化合物,推测S原子采取(3)科学家合成了一种阳离子为“N
 ”,其结构是对称的。5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N
”,其结构是对称的。5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N ”化学式为“N8”的离子晶体,写出“N
”化学式为“N8”的离子晶体,写出“N ”结构式
”结构式(4)N4H
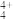 易被植物吸收,但它遇到碱时会生成类似白磷的N4分子,不能被吸收。1个N4H
易被植物吸收,但它遇到碱时会生成类似白磷的N4分子,不能被吸收。1个N4H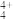 中含有
中含有(5)某种磁性氮化铁的晶胞结构如图所示,该化合物的化学式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】黄丹粉可外用拔毒生肌、杀虫止痒等。以铅膏(主要成分 、
、 、PbO、Pb,还有少量
、PbO、Pb,还有少量 等)为原料制备黄丹粉的流程如下:
等)为原料制备黄丹粉的流程如下:
回答下列问题:
(1)“脱硫”中,为了提高反应速率宜采用的措施有_______ (填两条)。
(2)已知平衡常数大于10⁵的反应为不可逆反应(完全反应)。通过计算说明 能完全转化为
能完全转化为 的原因:
的原因:____ ; 开始转化
开始转化 的条件是
的条件是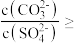
_______ 。
(3)已知: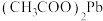 易溶于水、难电离。“酸浸”中,如果用浓盐酸替代醋酸,会产生有毒气体,写出生成该气体时发生反应的离子方程式:
易溶于水、难电离。“酸浸”中,如果用浓盐酸替代醋酸,会产生有毒气体,写出生成该气体时发生反应的离子方程式:___ (不考虑 转化为
转化为 )。
)。
(4)若“还原”时用木炭替代 ,其主要缺点是
,其主要缺点是_______ 。
(5)已知:“还原”步骤中测得如下数据:(甲)PbO起始质量为x g;(乙)消耗 总体积为V L(折合标准状况)(假设上述反应完全)。选择上述数据,计算理论上所得铅粉的质量
总体积为V L(折合标准状况)(假设上述反应完全)。选择上述数据,计算理论上所得铅粉的质量
_______ g。
(6)铅晶胞结构如图所示。已知 为阿伏加德罗常数的值,铅晶体密度为ρ g⋅cm
为阿伏加德罗常数的值,铅晶体密度为ρ g⋅cm ,则铅原子半径为
,则铅原子半径为_______ nm。
 、
、 、PbO、Pb,还有少量
、PbO、Pb,还有少量 等)为原料制备黄丹粉的流程如下:
等)为原料制备黄丹粉的流程如下: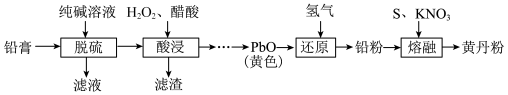
| 难溶电解质 |  |  |  |  |  |
 | 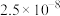 | 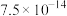 | 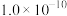 |  |  |
(1)“脱硫”中,为了提高反应速率宜采用的措施有
(2)已知平衡常数大于10⁵的反应为不可逆反应(完全反应)。通过计算说明
 能完全转化为
能完全转化为 的原因:
的原因: 开始转化
开始转化 的条件是
的条件是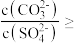
(3)已知:
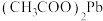 易溶于水、难电离。“酸浸”中,如果用浓盐酸替代醋酸,会产生有毒气体,写出生成该气体时发生反应的离子方程式:
易溶于水、难电离。“酸浸”中,如果用浓盐酸替代醋酸,会产生有毒气体,写出生成该气体时发生反应的离子方程式: 转化为
转化为 )。
)。(4)若“还原”时用木炭替代
 ,其主要缺点是
,其主要缺点是(5)已知:“还原”步骤中测得如下数据:(甲)PbO起始质量为x g;(乙)消耗
 总体积为V L(折合标准状况)(假设上述反应完全)。选择上述数据,计算理论上所得铅粉的质量
总体积为V L(折合标准状况)(假设上述反应完全)。选择上述数据,计算理论上所得铅粉的质量
(6)铅晶胞结构如图所示。已知
 为阿伏加德罗常数的值,铅晶体密度为ρ g⋅cm
为阿伏加德罗常数的值,铅晶体密度为ρ g⋅cm ,则铅原子半径为
,则铅原子半径为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】铬单质熔点高、硬度大,在新材料、医药、有机合成等多个领域有重要作用。以铬精矿(含 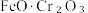 和少量
和少量 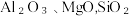 )冶炼 Cr的工艺流程如下:
)冶炼 Cr的工艺流程如下: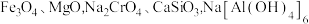
回答下列问题:
(1)“焙烧”之前常将原料混合后球磨,其目的为_______ ;“焙烧”过程中____ (填“有”或“无”)氧气参加反应。
(2)从浸渣中分离出Fe3O4的简单方法为________ 。
(3)“中和”和“酸化”两步工序不能合并的原因为_______ ;“结晶”所得母液中含有的主要金属阳离子为______ (填离子符号)。
(4)“转化”过程发生主要反应的化学方程式为_______ 。
(5)实际工业生产中、还原”工序常选用的金属还原剂为_______ (填化学式)。
(6) 的立方晶胞可看作4个如图1所示的结构单元移至图2的相应位置。图1中M点在晶胞中的位置为面心或
的立方晶胞可看作4个如图1所示的结构单元移至图2的相应位置。图1中M点在晶胞中的位置为面心或_______ ;若M点在面心位置,则其原子坐标参数为________ 。
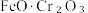 和少量
和少量 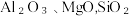 )冶炼 Cr的工艺流程如下:
)冶炼 Cr的工艺流程如下: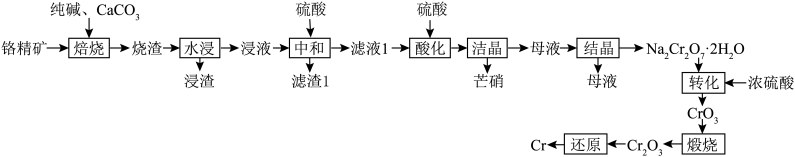
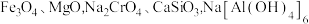
回答下列问题:
(1)“焙烧”之前常将原料混合后球磨,其目的为
(2)从浸渣中分离出Fe3O4的简单方法为
(3)“中和”和“酸化”两步工序不能合并的原因为
(4)“转化”过程发生主要反应的化学方程式为
(5)实际工业生产中、还原”工序常选用的金属还原剂为
(6)
 的立方晶胞可看作4个如图1所示的结构单元移至图2的相应位置。图1中M点在晶胞中的位置为面心或
的立方晶胞可看作4个如图1所示的结构单元移至图2的相应位置。图1中M点在晶胞中的位置为面心或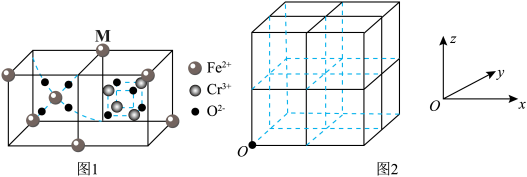
您最近一年使用:0次



