在室温下有0.1 mol·L-1的下列物质:①Na2CO3溶液;②NH4HCO3溶液;③NaHCO3溶液;④NaHSO3溶液;⑤NaHSO4溶液;⑥NaHS溶液。其中,既能跟NaOH溶液反应,又能跟盐酸反应,且pH>7的是
| A.①③④ | B.②④⑥ | C.②③⑥ | D.①③⑤ |
更新时间:2019-04-26 13:09:16
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是
| A.等体积、pH都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:HA>HB |
B.0.1 mol•L﹣1(NH4)2Fe(SO4)2溶液中:c(NH )+c(NH3•H2O)+c(Fe2+)=0.3 mol•L﹣1 )+c(NH3•H2O)+c(Fe2+)=0.3 mol•L﹣1 |
C.25℃时,0.1 mol/L的NaHSO3溶液pH=4,说明HSO 在水溶液中只存在电离平衡 在水溶液中只存在电离平衡 |
D.一定温度下,10mL 0.50mol·L-1 NH4Cl溶液与20mL 0.25mol·L-1 NH4Cl溶液含NH 物质的量前者大 物质的量前者大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知常温下几种弱酸的电离平衡常数如下,等物质的量浓度的Na2CO3溶液、NaHCO3溶液、NaH2PO4溶液、Na2HPO4溶液、Na3PO4溶液、NaH2BO3溶液、CH3COONa溶液的 由小到大的顺序如图,则②③④⑥代表的物质分别为( )
由小到大的顺序如图,则②③④⑥代表的物质分别为( )

 由小到大的顺序如图,则②③④⑥代表的物质分别为( )
由小到大的顺序如图,则②③④⑥代表的物质分别为( )弱酸 | CH3COOH | H3PO4 | H2CO3 | H3BO3 |
电离平衡常数 |
|
|
|
|

| A. Na3PO4、NaH2BO3、Na2HPO4、NaHCO3 |
| B. CH3COONa、NaHCO3、Na2HPO4、Na2CO3 |
| C. NaH2BO3、Na2HPO4、NaHCO3、CH3COONa |
| D. Na2CO3、NaH2BO3、Na2HPO4、NaHCO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】常温下联氨(N2H4)的水溶液中有:
①N2H4+H2O N2H5++OH- K1
N2H5++OH- K1
②N2H5++H2O N2H62++OH- K2
N2H62++OH- K2
(提示:二元弱碱的电离也是分步电离)
该溶液中的微粒的物质的量分数δ(X)随-lgc(OH-)变化的关系如图所示。下列叙述错误的是
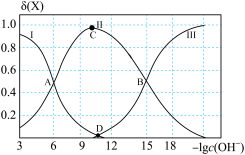
①N2H4+H2O
 N2H5++OH- K1
N2H5++OH- K1②N2H5++H2O
 N2H62++OH- K2
N2H62++OH- K2(提示:二元弱碱的电离也是分步电离)
该溶液中的微粒的物质的量分数δ(X)随-lgc(OH-)变化的关系如图所示。下列叙述错误的是

| A.据A点可求:K1=10-6 |
| B.D点溶液的c(OH-)=10-l1 |
| C.若C点为N2H5Cl溶液,则存在:c(Cl-)>c(N2H5+)+2c(N2H62+) |
| D.在N2H5Cl水溶液中,c(N2H4)+c(OH-)=2c(N2H62+)+c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列图示与对应的叙述相符的是( )
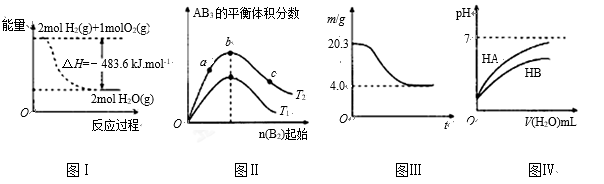

| A.图Ⅰ表示H2与O2发生反应过程中的能量变化,则H2的燃烧热△H =-241.8 kJ·mol-1 |
B.图Ⅱ表示反应A2 (g)+ 3B2 (g) 2AB3(g),达到平衡时A2的转化率大小为:b>a>c 2AB3(g),达到平衡时A2的转化率大小为:b>a>c |
| C.图Ⅲ表示0.1mol MgCl2·6H2O在空气中充分加热时固体质量随时间的变化 |
| D.图Ⅳ表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH大于同浓度NaB溶液的pH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用含铁废铜制备胆矾的流程如图所示,下列说法错误的是


| A.流程中Cu2(OH)2CO3可用CuO代替 |
| B.“溶解”中加H2O2只是将Fe2+氧化为Fe3+ |
| C.加热煮沸的目的是使Fe3+充分水解进而沉淀去除 |
| D.“系列操作”前加入H2SO4的目的是抑制Cu2+的水解 |
您最近一年使用:0次

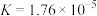
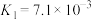
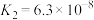
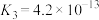


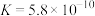
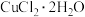 晶体的工艺流程如图:
晶体的工艺流程如图:

 则可以生成2.0molCuO (不考虑其他物质与氧气的反应)
则可以生成2.0molCuO (不考虑其他物质与氧气的反应) 固体
固体

