锆(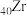 )是现代工业的重要金属原料,具有良好的可塑性,抗蚀性能超过钛。以锆英石(主要成分是
)是现代工业的重要金属原料,具有良好的可塑性,抗蚀性能超过钛。以锆英石(主要成分是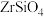 ,还含有少量
,还含有少量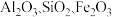 等杂质)为原料生产锆及其化合物的流程如图所示
等杂质)为原料生产锆及其化合物的流程如图所示
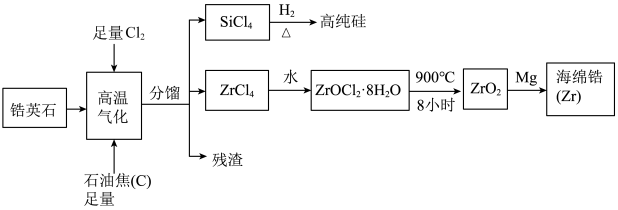
(1)写出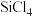 的电子式
的电子式____________________ 。
(2)高温气化过程中,不考虑损失,发现分馏后得到的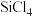 质量通常比由纯
质量通常比由纯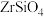 发生的反应得到的
发生的反应得到的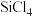 质量大,用化学方程式来解释原因
质量大,用化学方程式来解释原因_________________________ 。
(3)高温气化后的固体残渣除碳外,还有 和
和 ,加水浸取得氯化铁溶液,过滤,从滤渣中分离出碳和
,加水浸取得氯化铁溶液,过滤,从滤渣中分离出碳和 两种固体的方法是
两种固体的方法是____________________ 。
(4)写出上述流程中 与水反应的化学方程式:
与水反应的化学方程式:____________________________ 。
(5)已知氧化锆(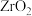 )是一种两性氧化物,与氢氧化钠共熔融可形成酸盐,请写出化学方程式
)是一种两性氧化物,与氢氧化钠共熔融可形成酸盐,请写出化学方程式_________________________________________ 。
(6)工业上可用钾还原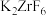 时制得金属
时制得金属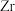 ,
,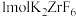 被还原时生成的钾盐的物质的量为
被还原时生成的钾盐的物质的量为_________________ 。
(7)已知 ,
, 。下列说法正确的是
。下列说法正确的是__________
A.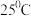 ,电解质溶液的
,电解质溶液的 与
与 之和均为14
之和均为14
B.用盐酸滴定某浓度的 溶液,滴定过程中
溶液,滴定过程中 逐渐增大
逐渐增大
C. 溶液中逐滴加入硫酸溶液,滴加过程中
溶液中逐滴加入硫酸溶液,滴加过程中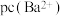 逐渐减小
逐渐减小
D.某温度下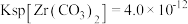 ,则其溶液中
,则其溶液中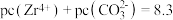
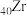 )是现代工业的重要金属原料,具有良好的可塑性,抗蚀性能超过钛。以锆英石(主要成分是
)是现代工业的重要金属原料,具有良好的可塑性,抗蚀性能超过钛。以锆英石(主要成分是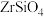 ,还含有少量
,还含有少量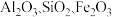 等杂质)为原料生产锆及其化合物的流程如图所示
等杂质)为原料生产锆及其化合物的流程如图所示
(1)写出
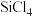 的电子式
的电子式(2)高温气化过程中,不考虑损失,发现分馏后得到的
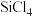 质量通常比由纯
质量通常比由纯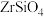 发生的反应得到的
发生的反应得到的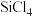 质量大,用化学方程式来解释原因
质量大,用化学方程式来解释原因(3)高温气化后的固体残渣除碳外,还有
 和
和 ,加水浸取得氯化铁溶液,过滤,从滤渣中分离出碳和
,加水浸取得氯化铁溶液,过滤,从滤渣中分离出碳和 两种固体的方法是
两种固体的方法是(4)写出上述流程中
 与水反应的化学方程式:
与水反应的化学方程式:(5)已知氧化锆(
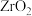 )是一种两性氧化物,与氢氧化钠共熔融可形成酸盐,请写出化学方程式
)是一种两性氧化物,与氢氧化钠共熔融可形成酸盐,请写出化学方程式(6)工业上可用钾还原
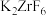 时制得金属
时制得金属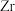 ,
,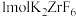 被还原时生成的钾盐的物质的量为
被还原时生成的钾盐的物质的量为(7)已知
 ,
, 。下列说法正确的是
。下列说法正确的是A.
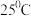 ,电解质溶液的
,电解质溶液的 与
与 之和均为14
之和均为14B.用盐酸滴定某浓度的
 溶液,滴定过程中
溶液,滴定过程中 逐渐增大
逐渐增大C.
 溶液中逐滴加入硫酸溶液,滴加过程中
溶液中逐滴加入硫酸溶液,滴加过程中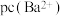 逐渐减小
逐渐减小D.某温度下
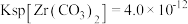 ,则其溶液中
,则其溶液中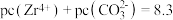
更新时间:2019/05/09 15:07:08
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】皮革厂的废水中含有一定量的氨氮(以NH3、 形式存在),可通过电化学、沉淀和氧化等方法进行处理以达到国家规定的排放标准。
形式存在),可通过电化学、沉淀和氧化等方法进行处理以达到国家规定的排放标准。
(1)如图是用一种新型锂电池电解处理含NH4+的工业废水的装置图。处理过程中, 转化为可参与大气循环的气体。其中,W极为
转化为可参与大气循环的气体。其中,W极为_____ 极,X极的电极反应式为:___________ 。
①该反应的离子方程式为___________ 。
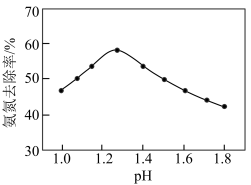
②废水中氨氮去除率随pH的变化如图所示,当1.3<pH<1.8时,氨氮去除率随pH升高而降低的原因是___________ 。
①NaC1O将废水中的氨氨转化为N2,该反应的离子方程式为___________
②研究发现,废水中氨氮去除率随温度升高呈先升后降趋势。当温度大于30℃时,废水中氨氮去除率随着温度升高而降低,其原因是___________
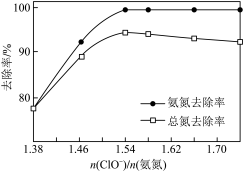
③n(ClO)/n(氨氮)对废水中氨氮去除率和总氮去除率的影响如图所示。当n(ClO)/n(氨氮)>1.54后,总氮去除率下降的原因是___________ 。
 形式存在),可通过电化学、沉淀和氧化等方法进行处理以达到国家规定的排放标准。
形式存在),可通过电化学、沉淀和氧化等方法进行处理以达到国家规定的排放标准。(1)如图是用一种新型锂电池电解处理含NH4+的工业废水的装置图。处理过程中,
 转化为可参与大气循环的气体。其中,W极为
转化为可参与大气循环的气体。其中,W极为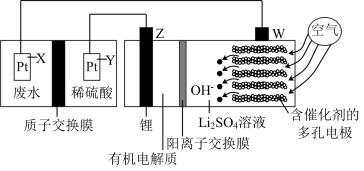
①该反应的离子方程式为
②废水中氨氮去除率随pH的变化如图所示,当1.3<pH<1.8时,氨氮去除率随pH升高而降低的原因是
①NaC1O将废水中的氨氨转化为N2,该反应的离子方程式为
②研究发现,废水中氨氮去除率随温度升高呈先升后降趋势。当温度大于30℃时,废水中氨氮去除率随着温度升高而降低,其原因是
③n(ClO)/n(氨氮)对废水中氨氮去除率和总氮去除率的影响如图所示。当n(ClO)/n(氨氮)>1.54后,总氮去除率下降的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】(1)已知用含硫酸铁的废液(含少量杂质)可制备摩尔盐,即(NH4)2Fe(SO4)2·6H2O。其操作流程如下:
①试剂X是_______ ,操作Ⅰ的名称为:____ 。
②减压过滤的目的是:____ 。
③为测定(NH4)2Fe(SO4)2·6H2O晶体中铁的含量,某实验小组做了如下实验:用电子天平准确称量5.000g硫酸亚铁铵晶体,配制成250mL溶液。取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,用0.01000mol/LKMnO4溶液滴定,测得消耗KMnO4溶液的平均体积为23.00mL。滴定终点的现象为:_____________________________ ;该晶体中铁的质量分数为___________ 。(保留4位有效数字)
(2)某课题组通过实验检验摩尔盐晶体加热时的分解产物。
①摩尔盐受热分解,小组同学认为分解产物可能有以下几种情况:
a.Fe2O3、SO3、NH3、H2O b.FeO、SO2、NH3、H2O
c.FeO、NH3、SO3、H2O d.Fe2O3、NH3、SO2、SO3、H2O
经认真分析,通过推理即可确定,猜想___________ 不成立(填序号)。
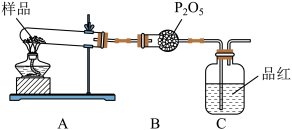
②乙同学设计了如图装置,其中A装置中的固体变为红棕色,则固体产物中含有______ C装置中红色褪去,说明气体产物中含有__________ 。______________ 、C中酚酞溶液。

①试剂X是
②减压过滤的目的是:
③为测定(NH4)2Fe(SO4)2·6H2O晶体中铁的含量,某实验小组做了如下实验:用电子天平准确称量5.000g硫酸亚铁铵晶体,配制成250mL溶液。取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,用0.01000mol/LKMnO4溶液滴定,测得消耗KMnO4溶液的平均体积为23.00mL。滴定终点的现象为:
(2)某课题组通过实验检验摩尔盐晶体加热时的分解产物。
①摩尔盐受热分解,小组同学认为分解产物可能有以下几种情况:
a.Fe2O3、SO3、NH3、H2O b.FeO、SO2、NH3、H2O
c.FeO、NH3、SO3、H2O d.Fe2O3、NH3、SO2、SO3、H2O
经认真分析,通过推理即可确定,猜想
②乙同学设计了如图装置,其中A装置中的固体变为红棕色,则固体产物中含有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】海洋是富饶的自然资源宝库。回答下列问题:
(1)从海洋锰结核可提取多种重要金属,其中Al高温还原MnO2的化学方程式为__________ 。
(2)海水淡化的方法有很多。
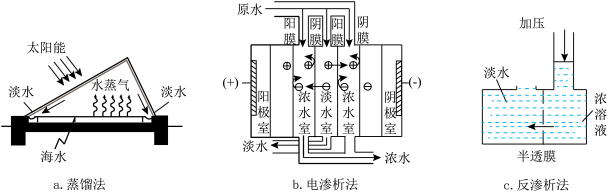
①下列三种海水淡化方法中,发生氧化还原反应的是_________ (填字母)。
②离子交换法淡化海水的示意图如下:
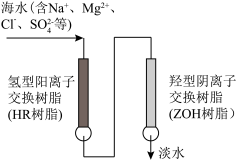
通过ZOH树脂时,溶液中发生的离子反应为_____________ ;能否先通过ZOH树脂再通过HR树脂,并说明理由:____________________________ 。
(3)以海带浸取液为原料制取NaI晶体的一种实验流程如下:
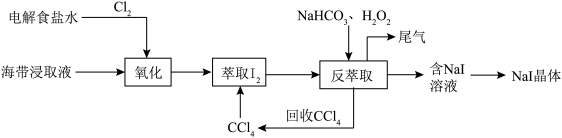
①“萃取”、“反萃取”使用的玻璃仪器除烧杯外,另一主要玻璃仪器是_________ 。
②“电解食盐水”的化学方程式为__________ 。“反萃取”的离子方程式为_________________ 。
③由NaI溶液制取NaI晶体的步骤为_________ 、过滤、洗涤及干燥。
(1)从海洋锰结核可提取多种重要金属,其中Al高温还原MnO2的化学方程式为
(2)海水淡化的方法有很多。
①下列三种海水淡化方法中,发生氧化还原反应的是

②离子交换法淡化海水的示意图如下:

通过ZOH树脂时,溶液中发生的离子反应为
(3)以海带浸取液为原料制取NaI晶体的一种实验流程如下:

①“萃取”、“反萃取”使用的玻璃仪器除烧杯外,另一主要玻璃仪器是
②“电解食盐水”的化学方程式为
③由NaI溶液制取NaI晶体的步骤为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】ZrO2常用作陶瓷材料,可由锆英砂(主要成分为ZrSiO4,也可表示为ZrO2·SiO2,还含有少量Fe2O3、Al2O3、SiO2等杂质)通过如下方法制取。
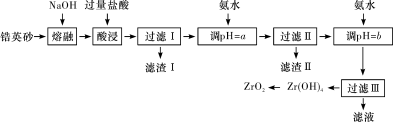
已知:①ZrO2能与烧碱反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+。
②部分金属离子在实验条件下开始沉淀和完全沉淀的pH如下表所示。
(1)“熔融”时ZrSiO4发生反应的化学方程式为________________________________ 。
(2)“滤渣Ⅰ”的化学式为________________ 。
(3)为使滤液Ⅰ中的杂质离子沉淀完全,需用氨水调pH=a,则a的范围是________ ;继续加氨水至pH=b时,所发生反应的离子方程式为__________________________________________ 。
(4)向“过滤Ⅲ”所得滤液中加入CaCO3粉末并加热,得到两种气体。该反应的离子方程式为____________________________ 。

已知:①ZrO2能与烧碱反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+。
②部分金属离子在实验条件下开始沉淀和完全沉淀的pH如下表所示。
| 金属离子 | Fe3+ | Al3+ | ZrO2+ |
| 开始沉淀时pH | 1.9 | 3.3 | 6.2 |
| 沉淀完全时pH | 3.2 | 5.2 | 8.0 |
(2)“滤渣Ⅰ”的化学式为
(3)为使滤液Ⅰ中的杂质离子沉淀完全,需用氨水调pH=a,则a的范围是
(4)向“过滤Ⅲ”所得滤液中加入CaCO3粉末并加热,得到两种气体。该反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】粉煤灰是燃煤产生的重要污染物,主要成分有Al2O3、Fe2O3、MgO和SiO2等物质。用硫酸铵固体等试剂提取粉煤灰中Al2O3并制取铝的工艺流程如图:
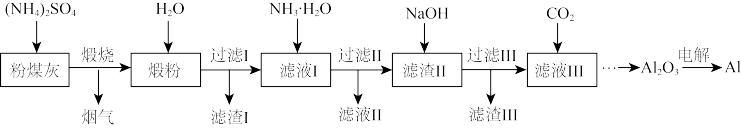
回答下列问题:
(1)已知烟气中含有NH3,煅烧工序中Al2O3参与反应的化学方程式为______ 。
(2)“滤渣Ⅰ”和“滤渣Ⅲ”主要成分的化学式分别为______ 、______ 。
(3)将“滤液Ⅱ”通过______ 、过滤、洗涤、干燥后得到的晶体可返回______ 工序中循环利用。
(4)向“滤液Ⅲ”中通入过量CO2,生成沉淀的离子方程式为______ 。
(5)电解Al2O3制备Al需要冰晶石(Na3AlF6)作助熔剂。Na3AlF6可由Al(OH)3、Na2CO3和HF反应制得,反应的化学方程式为______ 。

回答下列问题:
(1)已知烟气中含有NH3,煅烧工序中Al2O3参与反应的化学方程式为
(2)“滤渣Ⅰ”和“滤渣Ⅲ”主要成分的化学式分别为
(3)将“滤液Ⅱ”通过
(4)向“滤液Ⅲ”中通入过量CO2,生成沉淀的离子方程式为
(5)电解Al2O3制备Al需要冰晶石(Na3AlF6)作助熔剂。Na3AlF6可由Al(OH)3、Na2CO3和HF反应制得,反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上用含锰废料(主要成分MnO2,含有少量Fe2O3、Al2O3、CuO、CaO等)与烟气脱硫进行联合处理并制备MnSO4的流程如图:
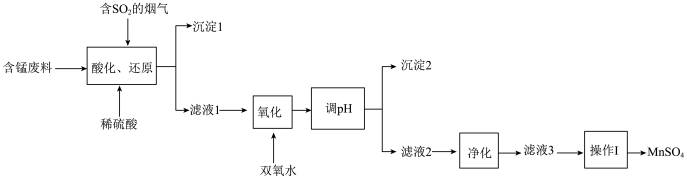
已知:25℃时,部分氢氧化物的溶度积常数(Ksp)如下表所示。
请回答:
(1)沉淀1的化学式为_____ 。
(2)室温下,加双氧水氧化后所得的溶液中c(Mn2+)=2mol/L,某种离子的浓度小于1×10-5mol/L时,可认为已完全沉淀,则生成沉淀2需调节pH的范围是_____ 。“净化”时,加入(NH4)2S的作用为____ 。
(3)“酸化、还原”中,发生的所有氧化还原反应的离子方程式为_____ 。
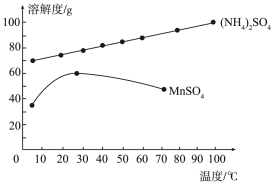
(4)已知:滤液3中除MnSO4外,还含有少量(NH4)2SO4。(NH4)2SO4、MnSO4的溶解度曲线如图所示。据此判断,操作“I”应为蒸发浓缩、_____ 、洗涤、干燥。
(5)工业上可用电解酸性MnSO4溶液的方法制备MnO2,其阳极反应式为_____ 。
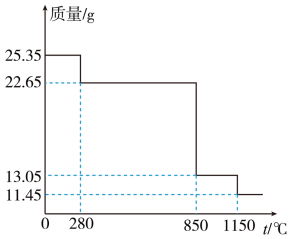
(6)25.35gMnSO4·H2O样品隔绝空气条件下受热分解过程的热重曲线(样品质量随温度变化的曲线)如图所示。则1150℃时,反应的化学方程式为_____ 。

已知:25℃时,部分氢氧化物的溶度积常数(Ksp)如下表所示。
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Cu(OH)2 | Mn(OH)2 |
| Ksp | 1.0×10-32 | 1.0×10-38 | 2.0×10-20 | 2.0×10-14 |
(1)沉淀1的化学式为
(2)室温下,加双氧水氧化后所得的溶液中c(Mn2+)=2mol/L,某种离子的浓度小于1×10-5mol/L时,可认为已完全沉淀,则生成沉淀2需调节pH的范围是
(3)“酸化、还原”中,发生的所有氧化还原反应的离子方程式为
(4)已知:滤液3中除MnSO4外,还含有少量(NH4)2SO4。(NH4)2SO4、MnSO4的溶解度曲线如图所示。据此判断,操作“I”应为蒸发浓缩、

(5)工业上可用电解酸性MnSO4溶液的方法制备MnO2,其阳极反应式为
(6)25.35gMnSO4·H2O样品隔绝空气条件下受热分解过程的热重曲线(样品质量随温度变化的曲线)如图所示。则1150℃时,反应的化学方程式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。利用反应:6NO2+8NH3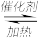 7N2+12H2O可处理NO2。
7N2+12H2O可处理NO2。
(1)若在120℃时该反应在一容积为2L的容器内反应,20min时达到平衡,10min时电子转移了1.2mol,则0~10min时,平均反应速率υ(NO2)=____________ 。
(2)一定条件下NO2与SO2可发生反应,其方程式为:NO2(g)+SO2(g)⇌SO3(g)+NO(g)-Q,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是__________ 。
A.体系压强保持不变
B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变
D.混合气体的平均相对分子质量保持不变
(3)若改变条件,使平衡常数变大,该反应__________ 。
A.一定向正反应方向移动 B.在平衡移动时,正反应速率先减小后增大
C.一定向逆反应方向移动 D.在平衡移动时,逆反应速率先增大后减小
(4)CO可用于合成甲醇,反应方程式为CO(g) + 2H2(g)⇌CH3OH(g) 。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应_________ (填“放热”或“吸热”)。实际生产条件控制在250℃、1.3×104 kPa左右,选择此压强的理由是:_______ 。

 7N2+12H2O可处理NO2。
7N2+12H2O可处理NO2。(1)若在120℃时该反应在一容积为2L的容器内反应,20min时达到平衡,10min时电子转移了1.2mol,则0~10min时,平均反应速率υ(NO2)=
(2)一定条件下NO2与SO2可发生反应,其方程式为:NO2(g)+SO2(g)⇌SO3(g)+NO(g)-Q,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
A.体系压强保持不变
B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变
D.混合气体的平均相对分子质量保持不变
(3)若改变条件,使平衡常数变大,该反应
A.一定向正反应方向移动 B.在平衡移动时,正反应速率先减小后增大
C.一定向逆反应方向移动 D.在平衡移动时,逆反应速率先增大后减小
(4)CO可用于合成甲醇,反应方程式为CO(g) + 2H2(g)⇌CH3OH(g) 。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】丙烯是一种重要的化工原料,可通过丙烷催化脱氢技术(PDH)或丙烷氧化脱氢(DOHP)得到,同时会生成甲烷、乙烷、乙烯等副产物﹑其中(PDH)涉及的主反应和部分副反如下:

 反应Ⅰ
反应Ⅰ

 反应Ⅱ
反应Ⅱ
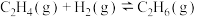
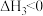 反应Ⅲ
反应Ⅲ
请回答下列问题。
(1) 的反应热
的反应热
_______ 。
(2)在一定温度下,向2L的刚性密闭容器中充入5mol (g),容器中只发生反应Ⅰ和反应Ⅱ,下列选项能说明体系达到平衡状态的是
(g),容器中只发生反应Ⅰ和反应Ⅱ,下列选项能说明体系达到平衡状态的是_______ (填标号)。
A.容器中的压强不再改变 B.混合气体的密度不再改变
C.甲烷与乙烯的物质的量之比不再改变 D.丙烷与氢气的物质的量之比不再改变
若反应5min后体系达平衡状态﹐此时丙烷的平衡转化率为60%,氢气与甲烷的物质的量之比为2∶1,则5min内反应Ⅰ的平均速率
_______  ,该温度下反应Ⅱ的平衡常数K=
,该温度下反应Ⅱ的平衡常数K=_______ mol/L。
(3)DOHP可大规模应用于页岩气生产丙烯,表是在原料气组成一定、流速一定的情况下,两种不同的催化剂B/S-1和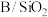 对DOHP中一些主要数据的影响:
对DOHP中一些主要数据的影响:
从数据判断,催化效果较好的催化剂是_______ ,工业生产时应控制的合适温度是_______ ℃。
(4)已知丙烷氧化脱氢法的主要反应为:

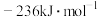 ,在催化剂作用下,
,在催化剂作用下, 氧化脱氢除生成
氧化脱氢除生成 外,还生成CO、
外,还生成CO、 等物质。
等物质。 的转化率和
的转化率和 的产率随温度变化关系如图所示。
的产率随温度变化关系如图所示。
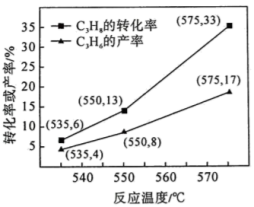
①在550℃时, 的选择性为
的选择性为_______ 。(保留1位小数)( 的选择性
的选择性
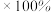 )。
)。
② 的选择性:550℃
的选择性:550℃_______ 575℃(填“大于”或“小于”)。

 反应Ⅰ
反应Ⅰ
 反应Ⅱ
反应Ⅱ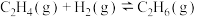
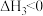 反应Ⅲ
反应Ⅲ请回答下列问题。
(1)
 的反应热
的反应热
(2)在一定温度下,向2L的刚性密闭容器中充入5mol
 (g),容器中只发生反应Ⅰ和反应Ⅱ,下列选项能说明体系达到平衡状态的是
(g),容器中只发生反应Ⅰ和反应Ⅱ,下列选项能说明体系达到平衡状态的是A.容器中的压强不再改变 B.混合气体的密度不再改变
C.甲烷与乙烯的物质的量之比不再改变 D.丙烷与氢气的物质的量之比不再改变
若反应5min后体系达平衡状态﹐此时丙烷的平衡转化率为60%,氢气与甲烷的物质的量之比为2∶1,则5min内反应Ⅰ的平均速率

 ,该温度下反应Ⅱ的平衡常数K=
,该温度下反应Ⅱ的平衡常数K=(3)DOHP可大规模应用于页岩气生产丙烯,表是在原料气组成一定、流速一定的情况下,两种不同的催化剂B/S-1和
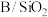 对DOHP中一些主要数据的影响:
对DOHP中一些主要数据的影响:| 催化剂 | 温度/℃ | 丙烷转化率/% | 丙烯选择性/% | 乙烯选择性/% |
| B/S-1 | 480 | 5.3 | 60.9 | 25.7 |
| 540 | 23.8 | 55.4 | 27.2 | |
| 560 | 41.4 | 54.9 | 26.3 | |
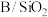 | 480 | 0.6 | 48.2 | 21.3 |
| 540 | 1.9 | 52.5 | 23.8 | |
| 560 | 8.5 | 56.6 | 24.9 |
(4)已知丙烷氧化脱氢法的主要反应为:


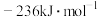 ,在催化剂作用下,
,在催化剂作用下, 氧化脱氢除生成
氧化脱氢除生成 外,还生成CO、
外,还生成CO、 等物质。
等物质。 的转化率和
的转化率和 的产率随温度变化关系如图所示。
的产率随温度变化关系如图所示。
①在550℃时,
 的选择性为
的选择性为 的选择性
的选择性
 )。
)。②
 的选择性:550℃
的选择性:550℃
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】以海绵铜(CuO、Cu)为原料制备氯化亚铜(CuCl)的一种工艺流程如下。
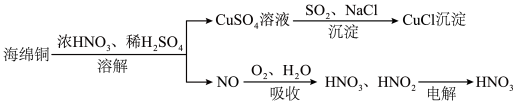
(1)“溶解”过程:生成CuSO4的反应方程式:CuO + H2SO4 === CuSO4 + H2O、________ 。
(2)“吸收”过程:
① 2NO(g) + O2(g) ⇌ 2NO2(g) H = -112.6 kJ·mol-1
提高NO平衡转化率的方法是________ (写出两种)。
② 吸收NO2的有关反应如下:
反应Ⅰ:2NO2(g) + H2O(l) === HNO3(aq) + HNO2(aq) H = -116.1 kJ·mol-1
反应Ⅱ:3HNO2(aq) === HNO3(aq) + 2NO(g) + H2O(l) H = -75.9 kJ·mol-1
用水吸收NO2生成HNO3和NO的热化学方程式是________ 。
(3)“电解”过程:
HNO2为弱酸。通过电解使HNO3得以再生,阳极的电极反应式是________ 。
(4)“沉淀”过程:
① 产生CuCl的离子方程式是_________ 。
② 加入适量Na2CO3,能使沉淀反应更完全,原因是_________ 。
(5)测定CuCl含量:
称取氯化亚铜样品m g,用过量的FeCl3溶液溶解,充分反应后加入适量稀硫酸,用x mol·L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液y mL。滴定时发生的离子反应:Cr2O72- + 6Fe2+ + 14H+ === 2Cr3+ + 6Fe3+ + 7H2O样品中CuCl(M=99.5 g·mol-1)的质量分数为________ 。

(1)“溶解”过程:生成CuSO4的反应方程式:CuO + H2SO4 === CuSO4 + H2O、
(2)“吸收”过程:
① 2NO(g) + O2(g) ⇌ 2NO2(g) H = -112.6 kJ·mol-1
提高NO平衡转化率的方法是
② 吸收NO2的有关反应如下:
反应Ⅰ:2NO2(g) + H2O(l) === HNO3(aq) + HNO2(aq) H = -116.1 kJ·mol-1
反应Ⅱ:3HNO2(aq) === HNO3(aq) + 2NO(g) + H2O(l) H = -75.9 kJ·mol-1
用水吸收NO2生成HNO3和NO的热化学方程式是
(3)“电解”过程:
HNO2为弱酸。通过电解使HNO3得以再生,阳极的电极反应式是
(4)“沉淀”过程:
① 产生CuCl的离子方程式是
② 加入适量Na2CO3,能使沉淀反应更完全,原因是
(5)测定CuCl含量:
称取氯化亚铜样品m g,用过量的FeCl3溶液溶解,充分反应后加入适量稀硫酸,用x mol·L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液y mL。滴定时发生的离子反应:Cr2O72- + 6Fe2+ + 14H+ === 2Cr3+ + 6Fe3+ + 7H2O样品中CuCl(M=99.5 g·mol-1)的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】高铁酸钾( )是一种新型、高效、多功能水处理剂。如图是以铁屑为原料制备
)是一种新型、高效、多功能水处理剂。如图是以铁屑为原料制备 的工艺流程图:
的工艺流程图:
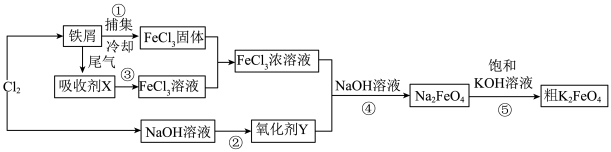
请回答下列问题:
(1)氯气与铁屑反应生成 的条件是
的条件是___________ 。其生成物氯化铁也可用作净水剂,其净水原理为___________ (用离子方程式表示)。
(2)流程图中的吸收剂X为___________(填字母)。
(3)反应④的化学方程式中氧化剂与还原剂的物质的量之比为___________ 。
 )是一种新型、高效、多功能水处理剂。如图是以铁屑为原料制备
)是一种新型、高效、多功能水处理剂。如图是以铁屑为原料制备 的工艺流程图:
的工艺流程图:
请回答下列问题:
(1)氯气与铁屑反应生成
 的条件是
的条件是(2)流程图中的吸收剂X为___________(填字母)。
| A.NaOH溶液 | B.Fe粉 | C. 溶液 溶液 | D. 溶液 溶液 |
(3)反应④的化学方程式中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
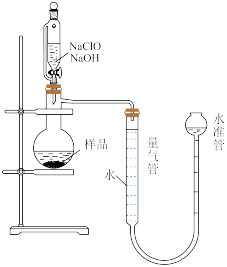
【推荐2】叠氮化钠(NaN3)是一种重要的化学分析试剂,已知NaN3无色无味,微溶于醇、易溶于水,在40℃以上会发生分解。实验室模仿工业“亚硝酸甲酯-水合肼法”制备NaN3,装置如图所示,基本操作如下:
步骤2:生成的亚硝酸甲酯(CH3ONO)蒸气通入到水合肼(N2H4·H2O)的烧碱溶液中,通过电磁加热器加热,生成叠氮化钠;
步骤3:减压蒸馏,回收甲醇;
步骤4:蒸馏后所得母液,冷却结晶、过滤、洗涤、干燥,得到叠氮化钠。
回答下列问题:
(1)仪器a的名称为___________ ;写出装置A中生成CH3ONO的化学方程式:___________ 。
(2)写出装置B中生成NaN3的化学方程式:___________ 。
(3)装置B反应结束后需采用减压蒸馏回收甲醇,不宜直接蒸馏的原因是___________ ;减压蒸馏中使用毛细管的优点是___________ 。
(4)量气法可有效测定产品的纯度,装置如图所示。___________ ;反应结束后水准管中液面会高于量气管,此时需要将水准管慢慢向下移动,则量气管中的液面会___________ (填“上移”“下移”或“不移动”),该产品的纯度(质量分数)为___________ (用含m、V的表达式表示)。
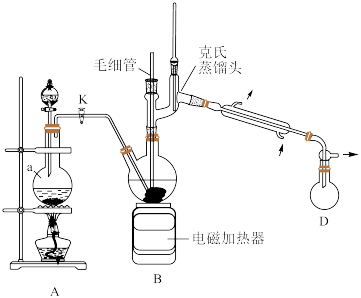
步骤2:生成的亚硝酸甲酯(CH3ONO)蒸气通入到水合肼(N2H4·H2O)的烧碱溶液中,通过电磁加热器加热,生成叠氮化钠;
步骤3:减压蒸馏,回收甲醇;
步骤4:蒸馏后所得母液,冷却结晶、过滤、洗涤、干燥,得到叠氮化钠。
回答下列问题:
(1)仪器a的名称为
(2)写出装置B中生成NaN3的化学方程式:
(3)装置B反应结束后需采用减压蒸馏回收甲醇,不宜直接蒸馏的原因是
(4)量气法可有效测定产品的纯度,装置如图所示。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献,他以饱和食盐水、 、
、 为原料先制得
为原料先制得 ,进而生产出纯碱。回答下列问题:某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计方案实验。一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图所示
,进而生产出纯碱。回答下列问题:某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计方案实验。一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图所示 图中夹持、固定用的仪器未画出
图中夹持、固定用的仪器未画出 。
。
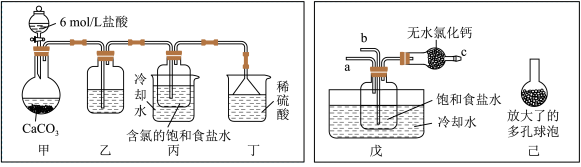
 乙装置中的试剂是
乙装置中的试剂是___________ 。丁装置中稀硫酸的作用是_________________ 。
 另一位同学用图中戊装置
另一位同学用图中戊装置 其他装置未画出
其他装置未画出 进行实验。实验时,须先从
进行实验。实验时,须先从______ 管通入_____ 气体。
 有同学建议在戊装置的b管下端连接己装置,理由是
有同学建议在戊装置的b管下端连接己装置,理由是________________ 。
 下表中所列出的是相关物质在不同温度下的溶解度数据
下表中所列出的是相关物质在不同温度下的溶解度数据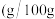 水
水 :
:
参照表中数据,请分析丙、戊装置中使用冷却水或者冰水的原因:____________ 。
 该小组同学为了测定丙中所得晶体的碳酸氢钠的纯度
该小组同学为了测定丙中所得晶体的碳酸氢钠的纯度 假设晶体中不含碳酸盐杂质
假设晶体中不含碳酸盐杂质 ,将晶体充分干燥后,称量质量为
,将晶体充分干燥后,称量质量为 。再将晶体加热到质量不再变化时,称量所得粉末质量为
。再将晶体加热到质量不再变化时,称量所得粉末质量为 。然后进行下图所示实验:
。然后进行下图所示实验:

①在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,其中正确的是______  填字母
填字母 。
。
a.在加入氯化钙溶液后,振荡、静置,向上层清液中继续加入少量氯化钙溶液
b.在加入氯化钙溶液后,振荡、静置,向上层清液中再加入少量碳酸钠溶液
c.在加入氯化钙溶液后,振荡、静置,取上层清液再加入少量碳酸钠溶液
②所得晶体中碳酸氢钠的纯度为_______________ 。
 、
、 为原料先制得
为原料先制得 ,进而生产出纯碱。回答下列问题:某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计方案实验。一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图所示
,进而生产出纯碱。回答下列问题:某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计方案实验。一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图所示 图中夹持、固定用的仪器未画出
图中夹持、固定用的仪器未画出 。
。
 乙装置中的试剂是
乙装置中的试剂是 另一位同学用图中戊装置
另一位同学用图中戊装置 其他装置未画出
其他装置未画出 进行实验。实验时,须先从
进行实验。实验时,须先从 有同学建议在戊装置的b管下端连接己装置,理由是
有同学建议在戊装置的b管下端连接己装置,理由是 下表中所列出的是相关物质在不同温度下的溶解度数据
下表中所列出的是相关物质在不同温度下的溶解度数据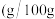 水
水 :
:| 0 | 10 | 20 | 30 | 40 | 50 | |
| NaCl | 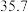 |  | 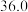 |  | 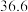 | 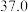 |
 |  | 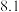 |  | 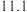 | 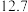 | 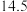 |
 | 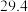 | 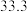 | 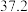 | 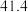 | 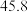 | 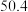 |
 该小组同学为了测定丙中所得晶体的碳酸氢钠的纯度
该小组同学为了测定丙中所得晶体的碳酸氢钠的纯度 假设晶体中不含碳酸盐杂质
假设晶体中不含碳酸盐杂质 ,将晶体充分干燥后,称量质量为
,将晶体充分干燥后,称量质量为 。再将晶体加热到质量不再变化时,称量所得粉末质量为
。再将晶体加热到质量不再变化时,称量所得粉末质量为 。然后进行下图所示实验:
。然后进行下图所示实验:
①在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,其中正确的是
 填字母
填字母 。
。a.在加入氯化钙溶液后,振荡、静置,向上层清液中继续加入少量氯化钙溶液
b.在加入氯化钙溶液后,振荡、静置,向上层清液中再加入少量碳酸钠溶液
c.在加入氯化钙溶液后,振荡、静置,取上层清液再加入少量碳酸钠溶液
②所得晶体中碳酸氢钠的纯度为
您最近一年使用:0次



