实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4 NH4++6HCHO===3H++6H2O+(CH2)6N4H+ [滴定时,1 mol(CH2)6N4H+与 l mol H+相当],然后用NaOH标准溶液滴定反应生成的酸,某兴趣小组用甲醛法进行了如下实验:
步骤I 称取样品1.500g。
步骤II 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤III 移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛溶液,摇匀、静置5 min后,加入1-2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤III填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数______ (填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积______ (填“偏大”、“偏小”或“无影响”)
③滴定时边滴边摇动锥形瓶,眼睛应观察____________
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由_______ 色,且_____________ 。
(2)滴定结果如下表所示:
若NaOH标准溶液的浓度为0.1010mol·L-1则该样品中氮的质量分数为______
(3)实验室现有3种酸碱指示剂,其pH变色范围如下:
甲基橙:3.1~4.4 石蕊:5.0~8.0 酚酞:8.2~10.0
用0.1000mol/LNaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述中正确的是__________ 。
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂
(4)在25 ℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成________ 沉淀(填化学式),生成该沉淀的离子方程式为_________ 。已知25 ℃时Ksp[Mg(OH)2]=1.8×10—11,Ksp[Cu(OH)2]=2.2×10—20。
(5)在25 ℃下,将a mol·L—1的氨水与0.01 mol·L—1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl—),则溶液显_______ 性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=_______ 。
步骤I 称取样品1.500g。
步骤II 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤III 移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛溶液,摇匀、静置5 min后,加入1-2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤III填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积
③滴定时边滴边摇动锥形瓶,眼睛应观察
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由
(2)滴定结果如下表所示:
| 测定次数 | 待测溶液的体积 /mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
若NaOH标准溶液的浓度为0.1010mol·L-1则该样品中氮的质量分数为
(3)实验室现有3种酸碱指示剂,其pH变色范围如下:
甲基橙:3.1~4.4 石蕊:5.0~8.0 酚酞:8.2~10.0
用0.1000mol/LNaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述中正确的是
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂
(4)在25 ℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成
(5)在25 ℃下,将a mol·L—1的氨水与0.01 mol·L—1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl—),则溶液显
更新时间:2019-09-14 09:08:22
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验,请完成下列填空:
(1)配制100mL0.1000 mol∙L-1NaOH标准溶液。滴定操作步骤:
①准备:检漏→洗涤→_______ →_______ →排气泡→读数。
②滴定:用移液管取25.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2-3滴酚酞作指示剂,用标准NaOH溶液进行滴定,重复上述滴定操作2-3次,记录数据如下。
(2)滴定达到终点的标志是_______ 。
(3)排去碱式滴定管中气泡的方法应采用操作_______ 。然后轻轻挤压玻璃球使尖嘴部分充满碱液。

(4)根据上述数据,可计算出该盐酸的浓度约为_______ mol·L-1
(5)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_______ 。
A.开始滴定前,滴定管尖悬挂的液滴未擦去
B.滴定终点读数时仰视读数
C.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
D.锥形瓶水洗后未干燥
E.碱式滴定管尖嘴部分有气泡,滴定后消失
(1)配制100mL0.1000 mol∙L-1NaOH标准溶液。滴定操作步骤:
①准备:检漏→洗涤→
②滴定:用移液管取25.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2-3滴酚酞作指示剂,用标准NaOH溶液进行滴定,重复上述滴定操作2-3次,记录数据如下。
| 实验编号 | NaOH溶液的浓度(mol·L-1) | NaOH标准液初始读数(mL) | NaOH标准液终点读数(mL) |
| 1 | 0.1000 | 0.62 | 20.60 |
| 2 | 0.1000 | 0.72 | 20.74 |
| 3 | 0.1000 | 0.00 | 23.00 |
(3)排去碱式滴定管中气泡的方法应采用操作

(4)根据上述数据,可计算出该盐酸的浓度约为
(5)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有
A.开始滴定前,滴定管尖悬挂的液滴未擦去
B.滴定终点读数时仰视读数
C.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
D.锥形瓶水洗后未干燥
E.碱式滴定管尖嘴部分有气泡,滴定后消失
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量8.2g含有少量杂质的中性易溶杂质的样品,并配成500ml待测溶液,下列操作或现象会引起误差的是 (填字母)
(2)滴定时,用0.2000mol/L的盐酸来滴定待测液,不可选用_______ (填字母)作指示剂。
A.甲基橙 B.石蕊 C.酚酞
(3)滴定过程中眼睛应注视_______ ,锥形瓶下垫一张白纸的作用是_______ 。
(4)滴定前滴定管尖嘴有气泡,滴定后尖嘴气泡消失,测定结果_______ ;未用标准液润洗滴定管,测定结果_______ 。(填“偏高”“偏低”或“无影响”)
(1)准确称量8.2g含有少量杂质的中性易溶杂质的样品,并配成500ml待测溶液,下列操作或现象会引起误差的是 (填字母)
| A.将样品放在托盘上进行称量 | B.容量瓶中有少量水 |
| C.溶解后未冷却至室温就转移 | D.定容摇匀后发现凹液面低于刻度线 |
A.甲基橙 B.石蕊 C.酚酞
(3)滴定过程中眼睛应注视
(4)滴定前滴定管尖嘴有气泡,滴定后尖嘴气泡消失,测定结果
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】在标准状况下充满HCl的烧瓶做完喷泉实验后,得到稀盐酸,用标准氢氧化钠溶液进行滴定,请你回答下列问题:
(1)用标准NaOH溶液滴定这种盐酸时,NaOH溶液应装在_______ 式滴定管中,若用酚酞作指示剂,达到滴定终点时,溶液从_______ 色变为_______ 色。
(2)请填写下列空白:
①若滴定开始和结束时,滴定管中的液面如下图所示:则所用NaOH溶液的体积为_______ mL。

②某学生根据三次实验分别记录有关数据如下表:
请选用其中合理的数据计算该洗厕盐酸的物质的量浓度:c(HCl)=_______ 。
(3)现配制三种浓度的标准NaOH溶液,你认为最合适的是下列第_______ (填序号)种。
①2.500mol·L-1 ②0.150mol·L-1 ③0.020mol·L-1
(1)用标准NaOH溶液滴定这种盐酸时,NaOH溶液应装在
(2)请填写下列空白:
①若滴定开始和结束时,滴定管中的液面如下图所示:则所用NaOH溶液的体积为

②某学生根据三次实验分别记录有关数据如下表:
| 滴定次数 | 待测盐酸体积/mL | 0.1000molL-1NaOH溶液的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 2.00 | 28.15 | 26.15 |
| 第二次 | 25.00 | 1.50 | 29.50 | 28.00 |
| 第三次 | 25.00 | 0.20 | 26.55 | 26.35 |
(3)现配制三种浓度的标准NaOH溶液,你认为最合适的是下列第
①2.500mol·L-1 ②0.150mol·L-1 ③0.020mol·L-1
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】人体血液里Ca2+的浓度一般采用mg·cm-3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
【配制KMnO4标准溶液】如图是配制50 mL KMnO4标准溶液的过程示意图。
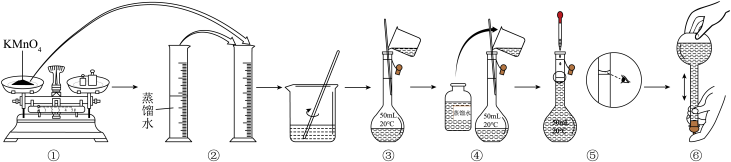
(1)请你观察图示判断,其中不正确的操作有_______ (填序号)。
(2)如果用图示的操作配制溶液,所配制的溶液浓度将_______ (填“偏大”或“偏小”)。
【测定血液样品中Ca2+的浓度】抽取血样20.00 mL,经过上述处理后得到草酸,再用0.020 mol·L-1 KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00 mL KMnO4溶液。
(3)已知草酸跟KMnO4溶液反应的离子方程式为2MnO +5H2C2O4+6H+=2Mnx++10CO2↑+8H2O则方程式中的x=
+5H2C2O4+6H+=2Mnx++10CO2↑+8H2O则方程式中的x=_______ 。
(4)经过计算,血液样品中Ca2+的浓度为_______ mg·cm-3。
(5)春秋末期工艺官书《考工记》中记载有“涑帛”的方法,即利用含有碳酸钠的水溶液来洗涤丝帛。请写出碳酸钠水溶液中通入CO2气体的化学方程式_______ ,将54.8g Na2CO3和NaHCO3的混合物分成等量的两份,一份溶于水后加入足量盐酸,收集到气体V L。另一份直接加热至恒重,生成气体2.24L(所有气体体积均在标准状况下测定),则原固体混合物中Na2CO3的物质的量:n(Na2CO3)=_______ ,气体V=_______ 。
【配制KMnO4标准溶液】如图是配制50 mL KMnO4标准溶液的过程示意图。

(1)请你观察图示判断,其中不正确的操作有
(2)如果用图示的操作配制溶液,所配制的溶液浓度将
【测定血液样品中Ca2+的浓度】抽取血样20.00 mL,经过上述处理后得到草酸,再用0.020 mol·L-1 KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00 mL KMnO4溶液。
(3)已知草酸跟KMnO4溶液反应的离子方程式为2MnO
 +5H2C2O4+6H+=2Mnx++10CO2↑+8H2O则方程式中的x=
+5H2C2O4+6H+=2Mnx++10CO2↑+8H2O则方程式中的x=(4)经过计算,血液样品中Ca2+的浓度为
(5)春秋末期工艺官书《考工记》中记载有“涑帛”的方法,即利用含有碳酸钠的水溶液来洗涤丝帛。请写出碳酸钠水溶液中通入CO2气体的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】用氧化还原滴定法可以测定市售双氧水中过氧化氢的浓度(单位g·L-1),实验过程包括标准溶液的准备和滴定待测溶液:
I.准备标准溶液
a.配制100mLKMnO4溶液备用;
b.准确称取Na2C2O4基准物质3.35g(0.025mol),配制成250mL标准溶液。取出25.00mL于锥形瓶中,加入适量3mol·L-1硫酸酸化后,用待标定的KMnO4溶液滴定至终点,记录数据,计算KMnO4溶液的浓度。
II.滴定主要步骤
a.取待测双氧水10.00mL于锥形瓶中;
b.锥形瓶中加入30.00mL蒸馏水和30.00mL3mol·L-1硫酸,然后用已标定的KMnO4溶液(0.1000mol·L-1)滴定至终点;
e.重复上述操作两次,三次测定的数据如下表:
d.数据处理。
回答下列问题:
(1)将称得的Na2C2O4配制成250mL标准溶液,所使用的仪器除烧杯和玻璃棒外还有___________ 。
(2)标定KMnO4溶液时,能否用稀硝酸调节溶液酸度___________ (填“能”或“不能”),简述理由___________ 。写出标定过程中发生反应的化学方程式___________ 。
(3)滴定待测双氧水时,标准溶液应装入___________ 滴定管,装入标准溶液的前一步应进行的操作是___________ 。
(4)滴定双氧水至终点的现象是___________ 。
(5)计算此双氧水的浓度为___________ g·L-1.
(6)若在配制Na2C2O4标准溶液时,烧杯中的溶液有少量溅出,则最后测定出的双氧水的浓度会___________ (填“偏高”、“偏低”或“无影响”)。
I.准备标准溶液
a.配制100mLKMnO4溶液备用;
b.准确称取Na2C2O4基准物质3.35g(0.025mol),配制成250mL标准溶液。取出25.00mL于锥形瓶中,加入适量3mol·L-1硫酸酸化后,用待标定的KMnO4溶液滴定至终点,记录数据,计算KMnO4溶液的浓度。
II.滴定主要步骤
a.取待测双氧水10.00mL于锥形瓶中;
b.锥形瓶中加入30.00mL蒸馏水和30.00mL3mol·L-1硫酸,然后用已标定的KMnO4溶液(0.1000mol·L-1)滴定至终点;
e.重复上述操作两次,三次测定的数据如下表:
| 组别 | 1 | 2 | 3 |
| 消耗标准溶液体积(mL) | 25.24 | 25.02 | 24.98 |
回答下列问题:
(1)将称得的Na2C2O4配制成250mL标准溶液,所使用的仪器除烧杯和玻璃棒外还有
(2)标定KMnO4溶液时,能否用稀硝酸调节溶液酸度
(3)滴定待测双氧水时,标准溶液应装入
(4)滴定双氧水至终点的现象是
(5)计算此双氧水的浓度为
(6)若在配制Na2C2O4标准溶液时,烧杯中的溶液有少量溅出,则最后测定出的双氧水的浓度会
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】工业废水中常含有一定量氧化性较强的 ,利用滴定原理测定
,利用滴定原理测定 含量方法如下:
含量方法如下:
步骤I:量取 废水于锥形瓶中,加入适量稀硫酸酸化。
废水于锥形瓶中,加入适量稀硫酸酸化。
步骤Ⅱ:加入过量的碘化钾溶液充分反应: 。
。
步骤Ⅲ:向锥形瓶中滴入几滴指示剂。用滴定管量取 溶液进行滴定,数据记录如下表:
溶液进行滴定,数据记录如下表: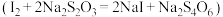
(1)写出水溶液中 和
和 相互转化的离子方程式
相互转化的离子方程式___________ 。
(2)量取 废水选择的仪器是
废水选择的仪器是___________ ,步骤Ⅲ中滴加的指示剂为___________ ,滴定达到终点时的实验现象是___________ 。
(3)步骤Ⅲ中a的读数如图所示,则工业废水中 的含量为
的含量为___________  。
。

(4)以下操作会造成废水中 含量测定值偏高的是___________(填序号)。
含量测定值偏高的是___________(填序号)。
 ,利用滴定原理测定
,利用滴定原理测定 含量方法如下:
含量方法如下:步骤I:量取
 废水于锥形瓶中,加入适量稀硫酸酸化。
废水于锥形瓶中,加入适量稀硫酸酸化。步骤Ⅱ:加入过量的碘化钾溶液充分反应:
 。
。步骤Ⅲ:向锥形瓶中滴入几滴指示剂。用滴定管量取
 溶液进行滴定,数据记录如下表:
溶液进行滴定,数据记录如下表: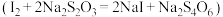
| 滴定次数 |  溶液起始读数 溶液起始读数 |  溶液终点读数 溶液终点读数 |
| 第一次 | 1.02 | 19.03 |
| 第二次 | 2.00 | 19.99 |
| 第三次 | 0.20 | a |
 和
和 相互转化的离子方程式
相互转化的离子方程式(2)量取
 废水选择的仪器是
废水选择的仪器是(3)步骤Ⅲ中a的读数如图所示,则工业废水中
 的含量为
的含量为 。
。
(4)以下操作会造成废水中
 含量测定值偏高的是___________(填序号)。
含量测定值偏高的是___________(填序号)。| A.滴定终点读数时,俯视滴定管的刻度 |
| B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗 |
| C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液 |
D.量取 溶液的滴定管用蒸馏水洗后未用标准液润洗 溶液的滴定管用蒸馏水洗后未用标准液润洗 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)25℃时,10L 0.05 mol/L H2SO4溶液的c(H+)=___________ ,向其中加入蒸馏水稀释至100L,在此过程中,水的电离程度___________ (填增大、减少或不变)。
(2)某温度下纯水的c(H+)=4.0×10-7mol/L,若温度不变,滴入稀盐酸,使c(H+)=2.0×10-4 mol/L,则此溶液中由水电离产生的c(H+)=___________ 。
(3)25℃时不断将水滴入0.1 mol/L的氨水中,下列图象变化合理的是___________。
(4)某浓度的氨水中存在平衡:NH3·H2O 
 +OH-,如想增大
+OH-,如想增大 的浓度而不增大OH-的浓度,应采取的措施是___________ (填字母)。
的浓度而不增大OH-的浓度,应采取的措施是___________ (填字母)。
(5)往5mL0.1mol/L的K2Cr2O7溶液中滴加5滴6mol/L NaOH溶液,则溶液的颜色变化为___________ ,请用平衡移动原理结合化学用语解释产生该变化的原因___________ 。
(1)25℃时,10L 0.05 mol/L H2SO4溶液的c(H+)=
(2)某温度下纯水的c(H+)=4.0×10-7mol/L,若温度不变,滴入稀盐酸,使c(H+)=2.0×10-4 mol/L,则此溶液中由水电离产生的c(H+)=
(3)25℃时不断将水滴入0.1 mol/L的氨水中,下列图象变化合理的是___________。
A. | B. | C. | D. |

 +OH-,如想增大
+OH-,如想增大 的浓度而不增大OH-的浓度,应采取的措施是___________ (填字母)。
的浓度而不增大OH-的浓度,应采取的措施是___________ (填字母)。| A.适当升高温度 | B.加入NH4Cl固体 | C.通入NH3 | D.加入少量浓盐酸 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】我们的生活离不开化学.化学物质在不同的领域发挥着重要的作用。
(1)食醋是生活中常用的调味剂,写出醋酸电离的方程式:_______ ;常温下,体积均为10mL 的醋酸溶液与硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者
的醋酸溶液与硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者_______ 后者(填“>”、“<”或“=”)。
(2)铵盐是重要的化肥, 溶液显
溶液显_______ 性(填“酸”、“中”或“碱”)。
(3)已知:
 可以中和胃酸又是常用的食品添加剂,根据上表数据计算
可以中和胃酸又是常用的食品添加剂,根据上表数据计算 常温下的水解常数
常温下的水解常数_______ 。(保留两位有效数字)
(4)泡沫灭火器含有的试剂为 溶液、
溶液、 溶液和起泡剂.使用时发生反应的离子方程式是
溶液和起泡剂.使用时发生反应的离子方程式是_______ 。
(5) 又称臭碱、硫化碱,是应用广泛的化工原料,向AgCl悬浊液中滴加
又称臭碱、硫化碱,是应用广泛的化工原料,向AgCl悬浊液中滴加 溶液,生成黑色沉淀,写出反应的离子方程式
溶液,生成黑色沉淀,写出反应的离子方程式_______ 。
(1)食醋是生活中常用的调味剂,写出醋酸电离的方程式:
 的醋酸溶液与硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者
的醋酸溶液与硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者(2)铵盐是重要的化肥,
 溶液显
溶液显(3)已知:
| 化学式 | NH3·H2O |  |
| 电离常数K(常温) | 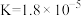 | 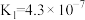 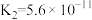 |
 可以中和胃酸又是常用的食品添加剂,根据上表数据计算
可以中和胃酸又是常用的食品添加剂,根据上表数据计算 常温下的水解常数
常温下的水解常数(4)泡沫灭火器含有的试剂为
 溶液、
溶液、 溶液和起泡剂.使用时发生反应的离子方程式是
溶液和起泡剂.使用时发生反应的离子方程式是(5)
 又称臭碱、硫化碱,是应用广泛的化工原料,向AgCl悬浊液中滴加
又称臭碱、硫化碱,是应用广泛的化工原料,向AgCl悬浊液中滴加 溶液,生成黑色沉淀,写出反应的离子方程式
溶液,生成黑色沉淀,写出反应的离子方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】氨是重要的基础化工原料,可以制备亚硝酸(HNO2)、连二次硝酸(H2N2O2)、尿素[CO(NH2)2]等多种含氮的化工产品。
(1)NH3极易溶于水且溶液显碱性,请用化学方程式解释原因:___________ 。
(2)25℃时,亚硝酸和连二次硝酸的电离常数如下表所示:
①物质的量浓度相同的NaNO2和NaHN2O2溶液的pH(NaHN2O2)___________ pH(NaNO2)(填“>”、“<”或“=”)。
②25℃时NaHN2O2溶液中存在水解平衡,其水解常数Kh=___________ (保留三位有效数字)。
③0.1mol/LNa2N2O2溶液中离子浓度由大到小的顺序为___________ 。
(3)以NH3与CO2为原料可以合成尿素[CO(NH2)2],涉及的化学反应如下:
反应Ⅰ:2NH3(g)+CO2(g) NH2CO2NH4(s) ΔH1=﹣159.5kJ•mol-1;
NH2CO2NH4(s) ΔH1=﹣159.5kJ•mol-1;
反应Ⅱ:NH2CO2NH4(s) CO(NH2)2(s)+H2O(g) ΔH2=+116.5kJ•mol-1;
CO(NH2)2(s)+H2O(g) ΔH2=+116.5kJ•mol-1;
反应Ⅲ:H2O(l)=H2O(g) ΔH3=+44.0kJ•mol-1。
则反应Ⅳ:NH3与CO2合成尿素同时生成液态水的热化学方程式为___________ 。
(4)T1℃时,向容积为2L的恒容密闭容器中充入n(NH3):n(CO2)=2:l的原料气,使之发生反应Ⅳ,反应结束后得到尿素的质量为30g

①T1℃时,NH3的平衡转化率=______ ,该反应的平衡常数K的值为_____ 。
②图2中能正确反应平衡常数K随温度变化关系的曲线为_____ (填字母标号)。
(1)NH3极易溶于水且溶液显碱性,请用化学方程式解释原因:
(2)25℃时,亚硝酸和连二次硝酸的电离常数如下表所示:
| 化学式 | HNO2 | H2N2O2 |
| 电离常数 | Ka=5.1×10-4 | Ka1=6.17×10-8、Ka2=2.88×10-12 |
②25℃时NaHN2O2溶液中存在水解平衡,其水解常数Kh=
③0.1mol/LNa2N2O2溶液中离子浓度由大到小的顺序为
(3)以NH3与CO2为原料可以合成尿素[CO(NH2)2],涉及的化学反应如下:
反应Ⅰ:2NH3(g)+CO2(g)
 NH2CO2NH4(s) ΔH1=﹣159.5kJ•mol-1;
NH2CO2NH4(s) ΔH1=﹣159.5kJ•mol-1;反应Ⅱ:NH2CO2NH4(s)
 CO(NH2)2(s)+H2O(g) ΔH2=+116.5kJ•mol-1;
CO(NH2)2(s)+H2O(g) ΔH2=+116.5kJ•mol-1;反应Ⅲ:H2O(l)=H2O(g) ΔH3=+44.0kJ•mol-1。
则反应Ⅳ:NH3与CO2合成尿素同时生成液态水的热化学方程式为
(4)T1℃时,向容积为2L的恒容密闭容器中充入n(NH3):n(CO2)=2:l的原料气,使之发生反应Ⅳ,反应结束后得到尿素的质量为30g

①T1℃时,NH3的平衡转化率=
②图2中能正确反应平衡常数K随温度变化关系的曲线为
您最近一年使用:0次



