四氢铝锂(LiAlH4)常作有机合成的重要还原剂。以辉锂矿(主要成分Li2O•Al2O3•4SiO2,含少量Fe2O3)为原料合成四氢铝锂的流程如图:
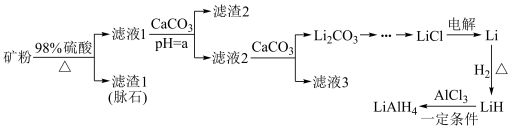
已知:①几种金属氢氧化物沉淀的pH如表所示:
②常温下,Ksp(Li2CO3)=2.0×10-3。Li2CO3在水中溶解度随着温度升高而减小。
回答下列问题:
(1)上述流程中,提高“酸浸”速率的措施有____ (写两条);加入CaCO3的作用是____ ,“a”的最小值为____ 。
(2)用热水洗涤Li2CO3固体,而不用冷水洗涤,其目的是___ ;检验碳酸锂是否洗净的实验操作是___ 。
(3)写出LiH和AlCl3反应的化学方程式:___ (条件不作要求)
(4)设计简单方案由Li2CO3制备无水LiCl:___ 。
(5)在有机合成中,还原剂的还原能力通常用“有效氢”表示,其含义是1克还原剂相当于多少克氢气的还原能力,LiAlH4的“有效氢"为___ 。(结果保留2位小数)

已知:①几种金属氢氧化物沉淀的pH如表所示:
| 物质 | Fe(OH)3 | A1(OH)3 |
| 开始沉淀的pH | 2.3 | 4.0 |
| 完全沉淀的pH | 3.7 | 6.5 |
②常温下,Ksp(Li2CO3)=2.0×10-3。Li2CO3在水中溶解度随着温度升高而减小。
回答下列问题:
(1)上述流程中,提高“酸浸”速率的措施有
(2)用热水洗涤Li2CO3固体,而不用冷水洗涤,其目的是
(3)写出LiH和AlCl3反应的化学方程式:
(4)设计简单方案由Li2CO3制备无水LiCl:
(5)在有机合成中,还原剂的还原能力通常用“有效氢”表示,其含义是1克还原剂相当于多少克氢气的还原能力,LiAlH4的“有效氢"为
更新时间:2019-09-15 15:01:10
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉和氧化铁等涂在铝箔上制成。由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行回收研究,设计实验流程如下:

已知:a.NiCl2易溶于水,Fe3+不能氧化Ni2+。
b.某温度下一些金属氢氧化物的Ksp及开始沉淀和完全沉淀时的理论pH如表所示:
回答下列问题:
(1)根据表中数据判断步骤②依次析出的沉淀Ⅱ________ 和沉淀Ⅲ________ (填化学式),则pH1________ pH2(填“>”、“=”或“<”),控制两种沉淀析出可利用________ (填序号)。
A.pH试纸 B.石蕊指示剂 C.pH计
(2)已知溶解度:NiC2O4>NiC2O4·H2O>NiC2O4·2H2O,则步骤③的化学方程式是________________________________________________ 。
步骤③后,过滤沉淀所需的玻璃仪器有____________ 。若过滤时发现滤液中有少量浑浊,从实验操作的角度给出两种可能的原因:______ 、 ____________________________ 。
(3)④中阳极反应产生的气体E为________ ,验证该气体的试剂为__________________________________________________________ 。
(4)试写出步骤⑥的离子方程式:______________________________ 。

已知:a.NiCl2易溶于水,Fe3+不能氧化Ni2+。
b.某温度下一些金属氢氧化物的Ksp及开始沉淀和完全沉淀时的理论pH如表所示:
| M(OH)n | Ksp | pH | |
| 开始沉淀 | 沉淀完全 | ||
| Al(OH)3 | 1.9×10-33 | 3.43 | 4.19 |
| Fe(OH)3 | 3.9×10-38 | 2.53 | 2.94 |
| Ni(OH)2 | 1.6×10-14 | 7.60 | 9.75 |
回答下列问题:
(1)根据表中数据判断步骤②依次析出的沉淀Ⅱ
A.pH试纸 B.石蕊指示剂 C.pH计
(2)已知溶解度:NiC2O4>NiC2O4·H2O>NiC2O4·2H2O,则步骤③的化学方程式是
步骤③后,过滤沉淀所需的玻璃仪器有
(3)④中阳极反应产生的气体E为
(4)试写出步骤⑥的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】亚硝酰氯(ClNO)是有机物合成中的重要试剂,可由NO与Cl2在常温常压下反应得到。ClNO部分性质如下:黄色气体,熔点:-59.6℃,沸点:-6.4℃,遇水易水解。某研究性学习小组根据亚硝酰氯(ClNO)性质拟在通风橱中制取亚硝酰氯,设计了如下实验装置。、
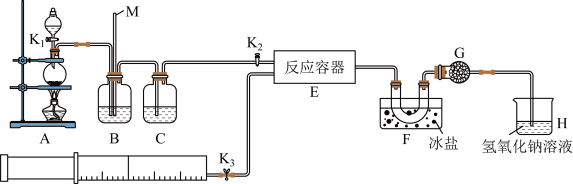
试回答下列问题:
(1)写出实验室利用装置A制备Cl2的离子反应方程式___ 。
(2)装置B的作用是①__ ,②___ 。
(3)若用A装置制取NO气体,B中应该盛放__ 。
(4)为使NO和Cl2恰好完全反应生成ClNO,理论上向E中通入NO和Cl2两种气体的流速比为__ 。
(5)装置H吸收尾气,有同学认为尾气中的某种气体不能完全被吸收。为了充分吸收尾气,可将尾气与__ 同时通入NaOH溶液中。
(6)已知:ClNO与H2O反应生成HNO2和HCl。
①设计实验证明HNO2是弱酸:__ 。(仅提供的试剂:1mol•L-1HCl、1mol•L-1HNO2溶液、NaNO2溶液、红色石蕊试纸、蓝色石蕊试纸)。
②通过以下实验测定ClNO样品的纯度。取F中所得液体3.0g溶于水,配制成250mL溶液;取出25.00mL样品溶液置于锥形瓶中,用0.20mol•L-1AgNO3标准溶液滴定至终点,根据表中所给信息,应选用___ 做指示剂。
消耗标准AgNO3溶液的体积为20.00ml,亚硝酰氯(ClNO)的质量分数为__ 。

试回答下列问题:
(1)写出实验室利用装置A制备Cl2的离子反应方程式
(2)装置B的作用是①
(3)若用A装置制取NO气体,B中应该盛放
(4)为使NO和Cl2恰好完全反应生成ClNO,理论上向E中通入NO和Cl2两种气体的流速比为
(5)装置H吸收尾气,有同学认为尾气中的某种气体不能完全被吸收。为了充分吸收尾气,可将尾气与
(6)已知:ClNO与H2O反应生成HNO2和HCl。
①设计实验证明HNO2是弱酸:
②通过以下实验测定ClNO样品的纯度。取F中所得液体3.0g溶于水,配制成250mL溶液;取出25.00mL样品溶液置于锥形瓶中,用0.20mol•L-1AgNO3标准溶液滴定至终点,根据表中所给信息,应选用
| 物质 | Ag2CrO4 | AgCl | AgI | Ag2S |
| 颜色 | 砖红色 | 白色 | 黄色 | 黑色 |
| Ksp | 1×10-12 | 1.56×10-10 | 8.3×10-17 | 6.3×10-50 |
消耗标准AgNO3溶液的体积为20.00ml,亚硝酰氯(ClNO)的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】碳酸钠的用途很广,可用做冶金、纺织、漂染等工业的基本原料.请根据题意回答下列问题:
Ⅰ 世界最早工业生产碳酸钠的方法是路布兰
世界最早工业生产碳酸钠的方法是路布兰 法.其流程如下:
法.其流程如下:
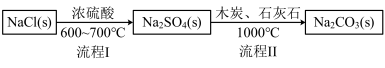
 流程I的另一产物是
流程I的另一产物是 ______ ,流程Ⅱ的反应分步进行: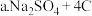
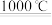
 ;
;
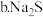 与石灰石发生复分解反应,总反应方程式可表示为
与石灰石发生复分解反应,总反应方程式可表示为 ______ .
Ⅱ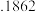 年,比利时人索尔维
年,比利时人索尔维
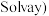 用氨碱法生产碳酸钠.反应原理如下:
用氨碱法生产碳酸钠.反应原理如下:
 时一些物质在水中的溶解度
时一些物质在水中的溶解度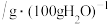
 氨碱法生成纯碱的原料是
氨碱法生成纯碱的原料是 ______ ,可循环利用的物质有 ______ .
 饱和NaCl溶液通
饱和NaCl溶液通 和
和 能生成
能生成 的原因有:
的原因有: ______ .
Ⅲ 我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原料利用率.
我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原料利用率.
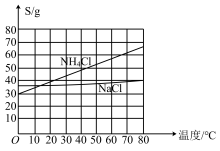
 生产中需向分离出
生产中需向分离出 后所得的溶液中加入NaCl固体并通入
后所得的溶液中加入NaCl固体并通入 ,在
,在 ______  填温度范围
填温度范围 下析出
下析出 ______ 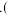 填化学式
填化学式
Ⅰ
 世界最早工业生产碳酸钠的方法是路布兰
世界最早工业生产碳酸钠的方法是路布兰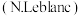 法.其流程如下:
法.其流程如下: 
 流程I的另一产物是
流程I的另一产物是 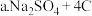
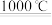
 ;
; 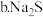 与石灰石发生复分解反应,总反应方程式可表示为
与石灰石发生复分解反应,总反应方程式可表示为 Ⅱ
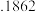 年,比利时人索尔维
年,比利时人索尔维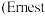
 用氨碱法生产碳酸钠.反应原理如下:
用氨碱法生产碳酸钠.反应原理如下: 
 时一些物质在水中的溶解度
时一些物质在水中的溶解度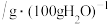
| NaCl |  |  |  |  |
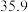 | 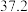 |  |  |  |
 氨碱法生成纯碱的原料是
氨碱法生成纯碱的原料是  饱和NaCl溶液通
饱和NaCl溶液通 和
和 能生成
能生成 的原因有:
的原因有: Ⅲ
 我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原料利用率.
我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原料利用率. 
 生产中需向分离出
生产中需向分离出 后所得的溶液中加入NaCl固体并通入
后所得的溶液中加入NaCl固体并通入 ,在
,在  填温度范围
填温度范围 下析出
下析出  填化学式
填化学式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】POCl3广泛用于染料等工业。某化学学习小组借助拉瓦锡研究空气成分的曲颈甑(装置甲)合成PC13,并采取PCl3氧化法制备POCl3。
已知:(1)PCl3的熔点为-112℃,沸点为75.5℃,遇水生成H3PO3和HCl;
(2)2PCl3+O2==2POCl3。
【实验Ⅰ】制备PCl3
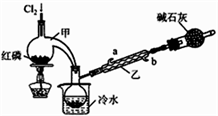
(1)实验室制备Cl2的原理是________________________ 。
(2)碱石灰的作用除了处理尾气外还有________________________ 。
(3)装置乙中冷凝水从_____ (选填a或b)进入。
【实验Ⅱ】制备POCl3
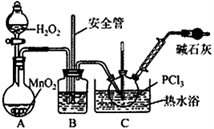
(4)实验室常用有微孔的试剂瓶保存H2O2,“微孔”与上述装置中的___________ (仪器名称)目的是一致的。
(5)C中反应温度控制在60~65℃,其原因是________________________ 。
【实验Ⅲ】测定POCl3含量
①准确称取30.70gPOC13产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解;
②将水解液配成100.00mL溶液,取10.00mL溶液于锥形瓶中;
③加入10.00mL3.200mol/LAgNO3标准溶液,并加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖;
④以Fe3+ 为指示剂,用0.2000mol/LKSCN 溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00 mL KSCN 溶液。
已知:Ag++SCN-==AgSCN↓ Ksp(AgCl)>Ksp(AgSCN )。
(6)POC13水解的化学反应方程式为________________________ 。
(7)滴定终点的现象为____________ ,用硝基苯覆盖沉淀的目的是________________________ 。
(8)反应中POC13的百分含量为________________ 。
已知:(1)PCl3的熔点为-112℃,沸点为75.5℃,遇水生成H3PO3和HCl;
(2)2PCl3+O2==2POCl3。
【实验Ⅰ】制备PCl3

(1)实验室制备Cl2的原理是
(2)碱石灰的作用除了处理尾气外还有
(3)装置乙中冷凝水从
【实验Ⅱ】制备POCl3

(4)实验室常用有微孔的试剂瓶保存H2O2,“微孔”与上述装置中的
(5)C中反应温度控制在60~65℃,其原因是
【实验Ⅲ】测定POCl3含量
①准确称取30.70gPOC13产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解;
②将水解液配成100.00mL溶液,取10.00mL溶液于锥形瓶中;
③加入10.00mL3.200mol/LAgNO3标准溶液,并加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖;
④以Fe3+ 为指示剂,用0.2000mol/LKSCN 溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00 mL KSCN 溶液。
已知:Ag++SCN-==AgSCN↓ Ksp(AgCl)>Ksp(AgSCN )。
(6)POC13水解的化学反应方程式为
(7)滴定终点的现象为
(8)反应中POC13的百分含量为
您最近一年使用:0次
【推荐2】现需设计一套实验装置来电解饱和食盐水,并测量电解产生的氢气的体积(约6 mL)和检验氯气的氧化性(不应将多余的氯气排入空气中)。
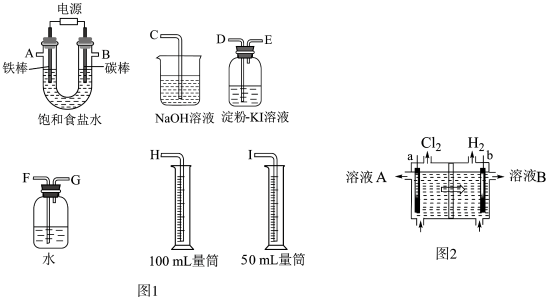
(1)试从上图图1中选用几种必要的仪器,连成一整套装置,各种仪器接口的连接顺序(填编号)是:A接______ ,B接______ 。
(2)碳棒上发生的电极反应为_______ 。
(3)能说明氯气具有氧化性的实验现象是_______ 。
(4)假定装入的饱和食盐水为50 mL(电解前后溶液体积变化可忽略),当测得的氢气为5.6 mL(已折算成标准状况)时,溶液的pH为____ 。
(5)工业上采用离子交换膜法电解饱和食盐水,如上图图2,该离子交换膜是__ (填“阳离子”或“阴离子”)交换膜,溶液B是_______ (填溶质的化学式)

(1)试从上图图1中选用几种必要的仪器,连成一整套装置,各种仪器接口的连接顺序(填编号)是:A接
(2)碳棒上发生的电极反应为
(3)能说明氯气具有氧化性的实验现象是
(4)假定装入的饱和食盐水为50 mL(电解前后溶液体积变化可忽略),当测得的氢气为5.6 mL(已折算成标准状况)时,溶液的pH为
(5)工业上采用离子交换膜法电解饱和食盐水,如上图图2,该离子交换膜是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】锡及其化合物在生产、生活中有着重要的用途。已知: Sn的熔点为231℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为-33℃、沸点为114℃。请回答下列问题:
(1)元素锡比同主族碳的周期数大3,锡的原子序数为_________ 。
(2)用于微电子器件生产的锡粉纯度测定(已知锡的相对原子质量为119): ①取1.19g试样溶于稀硫酸中(杂质不参与反应),使Sn 完全转化为Sn2+;②加入过量的Fe2(SO4)3;③用0.1000mol/LK2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00mL。步骤②中加入Fe2(SO4)3的作用是________ ;此锡粉样品中锡的质量分数为_________ 。若在滴定终点时俯视读数,则会导致测得的样品中锡的质量分数________ (填“偏高“偏低”或“无影响”)。
(2)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:

①步骤I加入Sn粉的作用:____________ 及调节溶液pH。
②步骤II用到的玻璃仪器有烧杯、____________ 。
③步骤III生成SnO的离子方程式:____________ 。
④步骤IV中检验SnO是否洗涤干净的操作是____________ ,证明已洗净。
⑤步骤V操作依次为____________ 、____________ 过滤、洗涤、低温干燥。
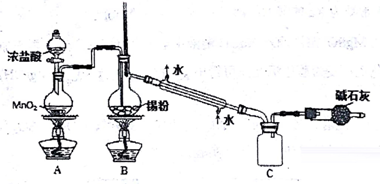
(4)实验室欲用下图装置制备少量SnCl4(夹持装置略),该装置存在明显缺陷,改进方法是____________ 。
(1)元素锡比同主族碳的周期数大3,锡的原子序数为
(2)用于微电子器件生产的锡粉纯度测定(已知锡的相对原子质量为119): ①取1.19g试样溶于稀硫酸中(杂质不参与反应),使Sn 完全转化为Sn2+;②加入过量的Fe2(SO4)3;③用0.1000mol/LK2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00mL。步骤②中加入Fe2(SO4)3的作用是
(2)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:

①步骤I加入Sn粉的作用:
②步骤II用到的玻璃仪器有烧杯、
③步骤III生成SnO的离子方程式:
④步骤IV中检验SnO是否洗涤干净的操作是
⑤步骤V操作依次为
(4)实验室欲用下图装置制备少量SnCl4(夹持装置略),该装置存在明显缺陷,改进方法是

您最近一年使用:0次
【推荐1】信息时代产生的大量电子垃圾对环境造成了极大的威胁.某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含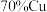 、
、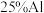 、
、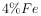 及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜晶体的路线:
及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜晶体的路线:
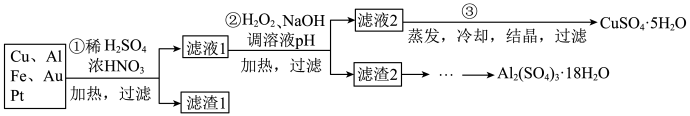
回答下列问题:
 第
第 步Cu与酸反应的离子方程式为
步Cu与酸反应的离子方程式为 ______ ;得到滤渣1的主要成分为 ______ .
 第
第 步加入
步加入 的作用是
的作用是 ______ ,使用 的优点是
的优点是 ______ ;调节pH的目的是使 ______ 生成沉淀.
 由滤渣2制取
由滤渣2制取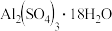 ,探究小组设计了三种方案:
,探究小组设计了三种方案:
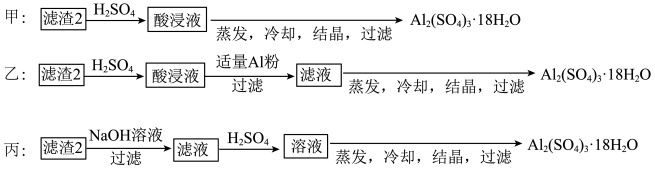
上述三种方案中,______ 方案不可行,原因是 ______ ;
 探究小组用滴定法测定
探究小组用滴定法测定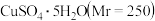 含量.取a g 试样配成100mL溶液,每次取
含量.取a g 试样配成100mL溶液,每次取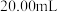 ,消除干扰离子后,用c
,消除干扰离子后,用c 
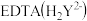 标准溶液滴定至终点,平均消耗EDTA溶液b
标准溶液滴定至终点,平均消耗EDTA溶液b  滴定反应如下:
滴定反应如下: 写出计算
写出计算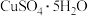 质量分数的表达式
质量分数的表达式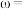
______ .
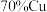 、
、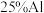 、
、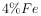 及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜晶体的路线:
及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜晶体的路线: 
回答下列问题:
 第
第 步Cu与酸反应的离子方程式为
步Cu与酸反应的离子方程式为  第
第 步加入
步加入 的作用是
的作用是  的优点是
的优点是  由滤渣2制取
由滤渣2制取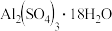 ,探究小组设计了三种方案:
,探究小组设计了三种方案: 
上述三种方案中,
 探究小组用滴定法测定
探究小组用滴定法测定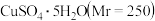 含量.取a g 试样配成100mL溶液,每次取
含量.取a g 试样配成100mL溶液,每次取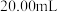 ,消除干扰离子后,用c
,消除干扰离子后,用c 
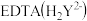 标准溶液滴定至终点,平均消耗EDTA溶液b
标准溶液滴定至终点,平均消耗EDTA溶液b  滴定反应如下:
滴定反应如下: 写出计算
写出计算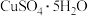 质量分数的表达式
质量分数的表达式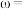
您最近一年使用:0次
【推荐2】废物利用有利于环境保护、资源节约,一种从废催化剂(含ZnO、CuO及少量石墨、Fe2O3及MnO2等)回收铜并制取活性氧化锌的工艺流程如图:
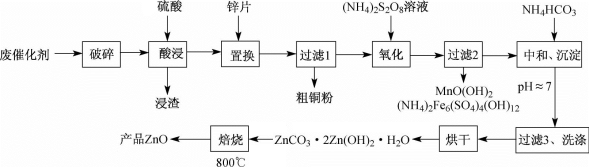
(1)为提高酸浸的速率,还可采取的措施为___ 。
(2)“氧化”时2molMn2+被氧化为MnO(OH)2,需要(NH4)2S2O8的物质的量为___ 。
(3)已知Zn(OH)2性质与Al(OH)3类似,在“中和、沉淀”时pH不能过大,请用文字结合离子方程式解释原因___ 。
(4)“过滤3、洗涤”时,对所得滤液蒸发浓缩、冷却结晶可得___ (填主要物质的化学式)固体。
(5)“焙烧”过程中化学方程式为___ 。
(6)经测定,1kg废催化剂可得160g粗铜粉,又知粗铜粉中铜的质量分数为80%,则废催化剂中铜的质量分数为___ %,若“酸浸”时硫酸浓度变小而又没有及时补充,则测定结果会比实际情况___ (填“偏大”“偏小”或“无影响”)。

(1)为提高酸浸的速率,还可采取的措施为
(2)“氧化”时2molMn2+被氧化为MnO(OH)2,需要(NH4)2S2O8的物质的量为
(3)已知Zn(OH)2性质与Al(OH)3类似,在“中和、沉淀”时pH不能过大,请用文字结合离子方程式解释原因
(4)“过滤3、洗涤”时,对所得滤液蒸发浓缩、冷却结晶可得
(5)“焙烧”过程中化学方程式为
(6)经测定,1kg废催化剂可得160g粗铜粉,又知粗铜粉中铜的质量分数为80%,则废催化剂中铜的质量分数为
您最近一年使用:0次
【推荐3】氧化铈 (CeO2) 是一种广泛应用的稀土氧化物。现以氟碳铈矿 (含 CeFCO3、BaO、SiO2等)为原料制备氧化铈,其工艺流程如图所示;
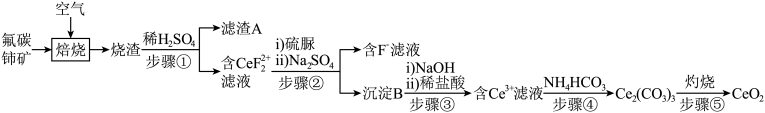
已知:
①稀土离子易与 形成复盐沉淀。
形成复盐沉淀。
②硫脲: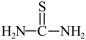 具有还原性,酸性条件下易被氧化为(SCN2H3)2.
具有还原性,酸性条件下易被氧化为(SCN2H3)2.
③Ce3+在空气中易被氧化为Ce4+,两者均能形成氢氧化物沉淀。
回答下列问题:
(1)“焙烧”时,氧化数据如表所示:
在对流空气氧化炉中可大大缩短氧化时间的原因是 ___________ 。
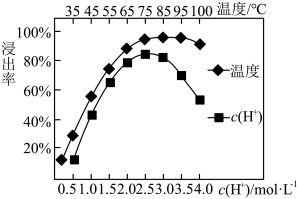
(2)焙烧后加入稀硫酸浸出,Ce的浸出率和稀硫酸浓度、温度有关,其关系如图所示,则使Ce的浸出率最高应该选择的条件是___________ 。
(3)加入硫脲的目的是将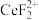 还原为Ce3+,反应的离子方程式为
还原为Ce3+,反应的离子方程式为 ___________ 。步骤③加入盐酸后,通常还需加另一种化学试剂X,根据题中信息推测___________ 。
(4)步骤④的离子方程式为___________ 。若“沉铈”中,Ce3+恰好沉淀完全[c(Ce3+)为1.0×10﹣5mol/L,此时溶液的pH为5,则溶液中c( )=
)=___________ mol/L(保留2位有效数字)。{已知常温下Ka1(H2CO3)=4.3×10﹣7,Ka2(H2CO3)=5.6×10﹣11,Ksp[Ce2(CO3)3]=1.0×10﹣28}。
(5)若Ce2(CO3)3经步骤⑤充分灼烧后质量减少5.8t,则获得CeO2的质量为___________ t。
(6)Ce4+溶液可以吸收大气中的污染物NOx减少空气污染,其转化过程如图所示(以NO2为例)该转化过程中的催化剂为___________ 。


已知:
①稀土离子易与
 形成复盐沉淀。
形成复盐沉淀。②硫脲:
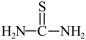 具有还原性,酸性条件下易被氧化为(SCN2H3)2.
具有还原性,酸性条件下易被氧化为(SCN2H3)2.③Ce3+在空气中易被氧化为Ce4+,两者均能形成氢氧化物沉淀。
回答下列问题:
(1)“焙烧”时,氧化数据如表所示:
| 空气氧化法 | 氧化温度/℃ | 氧化率/% | 氧化时间/h |
| 暴露空气中 | 450~500 | 80 | 14 |
| 对流空气氧化炉中 | 450~500 | 98 | 6 |
(2)焙烧后加入稀硫酸浸出,Ce的浸出率和稀硫酸浓度、温度有关,其关系如图所示,则使Ce的浸出率最高应该选择的条件是

(3)加入硫脲的目的是将
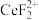 还原为Ce3+,反应的离子方程式为
还原为Ce3+,反应的离子方程式为 (4)步骤④的离子方程式为
 )=
)=(5)若Ce2(CO3)3经步骤⑤充分灼烧后质量减少5.8t,则获得CeO2的质量为
(6)Ce4+溶液可以吸收大气中的污染物NOx减少空气污染,其转化过程如图所示(以NO2为例)该转化过程中的催化剂为

您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】环己烯是合成赖氨酸、环己酮、苯酚等的重要原料,也常用作石油萃取剂及高辛烷值汽油稳定剂。
(一)制备环己烯的反应原理:
主反应: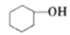

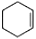 +H2O
+H2O
副反应:2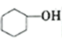

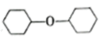 +H2O
+H2O
(二)查阅实验所涉及的反应物、催化剂、产物的各种物理性质,列表如下:
(三)实验流程

(四)制备环己烯的实验装置图如图(夹持装置及加热装置已省略):
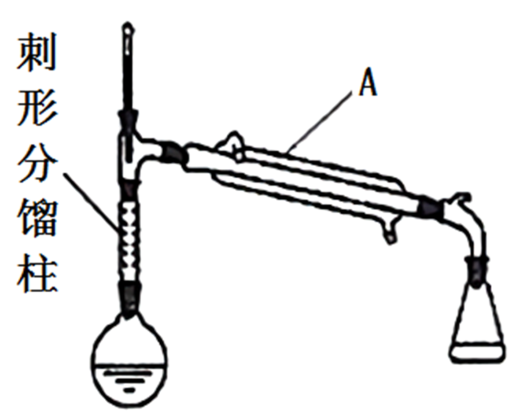
请回答:
(1)仪器A的名称是______ 。
(2)实验中不用浓硫酸,而用85% H3PO4溶液,说明理由_______ 。(写出一条即可)
(3)文献资料要求本实验的反应温度接近但又不超过90℃,根据图表数据分析其原因是_____ 。
(4)将较纯净环己烯样品按如图装置蒸馏,蒸馏时要加入生石灰,目的是____ 。
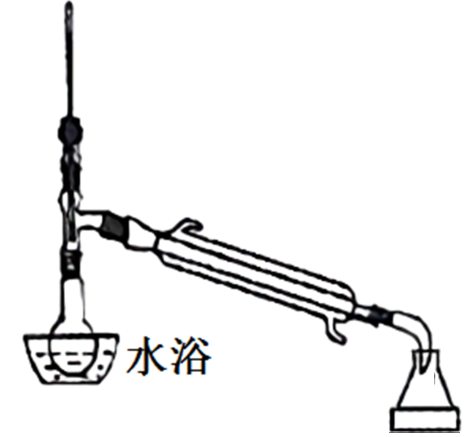
(5)在定条件下,向8.2 g环己烯样品中加入0.1 mol Br2,与环己烯充分反应后,剩余的Br2与足量KI作用生I2,用0.1 mol/L的Na2S2O3标准溶液滴定,发生反应:I2+2S2O = S4O
= S4O +2I-。终点时消耗Na2S2O3标准溶液40. 00ml (以上数据均已扣除干扰因素):
+2I-。终点时消耗Na2S2O3标准溶液40. 00ml (以上数据均已扣除干扰因素):
①滴定所用指示剂为______ , 样品中环己烯的质量分数为____ 。
②下列情况会导致测定结果偏低的是____ (填序号)。
a.在测定过程中部分环己烯挥发
b.样品中含有苯酚杂质
c.Na2S2O3标准溶液部分被氧化
d.滴定后读数时,俯视刻度线
(一)制备环己烯的反应原理:
主反应:


 +H2O
+H2O副反应:2


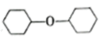 +H2O
+H2O(二)查阅实验所涉及的反应物、催化剂、产物的各种物理性质,列表如下:
| 沸点/℃ | 密度/(g· cm3) | 水中溶解性 | |
| 环己醇 | 161 | 0.962 4 | 可溶于水 |
| 环己烯 | 83 | 0.811 | 微溶于水 |
| 85%H3PO4溶液 | 1.69 | 易溶于水 | |
| 环己烯与水形成的共沸物(含水10%) | 70.8 | ||
| 环己醇与水形成的共沸物(含水80%) | 97.8 |

(四)制备环己烯的实验装置图如图(夹持装置及加热装置已省略):

请回答:
(1)仪器A的名称是
(2)实验中不用浓硫酸,而用85% H3PO4溶液,说明理由
(3)文献资料要求本实验的反应温度接近但又不超过90℃,根据图表数据分析其原因是
(4)将较纯净环己烯样品按如图装置蒸馏,蒸馏时要加入生石灰,目的是

(5)在定条件下,向8.2 g环己烯样品中加入0.1 mol Br2,与环己烯充分反应后,剩余的Br2与足量KI作用生I2,用0.1 mol/L的Na2S2O3标准溶液滴定,发生反应:I2+2S2O
 = S4O
= S4O +2I-。终点时消耗Na2S2O3标准溶液40. 00ml (以上数据均已扣除干扰因素):
+2I-。终点时消耗Na2S2O3标准溶液40. 00ml (以上数据均已扣除干扰因素):①滴定所用指示剂为
②下列情况会导致测定结果偏低的是
a.在测定过程中部分环己烯挥发
b.样品中含有苯酚杂质
c.Na2S2O3标准溶液部分被氧化
d.滴定后读数时,俯视刻度线
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】柠檬酸铁铵[(NH4)3Fe( C6 H5O7)2,摩尔质量488 g/mol] 是一种重要的食品添加剂。一种制备柠檬酸铁铵的实验步骤如下:
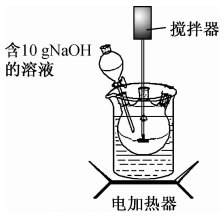
步骤1.在右图三颈烧瓶中加入16.7 g FeSO4·7H2O、40 ml.蒸馏水,3mL硫酸和1 g NaClO3,强力搅拌;
步骤2.升温至80℃,再补加l g NaClO3;
步骤3.向反应器中加入NaOH溶液,温度控制在80~90℃,剧烈搅拌;
步骤4.过滤,洗涤,沥干,得活性Fe(OH)3;
步骤5.将Fe(OH)3和一定量的水加入三颈烧瓶中,控制95℃以上,加入计算量的柠檬酸溶液,搅拌,并保温1h;
步骤6.冷却到50℃,搅拌下加入氨水40 mL,静置、浓缩至膏状,80℃干燥得柠檬酸铁铵24.9 g。
回答下列问题:
(1)步骤1发生反应的离子方程式为_____________________________ 。
(2)步骤2再补加NaClO3的目的是_____________________________ 。
(3)步骤3确定Fe3+已沉淀完全的方法是_____________________________ 。
(4)步骤4过滤时,所需硅酸盐质仪器除烧杯外,还需要_____________________________ ;证明Fe(OH)3已被洗涤干净的方法为__________________________ 。
(5)柠檬酸铁铵的产率为_________ (结果保留三位有效数字)。

步骤1.在右图三颈烧瓶中加入16.7 g FeSO4·7H2O、40 ml.蒸馏水,3mL硫酸和1 g NaClO3,强力搅拌;
步骤2.升温至80℃,再补加l g NaClO3;
步骤3.向反应器中加入NaOH溶液,温度控制在80~90℃,剧烈搅拌;
步骤4.过滤,洗涤,沥干,得活性Fe(OH)3;
步骤5.将Fe(OH)3和一定量的水加入三颈烧瓶中,控制95℃以上,加入计算量的柠檬酸溶液,搅拌,并保温1h;
步骤6.冷却到50℃,搅拌下加入氨水40 mL,静置、浓缩至膏状,80℃干燥得柠檬酸铁铵24.9 g。
回答下列问题:
(1)步骤1发生反应的离子方程式为
(2)步骤2再补加NaClO3的目的是
(3)步骤3确定Fe3+已沉淀完全的方法是
(4)步骤4过滤时,所需硅酸盐质仪器除烧杯外,还需要
(5)柠檬酸铁铵的产率为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】醋酸亚铬[(CH3COO)2Cr·2H2O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图所示。回答下列问题:
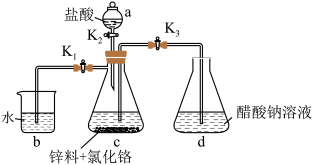
(1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是____________________________ 。仪器a的名称是________ 。
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置。打开K1、K2,关闭K3。
①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为_________________________________ 。
②同时c中有气体产生,该气体的作用是________________________________________ 。
(3)将三价铬还原为二价铬后,将c中溶液流入d的操作是_________________________ 。

(1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置。打开K1、K2,关闭K3。
①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为
②同时c中有气体产生,该气体的作用是
(3)将三价铬还原为二价铬后,将c中溶液流入d的操作是
您最近一年使用:0次



