随着汽车数量的逐年增多,汽车尾气污染已成为突出的环境问题之一。反应:2NO(g)+2CO(g)  2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是 ( )
2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是 ( )
 2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是 ( )
2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是 ( )| A.提高尾气净化速率的常用方法是降低温度 |
| B.提高尾气净化速率的最佳途径是研制高效催化剂 |
| C.装有尾气净化装置的汽车排出的气体中不再含有NO或CO |
| D.570 K时及时抽走CO2、N2,平衡常数将会增大,尾气净化效率更佳 |
更新时间:2019-10-29 21:51:13
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列实验过程能达到目的,且现象和结论正确的是
| 选项 | 实验目的 | 实验过程 | 现象和结论 |
| A | 比较 和 和 的 的 大小 大小 | 向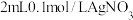 溶液中滴2滴 溶液中滴2滴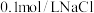 溶液,产生白色沉淀后再滴加2滴 溶液,产生白色沉淀后再滴加2滴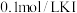 溶液 溶液 | 又生成黄色沉淀,说明: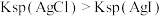 |
| B | 探究不同催化剂对反应速率的影响 | 在两支大小相同的试管中均加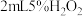 溶液,分别滴入2滴 溶液,分别滴入2滴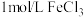 溶液和 溶液和 溶液 溶液 | 加 溶液的试管产生气泡速率更快,说明催化效果 溶液的试管产生气泡速率更快,说明催化效果 |
| C | 比较 和 和 的酸性强弱 的酸性强弱 | 量取一定浓度 溶液,滴加少量稀醋酸 溶液,滴加少量稀醋酸 | 无气泡产生,说明酸性: |
| D | 探究可逆反应的热效应 | 已知 溶液中存在下列平衡: 溶液中存在下列平衡: , ,取一定浓度的  溶液,升高温度, 溶液,升高温度, | 溶液由蓝色变为黄色,说明该反应 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列叙述中不正确的是
| A.可逆反应设计成双液电池,当反应达平衡时,外电路上没有电流通过 |
| B.将NO2、N2O4平衡混合气体的体积压缩为原来的一半,新平衡后气体颜色加深 |
| C.利用盖斯定律,可以计算某些难以直接测量的反应焓变 |
| D.抗腐蚀的金属一定排在金属活动性顺序表氢元素之后 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】一定温度下,在3个体积均为1L的恒容密闭容器中发生反应:CO(g)+H2S(g)  COS(g)+H2(g) △H=a kJ·mol﹣1达到平衡时,数据如下表:
COS(g)+H2(g) △H=a kJ·mol﹣1达到平衡时,数据如下表:
下列说法正确的是
 COS(g)+H2(g) △H=a kJ·mol﹣1达到平衡时,数据如下表:
COS(g)+H2(g) △H=a kJ·mol﹣1达到平衡时,数据如下表:| 容器编号 | 温度/K | 物质的起始浓度/mol·L﹣1 | 物质的平衡浓度/mol·L﹣1 | |||
| CO(g) | H2S(g) | COS(g) | H2(g) | COS(g) | ||
| 1 | T1 | 10.0 | 7.0 | 0 | 0 | 2.0 |
| 2 | T1 | 5.0 | 3.5 | 0 | 0 | |
| 3 | T2 | 3.0 | 0 | 7.0 | 7.0 | 1.5 |
| A.若T1<T2,则a>0 |
| B.T1K时,该反应的平衡常数K=10 |
| C.容器1中CO的平衡转化率比容器2小 |
| D.容器3中反应达到平衡后,再充入稀有气体氦气,平衡不移动 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】在一密闭容器中进行如下反应:A(g)+B(g)⇌2C(g)+2D,此反应符合图(其中C%是混合物中C的质量分数,t为反应时间)对此反应的叙述正确的是( )
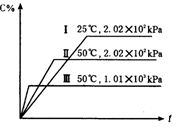

| A.正反应为吸热反应,D是固体 |
| B.正反应为吸热反应,D是气体 |
| C.正反应为放热反应,D是固体或液体 |
| D.正反应为放热反应,D是气体 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:C(s)+2NO(g) CO(g)+N2(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是( )
CO(g)+N2(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是( )

 CO(g)+N2(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是( )
CO(g)+N2(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是( )
| A.该反应的△H>0 |
| B.若该反应在T1、T2℃时的平衡常数分别为K1、K2,则K1<K2 |
| C.在T2℃时,若反应体系处于状态D,则此时v正>v逆 |
| D.若状态B、C、D的速率分别为v(B)、 v(C)、 v(D),则v(C)=v(D)>v(B) |
您最近半年使用:0次

 2SO3,2体积SO2与足量O2反应,能生成2体积SO3
2SO3,2体积SO2与足量O2反应,能生成2体积SO3 2HI(g) 在450℃时,其平衡常数为49;则反应HI(g)
2HI(g) 在450℃时,其平衡常数为49;则反应HI(g) 

