在T℃时,向1 L固定体积的密闭容器M中加入2 mol X和1 mol Y,发生如下反应:2X(g)+Y(g)  aZ(g)+W(g) ΔH=-Q kJ/mol(Q>0);该反应达到平衡后,放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小。请回答下列问题:
aZ(g)+W(g) ΔH=-Q kJ/mol(Q>0);该反应达到平衡后,放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小。请回答下列问题:
(1)化学计量数a的值为________ 。
(2)下列能说明该反应达到了化学平衡状态的是________ (填序号)。
a.容器内压强一定 b.容器内气体的密度一定
c.容器内Z的分子数一定 d.容器内气体的质量一定
(3)维持T℃温度不变,若起始时向容器M中加入2 mol X、1 mol Y和1 mol Ar(稀有气体不参与反应),则反应达到平衡后放出的热量是________ kJ。
(4)维持T℃温度不变,若在一个和原容器体积相等的恒压容器N中加入2 mol X和1 mol Y,发生题给反应并达到平衡,则________ (填“M”或“N”)容器中的反应先达到平衡状态,容器中X的质量分数M________ N(填“>”、“<”或“=”)。
(5)已知:该反应的平衡常数随温度的变化情况如表所示:
若在某温度下,2 mol X和1 mol Y在容器M中反应并达到平衡,X的平衡转化率为50%,则该温度为________ ℃。
 aZ(g)+W(g) ΔH=-Q kJ/mol(Q>0);该反应达到平衡后,放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小。请回答下列问题:
aZ(g)+W(g) ΔH=-Q kJ/mol(Q>0);该反应达到平衡后,放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小。请回答下列问题:(1)化学计量数a的值为
(2)下列能说明该反应达到了化学平衡状态的是
a.容器内压强一定 b.容器内气体的密度一定
c.容器内Z的分子数一定 d.容器内气体的质量一定
(3)维持T℃温度不变,若起始时向容器M中加入2 mol X、1 mol Y和1 mol Ar(稀有气体不参与反应),则反应达到平衡后放出的热量是
(4)维持T℃温度不变,若在一个和原容器体积相等的恒压容器N中加入2 mol X和1 mol Y,发生题给反应并达到平衡,则
(5)已知:该反应的平衡常数随温度的变化情况如表所示:
| 温度/℃ | 200 | 250 | 300 | 350 |
| 平衡常数K | 9.94 | 5.2 | 1 | 0.5 |
若在某温度下,2 mol X和1 mol Y在容器M中反应并达到平衡,X的平衡转化率为50%,则该温度为
更新时间:2019-11-14 09:59:39
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】近日,中国科学技术大学的江海龙教授调控催化剂中钴的价态,高选择性进行光催化还原CO2制备HCOOH。
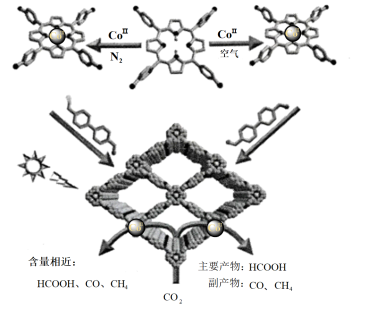
回答下列问题:
(1)根据图示可知,Co(II) →Co( III)中氧化剂是___________ ( 填化学式)。含Co(II)的催化剂对HCOOH的选择性___________ (填“ 高于”“低于”或“等于”)含Co( III)的催化剂。
(2)COF -367 – CoII和COF - 367 – CoIII催化CO2还原生成HCOOH的能垒图分别为a和b.注明: *代表吸附在催化剂表面,TS代表过渡态,能量单位为eV。

①CO2* +2H* =HCOOH * ΔH___________ 0(填“>”“<”或“=”)。
②在生成上述过渡态(TS)中,能垒最大为___________ eV。 COF - 367 – CoII和COF - 367 – CoIII中催化效能较高的是___________ (填“前者”或“后者”)。
(3)某催化剂作用下,CO2(g) + H2(g) HCOOH(g)的速率方程为 v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH)(k正、k逆为速率常数,只与温度、催化剂有关,与浓度无关)。某温度下,在容积均为2 L的恒容密闭容器甲、乙中投入下列物质,测得数据如表所示。
HCOOH(g)的速率方程为 v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH)(k正、k逆为速率常数,只与温度、催化剂有关,与浓度无关)。某温度下,在容积均为2 L的恒容密闭容器甲、乙中投入下列物质,测得数据如表所示。
 =
=___________ ,α___________ 50%(填“>”“<”或“=”)。
(4)在某催化剂作用下,向2 L恒容密闭反应器中充入1 mol CO2和2 mol H2发生如下反应:
主反应:CO2(g) +H2(g) HCOOH(g) ΔH >0
HCOOH(g) ΔH >0
副反应:CO2(g) +4H2(g) CH4(g) +2H2O(g) ΔH <0
CH4(g) +2H2O(g) ΔH <0
测得CO2的平衡转化率、HCOOH的选择性与温度关系如图所示。
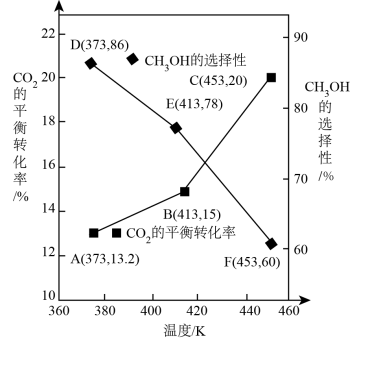
①已知:选择性等于HCOOH的物质的量与CO2转化的物质的量之比。其他条件不变,升高温度, CO2的平衡转化率增大的原因是___________ 。
②已知F点压强为27.2 kPa,主反应在F点对应的温度下,压强平衡常数Kp=___________ kPa-1(结果保留两位有效数字)。

回答下列问题:
(1)根据图示可知,Co(II) →Co( III)中氧化剂是
(2)COF -367 – CoII和COF - 367 – CoIII催化CO2还原生成HCOOH的能垒图分别为a和b.注明: *代表吸附在催化剂表面,TS代表过渡态,能量单位为eV。

①CO2* +2H* =HCOOH * ΔH
②在生成上述过渡态(TS)中,能垒最大为
(3)某催化剂作用下,CO2(g) + H2(g)
 HCOOH(g)的速率方程为 v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH)(k正、k逆为速率常数,只与温度、催化剂有关,与浓度无关)。某温度下,在容积均为2 L的恒容密闭容器甲、乙中投入下列物质,测得数据如表所示。
HCOOH(g)的速率方程为 v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH)(k正、k逆为速率常数,只与温度、催化剂有关,与浓度无关)。某温度下,在容积均为2 L的恒容密闭容器甲、乙中投入下列物质,测得数据如表所示。| 容器 | 起始投料/ mol | CO2的平衡转化率 | ||
| CO2 | H2 | HCOOH | ||
| 甲 | 1.0 | 1.0 | 0 | 50% |
| 乙 | 2.0 | 2.0 | 0 | α |
 =
=(4)在某催化剂作用下,向2 L恒容密闭反应器中充入1 mol CO2和2 mol H2发生如下反应:
主反应:CO2(g) +H2(g)
 HCOOH(g) ΔH >0
HCOOH(g) ΔH >0副反应:CO2(g) +4H2(g)
 CH4(g) +2H2O(g) ΔH <0
CH4(g) +2H2O(g) ΔH <0 测得CO2的平衡转化率、HCOOH的选择性与温度关系如图所示。

①已知:选择性等于HCOOH的物质的量与CO2转化的物质的量之比。其他条件不变,升高温度, CO2的平衡转化率增大的原因是
②已知F点压强为27.2 kPa,主反应在F点对应的温度下,压强平衡常数Kp=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】利用合成氨生产尿素[CO(NH2)2]是重要的化学工艺。在3个2L的密闭容器中,使用相同的催化剂,按不同方式投入反应物,分别进行反应:3H2(g)+N2(g) 2NH3(g)。保持恒温、恒容,测得反应达到平衡时有关数据如下:
2NH3(g)。保持恒温、恒容,测得反应达到平衡时有关数据如下:
(1)下列各项能说明该反应已达到平衡状态的是____________ (填写序号字母).
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
(2)容器乙中反应从开始到达平衡的反应速率为v(H2)=_________
(3)在该温度下甲容器中反应的平衡常数K________ (用含c1的代数式表示).
(4)分析上表数据,下列关系正确的是_________ (填序号):
a.2c1>1.5mol/L b.2ρ1=ρ2 c.ω3=ω1 d.K甲=K乙=K丙
(5)氨和尿素溶液都可以吸收硝酸工业尾气中的NO、NO2,将其转化为N2.写出尿素与NO、NO2三者等物质的量反应的化学方程式__________________ .
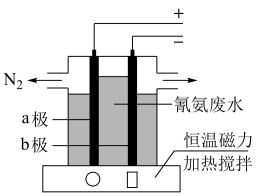
(6)氨氮废水(含NH3、NaOH和Na2SO4)超标排放会造成水体富营养化.如图通过直接电化学法能有效除去废水中的氨.其中阴离子的流动方向为__________ (填“a极”或“b极”),电解过程中,b极区的pH_____________ (填“增大”或“减小”或“不变”),阳极反应方程式为__________ .
 2NH3(g)。保持恒温、恒容,测得反应达到平衡时有关数据如下:
2NH3(g)。保持恒温、恒容,测得反应达到平衡时有关数据如下:| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3mol H2、2mol N2 | 6mol H2、4molN2 | 2molNH3 |
| 达到平衡的时间/min | 5 | 8 | |
| 平衡时N2的浓度/mol·L-1 | c1 | 1.5 | |
| NH3的体积分数 | ω1 | ω3 | |
| 混合气体密度/g·L-1 | ρ1 | ρ2 | |
| 平衡常数/L2·mol-2 | K甲 | K乙 | K丙 |
(1)下列各项能说明该反应已达到平衡状态的是
a.容器内N2、H2、NH3的浓度之比为1:3:2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
(2)容器乙中反应从开始到达平衡的反应速率为v(H2)=
(3)在该温度下甲容器中反应的平衡常数K
(4)分析上表数据,下列关系正确的是
a.2c1>1.5mol/L b.2ρ1=ρ2 c.ω3=ω1 d.K甲=K乙=K丙
(5)氨和尿素溶液都可以吸收硝酸工业尾气中的NO、NO2,将其转化为N2.写出尿素与NO、NO2三者等物质的量反应的化学方程式
(6)氨氮废水(含NH3、NaOH和Na2SO4)超标排放会造成水体富营养化.如图通过直接电化学法能有效除去废水中的氨.其中阴离子的流动方向为

您最近一年使用:0次
【推荐3】煤和石油通常都含有硫的化合物,燃烧生成的二氧化硫成为大气主要污染物之一。二氧化硫的治理已成为当前研究的课题。其催化氧化的过程如图1所示:

Ⅰ.已知:
①SO2(g)+V2O5(s) SO3(g)+V2O4(s) ΔH1=+24kJ•mol-1
SO3(g)+V2O4(s) ΔH1=+24kJ•mol-1
②2V2O4(s)+O2(g) 2V2O5(s) ΔH2=-244kJ•mol-1
2V2O5(s) ΔH2=-244kJ•mol-1
(1)2SO2(g)+O2(g) 2SO3(g) ΔH3=
2SO3(g) ΔH3=___ kJ•mol-1=___ (用字母E1~E6表示)kJ•mol-1。
(2)反应速率一般由慢反应决定,从图1中分析决定V2O5催化氧化SO2的反应速率的是反应___ (填“①”或“②”)。
Ⅱ.二氧化硫的催化氧化是工业上生产硫酸的主要反应。为研究该反应,某同学设计了以下三种已装固体V2O5催化剂的密闭容器装置:

(3)在初始体积与温度相同的条件下,甲、乙、丙中均按2molSO2、1molO2投料,达平衡时,三个容器中SO2的转化率从大到小的顺序为___ (用“甲、乙、丙”表示)。
(4)在容器丙中,0.1MPa条件下,在不同温度或不同投料方式下研究上述反应得到数据如表:
①表中:a=___ ;b=___ 。
②已知用平衡分压(分压=总压×物质的量分数)代替平衡浓度计算,得到的平衡常数即为压强平衡常数,则Kp1=___ ;Kp1___ Kp2(填“>”、“<”或“=”)。
③451℃时,若按0.4molSO2、0.4molO2、0.4molSO3进行投料,则反应开始时v正(SO2)___ v逆(SO2)(填“>”、“<”或“=”)。

Ⅰ.已知:
①SO2(g)+V2O5(s)
 SO3(g)+V2O4(s) ΔH1=+24kJ•mol-1
SO3(g)+V2O4(s) ΔH1=+24kJ•mol-1②2V2O4(s)+O2(g)
 2V2O5(s) ΔH2=-244kJ•mol-1
2V2O5(s) ΔH2=-244kJ•mol-1(1)2SO2(g)+O2(g)
 2SO3(g) ΔH3=
2SO3(g) ΔH3=(2)反应速率一般由慢反应决定,从图1中分析决定V2O5催化氧化SO2的反应速率的是反应
Ⅱ.二氧化硫的催化氧化是工业上生产硫酸的主要反应。为研究该反应,某同学设计了以下三种已装固体V2O5催化剂的密闭容器装置:

(3)在初始体积与温度相同的条件下,甲、乙、丙中均按2molSO2、1molO2投料,达平衡时,三个容器中SO2的转化率从大到小的顺序为
(4)在容器丙中,0.1MPa条件下,在不同温度或不同投料方式下研究上述反应得到数据如表:
| 实验序号 | A组 | B组 | C组 |
| 反应温度 | 451℃ | 451℃ | 551℃ |
| 投料方式(按照SO2、O2、SO3的顺序) | 2mol、1mol、0mol | 0mol、0mol、2mol | 2mol、1mol、0mol |
| 含硫化合物的转化率 | 60% | b | c |
| 反应的热量变化 | 放热a | 吸热78.4kJ | 放热d |
| 压强平衡常数(Kp) | Kp1 | Kp1 | Kp2 |
①表中:a=
②已知用平衡分压(分压=总压×物质的量分数)代替平衡浓度计算,得到的平衡常数即为压强平衡常数,则Kp1=
③451℃时,若按0.4molSO2、0.4molO2、0.4molSO3进行投料,则反应开始时v正(SO2)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】已知反应:
 kJ/mol可以有效转化汽车尾气。在密闭容器中充入2 mol CO和2 mol NO,平衡时NO的体积分数与温度、压强的关系如图所示;
kJ/mol可以有效转化汽车尾气。在密闭容器中充入2 mol CO和2 mol NO,平衡时NO的体积分数与温度、压强的关系如图所示;
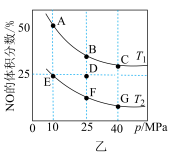
(1)充分反应达到平衡后,放出的热量Q___________ 746.5 kJ(选填“大于”、“小于”、“等于”)
(2)据图分析可知,
________  (选填“大于”、“小于”、“等于”);反应平衡后,改变以下条件能使速率和两种污染气体转化率都增大的是___________(填标号)
(选填“大于”、“小于”、“等于”);反应平衡后,改变以下条件能使速率和两种污染气体转化率都增大的是___________(填标号)
A.压缩容器体积 B.升高温度 C.恒压充入氦气 D.加入催化剂
(3)反应在D点达平衡后,若此时降低温度,同时压缩容器体积,在重新达到平衡过程中,D点会向A~G点中的___________ 点方向移动。
(4)工业上可用C与水蒸气在高温下制CO,反应原理为:
 。若向1 L容积不变的密闭容器中,加入24 g C,并使之均匀地平铺在容器底部,然后再加入18 g
。若向1 L容积不变的密闭容器中,加入24 g C,并使之均匀地平铺在容器底部,然后再加入18 g  ,发生上述反应。达到平衡后,测得
,发生上述反应。达到平衡后,测得 的浓度为0.75 mol/L。若按如下配比改变起始加入量,则达到平衡后,
的浓度为0.75 mol/L。若按如下配比改变起始加入量,则达到平衡后, 的浓度仍为0.75 mol/L的是___________(填字母)。
的浓度仍为0.75 mol/L的是___________(填字母)。
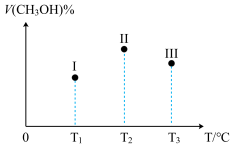
(5)工业上可用CO制备甲醇( )。原理为:
)。原理为:
 。
。
在Ⅰ、Ⅱ、Ⅲ三个相同密闭容器中充入相同的CO和 ,三个容器的反应温度分别为
,三个容器的反应温度分别为 、
、 、
、 且恒定不变,在其它条件相同的情况下,实验测得反应均进行到t min时
且恒定不变,在其它条件相同的情况下,实验测得反应均进行到t min时 的体积分数如图所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定处于化学平衡状态的是
的体积分数如图所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定处于化学平衡状态的是___________ 。据此判断上述反应的
___________ (填“>”或“<”)0。
(6)CO可用于工业炼铁。原理为: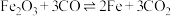 。在T℃、2 L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
。在T℃、2 L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
若甲容器中CO的平衡转化率为60%。则T℃时,乙容器中CO的平衡转化率为___________ 。

 kJ/mol可以有效转化汽车尾气。在密闭容器中充入2 mol CO和2 mol NO,平衡时NO的体积分数与温度、压强的关系如图所示;
kJ/mol可以有效转化汽车尾气。在密闭容器中充入2 mol CO和2 mol NO,平衡时NO的体积分数与温度、压强的关系如图所示;
(1)充分反应达到平衡后,放出的热量Q
(2)据图分析可知,

 (选填“大于”、“小于”、“等于”);反应平衡后,改变以下条件能使速率和两种污染气体转化率都增大的是___________(填标号)
(选填“大于”、“小于”、“等于”);反应平衡后,改变以下条件能使速率和两种污染气体转化率都增大的是___________(填标号)A.压缩容器体积 B.升高温度 C.恒压充入氦气 D.加入催化剂
(3)反应在D点达平衡后,若此时降低温度,同时压缩容器体积,在重新达到平衡过程中,D点会向A~G点中的
(4)工业上可用C与水蒸气在高温下制CO,反应原理为:

 。若向1 L容积不变的密闭容器中,加入24 g C,并使之均匀地平铺在容器底部,然后再加入18 g
。若向1 L容积不变的密闭容器中,加入24 g C,并使之均匀地平铺在容器底部,然后再加入18 g  ,发生上述反应。达到平衡后,测得
,发生上述反应。达到平衡后,测得 的浓度为0.75 mol/L。若按如下配比改变起始加入量,则达到平衡后,
的浓度为0.75 mol/L。若按如下配比改变起始加入量,则达到平衡后, 的浓度仍为0.75 mol/L的是___________(填字母)。
的浓度仍为0.75 mol/L的是___________(填字母)。A. | B.2 mol CO+2 mol  |
C.0.5 mol CO+0.5 mol  | D.27 g 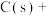 9 g 9 g  0.5 mol 0.5 mol 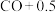 mol mol  |
(5)工业上可用CO制备甲醇(
 )。原理为:
)。原理为:
 。
。在Ⅰ、Ⅱ、Ⅲ三个相同密闭容器中充入相同的CO和
 ,三个容器的反应温度分别为
,三个容器的反应温度分别为 、
、 、
、 且恒定不变,在其它条件相同的情况下,实验测得反应均进行到t min时
且恒定不变,在其它条件相同的情况下,实验测得反应均进行到t min时 的体积分数如图所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定处于化学平衡状态的是
的体积分数如图所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定处于化学平衡状态的是

(6)CO可用于工业炼铁。原理为:
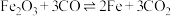 。在T℃、2 L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
。在T℃、2 L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。 | CO | Fe |  | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |
您最近一年使用:0次
【推荐2】2022年中国的汽车保有量达到3亿辆,如何在提供交通便利同时,缓解环境问题,是化学工作者研究的重要课题。
I.汽车安装尾气净化装置,可使CO和NO发生反应2NO(g)+2CO(g) N2(g)+2CO2(g)。
N2(g)+2CO2(g)。
(1)已知:
N2(g)+O2(g)=2NO(g) △H=+180kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H=-566kJ·mol-1
则2CO(g)+2NO(g)=N2(g)+2CO2 △H=_______ kJ·mol-1。
(2)为探究温度及不同催化剂对此反应的影响,分别在不同温度、不同催化剂(甲、乙)条件下,保持其他初始条件不变,重复实验,在相同时间内测得NO的转化率与温度的关系如图所示,结合图象,最合适的反应条件为_______ 。

(3)实验测得此反应:v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数_______ (填“大于”“小于”或“等于”)k逆增大的倍数。
②若在2L的容器中充入1molCO和1molNO,在一定温度下达到平衡时,达平衡时总压为起始时的0.9倍,则 =
=_______ 。(保留小数点后两位)
II.使用氢能源汽车可以从根源上解决汽车尾气污染问题。“制氢”“储氢”“用氢”一直都是能源研究的热点。当前,氨电解法制氢气取得了重要技术突破,利用电解原理,将氨转化为高纯氢气,其装置如图所示。

(4)电解过程中OH-的移动方向为_______ (填“从左往右”或“从右往左”);阳极的电极反应式为_______ 。
(5)上述方法制备H2所需能量可由太阳能提供。利用Na2CO3·10H2O可将太阳能储存,释放,结合方程式说明储存、释放太阳能的原理:_______ 。
I.汽车安装尾气净化装置,可使CO和NO发生反应2NO(g)+2CO(g)
 N2(g)+2CO2(g)。
N2(g)+2CO2(g)。(1)已知:
N2(g)+O2(g)=2NO(g) △H=+180kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H=-566kJ·mol-1
则2CO(g)+2NO(g)=N2(g)+2CO2 △H=
(2)为探究温度及不同催化剂对此反应的影响,分别在不同温度、不同催化剂(甲、乙)条件下,保持其他初始条件不变,重复实验,在相同时间内测得NO的转化率与温度的关系如图所示,结合图象,最合适的反应条件为

(3)实验测得此反应:v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数
②若在2L的容器中充入1molCO和1molNO,在一定温度下达到平衡时,达平衡时总压为起始时的0.9倍,则
 =
=II.使用氢能源汽车可以从根源上解决汽车尾气污染问题。“制氢”“储氢”“用氢”一直都是能源研究的热点。当前,氨电解法制氢气取得了重要技术突破,利用电解原理,将氨转化为高纯氢气,其装置如图所示。

(4)电解过程中OH-的移动方向为
(5)上述方法制备H2所需能量可由太阳能提供。利用Na2CO3·10H2O可将太阳能储存,释放,结合方程式说明储存、释放太阳能的原理:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】二甲醚( )是一种重要的燃料和化工原料。回答下列问题:
)是一种重要的燃料和化工原料。回答下列问题:
(1)工业上一种合成二甲醚的反应如下:
反应Ⅰ:
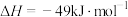
反应Ⅱ: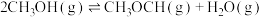

反应Ⅲ: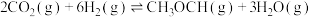

反应Ⅲ的
_______  。
。
(2)反应Ⅰ在起始物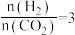 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为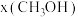 ,在
,在 下的
下的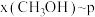 的曲线以及在
的曲线以及在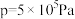 下的
下的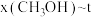 的曲线如图所示。
的曲线如图所示。
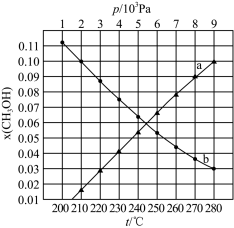
①图中对应恒温过程的曲线是_______ (填“a”或“b”)。
②当 的平衡转化率为
的平衡转化率为 时,
时,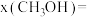
_______ ,反应条件可能为_______ 或_______ 。
(3)往一容积为2L的恒容密闭容器中通入2mol 和6mol
和6mol ,一定温度下发生反应Ⅲ,起始总压强为
,一定温度下发生反应Ⅲ,起始总压强为 ,反应达到平衡时测得
,反应达到平衡时测得 的物质的量分数为12.5%,该温度下,反应的平衡常数
的物质的量分数为12.5%,该温度下,反应的平衡常数
_______ 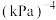 (用含p0的式子表达,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用含p0的式子表达,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 )是一种重要的燃料和化工原料。回答下列问题:
)是一种重要的燃料和化工原料。回答下列问题:(1)工业上一种合成二甲醚的反应如下:
反应Ⅰ:

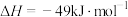
反应Ⅱ:
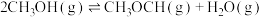

反应Ⅲ:
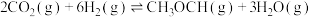

反应Ⅲ的

 。
。(2)反应Ⅰ在起始物
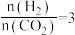 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为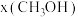 ,在
,在 下的
下的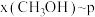 的曲线以及在
的曲线以及在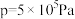 下的
下的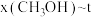 的曲线如图所示。
的曲线如图所示。
①图中对应恒温过程的曲线是
②当
 的平衡转化率为
的平衡转化率为 时,
时,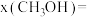
(3)往一容积为2L的恒容密闭容器中通入2mol
 和6mol
和6mol ,一定温度下发生反应Ⅲ,起始总压强为
,一定温度下发生反应Ⅲ,起始总压强为 ,反应达到平衡时测得
,反应达到平衡时测得 的物质的量分数为12.5%,该温度下,反应的平衡常数
的物质的量分数为12.5%,该温度下,反应的平衡常数
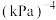 (用含p0的式子表达,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用含p0的式子表达,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
您最近一年使用:0次
【推荐1】研究和深度开发 CO、CO2的应用对构建生态文明社会具有重要的意义。回答下列问题:
Ⅰ.CO 可用于高炉炼铁
已知: Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g) △H1=akJ/mol;
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H2=bkJ/mol;
则反应 Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)的 △H3=______________ kJ/mol(用含 a、b 的代数式表示)。
Ⅱ.一定条件下,CO2和 CO 可以互相转化
(1)某温度下,在容积为 2 L 的密闭容器按甲、乙两种方式投入反应物发生反应:CO2(g)+H2(g)⇌CO(g)+H2O(g)。
甲容器 15min 后达到平衡,此时 CO2的转化率为 75%.则 0~15min 内平均反应速率 v(CO2)=____________ mol/(L·min),此条件下该反应的平衡常数 K=______________ 。欲使平衡后乙与甲中相同组分气体的体积分数相等,则ω、x、y、z 需满足的关系是 y _____________ z(填“>”、“<”或“=”),且 y=___________ (用含 x、w 的式子表示)。
(2)研究温度、压强对反应的影响:C6H5CH2CH3(g)+CO2(g)⇌C6H5CH=CH2(g)+CO(g)+H2O(g) △H C6H5CH2CH3(乙苯)的平衡转化率影响如下图所示:则△H_____ 0(填“>”“<”或“=”),压强 p1、p2、p3由小到大的排列顺序是____ 。

(3)CO 可被 NO2氧化,反应为 CO+NO2⇌CO2+NO,当温度高于 225℃时,反应速率 v 正=k 正⋅c(CO)⋅c(NO2)、v 逆=k 逆⋅c(CO2)⋅c(NO),k 正、k 逆分别为正、逆反应速率常数。在上述温度范围内,k 正、k 逆与该反应的平衡常数 K 之间的关系为________ 。
Ⅰ.CO 可用于高炉炼铁
已知: Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g) △H1=akJ/mol;
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H2=bkJ/mol;
则反应 Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)的 △H3=
Ⅱ.一定条件下,CO2和 CO 可以互相转化
(1)某温度下,在容积为 2 L 的密闭容器按甲、乙两种方式投入反应物发生反应:CO2(g)+H2(g)⇌CO(g)+H2O(g)。
| 容器 | 反应物 |
| 甲 | 8molCO2(g)、16molH2(g) |
| 乙 | wmolCO2(g)、xmolH2(g)、ymolCO(g)、zmolH2O(g) |
(2)研究温度、压强对反应的影响:C6H5CH2CH3(g)+CO2(g)⇌C6H5CH=CH2(g)+CO(g)+H2O(g) △H C6H5CH2CH3(乙苯)的平衡转化率影响如下图所示:则△H

(3)CO 可被 NO2氧化,反应为 CO+NO2⇌CO2+NO,当温度高于 225℃时,反应速率 v 正=k 正⋅c(CO)⋅c(NO2)、v 逆=k 逆⋅c(CO2)⋅c(NO),k 正、k 逆分别为正、逆反应速率常数。在上述温度范围内,k 正、k 逆与该反应的平衡常数 K 之间的关系为
您最近一年使用:0次
【推荐2】(1)在一个1 L的密闭容器中,加入2 mol A和1 mol B,发生下列反应:2A(g) + B(g)  3C(g) + D(s), 达到平衡时C的浓度为1.2 mol·L-1。
3C(g) + D(s), 达到平衡时C的浓度为1.2 mol·L-1。
①维持容器的温度不变,若缩小容器的体积,则平衡向____________ (填“正反应方向”、“逆反应方向”或“不”)移动。
②维持容器的体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍是1.2 mol·L-1的是______________ (填序号):
A.4 mol A+2 mol B B.3 mol C+2 mol D C.2 mol A+1 mol B+3 mol C
③达平衡后若升高温度,B的浓度增加,则正反应的△H____________ 0(填“>”、“<、“=”)
(2)下图a是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,图b是反应中的CO和NO的浓度随时间变化的示意图。回答下列问题:

①NO2和CO反应的热化学方程式为_________________ 。
②从反应开始到t1时刻,用NO2浓度变化表示平均反应速率v(NO2)=_____________ 。
③ 此温度下该反应的平衡常数K=_________ ;温度降低K________ (填“变大”、“变小”或“不变“)
 3C(g) + D(s), 达到平衡时C的浓度为1.2 mol·L-1。
3C(g) + D(s), 达到平衡时C的浓度为1.2 mol·L-1。①维持容器的温度不变,若缩小容器的体积,则平衡向
②维持容器的体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍是1.2 mol·L-1的是
A.4 mol A+2 mol B B.3 mol C+2 mol D C.2 mol A+1 mol B+3 mol C
③达平衡后若升高温度,B的浓度增加,则正反应的△H
(2)下图a是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,图b是反应中的CO和NO的浓度随时间变化的示意图。回答下列问题:

①NO2和CO反应的热化学方程式为
②从反应开始到t1时刻,用NO2浓度变化表示平均反应速率v(NO2)=
③ 此温度下该反应的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】按要求完成下列各题
(1)下列各变化过程是熵值明显增加的有__________ (填序号);
① NH4NO3爆炸:2NH4NO3(s)===2N2(g)+4H2O(g)+O2(g)
② 水煤气转化:CO(g)+H2O(g)===CO2(g)+H2(g)
③ 臭氧的生成:3O2(g)===2O3(g)
④ 2C4H10(g)+13O2(g)===8CO2(g)+10H2O(g)
(2)向某密闭容器中充入1 mol CO和2 mol H2O(g),发生反应:CO+H2O(g) CO2+H2。当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是
CO2+H2。当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是_______ ;
A.0.5 mol CO+2 mol H2O(g)+1 mol CO2+1 mol H2
B.1 mol CO+1 mol H2O(g)+1 mol CO2+1 mol H2
C.0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2
D.0.5 mol CO+1.5 mol H2O(g)+0.5 mol CO2+0.5 mol H2
(3)有下列物质:①铜 ②硫酸钡固体 ③氨水 ④氢氧化钠固体 ⑤熔融
硝酸钾 ⑥乙醇 ⑦稀硫酸 ⑧金刚石 ⑨二氧化硫 ⑩冰醋酸。
属于非电解质的有_________ ;属于强电解质的有_______ ;(填序号)
(4)常温下,0.010mol·L-1盐酸和0.010mol·L-1氨水的pH之和_____ 14,
pH=2的盐酸和pH=12的氨水,分别加水稀释10倍后,两溶液的pH之和________ 14(填>,<或=);
(5) 常温下,在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是____________ 。
(1)下列各变化过程是熵值明显增加的有
① NH4NO3爆炸:2NH4NO3(s)===2N2(g)+4H2O(g)+O2(g)
② 水煤气转化:CO(g)+H2O(g)===CO2(g)+H2(g)
③ 臭氧的生成:3O2(g)===2O3(g)
④ 2C4H10(g)+13O2(g)===8CO2(g)+10H2O(g)
(2)向某密闭容器中充入1 mol CO和2 mol H2O(g),发生反应:CO+H2O(g)
 CO2+H2。当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是
CO2+H2。当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是A.0.5 mol CO+2 mol H2O(g)+1 mol CO2+1 mol H2
B.1 mol CO+1 mol H2O(g)+1 mol CO2+1 mol H2
C.0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2
D.0.5 mol CO+1.5 mol H2O(g)+0.5 mol CO2+0.5 mol H2
(3)有下列物质:①铜 ②硫酸钡固体 ③氨水 ④氢氧化钠固体 ⑤熔融
硝酸钾 ⑥乙醇 ⑦稀硫酸 ⑧金刚石 ⑨二氧化硫 ⑩冰醋酸。
属于非电解质的有
(4)常温下,0.010mol·L-1盐酸和0.010mol·L-1氨水的pH之和
pH=2的盐酸和pH=12的氨水,分别加水稀释10倍后,两溶液的pH之和
(5) 常温下,在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】
(1)工业合成氨时,合成塔中每产生1molNH3,放出46.1kJ的热量。
某小组研究在500℃下该反应过程中的能量变化。他们分别在体积均为VL的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应。相关数据如下:
①容器a中,0~t1时间的平均反应速率为υ(H2)= ___________ 。
②下列叙述正确的是________ (填字母序号)。
A.容器b中反应达平衡状态时,Q>73.76kJ
B.平衡时,两容器中H2的体积分数相等
C.反应开始时,两容器中反应的化学反应速率相等
D.平衡时,容器中N2的转化率:a<b
(2)以氨为原料,合成尿素的反应原理为:2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g) ΔH = a kJ·mol-1。
CO(NH2)2(l)+H2O(g) ΔH = a kJ·mol-1。
为研究平衡时CO2的转化率与反应物投料比[ ]及温度的关系,研究小组在10 L恒容密闭容器中进行模拟反应。(Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系)。
]及温度的关系,研究小组在10 L恒容密闭容器中进行模拟反应。(Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系)。
①a_______ 0 (填“>”或“<”)。
②若n(CO2)起始 =10 mol,曲线Ⅱ的投料比为0.4,在100℃条件下发生反应,达平衡至A点,则A点与起始压强比为_______ 。
③A点平衡常数与B点平衡常数间的关系:KA_______ KB (填“>”或“<”或“=”)。
(3)利用氨气与空气催化氧化法制取联氨N2H4.如图是由“联氨—空气”形成的绿色燃料电池,以石墨为电极的电池工作原理示意图,b电极为_______ 极(填“正”或“负”),写出该电池工作时a电极的电极反应式_______ 。
(1)工业合成氨时,合成塔中每产生1molNH3,放出46.1kJ的热量。
某小组研究在500℃下该反应过程中的能量变化。他们分别在体积均为VL的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应。相关数据如下:
| 容器 | 起始时各物质物质的量/mol | 达到平衡的时间 | 达平衡时体系能量的变化/kJ | ||
| N2 | H2 | NH3 | |||
| a | 1 | 4 | 0 | t1 min | 放出热量:36.88kJ |
| b | 2 | 8 | 0 | t2 min | 放出热量:Q |
②下列叙述正确的是
A.容器b中反应达平衡状态时,Q>73.76kJ
B.平衡时,两容器中H2的体积分数相等
C.反应开始时,两容器中反应的化学反应速率相等
D.平衡时,容器中N2的转化率:a<b
(2)以氨为原料,合成尿素的反应原理为:2NH3(g)+CO2(g)
 CO(NH2)2(l)+H2O(g) ΔH = a kJ·mol-1。
CO(NH2)2(l)+H2O(g) ΔH = a kJ·mol-1。为研究平衡时CO2的转化率与反应物投料比[
 ]及温度的关系,研究小组在10 L恒容密闭容器中进行模拟反应。(Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系)。
]及温度的关系,研究小组在10 L恒容密闭容器中进行模拟反应。(Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系)。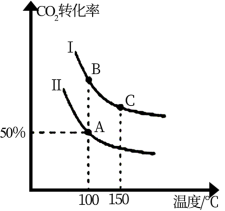
①a
②若n(CO2)起始 =10 mol,曲线Ⅱ的投料比为0.4,在100℃条件下发生反应,达平衡至A点,则A点与起始压强比为
③A点平衡常数与B点平衡常数间的关系:KA
(3)利用氨气与空气催化氧化法制取联氨N2H4.如图是由“联氨—空气”形成的绿色燃料电池,以石墨为电极的电池工作原理示意图,b电极为

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】研究含氮污染物的治理是环保的一项重要工作。合理应用和处理氮的化合物,在生产生活中有重要意义。
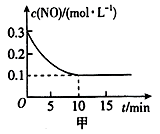
(l)T℃时,将0.6mol NO和0.2 mol O3气体充入到2L固定容积的恒温密闭容器中,NO的浓度随反应时间的变化如图甲所示。
①T℃时,反应3NO(g)+O3(g) 3NO2(g)的平衡常数K=
3NO2(g)的平衡常数K=________ .
②不能说明反应达到平衡状态的是_________ (填序号).
A.气体颜色不再改变
B.气体的平均摩尔质量不再改变
C.气体的密度不再改变
D.单位时间内生成O3和NO2物质的量之比为1:3
(2)已知2NO2 N2O4,如图乙所示,A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气囊,关闭K2,各将1molNO2通过K1、K3分别充入真空A、B中,反应起始时A、B的体积相同均为
N2O4,如图乙所示,A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气囊,关闭K2,各将1molNO2通过K1、K3分别充入真空A、B中,反应起始时A、B的体积相同均为 L(忽略导管中的气体体积).
L(忽略导管中的气体体积).

①若容器A中到达平衡所需时间 s,达到平衡后容器内压强为起始压强的0.8倍,则平均化学反应速率
s,达到平衡后容器内压强为起始压强的0.8倍,则平均化学反应速率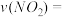
_____________________ .
②若打开K2,平衡后B容器的体积缩至0.4 L,则打开K2之前,气球B体积为
L,则打开K2之前,气球B体积为_________ L.
③若平衡后在A容器中再充入0.5molN2O4,则重新到达平衡后,平衡混合气中NO2的体积分数___________ (填“变大”“变小”或“不变”)。

(l)T℃时,将0.6mol NO和0.2 mol O3气体充入到2L固定容积的恒温密闭容器中,NO的浓度随反应时间的变化如图甲所示。
①T℃时,反应3NO(g)+O3(g)
 3NO2(g)的平衡常数K=
3NO2(g)的平衡常数K=②不能说明反应达到平衡状态的是
A.气体颜色不再改变
B.气体的平均摩尔质量不再改变
C.气体的密度不再改变
D.单位时间内生成O3和NO2物质的量之比为1:3
(2)已知2NO2
 N2O4,如图乙所示,A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气囊,关闭K2,各将1molNO2通过K1、K3分别充入真空A、B中,反应起始时A、B的体积相同均为
N2O4,如图乙所示,A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气囊,关闭K2,各将1molNO2通过K1、K3分别充入真空A、B中,反应起始时A、B的体积相同均为 L(忽略导管中的气体体积).
L(忽略导管中的气体体积).
①若容器A中到达平衡所需时间
 s,达到平衡后容器内压强为起始压强的0.8倍,则平均化学反应速率
s,达到平衡后容器内压强为起始压强的0.8倍,则平均化学反应速率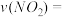
②若打开K2,平衡后B容器的体积缩至0.4
 L,则打开K2之前,气球B体积为
L,则打开K2之前,气球B体积为③若平衡后在A容器中再充入0.5molN2O4,则重新到达平衡后,平衡混合气中NO2的体积分数
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】二氧化碳的捕集、利用与封存(CCUS)是我国能源领域的一个重要战略方向,CO2的综合利用是解决温室及能源问题的有效途径。
(1)CO2催化加氢能合成低碳烯烃: 2CO2(g)+ 6H2(g) C2H4(g)+ 4H2O(g)。不同温度下平衡时的四种气态物质的物质的量如图所示,则曲线b表示的物质为
C2H4(g)+ 4H2O(g)。不同温度下平衡时的四种气态物质的物质的量如图所示,则曲线b表示的物质为_______ (填化学式),该反应的△H_______ 0 (填:“>”或“<”) 。

(2)工业中,CO2和H2在催化剂Cu/ZnO作用下可发生两个平行反应,分别生成CH3OH和CO。
反应A: CO2(g)+ 3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
反应B: CO2(g)+ H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
控制CO2和H2初始投料比为1:3时,温度对CO2平衡转化率及甲醇和CO产率的影响如图所示。

①由图可知温度升高时CO的产率上升,其主要原因可能是_______ 。
②由图可知获取CH3OH最适宜的温度是_______ 。下列措施有利于提高CO2转化为CH3OH的平衡转化率的有_______ 。
A.使用催化剂
B.增大体系压强
C.增大CO2和H2的初始投料比
D.投料比和容器体积不变,增加反应物的浓度
(3)工业上利用水煤气合成甲醇的主要反应可表示为CO(g)+2H2(g) CH3OH(g)△H= — 90.8kJ·mol-1,在温度、容积相同的甲、乙两个密闭容器,若甲中加入1molCO和2molH2,乙中加入1molCH3OH(g),反应达到平衡时甲放出的热量为Q1kJ,乙吸收的热量为Q2kJ,甲中CO的转化率为a1,乙中CH3OH的转化率为a2,则Q1+Q2=
CH3OH(g)△H= — 90.8kJ·mol-1,在温度、容积相同的甲、乙两个密闭容器,若甲中加入1molCO和2molH2,乙中加入1molCH3OH(g),反应达到平衡时甲放出的热量为Q1kJ,乙吸收的热量为Q2kJ,甲中CO的转化率为a1,乙中CH3OH的转化率为a2,则Q1+Q2=_______ ,a1+a2=_______ 。
(1)CO2催化加氢能合成低碳烯烃: 2CO2(g)+ 6H2(g)
 C2H4(g)+ 4H2O(g)。不同温度下平衡时的四种气态物质的物质的量如图所示,则曲线b表示的物质为
C2H4(g)+ 4H2O(g)。不同温度下平衡时的四种气态物质的物质的量如图所示,则曲线b表示的物质为
(2)工业中,CO2和H2在催化剂Cu/ZnO作用下可发生两个平行反应,分别生成CH3OH和CO。
反应A: CO2(g)+ 3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)反应B: CO2(g)+ H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)控制CO2和H2初始投料比为1:3时,温度对CO2平衡转化率及甲醇和CO产率的影响如图所示。

①由图可知温度升高时CO的产率上升,其主要原因可能是
②由图可知获取CH3OH最适宜的温度是
A.使用催化剂
B.增大体系压强
C.增大CO2和H2的初始投料比
D.投料比和容器体积不变,增加反应物的浓度
(3)工业上利用水煤气合成甲醇的主要反应可表示为CO(g)+2H2(g)
 CH3OH(g)△H= — 90.8kJ·mol-1,在温度、容积相同的甲、乙两个密闭容器,若甲中加入1molCO和2molH2,乙中加入1molCH3OH(g),反应达到平衡时甲放出的热量为Q1kJ,乙吸收的热量为Q2kJ,甲中CO的转化率为a1,乙中CH3OH的转化率为a2,则Q1+Q2=
CH3OH(g)△H= — 90.8kJ·mol-1,在温度、容积相同的甲、乙两个密闭容器,若甲中加入1molCO和2molH2,乙中加入1molCH3OH(g),反应达到平衡时甲放出的热量为Q1kJ,乙吸收的热量为Q2kJ,甲中CO的转化率为a1,乙中CH3OH的转化率为a2,则Q1+Q2=
您最近一年使用:0次



